基于营养风险筛查下的早期肠内营养支持对食管癌光动力治疗后病人营养状态及肠黏膜屏障功能的影响
2023-10-23张丽娟王改琳
张丽娟,王改琳
对处于手术无法切除、无法耐受手术或无法耐受放化疗等情况的病人,光动力疗法为食管癌病人带来新的希望。但由于肿瘤组织的蛋白质合成及分解代谢强,增加了病人营养不良风险,且光动力疗法亦对机体造成损伤。肠外营养为短时间内补充营养的一种有效方法,可改善食管癌病人的营养不足,但可能出现感染。而营养风险筛查可量化病人营养状况,利于营养方案的针对性实施[1-4]。研究表明,早期肠内营养可促进食管癌病人术后恢复,改善其生活质量[5]。本研究则在营养风险筛查的基础上,应用早期肠内营养支持,探究该营养方式对食管癌光动力治疗后病人的应用价值,具体如下。
1 资料与方法
1.1 一般资料
选取我院2020年11月—2022年6月收治的105例食管癌光动力治疗后病人为研究对象。纳入标准:符合食管癌的诊断标准[6];均行光动力治疗;病人与家属签署知情同意书。排除标准:其他恶性肿瘤;消化道畸形;自身免疫性疾病;认知功能异常。依据营养方式不同分为对照组52例和观察组53例。对照组:男30例,女22例;年龄46~69(56.83±6.84)岁;初中以下27例,初中及以上25例;鳞癌39例,腺癌13例。观察组:男32例,女21例;年龄46~69(57.14±5.71)岁;初中以下30例,初中及以上23例;鳞癌41例,腺癌12例。两组病人基线资料比较差异无统计学意义(P>0.05),具有可比性。本研究经我院医学伦理委员会审核批准(伦理批号:20201109)。
1.2 干预方法
1.2.1 对照组干预方法
对照组病人给予常规营养支持,持续干预1周。术后予以病人深静脉置管,行肠外营养,所用营养液经我院营养科医生配制,依照50 mL/(kg·d)总入液量、104.65 kcal/(kg·d)的非蛋白质热量、1∶1的糖脂比、150 kcal∶1 g的热氮比、糖盐水与中长链脂肪乳按照1∶2的比例为病人提供非蛋白质热量,能量为10~25 kcal/(kg·d),待胃肠功能恢复拔除胃管,由流质饮食逐渐过渡为普食。
1.2.2 观察组干预方法
观察组病人给予基于营养风险筛查下的早期肠内营养支持,持续干预1周。依据相关指南[7]于术后 6 h开展肠内营养,将250~500 mL的5%葡萄糖氯化钠注入营养管;于术后24 h内病人生命体征稳定,20~30 mL/h自鼻肠管通过肠内营养泵恒速灌注肠内营养液,根据其耐受程度逐渐增加营养液输入量,总输入量在1 000 mL内;于第2 天以50~60 mL/h的滴速予肠内营养液1 000 mL;于第3 天以80~100 mL/h的滴速予肠内营养液1 500~2 000 mL,达全量;之后不超过125 mL/h予全量肠内营养液。依据总热量125.52 kJ/(kg·d)计算,初始阶段静脉补充,补充不足的液体量和热量。依据欧洲肠外肠内营养学会(ESPEN)推荐的2002营养风险筛查简表(NRS 2002)评分[8],行营养风险筛查,NRS 2002评分不足3分时行上述肠内营养,每隔2 d筛查1次;NRS2002评分不小于3分时依照病人的年龄、体质指数和疾病状态对其能量需求进行精确计算,静息状态能量消耗、食物动力消耗与机体活动消耗之和为每日消耗总能量,对蛋白质、糖类及脂肪比例予合理调整。
1.3 观察指标
1.3.1 营养状态
于干预前、干预1周末清晨病人空腹时抽取其2 mL肘静脉血,分离血清,BK-400型全自动生化分析仪测定前白蛋白(PA)、白蛋白(ALB)及血红蛋白(Hb)含量。
1.3.2 肠黏膜屏障功能
于干预前、干预1周末抽取病人清晨空腹肘静脉血3 mL,2 300 r/min离心10 min,取适量血清标本,酶联免疫法测定二胺氧化酶(DAO)、肿瘤坏死因子α(TNF-α)水平;免疫透射比浊法测定C反应蛋白(CRP)水平。
1.3.3 胃肠道功能
比较两组病人术后首次肛门排气时间、首次肠鸣音恢复时间及首次排便时间。
1.4 统计学方法
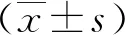
2 结果
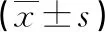
表1 两组病人干预前、干预1周末营养状态比较
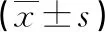
表2 两组病人干预前、干预1周末肠黏膜屏障功能比较
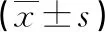
表3 两组病人胃肠道功能比较
3 讨论
3.1 基于营养风险筛查下的早期肠内营养支持可调节营养状态
临床上对于不能耐受手术或手术无法切除等类型的食管癌病人常应用光动力疗法,但由于癌症本身引起机体处于高代谢状态,易引起机体能量过度消耗,造成营养不良[9-11]。常规营养支持可纠正体液丢失及电解质紊乱,可较短时间内纠正机体营养不良状况,对营养状态具有一定调节效果[12]。而基于营养风险筛查下的早期肠内营养支持,NRS 2002评分可针对病人情况予以量化评估,精准划分病人所处的营养风险等级,不仅使得营养方案更具有针对性,且定期筛查可便于及时掌握其营养需求,及时调整营养方案,更高效地进行营养干预;早期进食可对肠道黏膜进行直接作用,改善肠黏膜通透性,加快肠道正常消化吸收功能的恢复进程,加快机体代谢,扭转机体营养不良状态[13]。与黄双双等[14-15]研究结果一致。本研究结果显示,观察组病人干预1周末PA、ALB、Hb水平高于对照组,表明基于营养风险筛查下的早期肠内营养支持可改善营养状态。
3.2 基于营养风险筛查下的早期肠内营养支持可调节肠黏膜屏障功能
本研究结果显示,观察组病人干预1周末DAO、TNF-α、CRP水平低于对照组,表明基于营养风险筛查下的早期肠内营养支持可改善肠黏膜屏障功能。静脉输注较为方便,病人易于接受,可较快达到所需热量,但较长时间应用,易增加肠黏膜萎缩风险,影响肠黏膜屏障功能的调节[16]。而NRS 2002评分的应用可对病人当前营养状态予以直接评估,便于临床医生及时掌握其当前营养水平,利于术后营养干预方案的制订更具有针对性及目的性,避免长时间禁食增加肠黏膜萎缩风险;当营养液通过消化道黏膜时可兴奋肠黏膜感受器,推动肠黏膜生长。早期进食一方面及时为肠黏膜提供营养,提高肠道血液循环速度,利于术后机体应激反应的减轻,避免胃肠道黏膜萎缩,加快肠黏膜屏障功能恢复;另一方面,抑制内生脂肪氧化分解,改善肠道黏膜厚度及绒毛高度,利于胃肠黏膜修复[17]。杨琼等[18]研究表明,营养筛查下的营养干预可改善病人免疫能力,便于减轻术后应激反应,对肠黏膜屏障功能具有间接改善作用。
3.3 基于营养风险筛查下的早期肠内营养支持可调节胃肠道功能
肠外营养通过静脉途径输注能量和各种营养素,利于维持营养平衡,但长时间应用可使小肠黏膜细胞及营养酶系的活性退化,增加消化道负担,造成胃肠道功能的调节效果一般[19]。NRS 2002评分具有较高的特异性,可于人群中有效检出营养风险阳性者,提高临床护理干预的效率,且其对评估者的专业性没有过高要求,便于病人更好地理解营养风险筛查的重要性,促使病人更好地配合临床干预;相对静脉肠外营养,于早期肠内营养更安全,输入营养液可刺激肠黏膜,加快肠黏膜的血液循环,提高肠黏膜代谢,促使肠道固有菌群得以维持正常生长,并使消化液以及胃肠道激素的分泌增多,促使胃肠逐渐恢复正常蠕动;且早期肠内营养可对消化道黏膜及时予以有效刺激,增加肠胃动力,加快肠鸣音恢复,促进术后尽早排气[20]。与何建冰等[21]研究结果相似。本研究结果显示,观察组病人术后首次肛门排气时间、首次肠鸣音恢复时间、首次排便时间短于对照组,表明基于营养风险筛查下的早期肠内营养支持可改善胃肠道功能。
综上所述,基于营养风险筛查下的早期肠内营养支持可改善食管癌光动力治疗后病人营养状态,调节胃肠道功能,改善肠黏膜屏障功能,疗效优于常规营养支持干预。本研究应用ESPEN推荐的NRS 2002评分,对病人当前营养状况予以精准量化评估,并依据《食管癌病人营养治疗指南》行早期肠内营养支持,符合机体生理状态,利于术后尽早恢复,对食管癌病人的临床应用干预具有重要的指导意义。但由于研究时间相对较短,入选的样本数较有限,在所得的结果中可能存在偏倚,应扩大样本入选量,增加研究时间,以便更深入地研究。
