纳米氧化铬的制备与应用研究进展
2023-10-19徐恩浩武开鹏
徐恩浩,武开鹏
(四川大学材料科学与工程学院,四川成都 610064)
作为功能和保护材料,铬氧化物因具有良好的光学、磁学和力学性能被广泛应用[1]。作为铬氧化物的一种,三氧化二铬(Cr2O3)是一种具有金属光泽的墨绿色粉末,相对分子质量为151.99,具有较高的熔点(2 266 ℃)和沸点(3 000 ℃)[2]。当温度发生较大变化时,Cr2O3依旧可以稳定存在,几乎不发生热变化[3]。大量有关纳米Cr2O3的研究和应用等报道的涌现,表明其是一种极具潜力的氧化物,特别是表现出来的小尺寸效应、表面效应等使纳米Cr2O3的工业价值受到了广泛关注。
近年来,随着国内外对Cr2O3研究的不断深入,有关纳米Cr2O3粉体及其复合材料的制备方法和应用场景层出不穷。例如,SADEGHI 等[4]通过溶液燃烧的方式制备了粒径为20~30 nm 的Cr2O3纳米颗粒,并与多壁碳纳米管(MWCNTs)复合得到Cr2O3/MWCNTs 纳米复合材料。当将其作为氧化还原反应催化剂时,表现出较10%(质量分数)Pt/C 优异的催化性能。除作为高效催化剂外,Cr2O3还可作为结构和功能材料用于耐磨防腐涂层[5]、颜料[6]、气敏传感器[7]、新能源材料[8]等领域。需要指出的是,纳米Cr2O3在上述领域的应用在一定程度上取决于其微观结构特征,特别是将其作为关键功能材料时的应用场景,而Cr2O3的制备方法对其形貌结构的影响很大。为此,本文结合近年来国内外在纳米Cr2O3的制备和应用领域取得的最新研究成果,对纳米Cr2O3的制备方法进行了详细综述,并对其现有和潜在应用领域进行了介绍和展望,为纳米Cr2O3的研究和应用提供一定的参考和借鉴。
1 制备方法
1.1 气相法
气相法是先将原料转化成蒸气并在气相中发生反应,最后冷却至室温获得纳米材料的方法。通常情况下,将原料激活为蒸气的方法有多种,如化学火焰加热、等离子体加热、激光诱导加热等。采用气相法制备的纳米材料具有颗粒均匀、纯度高、分散良好等优点,且制备过程易于控制,然而,该方法对设备要求苛刻、大规模生产成本较高、少见于工业生产。气相法主要有化学气相沉积、微波等离子体和激光气相沉积等制备方法。
1.1.1 化学气相沉积法
化学气相沉积法(CVD)是在中温或高温下,通过气体之间的化学反应在衬底表面沉积一层固体产物的工艺,被广泛应用于纳米材料制备领域。LIN等[9]利用六羰基铬[Cr(CO)6]的热解,在氧化铝颗粒表面沉积了粒径为20~40 nm 的纳米Cr2O3颗粒,结果显示,当控制热解温度为300 ℃和400 ℃时,分别得到非晶态和结晶态Cr2O3颗粒。HAFEEZ 等[10]以碘为辅助材料,以三氧化铬(CrO3)为前驱体,采用化学气相沉积法合成了具有良好光响应特性的六边形2D-Cr2O3(如图1 所示),在自旋电子器件中得到有效应用。此外,有报道采用金属-有机化学气相沉积技术(MOCVD)制备了铬和钕的氧化物复合薄膜(Cr2O3和Nd2O3的混合物),用于减缓不锈钢的高温腐蚀[11]。李帅等[12]也通过此方法制备氧化铬薄膜,该薄膜可用于材料表面耐磨、金属耐腐蚀、抗高温氧化、防氢渗透功能薄膜材料。总体上,金属-有机化学气相沉积利用金属有机前驱体的传输、吸附、热分解过程在衬底表面沉积氧化物层,具有沉积温度低、重复性好等优点。

图1 在SiO2/Si衬底上生长的六边形2D-Cr2O3的扫描电镜图像[10]Fig.1 SEM images of as-grown 2D-Cr2O3 hexagons on SiO2/Si substrate[10]
1.1.2 微波等离子体法
微波等离子体法是利用微波使反应分子离子化,产生等离子体,促进其在基体或其他反应物表面发生化学反应得到纳米Cr2O3。文献[13]报道了将六羰基铬[Cr(CO)6]在氩-氧混合气氛中(80%Ar 和20%O2)高温反应,利用冷表面收集得到粒径约为8~9 nm 的Cr2O3纳米颗粒。NADEEM 等[14]通过微波等离子体技术成功制备了包覆有Cr2O3的γ-氧化铁(γ-Fe2O3)纳米颗粒。NADEEM 等分别以液态五羰基铁[Fe(CO)5]和固态六羰基铬[Cr(CO)6]为铁源和铬源,利用带有2 个连续排列等离子区的2.45 GHz 磁控管激发原料,反应得到平均粒径为13 nm 且具有核壳结构的Cr2O3包覆γ-Fe2O3复合纳米颗粒(如图2所示)。

图2 Fe2O3/Cr2O3的XRD谱图(a)、在10 nm尺度下的透射电镜图像(b)[14]Fig.2 XRD pattern of Fe2O3/Cr2O3(a),TEM image of Fe2O3/Cr2O3 at 10 nm(b)[14]
1.1.3 激光气相沉积法
激光气相沉积法是采用激光照射反应源气体或靶材,受照射材料在激光能量的共振吸收和碰撞传热作用下体系温度瞬间达到反应温度,反应完成后沉积到基体表面,也是一种制备薄膜的有效方法。BALAKRISHNAN等[15]以Cr3C2为靶材,分别在Si(100)和玻璃衬底上制备了Cr2O3薄膜,结果显示,沉积在Si(100)衬底上的薄膜含有粒径为24~72 nm 的纳米晶,而沉积在玻璃衬底上的薄膜含有粒径为19~56 nm 的晶体,晶粒尺寸的轻微减小可能与等离子体物质附近基底的绝缘特性有关。SI 等[16]直接利用金属铬靶材,在氧气条件下利用激光束进行热激活得到纳米Cr2O3,随后在40 MPa 的高压氧条件下退火得到Cr2O3/CrO2纳米颗粒。此外,VILA 等[17]利用该技术首次在钛酸锶衬底上生长出单晶且单取向的外延Cr2O3薄膜。
1.2 湿化学法
湿化学法的最大特征是物料在溶液条件下进行反应。典型流程为先将可溶性金属盐或化合物在溶液体系下反应得到前驱体,再将其煅烧后即得到纳米颗粒。湿化学法主要包括沉淀法、微乳液法、溶胶-凝胶法、水热/溶剂热法和模板法等,不同制备方法对颗粒的形态结构影响很大。
1.2.1 沉淀法
沉淀法是基于湿化学反应合成金属氧化物最常用的方法,通常是在沉淀剂的辅助下首先获得前驱体沉淀物,然后煅烧得到粉体颗粒,被广泛用以合成单一或复合氧化物超细粉体。根据沉淀方式的不同,沉淀法可分为直接沉淀法、共沉淀法和均相沉淀法,其中,直接沉淀法操作简单且成本较低。ZHANG 等[18]将Cr(NO3)3·9H2O 水溶液加入到质量分数为10%的氨水溶液中获得沉淀浆液,在室温下老化后在空气中烧结得到粒径约为20 nm 的纳米Cr2O3颗粒,如图3 所示,纳米Cr2O3的晶格距离为0.369 nm 和0.265 nm,分别对应于(012)和(104)晶面的标准值。ABBAS 等[19]通过共沉淀法制备了粒径为20~30 nm 的Cr2O3与碳纳米管的复合材料。此外,ABECASSIS-WOLFOVICH 等[20]利用尿素作为辅助剂,通过均相沉淀法制备了比表面积为484~735 m2/g、孔径为3~9 nm的介孔气凝胶;虽然该方法得到的材料比表面积较大,但实验条件过于苛刻且对设备要求过高、原料消耗过多。
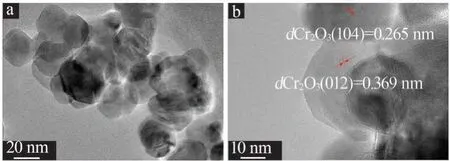
图3 Cr2O3-P的透射电镜图像[18]Fig.3 TEM images of Cr2O3-P[18]
在产业化方面,不同于作为大宗化工(冶金)原料的常规Cr2O3,市场对纳米Cr2O3的需求有限,市场空间较小。据不完全统计,目前国内有上海卜微应用材料技术有限公司、浙江亚美纳米科技有限公司、上海乃欧纳米科技有限公司、上海杳田新材料科技有限公司等少数几家企业从事相关生产。例如,卜微应用材料生产的高纯纳米Cr2O3的粒径可以控制在20~1 000 nm,主要面向高校和科研院所等客户的应用需求,年产量可达吨级甚至更大规模。
1.2.2 微乳液法
微乳液是指在表面活性剂的辅助下形成的透明或半透明液体,尺度在几纳米到几十纳米,分为油包水(W/O)和水包油(O/W)两种类型。目前,用来制备超细粒子的微乳液往往是W/O型体系,其中的分散相水核可以作为一个“微型反应器”[21]。利用微乳液间能够进行物质交换的原理可制备纳米材料并有效控制颗粒尺寸。BAI等[22]通过微乳液法制备了具有多孔结构的饼状纳米Cr2O3,如图4 所示,饼状Cr2O3微实体由小于100 nm的细小颗粒组成,颗粒间含有微小孔洞,比表面积高达32.4 m2/g,其选区电子衍射图表明Cr2O3为多晶结构。滕飞等[23]将铬(Ⅵ)盐与助剂按一定配比制成水相,将有机介质和表面活性剂按最佳配比均匀混合作为油相,在搅拌下将水相加入油相并在90~100 ℃下反应,然后经热处理得到球形Cr2O3超细粉体,其平均粒径小于100 nm。与沉淀法相比,微乳液法制备的材料具有均匀性好、粒径大小可控等优点。然而,该方法单批次制备的材料数量有限,溶剂的回收再利用面临较大挑战,尚无工业化应用趋势。

图4 Cr2O3的扫描电镜图像(a)、透射电镜图像(b)、高分辨率透射电镜图像及选区电子衍射插图(c)[22]Fig.4 (a)SEM image,(b)TEM image,(c)HRTEM image and SAED illustration of Cr2O3[22]
1.2.3 溶胶-凝胶法
溶胶-凝胶法是一种可以制备从零维到三维材料的湿化学制备方法。典型流程为先将反应物制备成凝胶,再将凝胶干燥焙烧去除有机成分后得到粉体材料。该方法制备过程能耗低,得到的材料组分均匀、纯度高,不足之处在于凝胶制备需要大量有机溶剂、制膜成本大、工艺时间长[24]。不过,鉴于纳米Cr2O3的市场需求较小,以及采用该方法制备的材料具有纯度高(≥99.9%)、粒度可控等优势,是目前部分企业所采用的主流方法。例如,亚美纳米科技制备的纳米Cr2O3的粒径可以控制在100 nm 以内;乃欧纳米科技生产的球形纳米Cr2O3的粒径为50~500 nm,且能够按需求定制其他粒度规格的产品。ALMONTASSER 等[25]将Cr(NO3)3和NaOH 溶液混合均匀后,转移至密闭容器中反应得到浅绿色产物,随后在100 ℃保温形成深绿色凝胶,经煅烧研磨得到平均粒径为13.5 nm 的Cr2O3纳米颗粒。进一步,以Cr(NO3)3·9H2O、NiCl2·6H2O、Co(NO3)2、Fe(NO3)3·9H2O 等为原料,通过该方法制备了粒径为13.82~19.15 nm 的纯相Cr2O3及Ni、Co、Fe 等元素掺杂的产物(NixCr2-xO3、CoxCr2-xO3、FexCr2-xO3,x=0.01、0.03、0.05、0.07)[26],体现了溶胶-凝胶法制备材料具有掺杂范围广、化学计量准确、易于调节等优点。
1.2.4 水热/溶剂热法
水热/溶剂热法是指在特制的密闭反应器中,以水或其他溶剂为反应介质,在高温高压条件下将难溶或不溶物质溶解并结晶进行无机合成和材料处理。PEI 等[27]以CrO3为原料,通过改变乙醇还原剂的用量和煅烧温度,利用水热法制备了粒径为29.28~60.74 nm 的Cr2O3纳米颗粒;当控制乙醇用量为5.03 g、煅烧温度为500 ℃时,得到平均粒径为30.32 nm 的产物,其比表面积为37.98 m2/g(如图5a所示);当煅烧温度升高到700 ℃时,产物粒径显著增大、比表面积急剧减小(如图5b 所示)。此外,也有文献报道以铬酸钠和还原氧化石墨烯(rGO)为原料,采用水热法制备了具有良好电化学特性的Cr2O3/rGO 复合纳米材料[28]。ANANDAN 等[29]通过调整水/醇溶剂的比例,制备了多种粒径和比表面积的Cr2O3纳米颗粒(见表1),结果表明,醇类介质对尺寸的控制优于水介质,其中,当采用甲醇为主要溶剂时,得到产物的粒径最小、比表面积最大(分别为25 nm 和45.97 m2/g)。青海盐湖研究所李波等[30]以多种六价铬化合物为原料,在还原剂的作用下首先制备了氢氧化铬纳米球,然后煅烧获得了纳米Cr2O3;该方法具有工艺简单、避免铬损失、无含铬废渣排放等优点,且制备的纳米Cr2O3的粒径形貌均一。总体上,通过水热/溶剂热法合成的纳米材料纯度高、晶粒发育良好、有效避免了杂质和结构缺陷,但在制备过程中无法直接观察生长过程、单次产量少、安全性较差。
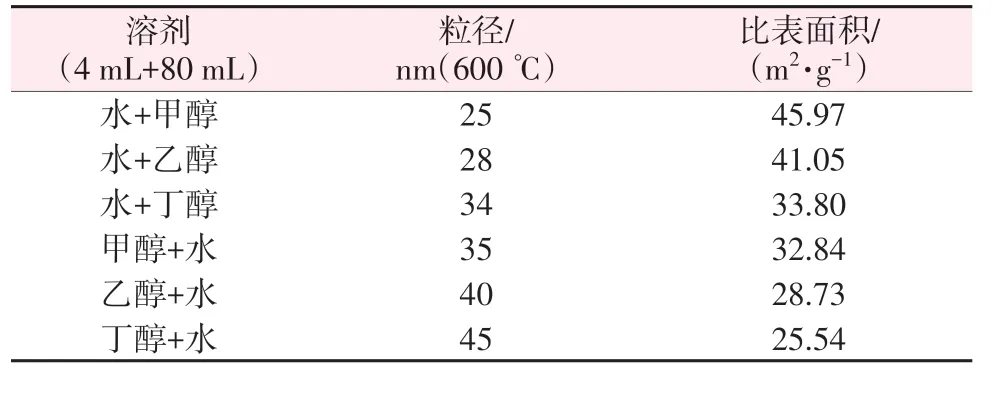
表1 Cr2O3纳米颗粒的粒径和比表面积对比[29]Table 1 Comparison of size and specific surface area of Cr2O3 nanoparticles[29]

图5 Cr2O3的场发射扫描电镜图像[27]Fig.5 FESEM images of Cr2O3[27]
1.2.5 模板法
模板法是一种利用基质模板控制材料尺寸和形貌制备纳米材料的方法,模板法可分为软模板法和硬模板法。软模板法主要以表面活性剂构成的胶团或胶束为模板,利用其结构中的空隙或外表面作为化学合成的载体。LI 等[31]将Cr(NO3)3·9H2O 与CTAB混合后置于高压反应釜中,在140~200 ℃反应后煅烧得到介孔结构的Cr2O3,结果显示,煅烧前Cr2O3孔径为3.8~8.6 nm、比表面积为125~143 m2/g;煅烧后Cr2O3孔径为27.6~34.9 nm、比表面积为34~44 m2/g;在煅烧过程中,小孔的坍塌和Cr2O3纳米晶体的生长导致材料的比表面积显著减小、孔径显著增大,这些较大的孔隙有利于提升其作为催化剂时的反应活性。硬模板法则是利用介孔硅、纳米管、金属模板、高分子薄膜等作为模板,将原料填充到模板的单体进行化学合成的一种方法。不同于软模板法高温煅烧时可能会破坏纳米颗粒的表面结构,硬模板法可以较好地保持纳米颗粒的大比表面积。KIM等[32]以介孔二氧化硅为模板、使用硝酸铬为原料,通过硬模板法制备了介孔Cr2O3纳米线,结果表明,150 ℃处理后得到的Cr2O3纳米线具有最大的比表面积(230 m2/g),其长度和直径分别为2 μm 和5 nm。除了人工合成的模板外,一些经过处理后的低价生物模板可用于工业生产。例如,奚亚男等[33]以稀盐酸浸泡处理后的蛋膜为模板,以Cr(NO3)3·9H2O 为原料,制备了纳米Cr2O3,既降低了成本,又简化了操作;当作为气敏传感器时,其对丙酮气体的检出限可达到1×10-6(体积分数)。
总体上,采用模板为载体可以精确控制纳米材料的尺寸和形状,有效解决纳米材料分散稳定性差等问题。然而,不足之处在于去除模板过程中容易引入杂质,同时也容易破坏纳米材料的结构。
1.3 固相法
固相法是将两种或两种以上的单质和金属化合物进行机械研磨,并在一定温度下煅烧处理制备目标产物的方法。固相法操作方便、设备简单、克服了气相法能耗高的缺点,但其难以实现均匀混料、得到的颗粒大小不一[34]。固相法主要分为固相热分解法和高能球磨法。
1.3.1 固相热分解法
固相热分解法是将金属盐、六价铬化合物、金属碱或金属氧化物按比例混合,通过高温分解和研磨得到超细粉体。GHOLAMI 等[35]将Al(NO3)3·9H2O、Cr(NO3)3·9H2O和碳酸铵混合后研磨20 min,得到的混合物通过释放原料中的结晶水而变湿并转化为均匀的糊状中间物,干燥煅烧后得到Cr2O3/Al2O3复合载体,并通过湿浸渍的方式制备了Ni 质量分数为15%的载镍催化剂。工业生产冶金级Cr2O3的主要方法有重铬酸钠与硫酸铵加热复分解、铬酸酐热分解、氢氧化铬热分解等方法[36]。与生产冶金级Cr2O3不同,生产纳米Cr2O3要先进行液相干燥处理,以保证前驱体的粒径控制在纳米范围内。梁建等[37]首先通过电化学反应和升华处理得到铬酸铵晶体,再将其与硝酸铵混合,在马弗炉中保温后得到粒径为80~90 nm 的球状纳米Cr2O3,其纯度达99%以上,可以满足颜料和磨料的应用需求。此外,徐国钻等[38]通过铬酸铵溶液喷雾干燥和两步煅烧制备了粒径为7~40 nm 的高纯度纳米Cr2O3,其比表面积为35~50 m2/g;该方法工艺流程短,制备的纳米氧化铬纯度高、比表面积大、热稳定性好,全过程不需要加任何添加剂,所需设备简单。
1.3.2 高能球磨法
高能球磨法是将原料按一定比例加入球磨机中进行研磨、搅拌和撞击,在该过程中通过降低其反应活化能,诱发低温化学反应,最后粉碎得到纳米粉体。TSUZUKI 等[39]根据Na2Cr2O7+S→Cr2O3+Na2SO4固相反应原理制备了非晶Cr2O3纳米颗粒,在使用Na2SO4作为稀释剂的情况下,制备的Cr2O3粒径为10~80 nm。SABYASACHI 等[40]直接以多晶Cr2O3为原料,在行星球磨中研磨得到Cr2O3纳米颗粒,其粒径分布在60~120 nm。根据反应过程和产物可知,单一的固相法虽然操作简单、适合批量制备,但所得到的纳米颗粒的纯度过低、颗粒均匀性得不到保证;而通过添加液相干燥工艺的方式可以显著降低这些缺点,也是未来工业化应用极为有效的途径之一。
纳米Cr2O3各种制备方法对比总结见表2。由表2 可以看出,气相法工艺多以有机铬化合物为原料,常用于制备小尺度纳米颗粒和薄膜;湿化学法多采用Cr(NO3)3为原料,适用于纳米颗粒的制备,并在模板剂的辅助下还可构建一维线状、三维介孔结构的纳米材料;固相法采用的原料广泛,制备的产物多为大尺度纳米颗粒,另外通过预先液相干燥处理后可得到均匀的小尺度纳米颗粒。从制备材料的方式来看,由于气相沉积工艺对设备和气氛条件的要求极高,且制备得到的颗粒结构相对有限,这也是目前工业生产不采用该方法的主要原因。相比之下,湿化学法虽然单次产量不高,但其优势在于设备简单、产物形貌可控、纯度高(可达99.9%以上),可以满足不同客户的需求。尤其是沉淀法与溶胶-凝胶法,既无需水热/溶剂热法的高温高压条件,又不局限于微乳液法的水/油溶剂体系,只要增大反应容器的体积即可实现较大批次量产。随着纳米Cr2O3应用面的拓宽,现有生产工艺体系将不能满足日益增长的需求,固相法虽然能够保证产量要求,但无法达到与湿化学法相媲美的粒度与纯度指标。笔者认为,通过预先液相干燥(如升华、喷雾干燥等)调控前驱体的粒度和提高纯度,继而经过后续的固相复分解得到目标产物,将是一条极为有效的途径。与此同时,纳米Cr2O3多元化的制备方式也将为规模化应用奠定基础。
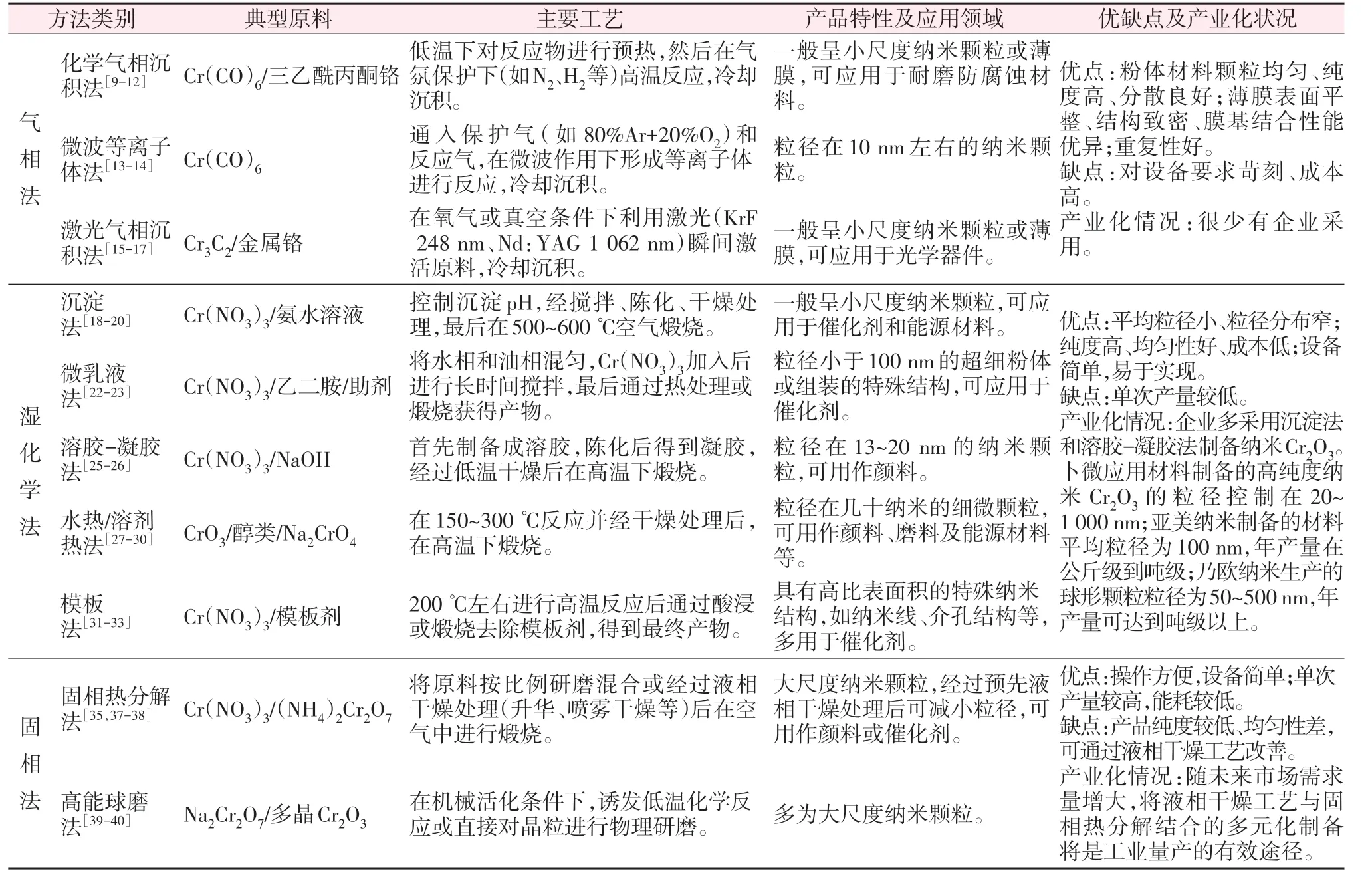
表2 纳米Cr2O3制备方法对比总结Table 2 Comparison and summary of preparation methods of nano-sized Cr2O3
2 应用场景
2.1 催化剂
通常情况下,某种材料的催化性能与其形貌结构密切相关。迄今为止,具有多种形貌的纳米Cr2O3(如纳米颗粒、纳米棒、纳米线等)均有所报道,其中不乏有催化用途的纳米材料。当将纳米Cr2O3用作催化剂时,表面Cr(Ⅵ)含量是衡量其催化活性的重要指标。例如,Cr2O3纳米棒对于2-氯-1,1,1-三氟乙烷的氟化作用要明显优于Cr2O3纳米颗粒,这与纳米棒具有更高的表面Cr(Ⅵ)含量和表面酸性位点密度有关[18]。究其原因,表面Cr(Ⅵ)含量高的基础是颗粒具有高的比表面积,可以暴露出更多的晶面,提高反应物与材料的整体接触面积。BAI等[22]分别采用水热模板法和微乳液法制备了棒状和多孔饼状Cr2O3,在甲苯体积分数为1×10-3和空速为20 L/(g·h)条件下,多孔饼状Cr2O3表现出更好的催化性能,在温度为229 ℃和240 ℃时甲苯转化率分别达到50%和90%,这可归因于其具有更大的比表面积。此外,纳米Cr2O3在催化咪唑衍生物的合成时也可表现出优异的性能[41]。在产业化应用方面,巴斯夫公司长期从事Cr2O3催化剂组合物的研发和生产,多用于环境保护等领域。
需要指出的是,单一纯相纳米Cr2O3催化剂往往不能满足实际催化需求,需要掺入其他金属以提高催化性能。CHEN等[42]发现少量金属Pt的加入能够有效降低介孔Cr2O3对甲苯转化的最佳工作温度。此外,加入Au 和Pd 也可以获得类似的效果[43]。由此可见,低载贵金属的复合催化剂在大幅降低成本的同时还能表现出优异的性能,对消除和控制工业生产中产生的挥发性有机物具有潜在的应用前景。
2.2 耐磨防腐蚀涂层
Cr2O3因其优异的机械性能和化学稳定性,常以涂层的形式用于耐磨、防腐蚀等领域。由于物相的结晶度对涂层的性能影响较大,在制备具有优异耐磨防腐蚀特性的Cr2O3涂层和薄膜时,常采用沉积、磁控溅射或喷涂等方式。例如,LIN 等[44]分别采取深振荡磁控溅射、中频脉冲直流磁控溅射和连续直流磁控溅射的方式在硅晶片和不锈钢片上沉积了Cr2O3涂层,结果显示,采用深振荡磁控溅射方式制备的涂层具有最好的结晶度,表现出更优异的性能。在产业化制备和应用方面,目前主要采用喷涂的方式,包括等离子喷涂、火焰喷涂、电弧喷涂等工艺。例如,德清德奥热喷涂有限公司制备的Cr2O3涂层在零部件的耐磨防腐蚀方面得到了很好的市场应用。
此外,为进一步提高Cr2O3涂层的耐磨防腐蚀性能,可以引入其他耐磨防腐蚀材料构建复合材料。以最常见的Al2O3为例,加入Al2O3硬颗粒后有助于提高耐磨性能。与Cr2O3涂层相比,Cr2O3-Al2O3复合涂层的脆性断裂程度更低,生成的颗粒更细小,有利于摩擦膜的形成[45]。此外,通过制备技术的改进还可进一步提高材料性能。例如,与传统等离子体喷涂制备的Cr2O3涂层相比,采用爆炸喷涂制备的Cr2O3-Al2O3复合涂层因其致密性和无裂纹结构表现出更好的耐磨防腐蚀性能[46]。在产业化应用方面,用爆炸喷涂制备的Cr2O3-Al2O3复合涂层具有替代等离子喷涂Cr2O3涂层的潜在能力,广泛应用于耐磨防腐蚀等严苛环境领域。
2.3 颜料
Cr2O3绿色颜料因其稳定性好、染色强度高、抗迁移能力强、成本低而得到广泛应用。然而,Cr2O3颜料的颜色单一,导致其应用仍有一定的限制。此外,由于传统方法制备Cr2O3颜料会产生有毒的Cr(Ⅵ)和污染性气体,Cr(Ⅲ)化合物前驱体受到广泛关注。LIANG等[6]采用两种不同结构的羟基氧化铬(α-CrOOH 和γ-CrOOH)制备出了不同颜色的纳米Cr2O3,结果表明,采用γ-CrOOH 制备的产物更加均匀,粒径为200~400 nm,呈黄绿色;而采用α-CrOOH 制备的产物粒径为0.3~3 μm,呈棕绿色;此外,通过改变制备过程中两种羟基氧化铬的比例,可以灵活调节产物的颜色,获得明亮的黄绿、蓝绿、绿色和棕绿色等多种颜色。此外,还发现当前驱体中有较多的非凝聚颗粒时,煅烧的Cr2O3颜料具有更好的着色特性[47]。Cr2O3是涂料工业主要的着色颜料,利用分散性好的Cr2O3配制的涂料具备更好的染色强度。XIE等[48]以乙酰丙酮铬为原料制备了一种具有长期分散稳定性的油墨,其在尼龙织物上的印刷图案与绿萝叶的光谱相关系数达到0.904 3,颜色相似度极高。这类与自然植物具有相似颜色的Cr2O3可用于伪装涂料的调制,协助特种作战。例如,洛阳峥洁新材料科技有限公司制备的Cr2O3系颜料就广泛应用于涂料、油墨、特种油漆等,其日产能在吨级以上规模。
物体吸收辐射会导致表面温度升高,给特种装备的使用带来不便。建筑物外墙温度过高会引起室内温度升高,增加夏天空调用电量的负荷。同时,太阳辐射能量的绝大部分集中在可见-近红外区。因此,在特种装备和建筑外墙表面添加可反射此波段光的涂层材料尤为重要。AI 等[49]通过在Cr2O3晶格中掺杂Ti、Co 和Fe 等,成功制备了在400~1 600 nm波长内与绿色植物具有相似光谱的纳米材料,粒径在400 nm 左右。其中,掺杂Ti 可以显著提高Cr2O3的近红外(NIR)反射率,兼具伪装和反射辐射的能力,利于其在特种装备和建筑材料中的应用。但当Ti含量超过一定量时,NIR反射率反而下降,分析可能是导电类型发生变化而带来的NIR 反射率下降[50]。需要指出的是,在实际应用中,要结合应用场景合理控制掺杂元素的浓度和粉末的粒度与分散性,获得最佳综合性能。
2.4 气敏传感器
半导体金属氧化物传感器因其成本低、操作简单、精度高、易于集成和便携等优点,在智能家居、环保、安全生产等领域用于有害气体的实时准确监测。Cr2O3作为一种宽带p 型半导体(Eg=3.4 eV),对部分有害气体具有良好的敏感性,通常与其他金属元素或半导体材料结合用于检测环境中的有害气体。CAO 等[7]分别制备了介孔Cr2O3和Ag/Cr2O3微球,并测量了不同工作温度下Cr2O3和Ag/Cr2O3微球对三乙胺(TEA)的气敏性能。结果显示,在工作温度为170 ℃时,Cr2O3微球对体积分数为5×10-5的TEA 响应值仅为15.2,而工作温度为92 ℃时,Ag/Cr2O3微球的响应值高达52.9。银纳米颗粒的改性不仅大幅降低了最佳工作温度,提高了Cr2O3微球对TEA 气体的响应,而且进一步提高了传感器对TEA 的选择性。Ag/Cr2O3微球对TEA 敏感性的提高可归因于Cr2O3微球的介孔结构及银的敏化和催化作用。TEA的沸点为90 ℃,具有急性毒性,而Ag修饰的Cr2O3微球的最佳温度极为接近TEA 的快速挥发温度,若能进一步降低该器件的最佳工作温度和气体检出限,将为涉及TEA的工业生产提供更加安全的环境。
单一纯相ZnO 对于乙醇等气体的敏感性并不高,与Cr2O3结合可以明显提高其对乙醇等气体的敏感性。WANG 等[51]利用Cr2O3对ZnO 纳米纤维进行修饰得到Cr2O3敏化ZnO纳米复合纤维,其对体积分数为1×10-6的乙醇蒸气的响应值高达3.6,响应时间和恢复时间分别约为1 s 和5 s。此外,也可以通过构建Cr2O3与ZnO、In2O3、SnO2等结合的异质材料来提高对甲醛、乙醇等气体的实时监测速度。例如,Cr2O3/In2O3异质材料对体积分数为2×10-4的乙醇响应值可从纯氧化铟的15.8 提高到30.3,而对体积分数为5×10-4的乙醇响应值可达46.4[52]。进一步,通过添加贵金属元素制备的Au@Cr2O3-In2O3复合材料可在180 ℃对低挥发性有机物浓度表现出明显的气体响应,异戊二烯、乙醇和甲醛的检测浓度可分别降低到5×10-8、2×10-7和2×10-7(体积分数)[53]。此外,与纯SnO2纳米线相比,Cr2O3纳米颗粒锚定的SnO2纳米线对乙醇的响应值可提高4 倍[54]。笔者认为,上述对乙醇具有高敏感性的传感器件可用于生产控制、酒驾检测和车载乙醇检测仪等领域。
2.5 新能源材料
“碳达峰、碳中和”的提出伴随着电动汽车的高速发展和广泛应用,市场对于高能量密度、长续航电动汽车的需求不断加大并持续推动二次电池产业的爆发式增长。Cr2O3因其高比容量(1 058 mA·h/g)和相对较低的工作电位(1.085 V)被认为是具有潜力的负极材料[55]。然而,单一纯相Cr2O3难以满足实际应用需求,需要与其他材料复合以改善综合性能。以最常见的碳基材料为例,利用蔗糖为碳源制备的Cr2O3@C 复合材料在300 次循环后的比容量仍有542 mA·h/g,明显高于Cr2O3[8]。此外,KHAMLICH等[56]在Ni基底与Cr2O3薄膜之间引入石墨烯层(FLG)构筑了Cr2O3/FLG/Ni 复合材料,结果显示,得益于石墨烯优异的导电性能和多组分材料的协同效应,复合材料的首次放电比容量提高至1 234.5 mA·h/g,100 次循环后仍保持在692.2 mA·h/g,远高于Cr2O3/Ni。除了与碳基材料复合之外,也可以与非碳基材料复合来提高材料的综合性能。例如,WANG 等[57]利用金属有机框架构建了Cr2O3@TiO2八面体核壳结构,该特殊结构有利于Li+的扩散并抑制充放电过程中的体积膨胀。要指出的是,尽管Cr2O3基复合材料的比容量远高于商业石墨,但其首次库伦效率较低(小于80%),需要改善后才能应用到全电池中。
近年来,钠离子电池因具有更低的成本优势成为储能体系的研究热点。Cr2O3不仅能作为锂离子电池的负极材料,还可以用作钠离子电池正极材料的关键原料。LUO 等[58]以商业碳酸钠和Cr2O3为原料制备了纯相O3 型NaCrO2,其首次放电比容量可达115 mA·h/g;材料在2.0~3.6 V时经50次循环后仍保持91%的比容量;虽然O3 型NaCrO2具有出色的性能,但由于Cr 迁移到Na 层的不可逆相变,每mol NaCrO2中只有大约0.5 mol Na+可以使用,限制了容量的释放,因此,增加O3型NaCrO2中可逆Na+的含量极为重要。前人研究表明,向NaCrO2中掺杂其他过渡金属元素能有效抑制钠脱出过程中Cr3+的迁移。XI等[59]通过掺入金属Ru得到Na0.88Cr0.88Ru0.12O2,材料在2.0~3.8 V 时可提供156 mA·h/g 的可逆容量。此外,KO 等[60]发 现引 入Sb5+得到的O3 型Na0.72Cr0.86Sb0.14O2即使充电到4.1 V 时,Cr3+的迁移也能得到抑制,材料的首次放电比容量可达175 mA·h/g(对应0.72 mol Na+的嵌入/脱出)。在应用方面,层状结构的O3 型NaCrO2具有较好的电化学活性,将助力其在低成本储能领域的应用。与此同时,钠离子电池的发展或将带动高纯(纳米)Cr2O3需求量的增长,以此推动材料制备方法的迭代和创新。
除作为锂/钠离子电池关键材料外,Cr2O3还可用于光伏发电领域。太阳能作为一种无限供应且易于获取的可再生能源,如何高效收集太阳能并将其转化为可直接利用的能源形式是多年来的研究热点。DONG 等[61]将Cr2O3插入TiO2与钙钛矿界面之间,将电池功率转化效率从17.10%提高到18.51%,这可归因于Cr2O3层对于电子反向运输的阻碍作用以及其避免了钙钛矿与底面电极的直接接触,减少了电流泄露和载流子复合。
目前,从能源资源角度看,全球经济发展逐渐从资源依赖向技术依赖转变。构建以新能源为主体的新型电力系统,广泛开发和使用太阳能、风能、水能等可再生能源作为发电系统的动力源,将是未来优化布局推动新能源可持续发展的重要方向。在这种背景下,纳米Cr2O3在新能源领域展现出较好的应用潜力,尤其是在钠离子二次电池储能领域,将Cr2O3钠化合成的O3型NaCrO2系列正极材料具有良好的发展机遇。
3 总结及展望
本文总结了纳米Cr2O3的制备方法,主要包括气相法、湿化学法和固相法三大类。得益于独特的沉积过程,气相法可制备纯度高、分散均匀的材料,且制备过程可控性好,但该方法对设备的要求苛刻、大规模生产成本高,主要用于制备薄膜和涂层等领域。湿化学法具有设备简单、易于实现批量化生产等优点。其中,沉淀法和溶胶-凝胶法是目前企业使用的主流方法。此外,在模板剂的辅助下还能够构筑如纳米线、纳米棒等特殊的纳米结构。基于水热/溶剂热法合成的纳米Cr2O3纯度高、晶粒发育好,可以有效避免杂质和结构缺陷。相比之下,固相法虽然操作简单、适合批量制备,但得到的纳米颗粒的纯度低、颗粒均匀性不好、品质相对较差、难以直接使用。笔者认为,从宏量制备的角度出发,将湿化学法与固相法有机结合是实现规模化制备高稳定纳米Cr2O3的有效路径,可以发展为高效实用的技术。
此外,纳米Cr2O3因其优异的物理化学性能和机械稳定性而被应用于多种场景。首先,作为催化剂,表面Cr(Ⅵ)含量是衡量Cr2O3催化活性的重要标准,大的比表面积对于提高Cr2O3的催化活性至关重要,且在掺入Pt等元素后还能进一步提高其催化性能。在耐磨防腐蚀等领域,为了进一步提高Cr2O3涂层的综合性能,通常引入其他材料(如Al2O3等)构建复合材料。而作为颜料用Cr2O3,通过改变合成原料或方法及掺杂其他材料或金属元素,可以获得颜色不同且具有特殊性质的绿色系颜料。其次,作为一种宽带隙p 型半导体,Cr2O3对某些有害气体具有良好的敏感性,与其他金属氧化物(如ZnO、In2O3等)结合后则表现出更好的气体检测特性。最后,Cr2O3因其较高的比容量和良好的光学特性,可应用于新能源材料领域。特别是随着碳达峰、碳中和成为全球共识和全球储能产业的爆发式增长,有望催生纳米Cr2O3作为功能材料在新能源领域的市场需求。
