肺炎支原体感染致视神经炎为突出表现的儿童髓鞘少突胶质细胞糖蛋白抗体相关疾病1 例报告
2023-10-18杜非凡贾艳红徐梅先
郭 芳 康 磊 杜非凡 贾艳红 徐梅先
河北省儿童医院1.感染科,2.重症医学科,3.眼科(河北石家庄 050031)
肺炎支原体(Mycoplasma pneumoniae,MP)是儿童社区获得性肺炎主要病原之一[1],可引起心血管、消化、皮肤、神经和血液等肺外系统表现[2],但与MP感染相关的视神经炎(optic neuritis,ON)很少被描述,并且大多数情况下,它合并了神经系统其他并发症,如急性播散性脑脊髓炎(acute disseminated encephalomyelitis,ADEM)、脑膜炎、脑膜脑炎和周围神经病变。目前临床对MP 相关性视神经炎(Mycoplasma pneumoniaeassociated with optic neuritis,MP-ON)这一罕见并发症认识不足。本文回顾分析1例MP感染后以ON为主要表现的患儿的临床资料,同时检索国内外文献报道的MP-ON患儿的病例资料,探讨其临床特点、诊治及预后。
1 临床资料
患儿,女,10岁,因间断发热伴头痛半月于2022年2月6日收入院。入院前半月无明显诱因出现发热,最高体温38.0℃,热峰2次/d,伴头痛,双颞部为主,性质不详,无咳嗽流涕,无寒颤抽搐。入院前12天出现呕吐,为胃内容物,非喷射性,不含咖啡色及胆汁样物质,给予头孢唑肟钠(50 mg/kg,bid)静滴9天。入院前5天呕吐缓解,体温正常2天后再次出现发热,波动在38~38.5 ℃,仍伴头痛,部位同前,热退后头痛缓解。入院前1天左眼出现一过性视物模糊,持续2~3 min自行恢复正常。门诊查头颅CT平扫未见异常,左视神经局部密度稍高。患儿既往体健,生长发育正常,否认自身免疫性疾病、血液系统疾病、恶性肿瘤及遗传性视神经病变史及家族史,否认毒物服用史,否认传染病史,否认手术外伤史。体格检查未见异常阳性体征。
入院实验室检查:血常规中白细胞14.5×109/L,中性粒细胞69.9%,血红蛋白148 g/L,血小板209×109/L,C-反应蛋白4.60 mg/L;电解质、免疫球蛋白、血沉、肝肾功能、心肌酶、降钙素原、铁蛋白无异常;凝血酶原时间、活化部分凝血活酶时间、纤维蛋白原含量、凝血酶时间和D-二聚体无异常;抗核糖体P蛋白抗体、抗Ro52KD抗体、抗RNP/Sm抗体、抗SCL-70 抗体、抗JO-1 抗体、抗着丝点蛋白B抗体、抗核小体抗体、抗组蛋白抗体、抗ds-DNA 抗体、抗Smith抗体、抗SS-A抗体、抗SSB抗体及抗核抗体均阴性;血EBV、CMV 抗体及PCR 均阴性,血培养未见细菌生长,类风湿因子、ASO、肥达反应、外斐反应、PPD、T-SPOT、布氏杆菌病抗体及G、GM试验均阴性。胸部CT、心脏彩超、眼眶MRI 均未见异常。MP 抗体>1:1 280(颗粒凝集法,IgM 与IgG混合)。
考虑患儿存在MP感染,入院第2天给予阿奇霉素静滴(10 mg/kg,qd),疗程7天,入院第4天热退,无头痛发作。第7 天突发双眼视物不清,右眼为著,伴眼球转动痛,无眼脸下垂、眼球活动障碍及眼球震颤,无其他神经受累表现。查右眼视力0.08,左眼0.4,双眼眼压均为15 mmHg,双侧视乳头水肿;散瞳后眼底照相示双眼视盘边界欠清,黄斑中心凹反光可见,视网膜血管走形可,网膜未见出血及渗出(图1A);眼底光学相干断层扫描技术(OCT)示双眼视盘周围神经纤维层增厚,双眼黄斑区结构未见异常(图1B、1C);视觉诱发电位(VEP)示双眼部分P波潜时延长,振幅低平;视野检查示双眼视野缺损,考虑并发ON。考虑到儿童ON有合并及发展为ADEM的风险[3],行腰椎穿刺术,脑脊液无色透明,压力170 mmH2O,白细胞62×106/L、单核细胞47×106、多核细胞15×106/L,蛋白0.51 g/L,脑脊液墨汁、抗酸染色阴性,脑脊液MP、疱疹病毒Ⅰ/Ⅱ、EB 病毒PCR 均阴性。头颅MRI示多发异常信号;脊髓MRI示存在长节段脊髓内异常信号(颈6 至胸4),结合临床考虑中枢神经系统脱髓鞘病变(图2)。血清水通道蛋白4抗体(aquaporin 4 antibody,AQP4-Ab)阴性,细胞法(cell-based assay,CBA)检测血髓鞘少突胶质细胞糖蛋白抗体(myelin oligodendrocyte glycoprotein-antibody,MOG-Ab)滴度1:32。
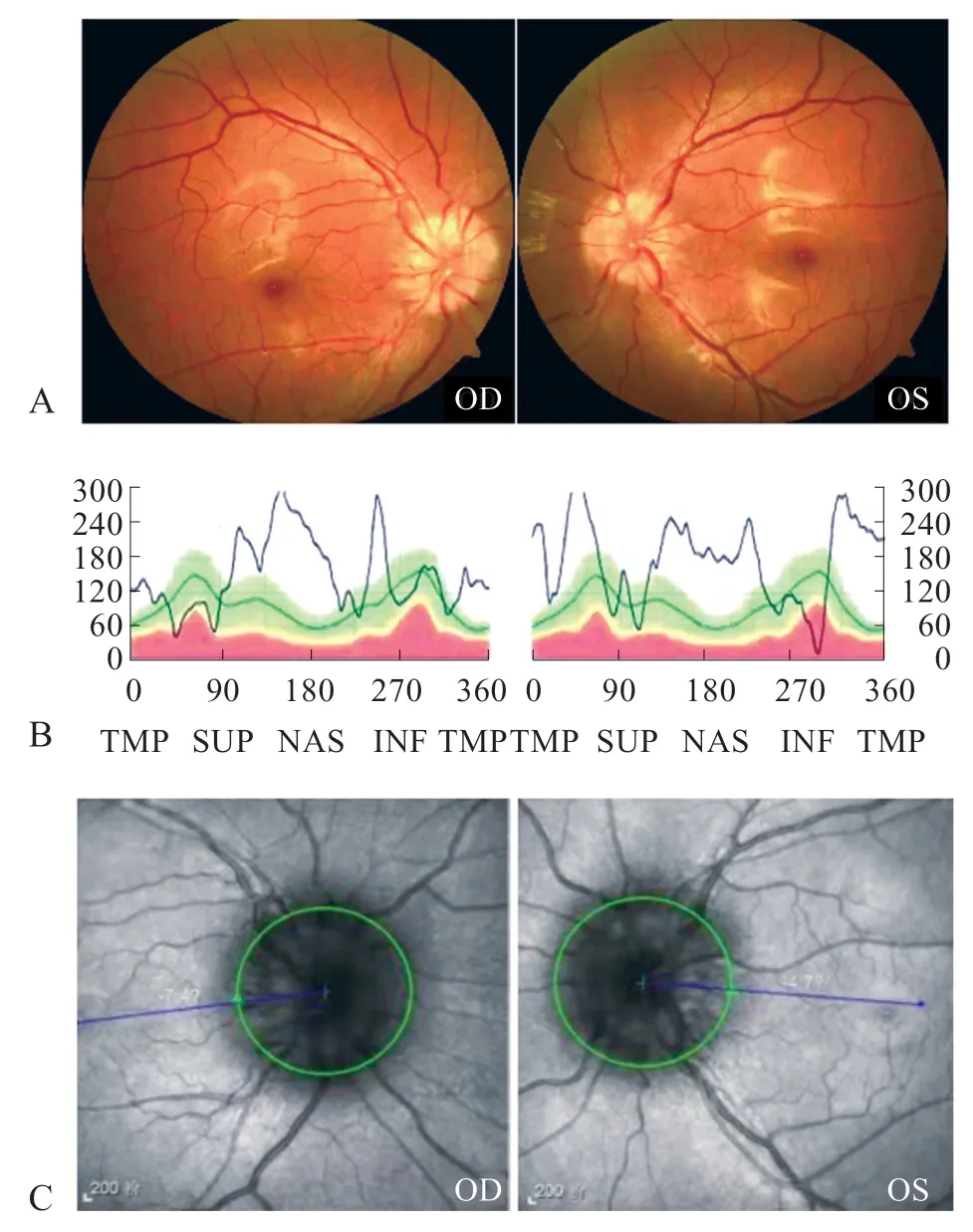
图1 患儿OCT表现
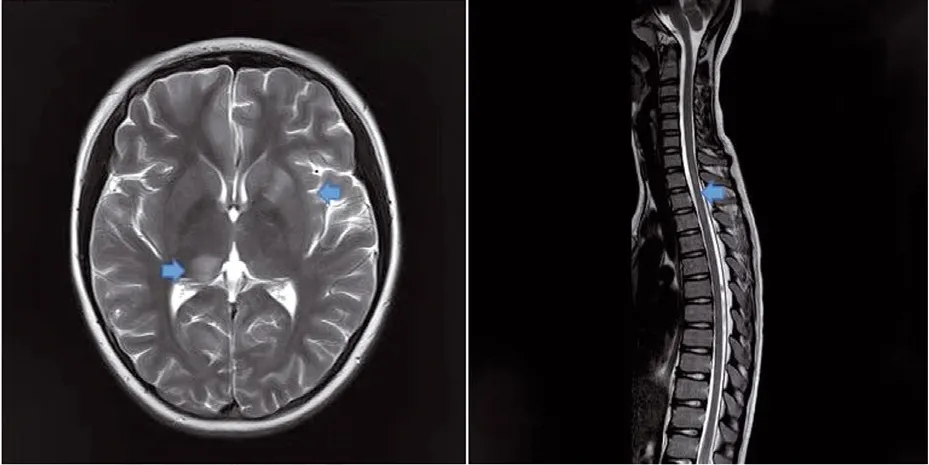
图2 患儿MRI表现
患儿有明确的ON表现,但整个病程中无意识、运动、感觉和其他颅神经受损症状及体征,病理反射阴性,不满足2012版国际儿童多发性硬化研究小组提出的ADEM 标准[4],而ON 又不能解释脑脊液及核磁共振异常结果,因此最终修正诊断为①MOG抗体相关性疾病;②MP感染。按照指南建议[5],予静脉注射甲基泼尼松龙琥珀酸钠20 mg/(kg·d),3 天后序贯减量;治疗1 周后患儿视力恢复到发病前水平,2周后复查头颅及脊髓MRI示异常信号消失,血MOG抗体阴性,遂改为口服醋酸泼尼松1 mg/(kg·d)维持治疗2周。出院后随访3个月至5月6日未再复发。
患儿诊治经过时间轴见图3。
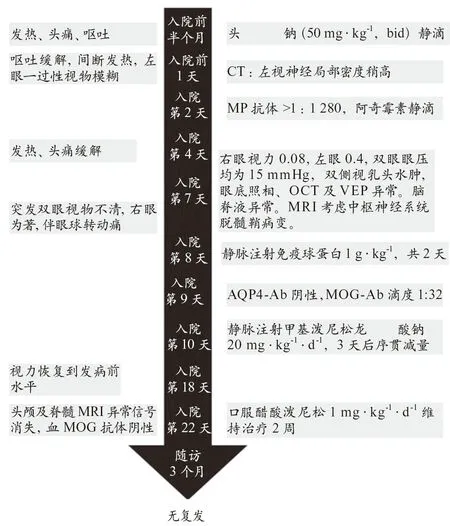
图3 患儿诊治经过时间轴
2 讨论
MOG 抗体相关疾病 (myelin oligodendrocyte glycoprotein associated disorders,MOGAD) 是儿童中最常见的神经炎症性疾病[6],典型表现包括ADEM、ON 和脊髓炎。MP 感染后MOGAD 的报道并不多见。Bonagiri 等[7]报道了1 例MP 感染后MOG 相关ADEM,但目前尚无MP 感染后ON 为主要表现的MOGAD报道。
分别以“儿童”、“肺炎支原体”和“视神经炎”以及“children”、“Mycoplasma pneumoniae”和“optic neuritis”为关键词,检索出中国知网、万方数据知识服务平台、PubMed数据库相关文献6篇[3,8-12],9例MP-ON,加本例共10例患儿。其中男、女各5例,平均发病年龄10.5(7~16)岁。5例有明确的头痛表现,从前驱感染到视力下降的平均时间间隔12.2 d(4例未提及),7例为双侧受累,6例视力低于0.1。7例有单侧或双侧视盘水肿(2例未提及),3例出现全身神经系统表现(脑膜炎、脑炎、播散性脑脊髓炎),4 例MRI 结果与ADEM 一致。5 例给予大环内酯类抗生素治疗,8 例予类固醇激素治疗,2 例予人免疫球蛋白治疗,10 例最终视力均恢复至发病前水平,随访者共4例均未复发。
儿童感染MP后可出现肺内、肺外等多种表现,且肺外并发症可作为MP感染的独立表现。据报道,5%~10%的急性发热性中枢神经系统疾病患者存在MP感染[13]。ON是既往健康儿童感染MP后的罕见表现,其临床特征为[14]:①急性视力下降,伴或不伴眼球转动痛及视乳头水肿;②至少合并以下2项异常——相对性瞳孔传入阻滞(双侧对称性视功能损伤时可缺乏本体征)、视野缺损、视觉诱发电位异常和色觉障碍;③排除缺血性、外伤性、压迫及浸润性、中毒性、营养代谢性及遗传性视神经病变等。本例患儿病程第16 天有一过性视力下降,病程第23 天突发持续性视力急性下降和视野缺损,而在病程前20 天存在顽固性头痛。Asseyer 等[15]发现49.6%的MOG相关ON患者存在1次及以上的头痛发作,其原因可能涉及视神经周围的脑膜和神经纤维损伤。因此在临床中对于持续存在的头痛,除了与偏头痛、占位性及血管性疾病鉴别外,还要警惕其可能作为免疫介导的ON 的前驱表现,应排查眼部病因并关注其潜在的与视神经相关的自身免疫性疾病。
关于MP 引起ON 的发病机制主要集中在MP直接侵袭和自身免疫介导两方面。Rappoport 等[3]认为,MP感染后延迟出现神经系统症状、40%患儿合并有ADEM表现以及类固醇治疗后ON快速恢复提示自身免疫或免疫复合物形成的脱髓鞘改变可能是MP相关ON的潜在机制。视神经的炎性脱髓鞘病变是引起ON最常见的病因之一[16],根据AQP4-Ab和MOG-Ab进行临床亚型分类。本例患儿是首例发现MP 感染后MOG 阳性的ON 患者,支持MP 引起的免疫介导的中枢脱髓鞘机制,患儿在感染MP 3周后出现ON表现,与文献报道的新冠病毒与MOGAD之间时间跨度一致[17]。当MP入侵机体后,一方面,通过细胞黏附与分子模拟等一系列作用[18-19],释放毒性物质,改变细胞抗原结构,刺激B细胞产生抗体;另一方面,破坏宿主血脑屏障,使MOG抗原漏入外周,激活CD4+T淋巴细胞,对MOG特异性B淋巴细胞募集活动增加,产生大量MOG-IgG,同时促炎T淋巴细胞进入中枢神经系统,募集MOG特异性B淋巴细胞产生相应抗体,产生包括ON 在内的各种神经系统疾病[20-21]。
目前MP-ON 的治疗主要包括全身应用大环内酯类药物和大剂量类固醇药物,对视力严重下降的患儿疗效显著[12],但对于合并ADEM 或激素耐药的脱髓鞘ON 可给予人免疫球蛋白和血浆置换治疗[22]。本患儿静滴阿奇霉素后感染症状迅速缓解,虽未达到ADEM诊断标准,但根据其脑脊液及头颅脊髓MRI异常的检查结果,后期给予大剂量甲基泼尼松龙联合免疫球蛋白静滴,1 周后视力好转,2 周后血MOG 抗体转阴,改为泼尼松口服维持。MOG阳性的ON 患者通常有复发倾向,且复发风险与血MOG-IgG 持续阳性相关[23],因此对MP 继发MOG相关的有ON表现的患者用药期间应监测血MOG抗体,定期复查,避免复发。
总之,MP 感染后急性视力下降需警惕儿童ON,其多与免疫介导的脱髓鞘病变有关,临床中应重视顽固性头痛这一具有提示意义的前驱症状,诊疗过程中完善并动态监测中枢脱髓鞘抗体可有助分型、指导治疗和避免复发。对于合并ADEM 或激素耐药的脱髓鞘ON,除积极给予大环内酯类及大剂量类固醇药物外,还可给予人免疫球蛋白和血浆置换治疗。
