黄铁矿与毒砂氧化行为差异的电极过程动力学研究
2023-10-13李新春焦芬覃文庆崔艳芳李佳磊
李新春,焦芬,覃文庆,崔艳芳,李佳磊
(1. 中南大学 资源加工与生物工程学院,湖南 长沙,410083;2. 中南大学 战略含钙矿物资源清洁高效利用湖南省重点实验室,湖南 长沙,410083)
毒砂在我国的储量非常丰富,常与方铅矿、闪锌矿和黄铁矿等金属硫化物伴生[1-3]。将伴生在一起的黄铁矿与毒砂进行浮选分离时,硫精矿中的砷含量将会严重影响硫精矿的价格,此外,当硫精矿中的砷含量过高时,在后续的冶炼与制酸工艺中产生的砷化氢和砷酸盐[4-5]等物质会污染环境,同时处理含砷冶炼废气的成本也会增高[6-9]。近年来,随着国家对环境问题的日益重视,提出了绿色矿山、环境友好型矿山等先进的发展理念,从各种金属中将伴生的砷矿物高效、绿色分离显得尤为重要。黄铁矿与毒砂是自然界伴生关系非常密切的2 种金属,黄铁矿与毒砂的热力学性质、成矿条件都非常相似[10],毒砂表面存在着[FeS]和[AsS]这两种化学键,其中[FeS]与黄铁矿表面的[FeS]的结构非常相似,在外界作用下,黄铁矿表面的[FeS]键断裂时,毒砂表面的[FeS]键也会断裂。因此,在浮选过程中很难单独利用两者的热力学性质的差异将两者分离。在分离黄铁矿与毒砂的过程中除了利用两者的热力学性质的差异外,还应充分利用动力学性质的差异。反应动力学因素的影响主要表现在以下2个方面:硫化矿物之间存在不同的氧化速度[11];硫化矿物在特定条件下的氧化反应和氧化产物由电极过程动力学因素决定。毒砂与黄铁矿浮选过程的电极过程动力学对于两者的浮选分离有重要影响,因此,本文采用动电位扫描、循环伏安和恒电位阶跃等电化学测试方法,测定了黄铁矿与毒砂在特定pH条件下的腐蚀电位、腐蚀电流、氧化起始电位和氧化峰电流等电极过程动力学参数,并且建立了黄铁矿与毒砂氧化的动力学方程,明确了两者在动力学行为的差异,对与通过电位控制浮选技术将黄铁矿与毒砂的分离具有重要意义。
1 试验材料与装置
1.1 试剂与电极
黄铁矿来自湖北十堰,毒砂来自内蒙古赤峰市,首先采用XRD和XRF测试对黄铁矿与毒砂纯矿物样品进行分析,结果分别如图1 和表1 所示。从图1可见,黄铁矿和毒砂样品中没有出现明显的杂质峰,结晶较好。由表1可见,黄铁矿与毒砂纯矿物的纯度分别为98.68%和96.82%。

表1 纯矿物化学多元素分析(质量分数)Table 1 Chemical multi-element analysis of pure minerals%
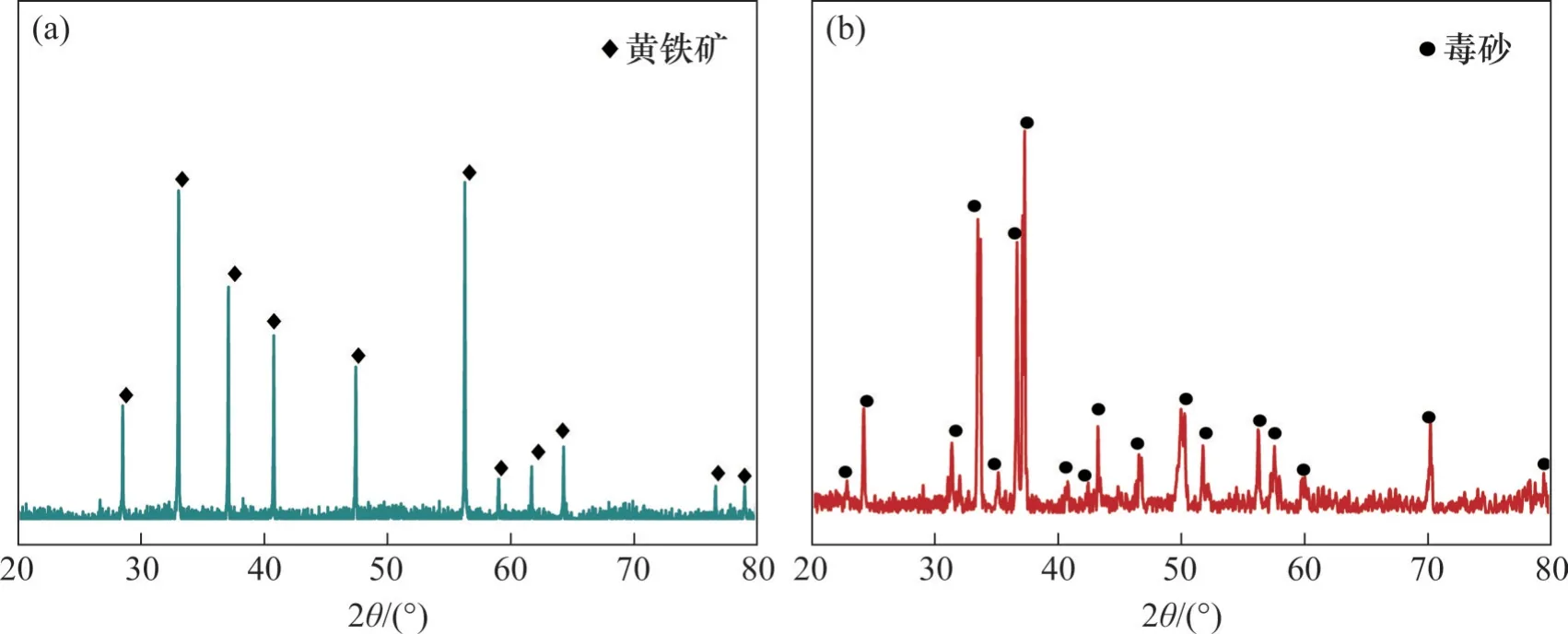
图1 黄铁矿与毒砂纯矿样的XRD图谱Fig. 1 XRD patterns of pyrite and arsenopyrite
电化学试验采用三电极体系,其中矿物电极作工作电极、碳棒电极作对电极,在酸性条件下,Ag/AgCl作参比电极,碱性条件下,甘汞电极作参比电极。制作矿物电极时,首先挑选结晶良好的FeS2和FeAsS,用切割机切成面积为1 cm2、厚度为3 mm左右的圆片,然后再将切好的圆柱状矿物电极依次用粒度为15.0、5.0 和2.6 μm 的砂纸打磨至表面光滑。
试验所用溶液为0.1 mol/L KNO3溶液,分别用邻苯二甲酸氢钾、混合磷酸盐、十四水硼酸钠和NaOH 将溶液pH 调至4.0、6.86、9.18 和11,试验中所用试剂均为分析纯。
1.2 试验方法
1.2.1 循环伏安测试
电化学测试试验在美国Gamry 电化学公司Interface多通道电化学工作站上进行,采用Gamry Framework 软件进行黄铁矿和毒砂的循环伏安测试。进行循环伏安测试时,由开路电位扫描至阳极电位上限,再扫描至阴极电位下限,电位扫描区间为-800~800 mV,扫描速率为20 mV/s,每次测试完毕后,需要将矿物电极的氧化面依次用粒度为15.0、5.0 和2.6 μm 的砂纸进行打磨,打磨完毕后用去离子水反复冲洗表面后方可进行下一次测试。
1.2.2 Tafel极化曲线测试
采用Gamry Framework 软件进行不同pH 条件下黄铁矿和毒砂的Tafel 极化曲线测试。进行Tafel极化曲线测试时,从阴极向阳极在相对于开路电位±250 mV 的电位区间进行扫描,扫描速率为1 mV/s,通过Tafel极化曲线获得黄铁矿在不同pH条件下的腐蚀电位Ecorr、Tafel 斜率(βa,βc)和腐蚀电流密度Icorr等电化学参数。
1.2.3 恒电位阶跃测试
电势阶跃法[12]通过向电极施加一个恒定的电位,记录电流随时间变化曲线,然后根据该曲线建立电极的氧化动力学方程,并求得其动力学参数。采用Gamry Framework软件进行黄铁矿和毒砂的恒电位阶跃测试。进行恒电位阶跃测试时,分别对矿物施加偏离平衡电位0.10、0.15、0.20、0.25 V 的恒定电位,记录在pH=11、0.1 mol/L KNO3溶液中电流随时间的变化曲线。
1.2.4 X射线光电子能谱测试
采用K-Alpha+型X射线光电子能谱仪(XPS)对氧化前后黄铁矿和毒砂表面进行分析。测试时,选取高纯度的块状黄铁矿和毒砂样品,首先将黄铁矿与毒砂样品用粒度为15.0、5.0 和2.6 μm 的砂纸进行打磨,打磨完毕后再用去离子水反复冲洗并擦干,然后在真空低温条件下保存;测量氧化后黄铁矿与毒砂的XPS 图谱时,需先将黄铁矿与毒砂电极置于0.6 V(相对于参比电极)的外加电位条件下,氧化2 h,氧化完毕后再用去离子水反复冲洗并轻轻擦干,然后在真空低温条件下保存,对氧化前后的矿物样品进行XPS测试。
2 试验结果与讨论
2.1 黄铁矿与毒砂的循环伏安曲线
在pH=11条件下0.1 mol/L KNO3溶液中黄铁矿与毒砂的循环伏安曲线如图2 所示。由图2 可见,黄铁矿的循环伏安曲线中出现了a1、a2和a3三个氧化峰,分别对应如下反应[13-16]:
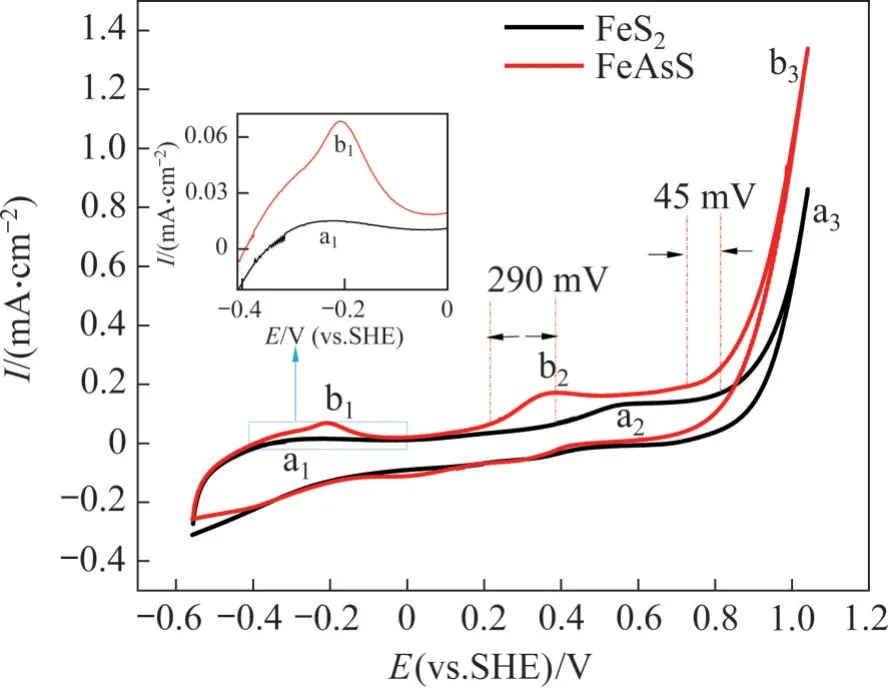
图2 pH=11条件下0.1 mol/L KNO3溶液中黄铁矿与毒砂的循环伏安曲线Fig. 2 Cyclic voltammetric curves of pyrite and arsenopyrite in 0.1 mol/L KNO3 solution at pH=11
随扫描电位增加,HS-首先在黄铁矿表面氧化生成单质S0,使黄铁矿表面产生钝化,黄铁矿的氧化电流降低;继续增加扫描电位,在410 mV左右出现黄铁矿氧化生成Fe(OH)3和S0的氧化峰,Fe(OH)3和S0在黄铁矿表面的积累使得黄铁矿钝化产生了较大的电阻,黄铁矿的氧化电流降低;随扫描电位的继续增加,在821 mV左右出现黄铁矿表面完全氧化生成SO24-的氧化峰,氧化电流迅速增加。
毒砂的循环伏安曲线中出现了b1、b2和b3三个氧化峰,分别对应反应(1)、反应(4)和(5)[17-19]:
毒砂的氧化过程与黄铁矿的相似,随扫描电位增加,HS-首先在毒砂表面氧化生成单质S0,在120 mV 左右毒砂自身氧化生成S0和Fe(OH)3,在775 mV 左右毒砂氧化生成SO24-。与黄铁矿相比,毒砂开始氧化电位较低,且毒砂的氧化峰电流均高于黄铁矿的氧化峰电流,表明在pH=11 的条件下毒砂更容易被氧化,且氧化速度更快。
毒砂与黄铁矿的表面氧化产物中均有Fe(OH)3、SO24-和S0等物质生成,这些物质在毒砂与黄铁矿的浮选过程中会影响黄铁矿与毒砂表面的亲水疏水性,因此可以利用黄铁矿与毒砂表面氧化速率的差异强化黄铁矿与毒砂表面亲水疏水性的差异,从而进一步强化两者的浮选分离。
2.2 黄铁矿与毒砂的Tafel极化曲线
Tafel 极化曲线是从腐蚀电化学的角度研究矿物在不同体系中发生氧化还原的电化学动力学特性,通过Tafel测试可以得到一系列的动力学参数,其中比较重要的是腐蚀电位和腐蚀电流密度,腐蚀电位可以反映矿物腐蚀的难易程度,腐蚀电流密度则可以反映矿物腐蚀速率[13]。图3所示为在不同pH 条件下0.1 mol/L KNO3溶液中黄铁矿的Tafel极化曲线,Tafel极化曲线拟合结果见表2。

表2 不同pH条件下0.1 mol/L KNO3溶液中黄铁矿的Tafel参数Table 2 Tafel parameters of pyrite in 0.1 mol/l KNO3 solution under different pH conditions
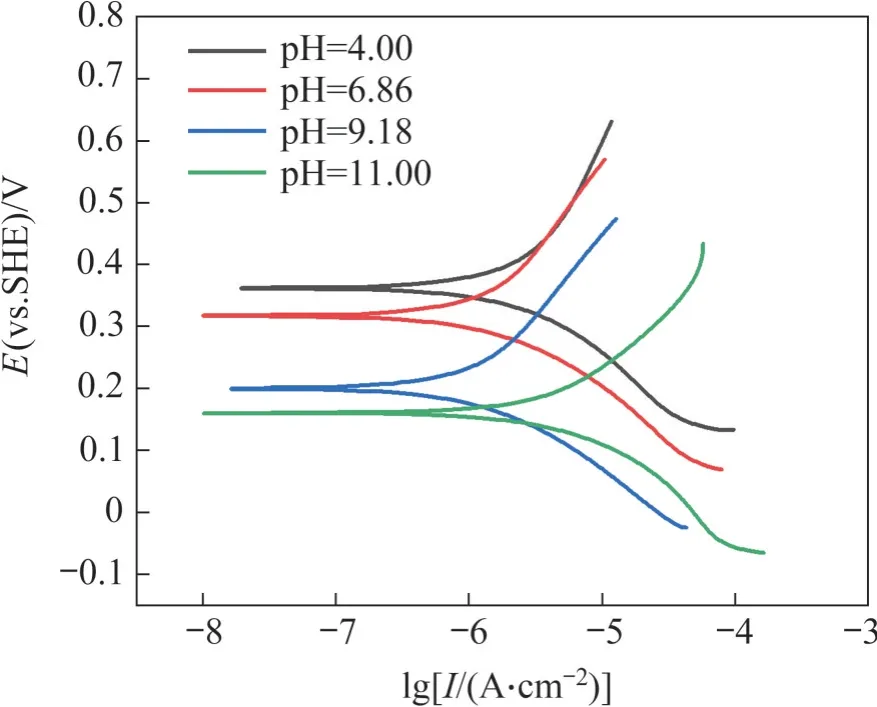
图3 不同pH下0.1 mol/L KNO3溶液中黄铁矿的Tafel极化曲线Fig. 3 Tafel polarization curve of pyrite in 0.1 mol/L KNO3 solution under different pH conditions
由表2可知,在pH为4,6.86,9.18和12时,黄铁矿的腐蚀电位分别为362、318、202 和162 mV,黄铁矿的腐蚀电位随着溶液pH 升高而降低,且Tafel 极化曲线的阳极斜率βa随pH 升高而逐渐降低,与黄铁矿的腐蚀电位变化规律相一致,表明黄铁矿在pH高的溶液中更容易被腐蚀;黄铁矿的腐蚀电流密度随pH增加而先降低后升高,表明黄铁矿在强酸强碱条件下的氧化速率更快。
不同pH 条件下毒砂的Tafel极化曲线如图4 所示,其Tafel 极化曲线拟合结果见表3。可见,当pH为4,6.86,9.18和12时,毒砂的腐蚀电位分别为334、268、146 和79 mV,随着pH 升高,毒砂的腐蚀电位逐渐降低,且毒砂的阳极斜率也逐渐变小,这表明毒砂在较在高pH条件下更容易被腐蚀,此外,毒砂的腐蚀电流密度随pH增加而先降低后增加,表明在强酸强碱条件下,毒砂的腐蚀速率更快。
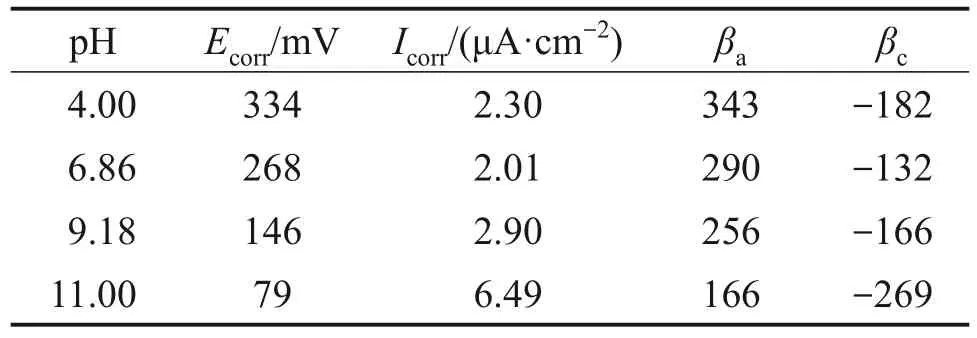
表3 不同pH条件下0.1 mol/L KNO3溶液中毒砂的Tafel参数Table 3 Tafel parameters of arsenopyrite in 0.1 mol/L KNO3 solution under different pH conditions
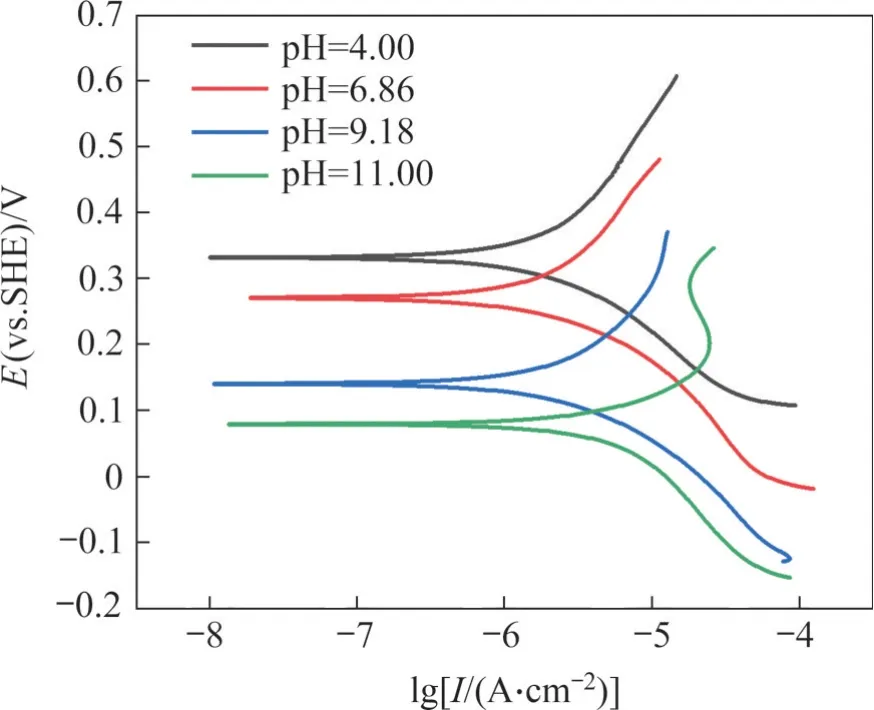
图4 不同pH条件下0.1 mol/L KNO3溶液中毒砂的Tafel极化曲线Fig. 4 Tafel polarization curve of arsenopyrite in 0.1 mol/L KNO3 solution under different pH condition
随着pH 升高,黄铁矿与毒砂腐蚀电位的差值逐渐增大,表明在相同pH条件下毒砂比黄铁矿更容易氧化,且在相同pH条件下黄铁矿的腐蚀速率与毒砂的腐蚀速率存在显著差异,可以考虑通过调整溶液的pH去强化黄铁矿与毒砂氧化速率的差异,改变黄铁矿与毒砂表面氧化产物的含量,从而强化黄铁矿与毒砂的浮选分离。
2.3 黄铁矿与毒砂的动力学方程
恒电位阶跃通常用来研究电极过程的动力学,当电极偏离平衡电位后,黄铁矿电极可能发生以下反应:
反应式(6)的过电位与反应电流的关系可以通过下式确定:
式中:η为反应的过电位;T为反应温度;i0为交换电流密度;it→0为某一个电位下完全无浓差极化的电流密度;t为反应时间;β为反应的传递系数;F为法拉第常数;n为反应的电子数。
图5(a)所示为黄铁矿电极在不同电位下的恒电位阶跃曲线。在图5(a)中选取适当的时间范围,利用i-t-0.5关系可求出黄铁矿在0.10、0.15、0.20和0.25 V 下的it→0分别为36.4、61.8、112.2 和130.6 μA/cm2。用所求出的不同电位下的it→0作η-logit→0曲线,在pH=11 时黄铁矿过电位η与logit→0的关系如图5(b)所示。根据图5(b)可求出黄铁矿电极在pH=11 体系中的氧化动力学方程为η=0.209 logit→0+1.140,其中,i0=3.71 μA/cm2。

图5 pH=11条件下0.1 mol/L KNO3溶液中黄铁矿的恒电位阶跃曲线及电极过电位η与logit→0的关系Fig. 5 Constant potential step curve and relationship between overpotential η and logit→0 of pyrite in 0.1 mol/L KNO3 solution at pH=11
毒砂在pH=11、0.1 mol/L KNO3溶液中有可能发生以下反应:
毒砂在pH=11、0.1 mol/L KNO3溶液中的恒电位阶跃曲线如图6(a)所示。同理可求出毒砂在0.10、0.15、0.20、0.25 V 下的it→0分别为41.1、82.9、106.3、117.4 μA/cm2。毒砂的电极过电位η与logit→0的关系如图6(b)所示。由图6(b)可求出毒砂电极在pH=11 体系中的氧化动力学方程为η=0.282 logit→0+1.463,计算得到i0=6.48 μA/cm2,与Tafel曲线求得的i0=6.49 μA/cm2结果相近。
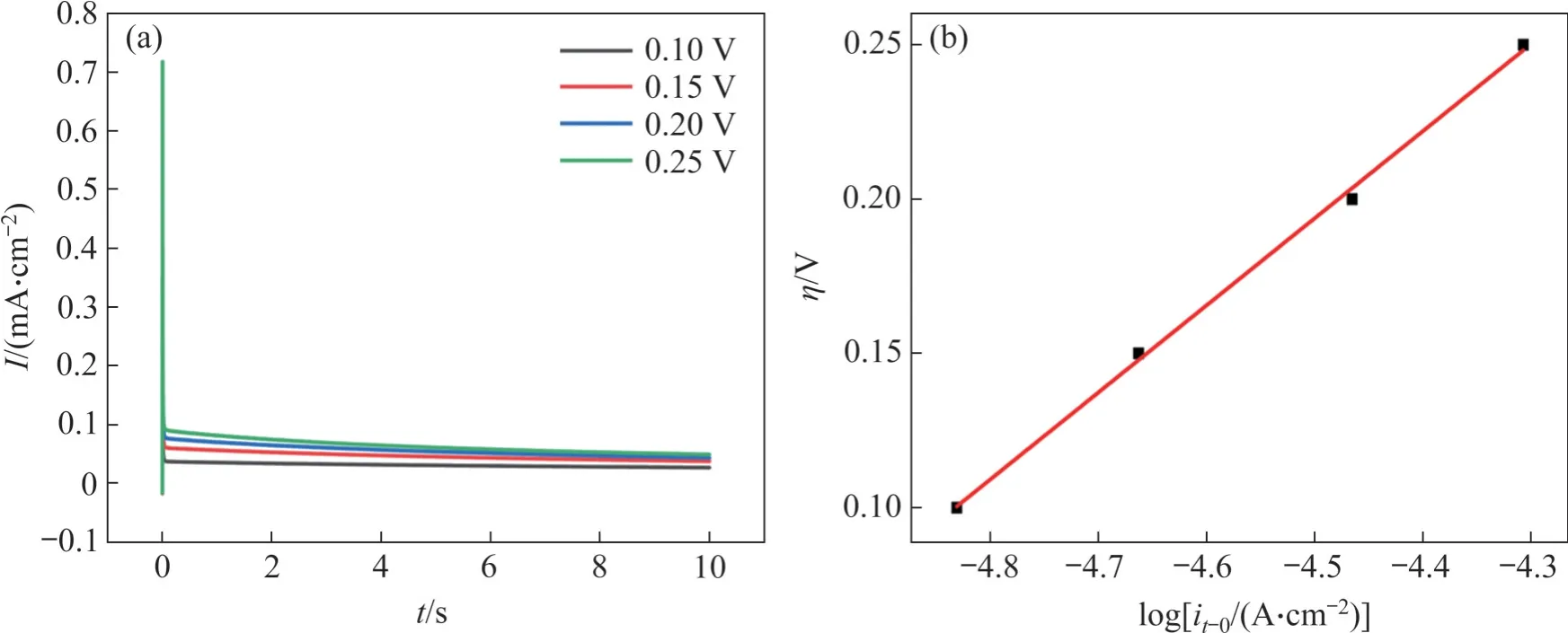
图6 pH=11条件下0.1 mol/L KNO3溶液中毒砂的恒电位阶跃曲线及电极过电位η与logit→0的关系Fig. 6 Constant potential step curve and relationship between overpotential η and logit→0 of arsenopyrite in 0.1 mol/L KNO3 solution at pH=11
从图5和图6可知,在pH=11、浓度为0.1 mol/L KNO3溶液中,黄铁矿与毒砂的完全无浓差极化条件下的电流分别为3.8 μA/cm2和6.18 μA/cm2,其中,毒砂的腐蚀电流大于黄铁矿的腐蚀电流,说明毒砂的氧化速度要大于黄铁矿的氧化速度,这与Tafel极化曲线所得到结论相一致。
2.4 黄铁矿与毒砂表面氧化研究
黄铁矿和毒砂表面氧化前后S 2p XPS 分析拟合结果如图7所示,黄铁矿与毒砂氧化前后不同价态S元素的含量分布见表4。黄铁矿XPS图谱中的S 2p峰[20]分别用S2-(161.79 eV)、S22-(162.51 eV)、S2n-(164.55 eV)和SO24-(168.55 eV)进行分峰拟合,毒砂XPS图谱中的S 2p峰[21-22]分别用S2-(161.47 eV)、S22-(162.3 eV)、S2n-(163.59 eV)和SO24-(168.21 eV)进行分峰拟合。

表4 黄铁矿与毒砂氧化前后不同价态S元素的含量(质量分数)Table 4 Contents of different valences of S before and after oxidation of pyrite and arsenopyrite%
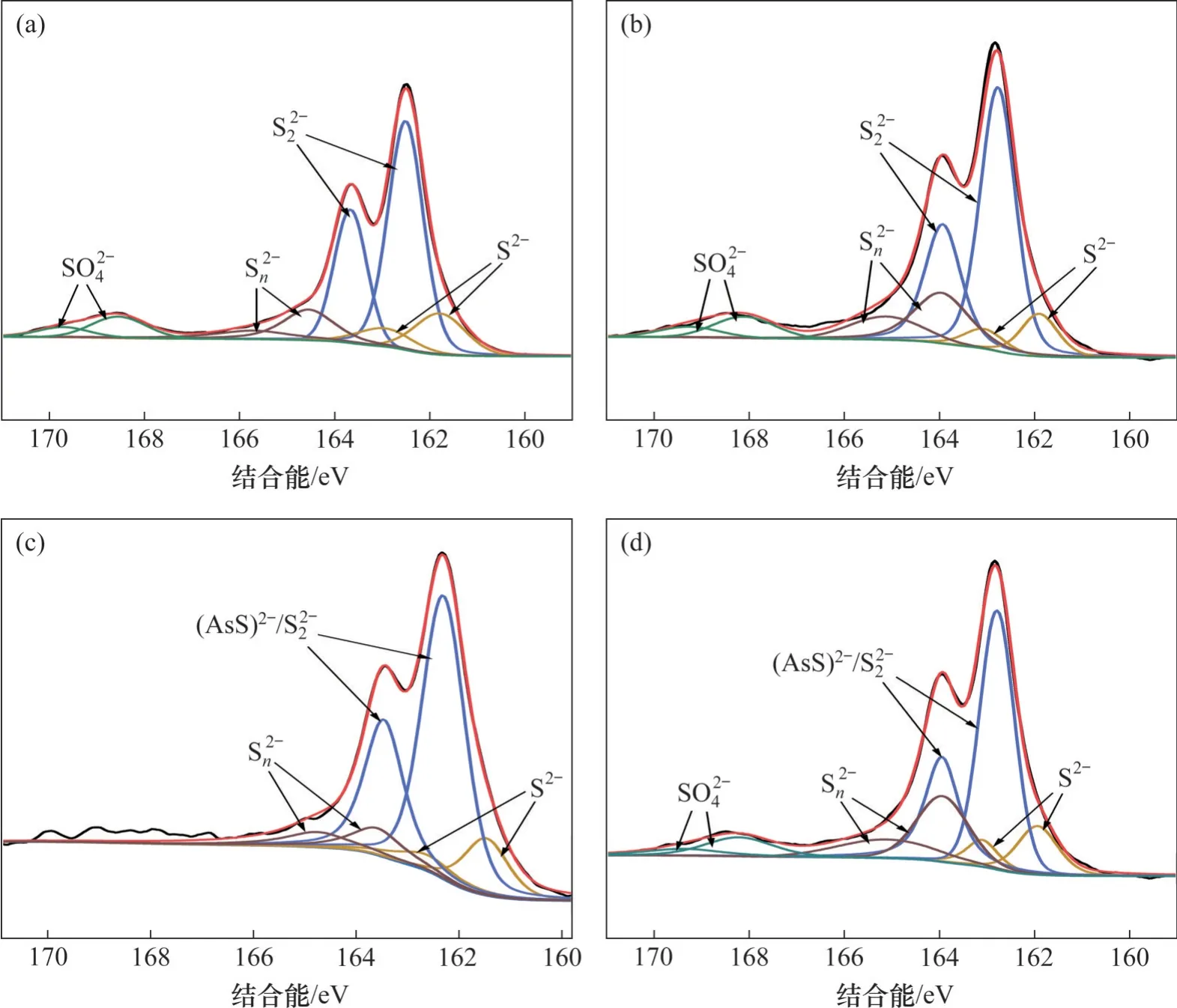
图7 黄铁矿与毒砂氧化前后S 2p XPS分析Fig. 7 S 2p XPS analysis of pyrite and arsenopyrite before and after oxidation
黄铁矿氧化前后XPS 图谱中均有SO24-的拟合峰出现,但拟合峰的强度并未发生太大变化,这表明该SO24-可能是黄铁矿电极中的杂质所携带的,而并非是黄铁矿表面氧化之后所生成的,而毒砂在氧化之后新增了明显的SO24-的氧化峰。此外,由表4可知:黄铁矿氧化后,S2n-和SO24-在总硫元素中的质量分数比氧化前增加5.36%;毒砂氧化后,S2n-和SO24-在总硫元素中的质量分数增加了18.58%,这表明毒砂比黄铁矿更容易氧化,且氧化速度更快、更容易生成亲水性表面,这与Tafel曲线的结果一致。
3 结论
1) 在pH=11 的条件下,黄铁矿的氧化电位比毒砂的更高,毒砂与黄铁矿的表面氧化产物中均有Fe(OH)3、SO24-和S0等物质生成,这些产物在毒砂与黄铁矿表面的吸附会严重影响浮选过程中黄铁矿与毒砂表面的亲水疏水性。
2) 在高pH条件下,毒砂更容易被氧化,当pH为9.18 时,毒砂的氧化速率是黄铁矿的2.57 倍,两者的氧化速率的差异性最大;且在pH=9.18,外加0.6 V 极化电位条件下氧化后,黄铁矿的S2n-和SO24-在总硫元素中质量分数的增量比毒砂的高,可以通过调整溶液的pH去强化黄铁矿与毒砂氧化速率的差异,改变黄铁矿与毒砂表面氧化产物的含量,从而强化黄铁矿与毒砂的浮选分离。
3) 当pH=11 时,黄铁矿电极的氧化动力学方程为η=0.209 logit→0+1.140,其中i0=3.71 μA/cm2;毒砂电极的氧化动力学方程为η=0.282 logit→0+1.463,其中i0=6.48 μA/cm2。
