食品中霉菌与酵母菌计数能力验证结果的分析探讨
2023-10-08刘永泽卢福荣
◎ 邵 悦,刘永泽,卢福荣
(营口市食品药品检验检测中心,辽宁 营口 115000)
霉菌和酵母菌同属于真菌,其中,霉菌是一些“丝状真菌”的统称;酵母菌是一群以芽殖或裂殖来进行无性繁殖的单细胞真菌,没有菌丝体的圆形、杆状、腊肠形的真菌。它们广泛分布于自然界的每个角落,具有很强的新陈代谢能力,并可作为食品正常菌群的一部分。研究表明,如果长期食用霉菌和酵母菌可诱发癌症。因此,检测机构常选择霉菌和酵母菌作为指示菌,通过其数量判断食品的污染程度,来评价食品的卫生质量。
实验室能力验证是利用实验室间比对来判定实验室和检查机构能力的活动,也是认可机构加入和维持国际相互承认协议(MRA)的必要条件之一[1-2]。通过实验室能力验证,可帮助实验室了解自身的检测能力,证实检测数据的准确性,在评价人员能力和验证实验方法、实验数据或实验结果准确性等方面具有非常重要的意义[3]。因此,本研究旨在通过分析检测样品中的霉菌和酵母菌,对本实验室进行能力验证。
1 材料与方法
1.1 样品来源
本实验室收到2份待测样品:ACAS—PT1588(2023)霉菌和酵母计数能力验证样品,均由中国检验检疫科学院测试评价中心发放,编号分别为23-T787和23-T269。
1.2 材料与试剂
孟加拉红琼脂,购于广东环凯微生物科技有限公司,批号:1110795,规格:250 g/瓶;氯化钠(分析纯),国药集团化学试剂有限公司,批号:20220927,规格:500 g/瓶;无菌水,实验室纯水机(UPH-IV-207)自制。
1.3 仪器与设备
霉菌培养箱:型号DMJ-250C,编号1503059,上海博讯实业有限公司医疗设备厂;立式压力灭菌器:型号YXQ-75G,编号20-B2954,上海博讯医疗生物仪器股份有限公司;恒温水浴锅:型号HH-ZK6,编号1706062,巩义市予华仪器有限责任公司;生物安全柜:型号HR1500-IIA2,编号KECC94VCA,青岛海尔生物医疗股份有限公司。
1.4 实验方法
1.4.1 样品前处理
样品前处理的步骤参照ACAS—PT1588(2023)食品中霉菌和酵母计数能力验证(第一轮)参试指导书。将样品开启后,立即向西林瓶内加入5 mL稀释液,待样品充分溶解后,吸出放入灭菌后的100 mL无菌瓶中,然后用余下的55 mL稀释液反复冲洗西林瓶内壁2~3次,回收清洗液存入100 mL无菌瓶中,得到的溶液即是待测样品原液(各环节操作保证无菌和充分混匀)。
1.4.2 样品稀释
样品稀释的步骤参照GB 4789.15—2016 《食品安全国家标准 食品微生物学检验 霉菌和酵母计数》第一法。用无菌吸管准确吸取25 mL待测样品原液,加入225 mL无菌稀释液,均质器拍打充分混匀,即为1∶10样品匀液。取1 mL 1∶10匀液注入含有9 mL无菌稀释液试管中,旋涡混匀,即为1∶100样品匀液。如此,制备10倍递增系列稀释样品匀液,同时以1 mL无菌生理盐水作为空白对照,每个实验重复平行2次。将20~25 mL冷却至46±1 ℃的孟加拉红琼脂倾注平皿,并顺时针转动平皿10次,使其混合均匀,并置水平台面,待培养基完全凝固。
1.4.3 培养计数
培养计数的步骤参照GB 4789.15—2016 《食品安全国家标准 食品微生物学检验 霉菌和酵母计数》第一法。待孟加拉红琼脂凝固后,将平皿放置28±1 ℃的霉菌培养箱中正置进行培养,实验人员观察并记录培养5 d的结果。
2 结果与分析
2.1 结果观察与计数
收到样品后,实验室人员先检查样品是否存在破损、污染、密封性不强的问题,确认样品没有问题后再进行检测。样品溶解应保持在西林瓶内进行操作,严禁将白色冻干样品倒出西林瓶进行水化[2]。样品23-C787和样品23-T269的霉菌与酵母菌在孟加拉红琼脂平板上的生长情况如表1所示。

表1 孟加拉红琼脂平板上的霉菌与酵母计数结果表
样品23-T787霉菌选取10-2梯度进行计算,结果为2 900 CFU/mL,酵母菌选取原液和10-1液进行计算,结果为108 CFU/mL,总数为3.0×103CFU/mL;样品23-T269霉菌选择10-2梯度进行计算,结果为2 600 CFU/mL,酵母菌选择原液进行计算,结果为81 CFU/mL,总数为2.7×103CFU/mL。因为菌落数在10-150 CFU之间,所以选择采用两位有效数字报告。在实验过程中,空白对照分别做了培养基对照和生理盐水空白对照。空白实验均无菌落生长,证明实验有效。
2.2 能力验证结果分析
能力验证结果如表2所示。
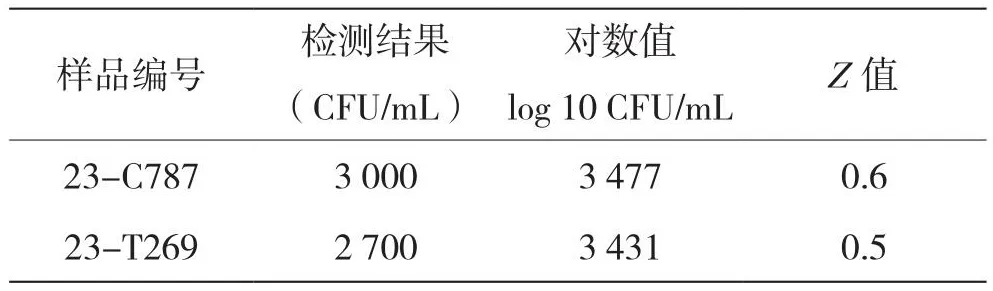
表2 能力验证评价结果表
能力验证评价准则为当|Z|值≤2.0时,实验结果为满意;当2.0<|Z|<3.0时,实验结果为可疑;当|Z|≥3.0时,实验结果为不满意。其中,样品23-C787的|Z|值为0.6,23-T269的|Z|值为0.5,2种样品的|Z|值均<2.0,评价结果为满意。
2.3 检测过程关键点分析
2.3.1 关于灭菌
微生物实验通常是在无菌环境中,整个实验过程要确保无菌操作,在做实验之前要充分准备好实验所需要的试剂和耗材。无菌水、0.85%生理盐水、孟加拉红琼脂培养基以及试剂瓶,都需要在高压灭菌容器内121 ℃高温下灭菌15 min,待冷却至室温时方可使用。在实验开始之前,实验室要用紫外灯照射30 min消毒杀菌;实验人员要戴好一次性无菌帽、口罩和手套,实验室台面以及放有样品的西林瓶要用75%酒精擦拭一遍。在实验结束后,用紫外灯照射实验室30 min。
2.3.2 关于检测
整个实验过程中,必须保证无菌操作;样品稀释液一共要用60 mL,要定容准确;每次递增稀释倍数时,应换一个1 mL的无菌枪头;培养基在倾注平皿时要注意培养基温度,及时将20~25 mL冷却至46±1 ℃的孟加拉红琼脂培养基倾注平皿,培养基倾注完成后,充分转动平皿使其混合均匀,如果混合不均匀会影响霉菌与酵母菌的计数。此外,由于霉菌和酵母孢子会扩散,因此在新版标准GB 4789.15—2016中,明确规定将培养方式调整为正置培养[4]。
2.3.3 关于对比实验
快速测试片法是以纸片作为菌落的培养基载体,通过特定培养基和显色物与菌落发生特异性反应,培养适当时间,进行菌落数观测。在进行本次能力验证时,采取纸片法做对比,将霉菌与酵母菌测试片置于适合其生长的培养基中。其中,抗生素可抑制细菌生长,再加入菌落生长指示剂和专一性强的酶作显色剂,继而可以通过观察有显色的菌落,确定霉菌和酵母菌的数量[5]。这种检测方法操作简单,方便与孟加拉红琼脂平板上所显示的菌落数进行对比,用来作为计数参考,最终报告结果时,以孟加拉红琼脂培养基上的结果为准。
2.3.4 关于计数
霉菌与酵母菌属于同一种培养基进行同步实验,在计数时应该分别计数。由于霉菌生长速度很快,最好在培养第二天时,每天记录平板上的菌落数,防止后期霉菌生长太快影响实验结果准确性。在进行计数时不要拿着平板上下翻转,防止孢子扩散。培养24 h时后,培养基肉眼观察并无菌落生长;培养48 h后,霉菌已经生长达到峰值;培养60 h后,霉菌没有明显的增值现象;培养72 h后,霉菌已产生大量孢子。由此可见,培养时间越长,霉菌的菌丝生长越大,到最后会覆盖平皿,造成计数困难。因此,建议在培养40~48 h内进行实验计数,所得结果较为准确。
3 结语
本实验室此次能力验证结果满意,提高了检验人员的技术水平,为扩大实验室核心竞争力奠定了良好的基础。同时,实验过程符合标准要求,能够为食品中霉菌和酵母菌检测提供可靠的数据,从而为营口市食品药品检验检测中心承担国家抽检工作奠定良好的基础。
