内镜下切除与腹腔镜手术切除治疗胃间质瘤适应证及预后对比分析
2023-09-26陈爱锦
陈爱锦
福建医科大学附属协和医院消化内科,福建福州 350000
胃肠间质瘤是常见的间叶源性肿瘤,多起源于消化道固有肌层,具有恶变的潜在可能,其中胃间质瘤占50%~60%,小肠间质瘤占20%~30%[1-2]。据统计,胃肠间质瘤的发病率为8/100 万,发病群体集中在70~79 岁高龄人群中,其5 年内的生存率约为79%,有10%~30%的肿瘤属于恶性程度[3]。目前,手术切除是治愈的唯一方法,外科手术下完整切除病变肿瘤是治疗的金标准,腹腔镜手术是应用于胃肠间质瘤的一种微创外科手术,相对传统的开腹手术具有创伤小、术后肠胃恢复快和住院时间短等优势,但同时对肿瘤较大、不易解剖和质地脆的胃间质瘤存在着操作困难的问题[4]。随着内镜设备的提高和推广,近年来内镜手术逐渐应用于胃间质瘤的治疗当中,其能通过内镜迅速定位病灶,并通过黏膜下剥离切除病灶,切除效果较好,能避免切除过多的不可再生组织,且该手术消耗时间短,能保持胃壁的完整性,达到较好的治疗效果,同时并发症的发生风险较低[5]。但临床对于两种手术的选择、术后适应证和病情预后情况仍存在着较大的争议,因此,本研究通过比较两种手术方法治疗胃间质瘤的适应证和预后进行对比分析,旨在为临床胃间质瘤的治疗提供参考。
1 资料与方法
1.1 一般资料
回顾性选取2021 年1 月至2022 年6 月福建医科大学附属协和医院109 例胃间质瘤患者,按照手术方法不同将其分为内镜切除组(n=54)和腹腔镜手术组(n=55)。样本量估算:α 取双侧0.05,β 取单侧0.1,利用统计学软件计算得到N内镜切除组=43,N腹腔镜手术组=44,假设研究对象的失访率为20%,则需样本量N内镜切除组=43/0.8 ≈54,N腹腔镜手术组=44/0.8 ≈55,因此内镜切除组至少纳入54 例患者,腹腔镜手术组至少纳入55 例患者。其中,内镜切除组:男25 例,女29 例;胃间质瘤位于胃底12 例,胃体25 例,胃窦17 例;年龄34~78 岁,平均(54.09±11.17)岁;病程0.5~2.5 年,平均(1.47±0.59)年;肿瘤直径6~40 mm,平均(13.56±3.61)mm。腹腔镜手术组:男34 例,女21 例;胃间质瘤位于胃底15 例,胃体21 例,胃窦19 例;年龄32~78 岁,平均(54.95±13.18)岁;病程0.5~3.0 年,平均(1.67±0.68)年;肿瘤直径7~79 mm,平均(13.27±3.91)mm。两组患者一般资料比较,差异无统计学意义(P> 0.05),具有可比性。本研究经医院医学伦理委员会批准(伦理号:2023KY066),所有患者及家属均知情同意。
纳入标准:①年龄≥18 岁;②诊断符合《中国胃肠间质瘤诊断治疗专家共识(2017 年版)》[6]标准,且经CT 扫描和超声内镜等检查确诊为胃间质瘤患者;③胃部单发病灶患者。排除标准:①间质瘤位于食管和胃交接部位患者;②存在其他功能障碍性的全身性疾病患者;③CT 检查提示肿瘤有远处转移患者;④食管、胃急性炎症患者。
1.2 方法
1.2.1 腹腔镜手术组 患者取仰卧位,行常规麻醉后进行气管插管。常规消毒、铺巾,于患者脐上1 cm处建立人工气腹,置入各型号Trocar,置入腹腔镜器械,探查见腹腔内无腹水,盆腔、肝、网膜未见转移结节,明确间质瘤的位置和生长方式,在确认肿瘤位置后,沿肿瘤表面打开浆肌层提起肿物,距离肿瘤基底部约1 cm 处用60 mm 蓝钉威高切除肿瘤及部分胃组织,胃切缘用1 根倒刺线缝合止血,撤除腹腔镜器械。延长脐旁Trocar 切口长约3 cm 依次切开腹壁各层进入腹腔,将肿瘤及部分胃标本取出,仔细止血,检查无活动性出血,于胃段缘留置一腹腔引流管,清点纱布器械无误后逐层关闭腹腔。
1.2.2 内镜切除组 患者取仰卧位,行常规麻醉后进行气管插管。根据患者超声内镜和腹部CT 影响选择合适内镜切除方式,主要ESE 术、ESD 术、STER 术和EFTR 术。ESE 术:用啄木鸟刀在隆起的病灶边缘标记,用美兰+甘油果糖在其周围行黏膜下注射,用啄木鸟刀切开病灶的外侧黏膜层,可见一粘膜下肿物,逐渐分离粘膜,见病灶来源于固有肌层,沿包膜进行完整的剥离,并用热活检钳对创面进行处理,后用金属钛夹缝合。ESD 术:用Dual 刀标记预切除病变部位环周,用Dual 刀逐层切开病变周围黏膜,完整剥离出间质瘤体,后处理创面,以金属钛夹关闭黏膜切口处,利用圈套器取出瘤体。STER 术:以Dual 刀切开1.5 cm 左右长度的纵向切口,向瘤体方向将黏膜下组织进行分离,随后建立黏膜下隧道,在间质瘤周围组织剥离后充分暴露出间质瘤体,采用Dual 刀逐步剥离出完整的瘤体,以金属钛夹关闭隧道开口。EFTR 术:用Dual 刀在病灶边缘外标记,并切开其周围黏膜,在内镜直视下,采用主动穿孔的方式将瘤体逐渐剥离完整,用金属钛夹和尼龙绳缝合夹闭创面。
1.3 观察指标及评价标准
1.3.1 手术指标 记录两组患者手术时间和术中出血量,观察两组患者术后肛门排气时间和术后住院时间。
1.3.2 术后并发症 记录并观察术后7 d 内并发症的发生情况,主要包括穿孔、腹痛、出血、切口感染和发热等,计算并比较两组患者并发症的总发生率。
1.3.3 术后危险程度分级 于术后第2 天根据《中国胃肠间质瘤诊断治疗共识(2017 年版)》[6]对患者术后复发危险程度分级进行评价,共有极低危、低危、中危和高危四种分级,分级越高,表明患者术后复发的风险更大。
1.3.4 复发转移情况 于患者出院6 个月内进行随访,记录患者的复发和疾病转移情况,计算并比较两组复发率和转移率的差异。
1.4 统计学方法
采用SPSS 21.0 统计学软件处理数据,计量资料用均数±标准差()表示,采用t检验;计数资料采用[n(%)]表示,采用χ2检验和秩和检验,P< 0.05 为差异有统计学意义。
2 结果
2.1 两组患者手术指标比较
内镜切除组患者的手术时间、术中出血量和术后肛门排气时间均明显低于腹腔镜手术组,差异有统计学意义(P< 0.05);两组患者的术后住院时间比较,差异无统计学意义(P> 0.05)。见表1。
表1 两组患者手术指标比较()
2.2 两组患者术后并发症发生情况比较
内镜切除组患者术后并发症的总发生率为3.70%,明显低于腹腔镜手术组的16.36%,差异有统计学意义(P< 0.05),见表2。

表2 两组患者术后并发症发生情况比较[n(%)]
2.3 两组患者术后危险程度分级比较
内镜切除组术后患者危险分级为中危2 例、低危25 例、极低危27 例,与腹腔镜手术组的高危3 例、中危21 例、低危23 例、极低危8 例比较,差异有统计学意义(P< 0.05),见表3。
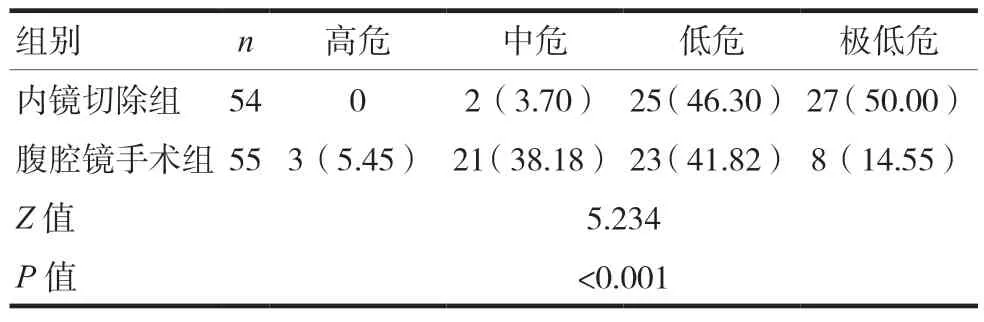
表3 两组患者术后危险程度分级比较[n(%)]
2.4 两组患者术后复发转移情况比较
内镜切除组患者术后6 个月内的复发率为1.85%(1/54),无转移病例,腹腔镜手术组患者的复发率为5.45%(3/55),转移率为1.82%(1/55),两组比较差异无统计学意义(P> 0.05),见表4。

表4 两组患者术后复发转移情况比较[n(%)]
3 讨论
胃间质瘤淋巴结转移的发生情况较少,手术切除作为的一线治疗方法,不需要进行淋巴结清扫,传统开腹手术适用于所有大小的间质瘤,对于直径<5 cm 的胃间质瘤多项指南推荐使用腹腔镜手术,而随着内镜技术的发展,其实用性和安全有效性亦得到了多种认可[7]。故本研究通过比较内镜切除和腹腔镜切除的适应证及其预后,探讨其可行性。
本研究结果显示,内镜切除组患者的手术时间、术中出血量和术后肛门排气时间均明显低于腹腔镜手术组,差异有统计学意义(P< 0.05),表明内镜切除术相较于腹腔手术组,能有效减少手术时间、出血量和术后肛门排气时间。其可能原因如下:内镜切除能够根据病变部位的起源层次、肿瘤与其周围的关系选择不同的手术方式,ESD 术适用于固有肌浅层间质瘤,ESE 术适用于较深处的病灶,EFTR 术主要用于突向腔内外、腹膜或腹内器官粘连的病变,STER 术适用于贲门和胃底的病变[8]。相对而言,腹腔镜切除在较小的内生型间质瘤中定位困难,如若完整切除肿瘤,则对正常的组织会有过多的切除,或需在术中行胃镜辅助检查进行定位,同时在贲门或大弯处的胃底病灶,腹腔镜下暴露或操作较困难[9]。因此,腹腔镜手术组的手术时间较内镜切除组长,出血量更大。
在适应证方面,研究对患者术后并发症进行统计,结果发现,内镜切除组患者术后并发症的总发生率为3.70%,明显低于腹腔镜手术组的16.36%,差异有统计学意义(P< 0.05),表明内镜治疗能有效降低胃间质瘤术后并发症发生率,可行性较高。童锦等[10]采用EFTR 术对直径2~5 cm 的腔外生长型胃间质瘤进行切除,并采用金属钛夹与尼龙绳进行内镜荷包线缝合,发现对>2 cm 的胃壁缺损患者无出现迟发性穿孔和出血。陈非等[11]研究发现,采用EFTR 术治疗胃肠间质瘤患者,术后72 h内无严重的并发症发生,上述报道均与本研究结果相似。内镜相较于腹腔镜具有准确定位的特点,虽能减少对胃正常组织的损伤和并发症的发生,但因EFTR 术需要进行腹腔主动穿孔操作,而内镜手术属于有菌操作,该过程腹腔有被胃液和手术器械污染的风险,故在术前应在浆膜层切开之前将胃液尽量吸尽,以避免胃液进入腹腔[12],而STER 术则需要建立黏膜下隧道,难度较高,因此本研究中仅有3 例患者采用STER 术,11 例患者采用EFTR 术,EFTR 术后内镜切除组仍有2 例患者出现感染现象,提示了对该术式实操过程中的抗感染治疗应加以重视。在Chen 等[13-14]的报道指出,因内镜切除的严重并发症和腹内组织粘连与病变浆膜层有关,在全层切除后有气体进入腹腔,能增加腹腔感染和转移的风险,故对突向腔内外生长和与腹内组织粘连紧密的间质瘤不建议行内镜手术,在本研究中,行EFTR 术例数较少,内镜切除组并发症总体发生率虽低于腹腔镜手术组,但内镜组感染率较腹腔镜组高,与上述报道理论相符合。因此,在后续临床实践中,应根据患者病变部位的实际情况选择手术方法。
另一方面,研究从患者的术后患者危险分级、复发转移等预后情况评价两种手术方法,结果显示,两组患者术后6 个月内的复发、转移情况无显著差异,表明了两种手术方法对患者的预后效果相仿。但通过对患者危险分级发现,内镜切除组不存在高危级患者,仅存在2 例中危患者,占3.70%,其余多数患者集中在低危和极低危级别,而腹腔镜手术组的高危和中危患者共有24 例,占43.63%,其比例相对内镜切除组较高,患者的复发和转移的风险更大,但因本研究时限问题,术后随访时间较短,未进行年限较长的回访,且样本为单中心小样本,产生的研究结果可能存在一定的偏倚。李林波[15]对行内镜治疗的36 例胃间质瘤患者进行危险分级,结果提示了高危患者有0 例、中危2 例、低危5 例、极低危29 例;杨秋子[16]对内镜下小胃间质瘤切除患者进行分级,结果提示高危患者存在1 例、中危8 例、低危19 例、极低危92 例;刘茹等[17]报道指出,行内镜治疗的胃肠间质瘤存在高危患者0 例、中危2 例、低危35 例、极低危61 例。上述报道结果均支持了本研究结果。
综上所述,内镜切除术治疗胃间质瘤患者可有效改善手术相关指标,降低并发症发生率和危险程度,且复发、转移情况与腹腔镜手术相比无明显差异。
