左乙拉西坦联合吡仑帕奈治疗儿童良性癫痫的临床研究
2023-09-26汪学静马燕石红蕾
汪学静,马燕,石红蕾
聊城市第二人民医院 小儿内科,山东 聊城 252600
儿童良性癫痫是小儿癫痫最常见的类型之一,具有特发于儿童时期(2~14 岁)、有明显遗传因素、良性部分发作、临床表现与脑电图(往往伴中央颞区棘波)有一定特征、青春期前自愈等特点,5~10岁为发病高峰,男孩多于女孩。该病多于睡眠期局灶性发作,以口咽部感觉异常、运动性发作最为常见,主要表现为流涎、唇舌僵硬、不能吞咽、一侧肢体阵挛性抽动、躯体感觉障碍等,严重影响儿童身心健康及生长发育[1]。目前针对儿童良性癫痫以控制癫痫发作为主要治疗目的,大多数患儿采用抗癫痫药物单药治疗即可获得良好效果[2]。但越来越多证据显示其预后并非都是良性,部分患儿不能达到完全无发作或伴睡眠中癫痫性电持续状态(ESES,即棘波指数≥85%)者对药物反应性差,最终可引起认知损害及精神行为异常。因此,采用耐受性良好且合理的联合用药方案有利于提高治疗效果、改善患儿生活质量。吡仑帕奈为新型抗癫痫药物,能抑制神经元过度兴奋、控制癫痫发作,是临床治疗儿童良性癫痫的常用药[3]。左乙拉西坦片为吡咯烷酮类抗癫痫新药,有减少痫性放电、保护神经功能等作用,是当前儿童良性癫痫的一线治疗用药[4]。故而本研究采用左乙拉西坦片联用吡仑帕奈治疗儿童良性癫痫,取得了较好的临床疗效。
1 资料与方法
1.1 一般资料
选取2020 年5 月—2021 年12 月聊城市第二人民医院收治的78 例良性癫痫患儿,其中男46 例,女32 例;体质量20.17~46.85 kg,平均体质量(34.43±8.26)kg;年龄4~12 岁,平均年龄(9.20±1.51)岁;病程6 个月~5 年,平均病程(2.35±0.52)年。
纳入标准:(1)满足儿童良性癫痫的诊断标准[5];(2)入组前发作频率≥1 次/月;(3)年龄4~12 岁;(4)伴中央颞区棘波和ESES;(5)患儿家属自愿签订知情同意书;(6)无吡仑帕奈使用禁忌证;(7)家属能遵医嘱要求坚持长期、规律给患儿用药。
排除标准:(1)继发性癫痫或难治性癫痫;(2)存在急慢性感染、免疫缺陷或血液系统疾病;(3)对左乙拉西坦片中任何成分过敏;(4)伴孤独症谱系障碍或注意缺陷多动障碍等共患病;(5)肝肾功能不全;(6)合并葡萄糖-半乳糖吸收不良或遗传性半乳糖不耐受;(7)伴有进行性神经系统疾病或占位性病变。
1.2 药物
左乙拉西坦片由珠海联邦制药股份有限公司中山分公司生产,规格0.25 g/片,产品批号202004032、202 107095;吡仑帕奈片由卫材(中国)药业有限公司生产,规格2 mg/片,产品批号200357A、211189A。
1.3 分组和治疗方法
按随机数字表法将所有患者分为对照组和治疗组,每组各39 例。其中对照组男22 例,女17 例;体质量20.31~46.85 kg,平均体质量(34.95±8.58)kg;年龄4~12 岁,平均年龄(9.38±1.62)岁;病程8 个月~5 年,平均病程(2.41±0.63)年。治疗组男24 例,女15 例;体质量20.17~45.78 kg,平均体质量(34.03.±7.94)kg;年龄4~12 岁,平均年龄(8.92±1.34)岁;病程6 个月~5 年,平均病程(2.23±0.44)年。两组基线资料相比差异无统计学意义,具有可比性。
每位患儿均接受相同的合理膳食、作息规律、保证充足的休息时间、避免不良因素等非药物治疗。对照组口服吡仑帕奈片,起始剂量根据患儿体质量计算,体质量>30 kg 为2 mg/d、20~30 kg 为1 mg/d,睡前吞服,每隔2 周加量1 次,每次加量为1 个起始剂量,直至以4 mg/d 的剂量维持治疗。治疗组在对照组基础上口服左乙拉西坦片,起始剂量每次10 mg/kg,2 次/d,每隔2 周加量1 次,每次加量为1 个起始剂量(如第1 次加量后剂量调整为每次20 mg/kg,2 次/d),直至以每次30 mg/kg,2次/d 的剂量维持治疗。两组疗程均为6 个月。
1.4 疗效判定标准[6]
显效:治疗后,疗效指数(N)≥75%;有效:治疗后,50%≤N<75%;改善:治疗后,25%≤N<50%;无效:治疗后,N<25%。
N=治疗前后发作频率差值/治疗前发作频率
总有效率=(显效例数+有效例数+改善例数)/总例数
1.5 观察指标
1.5.1 癫痫发作情况 统计两组治疗前后癫痫发作频率(次/月)、持续时间(次/min)。
1.5.2 国立医院癫痫发作严重程度量表(NHS3)评分 共包含意识丧失、摔倒、恢复时间等7 个项目,评分范围为1~27 分,得分越高则癫痫发作的程度越严重[7]。
1.5.3 脑电图相关指标 治疗前后使用 EEG-1200C 型视频脑电图仪(日本光电公司)监测患儿24 h 动态脑电图,记录至少一个完整睡眠周期,由描记结果分析受试患儿痫性放电情况,计算两组痫性放电率。
痫性放电率=痫性放电例数/总例数
1.5.4 P300 潜伏期、波幅 治疗前后运用NDI-092型肌电诱发电位仪(上海海神医疗公司)采集试验患儿P300 成分的波幅和潜伏期,检查操作均于安静屏蔽的检查室内进行,受检患儿保持注意力集中,在非靶刺激与靶刺激中做出相应的判断和反应。
1.5.5 血清细胞因子水平 治疗前后抽取所有患儿3 mL 空腹肘静脉血,离心(3 000 r/min,15 min)分离血清,分装,冻存待测。选用HM-SY96S 型酶标仪(山东恒美科技)检测血清高迁移率族蛋白B1(HMGB1)、肿瘤坏死因子(TNF)-α、胶质纤维酸性蛋白(GFAP)、γ-氨基丁酸(GABA)水平,试剂盒(酶联免疫法)均购自杭州艾康生物,操作均按说明书进行。
1.6 不良反应观察
记录受试患儿相关不良反应情况。
1.7 统计学分析
2 结果
2.1 两组临床疗效比较
治疗后,治疗组总有效率是94.87%,显著高于对照组的79.49%(P<0.05),见表1。

表1 两组临床疗效比较Table 1 Comparison on clinical efficacy between two groups
2.2 两组患者癫痫发作频率、持续时间和NHS3 评分比较
治疗后,两组癫痫发作频率、NHS3 评分均显著降低,持续时间均显著缩短(P<0.05);且以治疗组降低更显著(P<0.05),见表2。
表2 两组癫痫发作频率、持续时间和NHS3 评分比较()Table 2 Comparison on seizure frequency,duration and NHS3 score between two groups ()

表2 两组癫痫发作频率、持续时间和NHS3 评分比较()Table 2 Comparison on seizure frequency,duration and NHS3 score between two groups ()
与同组治疗前比较:*P<0.05;与对照组治疗后比较:▲P<0.05*P <0.05 vs same group before treatment;▲P <0.05 vs control group after treatment
2.3 两组痫性放电率和P300 潜伏期、波幅比较
治疗后,两组痫性放电率、P300 潜伏期均显著缩短,P300 波幅均显著增加(P<0.05);且以治疗组改善更显著(P<0.05),见表3。
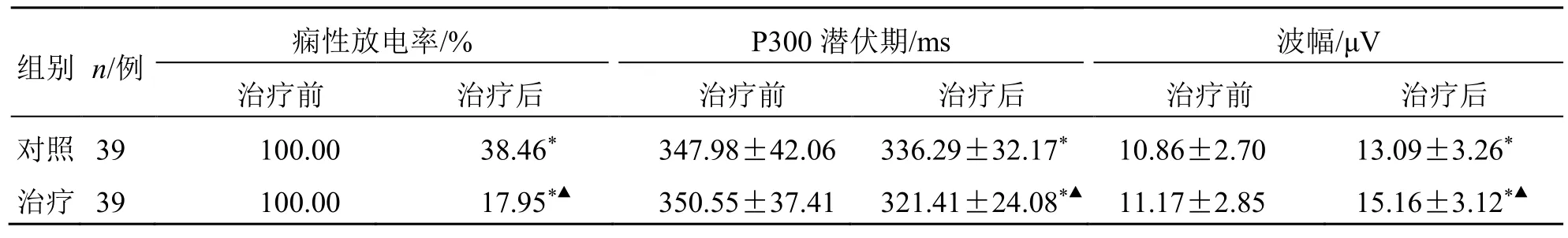
表3 两组痫性放电率和P300 潜伏期、波幅比较Table 3 Comparison on epileptic discharge rate,P300 latency and amplitude between two groups
2.4 两组血清HMGB1、TNF-α、GFAP、GABA 水平比较
治疗后,两组血清HMGB1、TNF-α、GFAP 水平均显著下降,GABA 水平均显著上升(P<0.05);且治疗后,治疗组血清HMGB1、TNF-α、GFAP、GABA 水平均显著优于对照组(P<0.05),见表4。
表4 两组血清HMGB1、TNF-α、GFAP、GABA 水平比较()Table 4 Comparison on serum HMGB1,TNF-α,GFAP and GABA levels between two groups ()
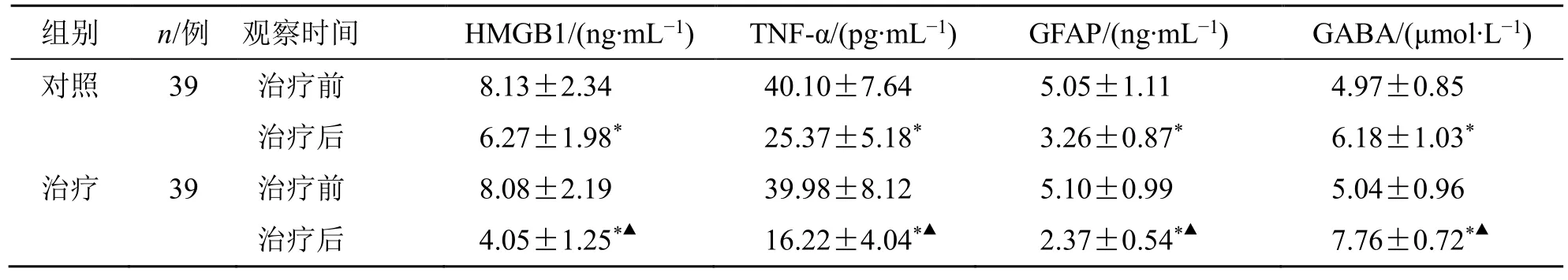
表4 两组血清HMGB1、TNF-α、GFAP、GABA 水平比较()Table 4 Comparison on serum HMGB1,TNF-α,GFAP and GABA levels between two groups ()
与同组治疗前比较:*P<0.05;与对照组治疗后比较:▲P<0.05*P <0.05 vs same group before treatment;▲P <0.05 vs control group after treatment
2.5 两组不良反应比较
对照组发生嗜睡2 例,头晕、易激怒各1 例,不良反应发生率是10.26%;治疗组发生嗜睡2 例,乏力、易激怒、食欲不振、头晕各1 例,不良反应发生率是15.38%,两组不良反应发生率比较差异无统计学意义。
3 讨论
资料显示,我国儿童癫痫患病率约0.345%,其中儿童良性癫痫伴中央颞区棘波占15%~25%,是小儿神经系统常见疾病[8]。该病为多病因疾病,主要是由先天脑发育畸形、遗传代谢病、围产期脑损伤、颅内感染、神经皮肤综合症等因素引起神经兴奋与抑制障碍,从而导致脑电改变。传统观念认为儿童良性癫痫无神经系统异常或认知功能损伤,预后良好,然而发作间期放电在非快速眼动睡眠期显著增加,可出现癫痫性电持续状态现象产生多样化发作形式,导致高级皮层功能受累引发神经心理损伤[9]。且儿童处于认知发育的关键时期,癫痫的发作性与反复性可导致神经递质异常兴奋、缺氧、乳酸中毒等不良反应,损伤神经元及代谢活动,引起神经元脱失、胶质细胞增生、钙离子超载、海马结构变化等一系列病理生理变化,并根据癫痫发作类型、起病年龄、持续时间、发作频率、病程等的不同,对患儿认知、精神心理、社会功能等造成不同程度的不可逆损害,故及时、规范的治疗对改善患儿预后尤为重要。从安全、有效、经济等方面考虑,口服抗癫痫药物仍是目前儿童良性癫痫各种治疗手段(药物、外科手术、生酮饮食等)中的主要方法,理想的治疗目标是尽可能降低药物不良反应、抑制痫性放电及达到癫痫完全无发作、保护认知功能[10]。随着不同作用机制、耐受性良好的新型抗癫痫药物的出现,机制互补、疗效叠加、无额外不良反应的抗癫痫药物联合用药有助于提高治疗指数及改善患儿预后。
吡仑帕奈是第3 代潜在的广谱抗癫痫药物,口服吸收快速而完全,主要可通过选择性拮抗突触后膜重要的兴奋性神经递质—谷氨酸的受体,抑制兴奋性神经递质活性及癫痫发作,达到安全有效地治疗儿童良性癫痫的目的[11]。左乙拉西坦作为新型作用机制的抗癫痫药物,其发挥良好抗癫痫效果的途径可能包括:①阻滞高电压激活的N-型钙离子通道;②解除负性变构剂,通过提高GABA 水平而阻碍神经元回路形成;③结合脑内突触囊泡蛋白2A,从而直接作用于癫痫活动区,抑制痫性放电;④维持突触兴奋-抑制功能平衡、抗继发的兴奋毒性损伤、抗氧化应激等作用,可发挥一定的神经保护效应[12]。同时本品因可用于癫痫单独治疗、不受其他药物与食物影响、治疗指数高、不良反应轻微等优点而成为儿童良性癫痫治疗的较佳选择。李志鹏等[13]研究表明,左乙拉西坦可能通过重塑癫痫相关皮层区域及丘脑、症状(语言、运动、认知等)相关脑区的灰质结构,对伴中央颞区棘波的良性癫痫患儿发挥良好的抗癫痫及抑制神经损伤的作用。同时相关文献显示,针对良性癫痫伴中央颞区棘波患儿给予左乙拉西坦治疗相较传统抗癫痫药物在提高临床疗效、控制癫痫发作等方面更具优势,且对患儿P300 潜伏期和智力水平亦有更积极的影响,患儿耐受性较好[14]。另外,有报道指出,癫痫患儿存在一定的认知功能损害,事件相关电位P300 能客观反映患儿认知功能受损情况,患儿主要表现为P300 潜伏期延长,P300 波幅降低[15]。本研究中,较之对照组(79.49%),治疗组总有效率(94.87%)显著提高;治疗后,治疗组癫痫发作频率、持续时间、发作程度(NHS3 评分)均较对照组改善更显著,且痫性放电率显著低于对照组,P300 潜伏期显著短于对照组,P300 波幅显著大于对照组。同时对照组与治疗组不良反应发生率(10.26%vs15.38%)无明显差异,且均未见严重不良事件。说明左乙拉西坦片联合吡仑帕奈治疗儿童良性癫痫具备良好的有效性与安全性,利于患儿痫性放电及认知功能的改善。
炎症反应与儿童良性癫痫的发生发展密切相关。HMGB1 作为致炎因子网络的中心环节,主要存在于细胞核内,当良性癫痫患儿神经元及神经胶质细胞受损时,HMGB1 被释放至胞外,并通过激活核转录因子-κB 与TNF-α、白细胞介素-6 等促炎因子,促进N-甲基-D-天冬氨酸介导的钙离子流入胞内,调节谷氨酸代谢酶表达等途径,导致神经元过度兴奋,诱导癫痫发作;而脑组织损伤和炎症反应的加剧,致使HMGB1 进一步释放,形成恶性循环,加重患儿病情[16]。TNF-α 为重要的促炎因子,可通过破坏血脑屏障通透性和完整性、促进白细胞浸润和炎性细胞因子分泌、增强细胞毒活性、促使胶质细胞活化增生、上调相关受体表达来提高神经元兴奋性等作用,参与神经元异常放电及良性癫痫的反复发作[17]。GFAP 是判断中枢神经发育状况的特异性标志物,可维持星形角质细胞的基本形态,其表达异常增高可导致钾离子稳态调节功能紊乱,引起神经元异常兴奋,其血清水平高低可反映良性癫痫患儿神经损伤程度[18]。儿童良性癫痫的发病与大脑皮质化学介质失衡有关,GABA 作为脑内主要抑制性神经递质,可通过与受体结合产生开放氯离子通道、促使突触后膜超极化等作用,防止神经元过度兴奋,同时其对大脑皮质、丘脑、海马等部位起着重要调控作用,参与调节神经系统功能,血中GABA 水平异常下降可促使癫痫发作及认知功能下降[19]。本研究中,治疗后治疗组对血清HMGB1、TNF-α、GFAP 水平的降低作用及对血清GABA 水平的升高作用均较对照组更显著;提示儿童良性癫痫采用左乙拉西坦片联合吡仑帕奈治疗在减轻患儿体内炎症反应、调节氨基酸类神经递质表达方面更具优势。
综上所述,左乙拉西坦片联合吡仑帕奈治疗儿童良性癫痫有确切疗效,在控制患儿癫痫发作、减少痫性放电、改善认知功能方面均可获得较为满意的效果,并可进一步降低血清HMGB1、TNF-α、GFAP 水平及升高血清GABA 水平,且安全性较好,值得临床推广应用。
利益冲突所有作者均声明不存在利益冲突
