艰难梭菌疫苗临床试验的研究现状及挑战
2023-09-23陶薇傅婷综述洪艳审校
陶薇,傅婷 综述,洪艳 审校
杭州医学院检验医学院、生物工程学院,浙江杭州310013
艰难梭菌(Clostridiodes difficile,C.difficile),即难辨梭状芽孢杆菌,是一种厌氧生长的革兰阳性梭状产毒芽孢杆菌,广泛分布于自然环境、动物和人的粪便中,其芽孢对高温、强酸、抗生素和辐射等均具有较强的抵抗力[1]。艰难梭菌是医院抗生素相关腹泻(antibiotic-associated diarrhea,ADD)的主要病因[2-3]。当个体肠道正常菌群平衡被抗生素破坏时,会造成艰难梭菌感染(C.difficileinfection,CDI)。艰难梭菌致病性菌株主要产生两种同源性糖基化毒素,艰难梭菌毒素A(C.difficiletoxin A,TcdA)和艰难梭菌毒素B(C.difficiletoxin B,TcdB),一些高致病菌株还会产生二元毒素(binary toxin),又称艰难梭菌转移酶(C.difficiletransferase,CDT),会造成从腹泻到高致死的中毒型巨结肠等症状[4-5]。自2003 年,由于艰难梭菌强毒力株核糖体型027(ribotype 027,RT027)的出现,CDI 的发病率、复发率及死亡率在全球范围内均大幅上升[6-7]。在北美、欧洲等国家均出现艰难梭菌高毒力株暴发流行。在欧洲,根据欧洲疾病预防和控制中心(EuropeanCentreforDiseasePreventionandControl,ECDC)对医疗保健相关感染的调查,2011—2012年期间,欧洲CDI 病例数为123 997 例[95%置信区间(confidence interval,CI):61 018 ~ 284 857 例][8-9]。自2016 年1 月,ECDC 开始收集欧洲急诊医院CDI发病率的监测数据。作为ECDC监测数据的一部分,来自20 个国家的556 家医院共报告了7 711 例CDI 病例[10]。而美国CDI 的感染率更高。美国疾病预防控制中心2019年抗生素耐药报告显示,美国2017年艰难梭菌感染病例数为223 900,其中15% ~ 35%的CDI患者有1次或多次反复感染,死亡病例数为12 800[11]。亚洲多数国家也出现了RT027 型菌株。2014 年,中国报道了首例RT027 型菌株的临床感染病例[7,12]。但目前RT027型菌株在亚洲国家并不常见[13]。鉴于CDI对患者、医疗机构和社会造成的巨大疾病负担,预防性疫苗的研发尤为重要。国内外对艰难梭菌疫苗的研究方案中,主要以TcdA和TcdB作为靶抗原[14-17];此外还有TcdA、TcdB 和CDT 的联合疫苗研究方案,非产毒艰难梭菌肠道上皮定植和黏附,以及艰难梭菌鞭毛帽蛋白、表面多糖和脂磷壁酸等作为疫苗的候选方案[18-22]。迄今尚无获得使用许可的艰难梭菌疫苗,本文对艰难梭菌疫苗临床试验的研究现状和挑战作一综述。
目前已进入临床试验的候选疫苗主要为TcdA和TcdB 相关疫苗。TcdA 和TcdB 是艰难梭菌重要的致病物质。它们通过糖基化修饰引起结肠上皮细胞内Rho 蛋白家族鸟苷三磷酸酶(GTPases)失活,改变结肠上皮细胞结构和破坏上皮黏膜屏障,并诱发强烈的炎性反应[23-24]。既往研究表明,患者抗毒素抗体水平与CDI复发风险呈负相关[25]。因此,TcdA和TcdB被作为艰难梭菌主要的疫苗候选抗原。目前,赛诺菲巴斯德、辉瑞、Valneva、默克和Synthetic Biologics 5家药企均有TcdA 和TcdB 相关疫苗投入临床试验。此外其他疫苗方案的生物制品也投入临床试验,如Takeda/Shire和葛兰素史克。以下逐一对这些处于临床试验的艰难梭菌疫苗进行介绍(见表1)。
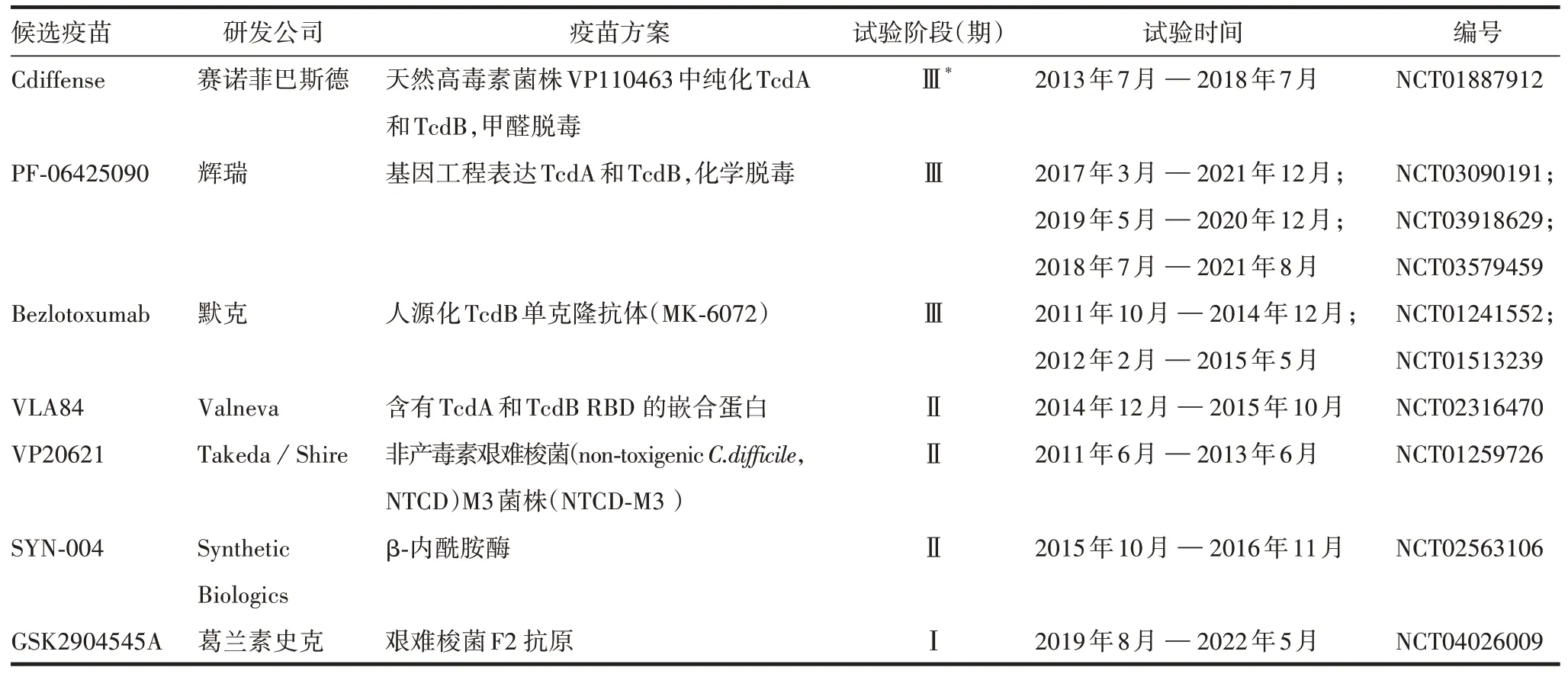
表1 艰难梭菌候选疫苗临床试验阶段研究现状Tab.1 Research status of C.difficile candidate vaccine in clinical trial stage
1 Cdiffense
Cdiffense 是赛诺菲巴斯德研制的一种二价类毒素疫苗。采用传统方法,从天然高毒素艰难梭菌菌株VP110463 中纯化TcdA 和TcdB,经甲醛处理脱去其毒性后,以氢氧化铝作为佐剂,制备二价类毒素疫苗。在已报道的临床Ⅱ期试验中(2011年6月—2013 年6月),40~64岁患者接种100µg二价类毒素疫苗,免疫3次(0、7和30 d)后,约90%检测出高效价中和抗体;老年患者(65~75岁)在第180天进行第4次免疫后,60%抗体阴性患者阳转,中和抗体阳性率增加至90%[26];但临床Ⅲ期试验中期报告显示,该疫苗不能完成预防原发CDI的预期目标,终止在临床Ⅲ期试验[27]。
2 PF-06425090
与赛诺菲巴斯德二价类毒素疫苗Cdiffense 相比,辉瑞PF-06425090 疫苗采用基因工程技术构建TcdA和TcdB表达载体,并通过缺乏TcdA和TcdB基因的非孢子化艰难梭菌进行表达。该毒素同时采用基因修饰和化学法脱毒,以氢氧化铝作为佐剂[28]。2012年9月—2014年1月,192名50~85岁美国健康成人参与临床Ⅰ期试验。在第2次免疫后出现TcdA和TcdB 中和抗体,第7 个月产生预期浓度的TcdA和TcdB 中和抗体,类毒素组抗体滴度高于佐剂组。50~64与65~85岁组免疫效果相当。常见的不良反应为接种部位疼痛、头疼和疲劳[29]。2015 年7 月—2017 年3 月,对855 名年龄在65 ~ 85 岁之间的美国健康成人进行疫苗临床Ⅱ期试验,比较不同的接种剂量和不同免疫周期对TcdA 和TcdB 中和抗体的影响。临床Ⅱ期试验证明,该疫苗对65~85 岁健康美国成年人安全性、耐受性好,免疫原性强。200µg免疫剂量和月方案(0、1 和6 月)组产生的中和抗体效价更高[30]。2016 年2 月—2017 年2 月,该疫苗在日本进行临床Ⅰ期试验,也获得预期结果[31]。在临床Ⅲ期试验中(2017年3月—2021年12月),17 571名年龄≥50 岁健康成人参与,截至2022 年3 月1 日,基于次要终点,该疫苗在缩短病程和减轻疾病严重程度方面具有强大的潜在效应。
3 Bezlotoxumab
Bezlotoxumab 是由美国默克制药公司研发的人源化TcdB 单克隆抗体(MK-6072),用于预防艰难梭菌复发感染[32],目前已经完成临床Ⅲ期试验[33]。近期,JOHNSON 等[34]研究发现,单独使用Bezlotoxumab或联合actoxumab(KM-3415)均能有效降低B1 型艰难梭菌的复发率和死亡率。
4 VLA84疫苗
与类毒素疫苗不同,Valneva Austria VLA84 疫苗是一种含有TcdA 和TcdB 受体结合域(receptor binding domain,RBD)的嵌合蛋白,该疫苗可在异源表达系统中制备,无需培养艰难梭菌。在临床Ⅰ期试验(2010 年12 月— 2013 年5 月)中,佐剂对疫苗免疫原性的影响无差异,抗体能够中和VPI10463 产生的2 种毒素的活性[35]。目前该疫苗已完成临床Ⅱ期试验。
5 SYN-004(Ribaxamase)
SYN-004(Ribaxamase)是Synthetic Biologics 研发的第二代口服药β-内酰胺酶,旨在降解排泄至胃肠道的静脉注射β-内酰胺类抗生素,从而保护肠道微生物群,预防原发性艰难梭菌感染和抗生素相关性腹泻。第一代口服药P1A,主要是一种青霉素酶,对头孢菌素无活性[36]。SYN-004(Ribaxamase)扩大了降解谱,包括头孢菌素。临床Ⅱ期试验发现,412 名诊断为下呼吸道感染而接受静脉注射头孢曲松的住院患者中,安慰剂组艰难梭菌感染率为3.4%,而SYN-004(Ribaxamase)组为1%,证明降解抗生素可预防艰难梭菌感染[37]。
6 VP 20621
并非所有艰难梭菌均产生毒素,缺乏产生毒素基因的非产毒素艰难梭菌(non-toxigenicC.difficile,NTCD)也存在于医院环境和住院患者中,患者通常无症状。既往研究表明,NTCD在患者和仓鼠的胃肠道定植后,可预防产毒菌株引起的CDI[38]。根据这一生物学特征,Takeda/Shire 研制了NTCD M3 菌株(NTCD-M3)孢子疫苗VP 20621。该疫苗目前已完成临床Ⅱ期试验。经甲硝唑或万古霉素治疗后的CDI患者口服VP 20621 疫苗后,NTCD-M3 肠道定殖率为69%,其中NTCD-M3 肠道定殖成功的86 例中仅2 例(2%)复发CDI,而NTCD-M3肠道定殖不成功的39例患者中12例(31%)复发CDI。表明NTCD-M3定植肠道,占据肠道的生存环境,可有效阻止致病艰难梭菌定植,显著减少CDI复发[39]。
7 GSK2904545A
葛兰素史克研制的一种含有艰难梭菌F2 抗原GSK2904545A(疫苗方案未公布)在2019 年8 月进入临床Ⅰ期试验,目前尚未结束临床Ⅰ期试验。
8 挑战
对艰难梭菌疫苗的研究已超过20 年,但目前仍无许可的人用疫苗。尽管艰难梭菌类毒素疫苗可中和毒素,预防毒素引发的肠道症状,但具有局限性。既往研究表明,类毒素疫苗不能防止艰难梭菌在胃肠道定殖[40]。此外,也不能阻止艰难梭菌产孢子,因此可能增加无症状感染者的数量[41]。含有RBD 嵌合蛋白疫苗VLA84 具有1 个明显的缺陷,即缺乏位于毒素其他部位的中和抗原表位。此外,一些艰难梭菌菌株的变异,可能限制了该疫苗的有效免疫能力。在艰难梭菌毒素单克隆抗体Bezlotoxumab 的临床Ⅲ期试验中显著降低了复发/继发性CDI 的风险[33],预示着一个良好的研究方向,但同时也提出了一些问题:如何时接种该疫苗、如何在CDI 治疗中发挥作用等,均需进一步探讨。鉴于目前正在进行临床试验的候选疫苗的试验范围,在未来5 年内获得许可的艰难梭菌疫苗是可行的。但由于赛诺菲巴斯德类毒素疫苗Cdiffense 在临床Ⅲ期试验中的失败,提醒研发者需考虑改进现有疫苗方案。
