大青叶化学成分的研究
2023-09-19袁铭铭李柯城周雷罡周国平吴良发
袁铭铭,李柯城,2,代 敏,2,周雷罡,周国平*,吴良发*
(1.江西省药品检验检测研究院,国家药品监督管理局中成药质量评价重点实验室,江西省药品与医疗器械质量工程技术研究中心,江西 南昌 330029;2.江西中医药大学,江西 南昌 330004)
大青叶为十字花科草本植物菘蓝Isatis indigoticaFort.的干燥叶,具有利咽止痛、凉血消斑、清热解毒等功效,临床上主要用于痈肿、痄腮、发斑发疹、神昏、温病高热[1],具有抗病毒、抗氧化、抗菌、解热等作用[2-4],目前报道大青叶的化学成分主要分为生物碱、有机酸、黄酮、苷类等[5-7]。为进一步开发该中药,明确其药效物质基础,课题组对大青叶75%醇提物的正丁醇部位进行提取分离,共分离得到16 个化合物,除化合物9 外均为首次从菘蓝属植物中分离得到。
1 材料
UltiMate 3000 型高效液相色谱仪(美国赛默飞公司);Varian UNITY INOVA 600 MHz 型超导核磁共振仪(美国Varian 公司);旋转蒸发仪(瑞士步琪公司);Agilent 1260infinity II Prep 型制备液相色谱仪(美国Agilent 公司);ME204TE 型电子天平(瑞士梅特勒-托利多公司);Sephadex LH-20 凝胶(瑞典Amersham Biosciences 公司);YMC-C18柱(日本YMC 公司);薄层硅胶板、柱层析硅胶(青岛海洋化工厂)。甲醇、乙腈为色谱纯 (美国Sigma 公司);其他所用试剂均为分析纯;水为纯化水。
大青叶由江西药都仁和制药有限公司提供,经江西省药品检验检测研究院周国平主任中药师鉴定为菘蓝IsatisindigoticaFort.的干燥叶。
2 提取与分离
取大青叶18 kg 粉碎,经75%乙醇加热回流提取,提取液浓缩至无醇味后加水混悬,依次用石油醚(60~90 ℃)、乙酸乙酯、水饱和正丁醇进行萃取,得到正丁醇萃取物(620 g)。
正丁醇萃取物经大孔树脂D101 分离,以乙醇-水(0 ∶100~95 ∶5) 梯度洗脱,得10%乙醇部位(31.2 g)、50%乙醇部位(104 g)、75%乙醇部位(27.4 g)。
10%乙醇部位(30.8 g) 经硅胶柱分离,以二氯甲烷-甲醇(15 ∶1~1 ∶1) 梯度洗脱,合并洗脱液,得Fr.1~Fr.16。Fr.1 (333 mg) 经制备HPLC纯化,以甲醇-0.02% 三氟乙酸水(8 ∶92) 洗脱(体积流量10 mL/min,检测波长210 nm),得化合物1 (5 mg,tR=46.8 min)。Fr.6 (148 mg) 经制备HPLC 纯化,以甲醇-0.05%三氟乙酸水(2 ∶98) 洗脱(体积流量10 mL/min,检测波长210 nm),得化合物2 (30.4 mg,tR=66.2 min)、4(20.8 mg,tR=78.4 min)、5 (12.6 mg,tR=83.5 min)。Fr.8 经硅胶柱分离,以二氯甲烷-甲醇(13 ∶1~8 ∶1)梯度洗脱,合并洗脱液,得Fr.8-1~Fr.8-4,Fr.8-2 (172 mg) 经制备HPLC 纯化,以甲醇-0.05%三氟乙酸水(8 ∶92) 洗脱(体积流量10 mL/min,检测波长210 nm),得化合物3(13.7 mg,tR=55.0 min)。Fr.13 (1.90 g) 经硅胶柱分离,以二氯甲烷-甲醇(8 ∶1~4 ∶1) 梯度洗脱,合并洗脱液,得Fr.13-1~Fr.13-4,Fr.13-4(100 mg) 经制备HPLC 纯化,以甲醇-0.01%三氟乙酸水(18 ∶82) 洗脱(体积流量10 mL/min,检测波长210 nm),得化合物6 (30.5 mg,tR=41.4 min)。
50%乙醇部位(104 g) 经硅胶柱分离,以二氯甲烷-甲醇(2.5 ∶1) 洗脱,抽干溶剂,收集溶剂部分,再将固定相切成11 份,用甲醇洗脱,合并得Fr.A~Fr.F。Fr.A (4.2 g) 经硅胶柱分离,以二氯甲烷-甲醇(15 ∶1~6 ∶1) 梯度洗脱,合并洗脱液,得Fr.A-1~Fr.A-8。Fr.A-7 (130 mg) 经制备HPLC 纯化,以甲醇-0.02%三氟乙酸水(8 ∶92) 洗脱(体积流量10 mL/min,检测波长210 nm),得化合物7 (37 mg,tR=77.1 min)。Fr.B(14.3 g) 经硅胶柱分离,以二氯甲烷-甲醇(8 ∶1~2 ∶ 1) 梯度洗脱,合并洗脱液,得Fr.B-1~Fr.B-12。Fr.B-7 (270 mg) 经制备HPLC纯化,以乙腈-0.02%三氟乙酸水(14 ∶82) 洗脱(体积流量10 mL/min,检测波长210 nm),得化合物8 (47 mg,tR=65.8 min)、11 (11 mg,tR=102.3 min)。Fr.B-10 (430 mg) 经制备HPLC 纯化,以乙腈-0.02% 三氟乙酸水 (18 ∶82) 洗脱(体积流量10 mL/min,检测波长210 nm),得化合物9 (27 mg,tR=71.4 min)、10 (30 mg,tR=84.8 min)。Fr.D (8.4 g) 经硅胶柱分离,以二氯甲烷-甲醇(4 ∶1~1 ∶1) 梯度洗脱,合并洗脱液,得Fr.D-1~Fr.D-4,Fr.D-2 (370 mg) 经制备HPLC 纯化,以乙腈-0.02%三氟乙酸水(17 ∶83)洗脱(体积流量10 mL/min,检测波长210 nm),得化合物12 (27 mg,tR=74.5 min)。
75%乙醇部位(27.4 g) 经硅胶柱分离,以二氯甲烷-甲醇(25 ∶1~9 ∶1) 洗脱,合并洗脱液,得Fr.Ⅰ~Fr.Ⅵ。Fr.Ⅱ(58 mg) 经制备HPLC 纯化,以乙腈-0.05% 三氟乙酸水 (48 ∶52) 洗脱(体积流量10 mL/min,检测波长210 nm),得化合物13 (18 mg,tR=52.2 min)。Fr.Ⅳ(610 mg)经Sephadex LH-20 凝胶柱分离,合并得Fr.Ⅳ-1~Fr.Ⅳ-4;Fr.Ⅳ-2 (27 mg) 经制备HPLC 纯化,以乙腈-0.02%三氟乙酸水(23 ∶77) 洗脱(体积流量10 mL/min,检测波长210 nm),得化合物14(8 mg,tR=58.1 min);Fr.Ⅳ-3 (98 mg) 经制备HPLC 纯化,以甲醇-0.02%三氟乙酸水(40 ∶60)洗脱(体积流量10 mL/min,检测波长210 nm),得化合物15 (18 mg,tR=82.4 min);Fr.Ⅳ-4 (76 mg) 经制备HPLC 纯化,以乙腈-0.02% 三氟乙酸水(40 ∶60) 洗脱(体积流量10 mL/min,检测波长210 nm),得化合物16 (14 mg,tR=65.3 min)。
3 结构鉴定
化合物1:淡黄色油状,ESI-MSm/z:291.1[M+Na]+,分子式C17H32O2。1H-NMR (600 MHz,DMSO-d6)δ:5.33 (2H,m,H-2~3),2.23(2H,t,J=7.2 Hz,H-11),0.86 (3H,t,J=7.2 Hz,H-17);13C-NMR (150 MHz,DMSO-d6)δ:129.2 (C-2~3),26.2 (C-4~5),28.6 (C-6),28.2 (C-7),28.3 (C-8),28.4 (C-9),24.7 (C-10),34.7 (C-11),28.6 (C-12),21.7(C-13),28.7 (C-14),30.9 (C-15),13.6 (C-16~17)。以上数据与文献[8] 报道基本一致,故鉴定为(Z)-9-heptadecenoic acid。
化合物2:白色粉末,ESI-MSm/z:237.1[M+Na]+,分子式C10H14O5。1H-NMR (600 MHz,DMSO-d6)δ:6.89 (1H,s,H-2),6.70 (1H,d,J=8.0 Hz,H-6),6.67 (1H,d,J=8.1 Hz,H-5),4.33 (1H,d,J=6.2 Hz,H-7),3.74(3H,s,-OCH3),3.44 (1H,dd,J=11.0,3.9 Hz,H-9a);13C-NMR (150 MHz,DMSO-d6)δ:134.8 (C-1),111.8 (C-2),147.4 (C-3),145.7 (C-4),115.0 (C-5),120.0 (C-6),74.4(C-8),75.8 (C-8),63.5 (C-9),56.0 (-OCH3)。以上数据与文献[9] 报道基本一致,故鉴定为(7R,8S)-赤式-愈创木基丙三醇。
化合物3:白色粉末,ESI-MSm/z:355.2[M+Na]+,分子式C14H20O9。1H-NMR (600 MHz,DMSO-d6)δ:9.22 (1H,s,-OH),6.06 (2H,s,H-3,5),4.64 (1H,d,J=6.0 Hz,H-1'),3.68 (6H,s,2×OCH3),3.59 (1H,d,J=11.6 Hz,H-6a'),3.41 (1H,d,J=13.7 Hz,H-6b'),3.17 (1H,d,J=6.1 Hz,H-3'),3.12 (1H,t,J=7.9 Hz,H-4');13C-NMR (150 MHz,DMSOd6)δ:127.9 (C-1),153.6 (C-2,6),94.2(C-3,5),154.4 (C-4),103.9 (C-1'),74.61(C-2'),77.5 (C-3'),70.43 (C-4'),76.9 (C-5'),61.5 (C-6'),56.5 (2×OCH3)。以上数据与文献[10] 报道基本一致,故鉴定为2,6-二甲氧基-4-羟基-苯酚-1-O-β-D-吡喃葡萄糖苷。
化合物4:白色粉末,ESI-MSm/z:301.1[M-H]-,分子式C13H18O8。1H-NMR (600 MHz,DMSO-d6)δ:9.04 (1H,s,7-OH),6.89 (1H,d,J=8.7 Hz,H-6),6.39 (1H,d,J=2.7 Hz,H-3),6.22 (1H,dd,J=8.7,2.7 Hz,H-5),4.67 (1H,d,J=7.4 Hz,H-1'),3.69 (3H,s,2-OCH3),3.66 (1H,dd,J=11.8,2.1 Hz,H-6a'),3.45 (1H,dd,J=11.8,5.6 Hz,H-6b'),3.13 (1H,dd,J=9.7,8.3 Hz,H-4');13C-NMR (150 MHz,DMSO-d6)δ:39.1 (C-1),149.7 (C-2),101.2 (C-3),152.5 (C-4),105.7 (C-5),117.0 (C-6),100.6 (C-1'),73.1 (C-2'),76.7 (C-3'),69.5 (C-4'),76.5(C-5'),60.5 (C-6'),55.3 (2-OCH3)。以上数据与文献 [11] 报道基本一致,故鉴定为isotachioside。
化合物5:白色粉末,ESI-MSm/z:301.0[M-H]-,分子式C13H18O8。1H-NMR (600 MHz,DMSO-d6),δ:6.69 (1H,d,J=2.8 Hz,H-2),6.66 (1H,d,J=8.5 Hz,H-6),6.46 (1H,dd,J=8.6,2.8 Hz,H-5),4.67 (1H,d,J=7.7 Hz,H-1'),3.73 (3H,s,3-OCH3),3.71 (1H,dd,J=11.8,2.2 Hz,H-6'),3.45 (1H,dd,J=11.8,6.2 Hz,H-6'),3.31~3.25 (1H,m,H-5'),3.24 (1H,dd,J=8.0,8.8 Hz,H-3'),3.12 (1H,dd,J=9.8,8.7 Hz,H-4');13C-NMR (150 MHz,DMSO-d6)δ:141.8 (C-1),148.2 (C-2),102.9 (C-3),151.2 (C-4),108.4 (C-5),115.6 (C-6),102.2 (C-1'),73.8 (C-2'),77.2 (C-3'),70.4 (C-4'),77.5(C-5'),61.3 (C-6'),55.9 (3-OCH3)。以上数据与文献 [11] 报道基本一致,故鉴定为tachioside。
化合物6:白色粉末,ESI-MSm/z:406.2[M-H]-,分子式C19H33O9。1H-NMR (600 MHz,DMSO-d6)δ:5.92 (1H,dd,J=16.0,1.3 Hz,H-7),5.68 (1H,dd,J=15.9,5.9 Hz,H-8),4.37 (1H,d,H-10),4.00 (1H,t,J=11.6,4.3 Hz,H-4'),1.79 (1H,ddd,J=12.6,4.3,2.1 Hz,H-4eq),1.62 (2H,dd,J=12.0,4.4 Hz,H-4ax,2ax),1.42 (1H,ddd,J=12.2,4.3,2.1 Hz,H-2eq),1.14 (3H,d,J=6.3 Hz,H-10),1.10 (3H,s,H-13),1.02 (3H,s,H-11),0.74 (3H,s,H-12);13C-NMR (150 MHz,DMSO-d6)δ:40.03 (C-1),43.6 (C-2),71.9(C-3),41.9 (C-4),76.0 (C-5),77.3 (C-6),129.1 (C-7),135.3 (C-8),67.3 (C-9),24.9(C-10),27.4 (C-11),26.0 (C-12),27.2 (C-13),101.5 (C-1'),73.8 (C-2'),77.1 (C-3'),70.3 (C-4'),76.9 (C-5'),61.3 (C-6')。以上数据与文献[12] 报道基本一致,故鉴定为(3S,5R,6R,7E,9S)-megastigman-7-ene-3,5,6,9-tetrol 3-O-β-D-glucopyranoside。
化合物7:黄色粉末,ESI-MSm/z:723.2[M-H]-,分子式C33H40O18。1H-NMR (600 MHz,DMSO-d6)δ:7.56 (1H,d,J=15.8 Hz,H-7'),7.53 (1H,d,J=15.7 Hz,H-7),7.31 (1H,d,J=2.1 Hz,H-2‴),7.06 (1H,m,H-6‴),6.98(2H,s,H-2″,6″),6.70 (1H,d,J=7.1 Hz,H-5‴),6.52 (1H,d,J=15.9 Hz,H-8'),6.44(1H,d,J=15.9 Hz,H-8),5.81 (1H,d,J=8.4 Hz,H-1),4.93 (1H,t,J=9.0 Hz,H-2),4.08 (1H,d,J=7.5 Hz,H-1'),3.98 (1H,d,H-6b),3.92 (3H,s,3‴-OCH3),3.78 (6H,s,3″,5″-OCH3),3.39 (1H,dd,H-4),3.23(1H,dd,H-3'),2.95 (1H,dd,H-2');13C-NMR (150 MHz,DMSO-d6)δ:92.0 (C-1),72.7 (C-2),73.8 (C-3),69.3 (C-4),76.4(C-5),67.4 (C-6),146.0 (C-7),113.4 (C-8),164.9 (C-9),102.9 (C-1'),73.2 (C-2'),76.4 (C-3'),69.9 (C-4'),76.4 (C-5'),60.3(C-6'),146.0 (C-7'),113.4 (C-8'),165.7(C-9'),124.0 (C-1″),106.2 (C-2″),148.0(C-3″),138.8 (C-4″),147.4 (C-5″),106.5(C-6″),124.3 (C-1‴),110.9 (C-2‴),148.0(C-3‴),148.1 (C-4‴),114.6 (C-5‴),121.8(C-6‴),56.1 (3″,5″,3‴-OCH3)。以上数据与文献[13] 报道基本一致,故鉴定为6-O-β-Dglucopyranosy-β-D-(1-O-sinapoyl-2-O-feruloyl)glucopyranose。
化合物8:白色粉末,ESI-MSm/z:180.1[M+H]+,分子式C9H9NO3。1H-NMR (600 MHz,DMSO-d6)δ:11.32 (1H,s,7-OH),8.45(1H,d,J=8.3 Hz,H-3),7.97 (1H,d,J=7.2 Hz,H-6),7.54 (1H,t,J=7.8 Hz,H-4),7.11 (1H,t,J=7.6 Hz,H-5),2.12 (3H,s,-CH3);13C-NMR (150 MHz,DMSO-d6)δ:119.6(C-1),140.6 (C-2),117.0 (C-3),133.4 (C-4),122.2 (C-5),130.8 (C-6),168.2 (C-8),24.78 (C-9),169.5 (-COOH)。以上数据与文献[14] 报道基本一致,故鉴定为2-(乙酰胺基)-苯甲酸。
化合物9:白色粉末,ESI-MSm/z:223.1[M-H]-,分子式C11H12O5。1H-NMR (600 MHz,DMSO-d6)δ:12.17 (1H,s,-COOH),8.93(1H,s,-OH),7.50 (1H,d,J=15.9 Hz,H-7),6.98 (2H,s,H-2,6),6.42 (1H,d,J=15.9 Hz,H-8),3.80 (6H,s,2 × OCH3);13C-NMR (150 MHz,DMSO-d6)δ:124.4 (C-1),105.8 (C-2),147.8 (C-3),137.8 (C-4),147.8 (C-5),105.8 (C-6),144.6 (C-7),115.9 (C-8),167.8 (-COOH),55.9 (-OCH3)。以上数据与文献[15] 报道基本一致,故鉴定为芥子酸。
化合物10:白色粉末,ESI-MSm/z:385.5[M-H]-,分子式C17H22O10。1H-NMR (600 MHz,DMSO-d6)δ:β-isomer 7.64 (1H,d,J=15.8 Hz,H-7'),α-isomer 7.55 (1H,d,J=15.8 Hz,H-7'),7.03 (4H,s,H-2'α,6'α,2'β,6'β),6.58 (1H,d,J=15.8 Hz,H-8'),6.53 (1H,d,J=15.9 Hz,H-8'),5.48 (1H,d,H-1),4.26 (1H,d,J=7.8 Hz,H-1),4.19 (1H,dd,J=11.9,5.9 Hz,H-6α),3.98 (1H,dd,J=11.7,2.4 Hz,H-6β),3.61 (1H,dd,J=11.4,5.6 Hz,H-6α),3.79 (12H,s,4×OCH3),3.45(1H,dd,J=10.2,5.7 Hz,H-6β);13C-NMR(150 MHz,DMSO-d6)δ:α-isomer 94.2 (C-1),73.8 (C-2),72.6 (C-3),69.8 (C-4),69.3(C-5),63.5 (C-6),124.5 (C-1'),106.4 (C-2',6'),148.1 (C-3',5'),138.6 (C-4'),146.7 (C-7'),114.8 (C-8'),166.8 (C-9'),56.1 (3',5'-OCH3),β-isomer 103.1 (C-1),76.3 (C-2),76.5 (C-3),73.4 (C-4),76.4(C-5),68.2 (C-6),124.3 (C-1'),106.3 (C-2',6'),148.0 (C-3',5'),138.3 (C-4'),145.6 (C-7'),114.3 (C-8'),165.4 (C-9'),6.11 (3',5'-OCH3)。以上数据与文献[16] 报道基本一致,故鉴定为 4-O-sinapoyl-α/β-Dglucopyranose。
化合物11:白色粉末,ESI-MSm/z:777.2[M+Na]+,分子式C34H42O19。1H-NMR (600 MHz,DMSO-d6)δ:7.58 (1H,d,J=15.8 Hz,H-7″),7.56 (1H,d,J=15.8 Hz,H-7‴),7.07 (2H,s,H-2″,6″),7.03 (2H,s,H-2‴,6‴),6.64(1H,d,J=15.8 Hz,H-8″),6.54 (1H,d,J=15.9 Hz,H-8‴),5.30 (1H,d,H-1),4.60(2H,m,H-6,6b'),4.42 (1H,m,J=9.4,12.1 Hz,H-6b'),4.10 (1H,m,H-5),3.81(1H,t,H-5'),3.77 (12H,s,4 × OCH3);13C-NMR (150 MHz,DMSO-d6)δ:92.0 (C-1),70.6 (C-2),74.0 (C-3),69.7 (C-4),69.8(C-5),63.7 (C-6),61.2 (C-1'),105.2 (C-2'),77.5 (C-3'),74.8 (C-4'),77.6 (C-5'),67.8 (C-6'),124.3 (C-1″),106.6 (C-2″,6″),147.6 (C-3″),138.9 (C-4″),147.6 (C-5″),143.7 (C-7″),115.7 (C-8″),165.1 (C-9″),125.1 (C-1‴),106.7 (C-2‴,6‴),148.3 (C-3‴),139.1 (C-4‴),148.4 (C-5‴),145.7 (C-7‴),116.6 (C-8‴),166.2 (C-9‴),56.43 (-OCH3)。以上数据与文献 [17] 报道基本一致,故鉴定为6,6'-di-O-sinapoylsurcose。
化合物12:黄色粉末,ESI-MSm/z:755.1[M+H]+,分子式C34H42O19。1H-NMR (600 MHz,DMSO-d6)δ:7.60 (1H,d,J=15.7 Hz,H-7'),7.51 (1H,d,J=15.7 Hz,H-7),7.00 (4H,s,H-2,2',6,6'),6.54 (1H,d,J=15.9 Hz,H-8'),6.49 (1H,d,J=15.9 Hz,H-8),5.44(1H,d,J=8.3 Hz,H-1),4.85 (1H,dd,J=8.5,Hz,H-2),4.32 (1H,d,H-1'),3.75(12H,s,4 × OCH3);13C-NMR (150 MHz,DMSO-d6)δ:93.74 (C-1),73.0 (C-2),73.4(C-3),69.4 (C-4),75.9 (C-5),67.7 (C-6),102.7 (C-1'),72.1 (C-2'),75.8 (C-3'),68.9(C-4'),76.1 (C-5'),63.1 (C-6'),55.68 (4×OCH3),acyl 123.9 (C-1),105.9 (C-2),147.6(C-3,5),137.9 (C-4),106.0 (C-6),145.1(C-7),113.9 (C-8),164.9 (C-9),124.0 (C-1'),105.9 (C-2'),147.6 (C-3',5'),138.2(C-4'),106.0 (C-6'),146.3 (C-7'),114.4(C-8'),166.3 (C-9')。以上数据与文献 [13]报道基本一致,故鉴定为6-O-β-D-glucopyranosy-β-D-(1-O-sinapoyl-2-O-sinapoyl) glucopyranose。
化合物13:黄色针状物,ESI-MSm/z:279.1[M+H]+,分子式C16H22O4。1H-NMR (600 MHz,DMSO-d6)δ:7.70 (4H,dd,J=5.9,3.3 Hz,H-2~3,5~6),4.23 (4H,t,H-9,9'),0.92 (6H,t,J=7.4 Hz,H-12,12');13C-NMR (150 MHz,DMSO-d6)δ:132.2 (C-1,4),132.0 (C-2,6),129.1 (C-3,5),167.5 (C-7,7'),65.5 (C-9,9'),30.5 (C-10,10'),19.1 (C-11,11'),14.0(C-12,12')。以上数据与文献[18] 报道基本一致,故鉴定为对苯二甲酸二丁酯。
化合物14:黄色粉末,ESI-MSm/z:249.2[M+H]+,分子式C16H8O3。1H-NMR (600 MHz,DMSO-d6)δ:8.48 (1H,dt,J=8.0,0.9 Hz,H-8),8.32 (1H,dt,J=7.9,1.1 Hz,H-6'),7.95 (1H,d,J=7.9 Hz,H-3'),7.94 (1H,t,J=7.7 Hz,H-5),7.88 (1H,m,H-4'),7.86(1H,t,J=7.7,1.4 Hz,H-7),7.78 (1H,m,H-5'),7.48 (1H,t,J=7.5,1.0 Hz,H-6);13C-NMR (150 MHz,DMSO-d6)δ:145.5 (C-2),158.2 (C-3),182.9 (C-4),125.2 (C-5),127.4(C-6),138.2 (C-7),117.5 (C-8),146.5 (C-9),122.7 (C-10),123.8 (C-1'),146.9 (C-2'),130.4 (C-3'),135.6 (C-4'),130.3 (C-5'),127.4 (C-6'),172.0 (C-7')。以上数据与文献[19] 报道基本一致,故鉴定为胭木二酮。
化合物15:白色晶体,EI-MSm/z:163.1[M+H]+,分子式C10H10O2。1H-NMR (600 MHz,DMSO-d6)δ:7.41 (2H,d,J=7.0 Hz,H-2,6),7.32 (2H,t,J=7.7 Hz,H-3,5),7.23(1H,t,J=7.1 Hz,H-4),6.49 (1H,d,J=15.4 Hz,H-7),6.31 (1H,dt,J=16.9,7.0 Hz,H-8),3.19 (2H,d,J=7.0 Hz,H-9);13C-NMR (150 MHz,DMSO-d6)δ:136.6 (C-1),128.5 (C-2,6),127.2 (C-3,5),125.9 (C-4),123.1 (C-7),132.1 (C-8),37.71 (C-9),172.5 (C-10)。以上数据与文献[20] 报道基本一致,故鉴定为反式-4-苯基-3-丁烯酸。
化合物16:白色无定形固体,ESI-MSm/z:238.2 [M + H]+,分子式C11H15N3O3。1H-NMR(600 MHz,pyridine-d5)δ:12.00 (1H,s,2-NH),8.87 (1H,d,J=8.1 Hz,H-3),8.49(1H,d,J=8.0 Hz,H-6),7.53 (1H,t,J=7.9 Hz,H-4),7.08 (1H,t,J=7.4 Hz,H-5),5.59 (1H,s,3-NH),0.79 (3H,t,J=7.4 Hz,H-1');13C-NMR (150 MHz,pyridine-d5)δ:132.1 (C-1),135.0 (C-2),122.9 (C-3),121.3 (C-4),133.5 (C-5),118.4 (C-6),13.6(C-1'),19.0 (C-2'),31.0 (C-3'),40.5 (C-4'),153.9 (C=O)。以上数据与文献[21] 报道基本一致,故鉴定为N-butyl-N'-(2'-nitrophenyl)urea。该化合物为首次从植物中发现,其1H-NMR、13C-NMR数据见表1,结构见图1。

图1 化合物16 结构Fig.1 Structure of compound 16
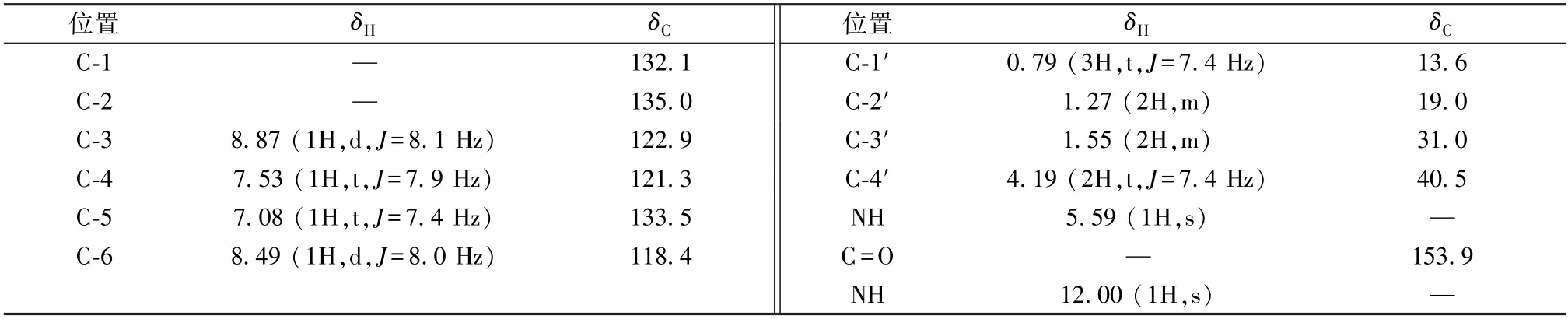
表1 化合物16 的1H-NMR、13C-NMR 数据Tab.1 1H-NMR and 13C-NMR data on compound 16
4 结论
本研究从大青叶75% 醇提物的正丁醇萃取部位共分离得到16 个化合物,包括13 个有机酸类、1 个生物碱类、1 个木脂素类、1 个单萜。有机酸类成分具有抗炎镇痛、抗血栓、抑菌作用[22-24];其中化合物1 具有抗真菌活性[8],化合物10 具有抗自由基活性[16],化合物15 具有保护农作物的作用(防止稻瘟病、炭疽病)[20]。其余化合物药理活性尚不明确。本研究通过对大青叶的化学成分研究,丰富了其物质基础,为后续大青叶活性物质筛选及临床应用研究提供参考,从而更好的开发利用该药用资源。
