两性霉素B脂质体引起低钾血症的危险因素分析Δ
2023-09-14符馨尹张纯萍郑秀芬林小茹刘启兵海南医学院第一附属医院药学部海口5700文昌市人民医院药学部海南文昌57399
符馨尹 ,张纯萍 ,郑秀芬 ,林小茹 ,刘启兵 (.海南医学院第一附属医院药学部,海口 5700;.文昌市人民医院药学部,海南 文昌 57399)
两性霉素B属于多烯类抗真菌药物,通过作用于真菌细胞膜的麦角固醇,引起细胞膜通透性改变,使细胞内钾离子、核苷酸和氨基酸等物质外漏,最终导致真菌细胞死亡,具有疗效稳定、不易诱导真菌耐药、抗菌谱广等优点,临床上常用于侵袭性真菌感染的治疗[1—2]。两性霉素B 脂质体较普通两性霉素B 的不良反应发生率更低,且疗效与后者相当,因此根据美国感染病学会相关指南,除了尿路及颅内感染,由两性霉素B 脂质体代替其普通制剂治疗侵袭性真菌感染[2]。但两性霉素B脂质体的剂量选择范围大、疗程长,其不良反应发生率仍不容忽视(20%~40%)[3—4],高发的不良反应包括低钾血症、肾功能异常、低血压、过敏反应、呕吐、输液反应、肝功能异常等[5—6]。
低钾血症是两性霉素B 脂质体常见的不良反应之一,据文献报道,两性霉素B 脂质体引起严重低钾血症的发生率为12%~51%[7]。低钾血症不仅会引起电解质失衡,严重情况下还可造成心律失常等心脏毒性,甚至引起心脏骤停[8]。本研究通过回顾性分析2012年1月至2021年12月在海南医学院第一附属医院(以下简称“我院”)住院并使用两性霉素B脂质体的患者资料,总结该药导致低钾血症的发生情况、该药的使用情况及患者补钾治疗情况,并分析引起该种不良反应的危险因素,以此为临床合理用药提供参考。
1 研究对象与方法
1.1 试验设计及纳入/排除标准
本研究为回顾性分析。通过电子病案系统调取2012年1月至2021年12月在我院住院期间使用两性霉素B脂质体的患者资料,根据患者在使用两性霉素B脂质体以后是否出现低钾血症分为低钾血症组和正常组。根据《中华人民共和国临床用药须知》对低钾血症的定义进行诊断分级[9]:血清钾浓度低于3.5 mmol/L 即为低钾血症;其中,血清钾浓度为3.0~3.5 mmol/L 为轻度低钾血症,2.5~<3.0 mmol/L为中度低钾血症,2.5 mmol/L以下为重度低钾血症。同时,计算两性霉素B脂质体引起低钾血症的发生率:发生率=出现低钾血症患者例数/纳入研究所有患者例数×100%。研究起点为两性霉素B 脂质体治疗当天,终点为结束两性霉素B 脂质体治疗1 周。本研究方案已通过我院医学伦理委员会审查,批件号为2020(科研)第(154)号。
本研究的纳入标准为:(1)使用两性霉素B 脂质体连续治疗天数≥3 d的患者;(2)年龄≥14岁;(3)治疗过程中使用两性霉素B脂质体的剂量在说明书范围内。
本研究的排除标准为:(1)临床资料信息不完整者;(2)治疗过程中未连续使用两性霉素B脂质体者。
1.2 数据收集
1.2.1 患者一般资料
记录纳入研究患者的性别、年龄、体重、吸烟史、饮酒史、治疗前血清钾浓度、低钾血症严重程度、基础肾功能水平、感染部位及菌种、饮食情况、联合用药情况。基础肾功能水平以血清肌酐水平表示,并按照公式计算肌酐清除率[10]。饮食情况分为流质饮食、普食及禁食。联合用药情况分为联用影响血清钾的药物和联用抗真菌药物,前者包括呋塞米、甘露醇、万古霉素、糖皮质激素、胰岛素等,后者包括卡泊芬净、氟康唑、伏立康唑等。
1.2.2 两性霉素B脂质体使用情况
本研究对患者使用两性霉素B 脂质体的治疗情况进行了详细记录,用以评价患者治疗后出现的低钾血症是否与两性霉素B 脂质体的使用有关。记录内容包括纳入研究患者使用两性霉素B脂质体的累积剂量、维持剂量、最大日剂量、治疗天数。
1.2.3 钾剂补充情况
记录纳入研究患者的每日补钾剂量、治疗时出现低钾血症的时间、总补钾天数等数据。每日补钾剂量指患者每日接受的口服、静脉以及营养制剂中总的钾含量,单位以g计算。治疗前已出现低钾血症的患者如开始两性霉素B脂质体治疗后血清钾浓度恢复正常,后续再次出现药物相关的低钾血症,需记录治疗过程中出现低钾血症的时间;如治疗过程中持续出现低钾血症,则不记录该项内容。
1.3 统计学处理
使用SPSS 26.0软件对数据进行统计处理。正态分布的计量资料以±s表示,非正态分布的计量资料以中位数(四分位数间距)[M(IQR)]表示;正态分布且方差齐性资料的组间比较采用t检验及单因素方差分析,非正态分布或方差不齐资料的组间比较采用非参数检验。计数资料以频数(例)或率(%)表示,组间比较采用χ2检验。检验水准α=0.05。
将纳入分析的患者信息进行共线性检验,将符合共线性检验的危险因素应用二元Logistic回归分析进行单因素分析,同时将单因素分析中P≤0.20 的变量纳入多因素回归分析,计算比值比(odds ratio,OR)及其95%置信区间(confidence interval,CI)。
2 结果
2.1 两组患者一般资料比较
共纳入符合上述纳入与排除标准的患者121 例,其中出现低钾血症的患者有60例,纳入低钾血症组,其余61例纳入正常组。两组患者间一般资料比较,差异无统计学意义(P>0.05),具有可比性。结果见表1。
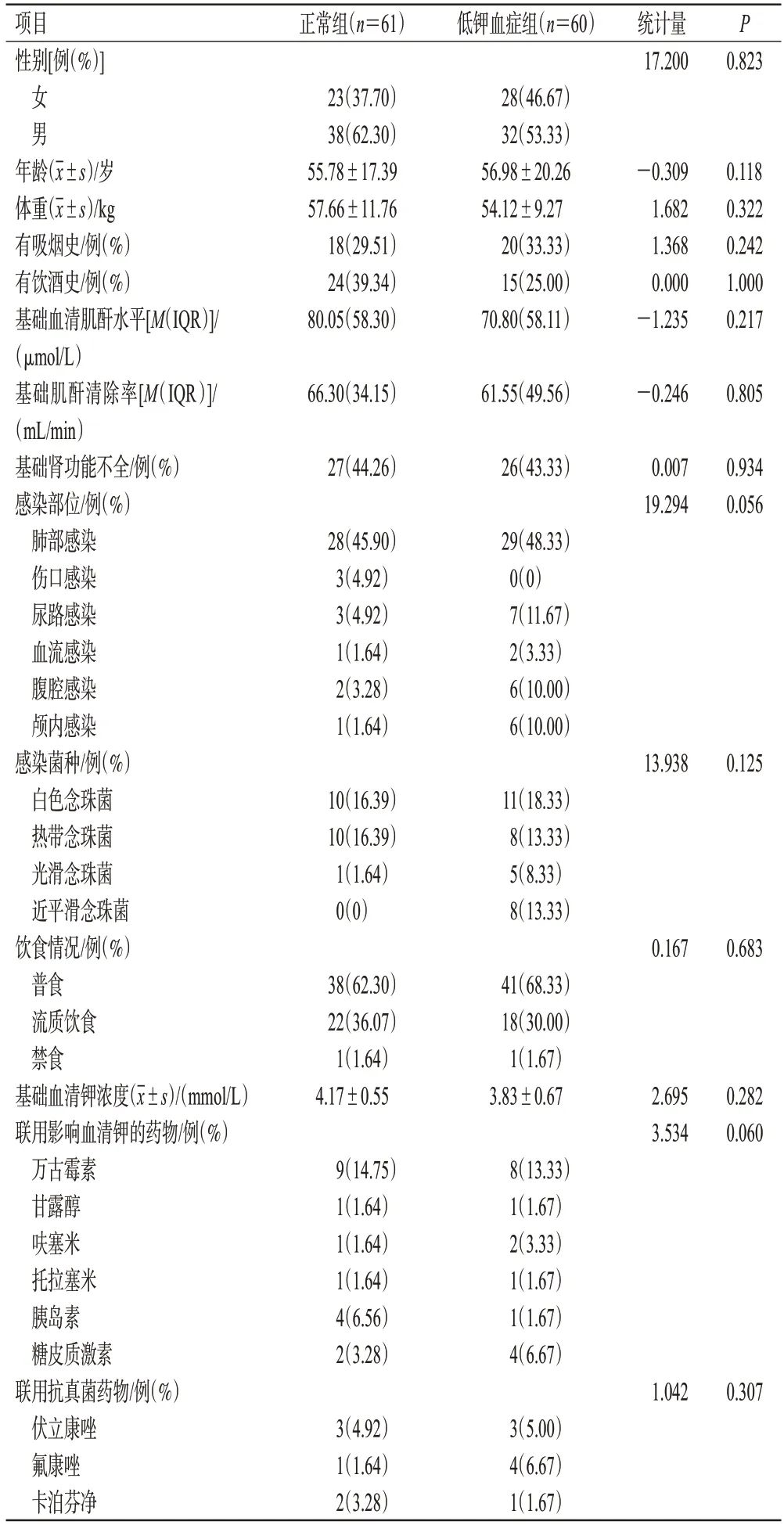
表1 两组患者一般资料比较
2.2 低钾血症发生情况
正常组患者中,基础有低钾血症的患者有2例,均为轻度低钾血症。而在低钾血症组患者中,基础有低钾血症的患者有18例,包括轻度低钾血症13例、中度4例、重度1例。使用两性霉素B脂质体引起低钾血症的发生率为34.71%(42/121),包括轻度低钾血症者15例、中度18例、重度9例;同时存在有基础肾功能不全的患者26例。
2.3 两组患者使用两性霉素B脂质体的情况比较
低钾血症组患者使用两性霉素B 脂质体的维持剂量、累计剂量均显著高于正常组,治疗天数显著长于正常组(P<0.05)。重度低钾血症组患者的最大日剂量显著高于正常组(P<0.05)。结果见表2。
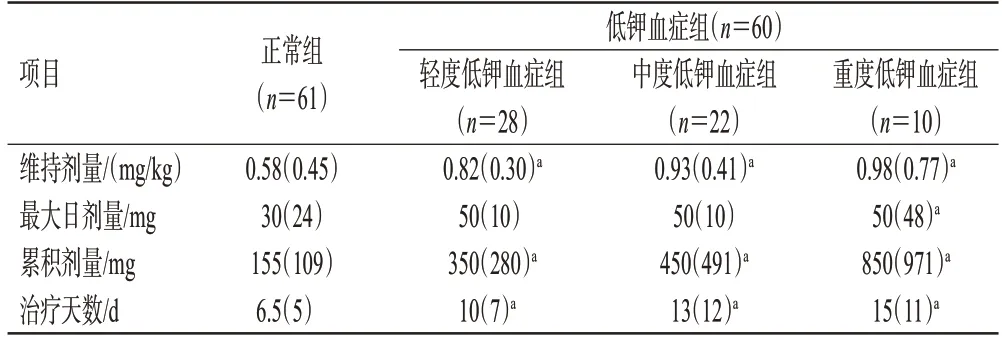
表2 两组患者使用两性霉素B 脂质体的情况比较[M(IQR)]
2.4 两组患者钾剂补充情况比较
121 例患者中,有99 例(81.82%)在应用两性霉素B脂质体的同时进行了补钾治疗,其中仅应用氯化钾注射液治疗者有26 例(26.26%),仅应用氯化钾缓释片治疗者有3 例(3.03%),仅应用氯化钾口服溶液治疗者有21例(21.21%),同时应用氯化钾注射液和口服溶液者有35例(35.35%),同时应用氯化钾注射液和缓释片者有8例(8.08%),同时应用氯化钾口服溶液和缓释片者有1 例(1.01%),3 种钾剂剂型均应用者有5 例(5.05%)。治疗过程中未应用钾剂者有22例(18.18%)。
从钾剂使用情况来看,低钾血症组患者治疗时出现低钾血症的时间显著长于正常组(P<0.05);中、重度低钾血症组患者每日补钾剂量显著高于正常组(P<0.05);中度低钾血症组患者的总补钾天数显著长于正常组(P<0.05)。结果见表3。
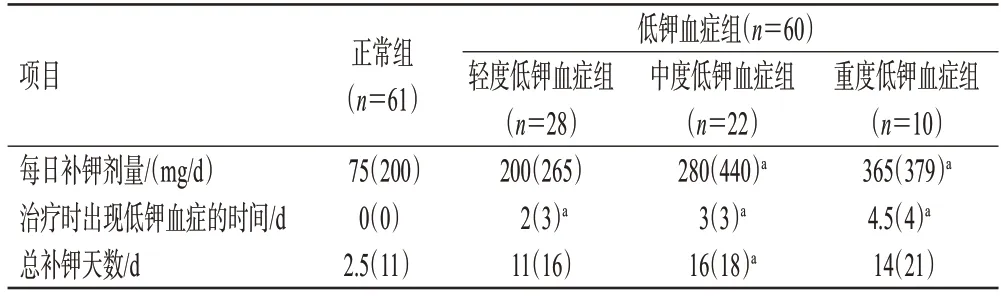
表3 两组患者钾剂补充情况比较[M(IQR)]
2.5 两性霉素B脂质体引起低钾血症的危险因素分析
2.5.1 单因素分析结果
在进行Logistic 回归分析之前,对本研究收集的14个影响因素(表4)进行共线性检验,结果显示,方差膨胀因子均小于10,表明纳入的影响因素之间不存在明显的共线性,提示所有纳入的影响因素均有意义。将所有影响因素纳入单因素分析,结果显示,两性霉素B 脂质体累积剂量≥200 mg和治疗天数≥5 d对两性霉素B脂质体引起低钾血症有显著影响(P<0.05)。

表4 两性霉素B脂质体引起低钾血症的单因素分析结果(例)
2.5.2 多因素分析结果
将单因素分析结果中P≤0.20的因素纳入多因素分析。结果显示,累积剂量≥200 mg、基础低钾血症、治疗天数≥5 d、体重<50 kg 均为引起两性霉素B 脂质体发生不同程度低钾血症的独立危险因素。结果见表5。
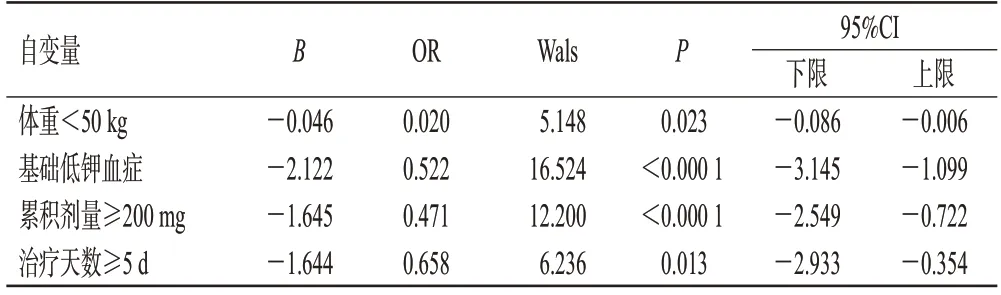
表5 两性霉素B脂质体引起低钾血症的多因素分析结果
3 讨论
3.1 两性霉素B脂质体引起低钾血症的机制和发生率
两性霉素B 引起低钾血症的原因与肾小管的酸中毒反应有关,酸中毒可干扰远端肾小管上皮细胞,导致细胞膜的通透性改变,使尿中钾离子排泄增加[11]。两性霉素B 脂质体相较于两性霉素B 拥有复杂的双层药物包封膜,可阻止两性霉素B被裂解酶水解从而增加进入感染部位的药量,起到在真菌感染部位浓集的作用,进而减少肾毒性,且引起低钾血症的发生率相对更低[12—13]。两性霉素B引起低钾血症的发生率高达75%~90%,而两性霉素B 脂质体可降低至12%~51%[7,14—15]。本研究中,两性霉素B 脂质体引起低钾血症的发生率(34.71%)与文献报道相近,但在使用该药期间依然要密切监测血清钾水平及肾功能指标变化情况。
3.2 两性霉素B脂质体引起低钾血症的危险因素
3.2.1 基础低钾血症
基础低钾血症是本研究得到的独立危险因素之一。目前,国内外仅有1项研究提及将治疗前7 d出现低钾血症的患者进行补钾治疗后再给予两性霉素B 脂质体治疗[16]。该研究结果显示,治疗前给予充足钾剂补充的患者,发生心力衰竭的风险更低,且使用两性霉素B 脂质体治疗后平均血清钾水平相对更高,后续药物引起低钾血症的持续时间更短,提示基础低钾血症可能与两性霉素B 脂质体治疗后引起低钾血症相关[16]。因此,患者在使用两性霉素B 脂质体治疗前应及时纠正基础低钾血症,从而降低治疗期间低钾血症的发生率。
3.2.2 联合用药
国外有研究显示,联用导致肾功能损伤的药物是两性霉素B脂质体引起低钾血症的独立危险因素,这些药物包括阿米卡星、万古霉素、他克莫司、环孢素等[17]。本研究也将联合用药作为危险因素之一进行考察,但组间差异无统计学意义。考虑原因可能与本研究中联合用药的患者例数较少有关。
3.2.3 两性霉素B脂质体的剂量与治疗天数
根据药品说明书和文献研究结果,两性霉素B脂质体不良反应的发生与剂量呈正相关性,累积剂量、治疗天数与低钾血症有相关性[18—20]。使用两性霉素B引起的低钾血症多发生于累积剂量达到500 mg以上,需要每天额外补充2~9 g 氯化钾来纠正的患者[21]。本研究结果显示,累积剂量≥200 mg 和治疗天数≥5 d 是两性霉素B脂质体引起低钾血症的独立危险因素;并且从本研究结果也可看出,与正常组比较,低钾血症组患者使用两性霉素B脂质体的维持剂量和累积剂量更高、治疗时间更长。因此,当经评估后将给予患者两性霉素B脂质体超过200 mg的累积剂量时,应注意低钾血症的发生。
3.2.4 体重
体重<50 kg 作为两性霉素B 脂质体引起低钾血症的独立危险因素暂未见研究报道,但因两性霉素B脂质体需根据患者体重调整给药剂量,因此体重与给药剂量密切相关。有研究提出,女性是引起两性霉素B脂质体致低钾血症的危险因素[17];因女性体重相对男性普遍偏低,因此该结论可能也与体重有一定关系,但该研究并未将体重列为危险因素进一步分析。
3.2.5 补钾治疗
本研究还评价了两性霉素B 脂质体使用期间钾剂的补充情况。从研究结果上看,与正常组比较,低钾血症组患者每日补钾剂量更高、总补钾天数更长。但本研究中的补钾方案均为对症补充,少有预防性补钾治疗。有研究提出,在开始采用两性霉素B脂质体治疗后给予钾剂补充是改善低钾血症的独立危险因素[7]。本研究将是否在开始采用两性霉素B 脂质体治疗的同时给予补钾剂列为危险因素之一进行分析,未得到显著性结果,分析原因可能为:(1)本研究患者基础伴有低钾血症的程度以轻度为主;(2)患者单日补钾量低;(3)在两性霉素B 脂质体开始治疗的同时进行补钾治疗的人数少。关于如何在使用两性霉素B 脂质体的同时进行补钾治疗,有研究提出:基础伴有低钾血症的患者初始血清钾浓度<2.83 mmol/L 是两性霉素B 脂质体治疗时出现低钾血症的独立危险因素,因此当初始开启两性霉素B脂质体治疗时,将基础血清钾浓度补充至>3 mmol/L(中度低血钾以上)可有效预防低钾血症的发生[19]。
3.3 研究局限性
本研究具有以下局限性:(1)本研究为回顾性分析,且研究的数据来自单家医院,可能存在患者资料单一、样本量较小等因素。(2)本研究无法对患者血清钾补充方式进行干预,患者均未经过系统的补钾治疗,因此无法明确哪种血清钾补充方式可以显著改善两性霉素B脂质体引起的低钾血症。下一步拟针对这些不足设计前瞻性试验以探讨血清钾补充方式的合理性。
综上所述,两性霉素B脂质体引起低钾血症的发生率较高,累积剂量≥200 mg、基础低钾血症、治疗天数≥5 d 和体重<50 kg 是该药引起低钾血症的独立危险因素。针对存在以上危险因素的患者,建议在开始使用两性霉素B脂质体治疗前将血清钾补充至正常水平,给药期间密切监测血清钾变化,以减少低钾血症的发生。
