同位素稀释-液相色谱-串联质谱法测定奶粉中五氯苯酚
2023-09-13李锦清许庆鹏
綦 艳,李锦清,李 聪,许庆鹏
(广东产品质量监督检验研究院,广东 顺德 528300)
五氯苯酚(又名五氯酚)及其钠盐五氯酚钠(又名五氯酚酸钠)是持久性环境污染物[1],常用作杀虫剂,皮革、木材防腐剂,农业除草剂以及吸血虫中间宿主钉螺的灭杀等[2-4]。五氯苯酚及其钠盐化学性质稳定,难降解,可在环境中扩散传播和在食物链中蓄积[5],通过环境或食物链进入动植物和人体内,当人体内五氯苯酚及其钠盐蓄积到一定量后可能会导致内分泌紊乱、致癌、致畸和诱发人体器官病变等[6-8]。五氯苯酚及其钠盐已成为重点监控的环境污染物之一,被多个国家禁用或限制使用[9]。环境中五氯苯酚及其钠盐的扩散传播可能造成的食品污染问题也引起了人们的高度重视。我国国家食品安全监督抽检实施细则(2019年版)将水产品、畜禽肉及其副产品中五氯苯酚及其钠盐作为必检项目,农业农村部公告第250号[10]规定食品动物中不得检出五氯苯酚及其钠盐。
五氯苯酚及其钠盐的检测方法以气相色谱法[11-13]、气相色谱-质谱联用法[14-19]、液相色谱-串联质谱(liquid chromatography-tandem mass spectrometry,LC-MS/MS)法[20-23]为主。五氯苯酚沸点约为310 ℃,难气化,分子结构中5 个氯原子的作用使得酚羟基极性较强,在气相色谱柱上保留能力强、难洗脱、色谱峰拖尾、峰形差、灵敏度低,一般采用乙酸酐将五氯苯酚衍生为五氯苯乙酸酯,然后用气相色谱法和气相色谱-质谱联用法检测,使之获得较好的峰形和较高的检测灵敏度,但衍生化操作繁琐,衍生条件难控制,而且由于五氯苯酚的酚羟基两边有氯基团,对衍生化起阻碍作用,不利于衍生化。LCMS/MS测定五氯苯酚及其钠盐无需衍生化,方法简单、灵敏度高,但容易受到基质抑制作用影响,导致定量结果不准确。为降低基质抑制作用,需对样品进行净化,常用的净化方法有阴离子交换固相萃取法或QuEChERS法。阴离子交换固相萃取法步骤多、较繁琐、效率低,不利于大批量样品快速检测,而QuEChERS法具有简单、快速、经济、高效等优点,适用于大批量样品快速检测,广泛应用于食品中农药残留和兽药残留检测。
奶粉是由液体牛奶经浓缩、干燥等加工步骤制成,使牛奶中可能存在的痕量五氯苯酚及其钠盐被浓缩富集,对人体的危害性更大。目前鲜见有针对奶粉中五氯苯酚残留量检测的标准或文献报道,相关风险监测尚未开展,因此建立奶粉中五氯苯酚的检测方法十分必要。GB 23200.92—2016《动物源性食品中五氯酚残留量的测定液相色谱-质谱法》[24]为食品中五氯苯酚的检测提供了依据,然而该方法存在前处理步骤繁琐、耗时长、易受复杂基质干扰,回收率低等不足,而且该方法适用范围未包括奶粉基质。因此,本研究建立QuEChERS萃取,Captiva EMR-Lipid脂质去除净化柱净化,基质匹配-同位素稀释内标法结合LC-MS/MS法测定奶粉中五氯苯酚的分析方法,缩短样品前处理时间、简化样品前处理过程、降低基质效应、提高大批量样品的检测效率,弥补奶粉基质中五氯苯酚检测方法缺失,以期为开展相关风险监测提供技术支持。
1 材料与方法
1.1 材料与试剂
乙腈(色谱纯)美国Thermo Fisher公司;甲醇(色谱纯)美国Tedia公司;甲酸、乙酸铵(均为色谱纯)上海安谱实验科技股份有限公司;无水硫酸镁(分析纯)天津市致远化学试剂有限公司;氢氧化钾、氢氧化钠(均为分析纯)上海阿拉丁生化科技股份有限公司;实验室用一级水符合GB/T 6682—2008《分析实验室用水规格和试验方法》要求;五氯苯酚的甲醇标准溶液(质量浓度为1000 μg/mL)、五氯苯酚-13C6标准品(纯度98.0%)北京曼哈格生物科技有限公司;Captiva EMR-Lipid脂质去除净化柱(300 mg/3 mL)、聚四氟乙烯针式滤头(polytetrafluoroethylene,PTFE,规格0.22 μm/13 mm)美国Agilent公司。
1.2 仪器与设备
Exion LC AD/SCIEX Triple Quad 4500 LC-MS/MS仪(配电喷雾离子源(electrospray ionization,ESI))美国AB SCIEX公司;5804R高速冷冻离心机 德国Eppendorf公司;MV-3000多位涡旋振荡器 广东晋元科技有限公司;FV64全自动智能氮吹仪 广州得泰仪器科技有限公司;Milli-Q去离子水发生器 美国Millipore公司;JJ500Y电子天平(精度0.01 g)福州华志科学仪器有限公司;MS105DU电子天平(精度0.1 mg)梅特勒-托利多科技(中国)有限公司;JP-C300超声波清洗机 广州吉普超声波电子设备有限公司;可调单道移液器 美国Thermo Fisher公司。
1.3 方法
1.3.1 同位素标准溶液的配制
称取五氯苯酚-13C6标准品约5 mg,置于10 mL容量瓶中,用甲醇溶解并定容至刻度,配得五氯苯酚-13C6储备液质量浓度为500 μg/mL,-16~-20 ℃条件下保存。吸取1.00 mL五氯苯酚-13C6储备液置于100 mL容量瓶中,用甲醇稀释并定容至刻度,配得标准品中间液质量浓度为5 μg/mL,-16~-20 ℃条件下保存。吸取1.00 mL五氯苯酚-13C6标准品中间液置于10 mL容量瓶中用甲醇稀释至刻度,配得五氯苯酚-13C6的标准品使用液质量浓度为0.5 μg/mL,-16~-20 ℃条件下保存。
1.3.2 标准曲线的配制
用甲醇将质量浓度为1000 μg/mL的五氯苯酚标准溶液逐级稀释,配制质量浓度为1 μg/mL的标准品中间液和质量浓度分别为0.1、0.01 μg/mL的五氯苯酚标准品使用液,-16~-20 ℃条件下保存。精密吸取适量五氯苯酚标准品中间液或标准品使用液以及五氯苯酚-13C6标准品使用液,用空白奶粉基质提取液稀释,配成五氯苯酚-13C6质量浓度均为5 μg/L以及质量浓度范围为0.2~150 μg/L的五氯苯酚标准工作曲线,用LC-MS/MS测定。
1.3.3 样品提取
称取经混合均匀的奶粉样品2 g(精确至0.01 g)置于50 mL聚丙烯离心管中,加入100 μL质量浓度为0.5 μg/mL的五氯苯酚-13C6标准工作液,加入10 mL一级水充分溶解奶粉,然后加入200 μL质量浓度为5 g/100 mL的氢氧化钾溶液或氢氧化钠溶液,摇匀后置于40~50 ℃水浴振荡器中振荡水解30 min,冷却后加入5.0 mL乙腈,用多位涡旋振荡器以2200 r/min涡旋振荡5 min,加入500 μL甲酸,摇匀,静置10 min,加入1 g无水硫酸镁后立即摇匀,继续用多位涡旋振荡器以2200 r/min涡旋10 min,以8000 r/min离心3 min,收集上层清液(乙腈层)作为待净化液。
1.3.4 样品净化
吸取待净化液约3 mL转移至Captiva EMR-Lipid脂质去除净化柱中,控制待净化液流出速率约为1 mL/min,弃去前1.5 mL流出液,收集后段流出液,吸取500 μL流出液置于离心管中,然后加入500 μL一级水,涡旋混匀,用PTFE过滤,供LC-MS/MS检测。
1.3.5 色谱条件
色谱柱:Waters ACQUITY BEHC18色谱柱(100 mm×2.1 mm,1.7 μm);流动相A:甲醇;流动相B:5 mmol/L乙酸铵溶液(含0.05%甲酸);柱温:25 ℃;进样量:15 μL。梯度洗脱程序:0~1.5 min,55% A、45% B;1.5~2.0 min,55%~85% A、45%~15% B;2.0~8.0 min,85% A、15% B;8.0~9.0 min,85%~55% A、15%~45% B;9.0~10.0 min,55% A、45% B。
1.3.6 质谱条件
电离源ESI-;数据采集:多反应监测(multiple reaction monition,MRM)模式;电喷雾电压-4500 V;脱溶剂温度550 ℃;气帘气压力30 psi;雾化气压力45 psi;干燥气压力45 psi。化合物保留时间、离子对、去簇电压、碰撞能量、驻留时间见表1。
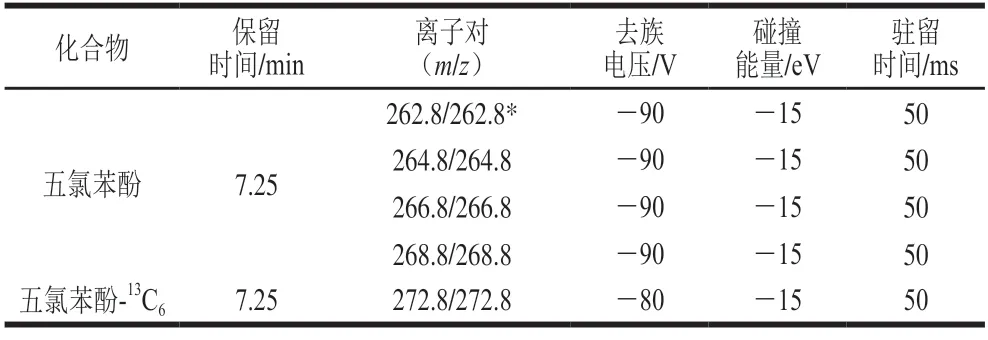
表1 五氯苯酚和五氯苯酚-13C6质谱参数Table 1 MS parameters of pentachlorophenol and pentachlorophenol-13C6
2 结果与分析
2.1 质谱方法优化
五氯苯酚分子中氯原子存在35Cl和37Cl同位数,在ESI-下,五氯苯酚和五氯苯酚-13C6分别监测到m/z相差为2的多个母离子(Q1)峰,如图1、2所示。五氯苯酚母离子质量数分别为262.8、264.8、266.8、268.8、270.8;五氯苯酚-13C6母离子质量数分别为268.8、270.8、272.8、274.8、276.8。对上述各个母离子进行碎裂,均未监测到任何子离子(Q3)碎片,分析其原因可能是五氯苯酚和五氯苯酚-13C6分子结构对称(图1、2),共轭性强,结构十分稳定,难以碎裂产生特征子离子碎片。
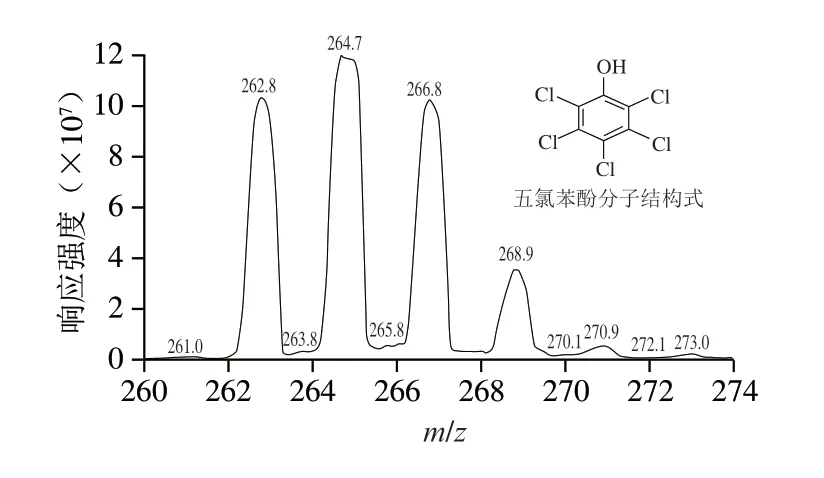
图1 五氯苯酚母离子(Q1)图谱Fig.1 Parent ion (Q1) spectrum of pentachlorophenol
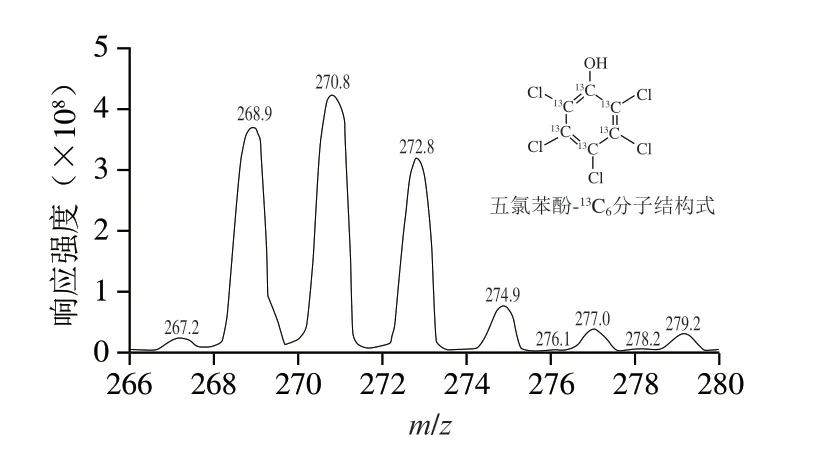
图2 五氯苯酚-13C6母离子(Q1)图谱Fig.2 Parent ion (Q1) spectrum of pentachlorophenol-13C6
有文献报道[25],五氯苯酚碎裂后产生质量数为35的氯离子碎片,但氯离子质量数低,容易受杂质离子干扰,同时也难以保证氯离子碎片在每次检测中都具有稳定的重复性。本实验选择离子对m/z262.8/262.8、264.8/264.8、266.8/266.8、268.8/268.8作为五氯苯酚监测离子,与田春霞等[26]的研究和GB 23200.92—2016一致。通过优化锥孔电压和碰撞能量后m/z264.8/264.8响应最高,但实际样品检测中发现该离子MRM图显示杂峰较多,m/z262.8/262.8杂峰最少,如图3所示。因此,选择m/z262.8/262.8作为定量离子对,其余离子作为定性离子,符合欧盟EC657/2002对串联三重四极杆质谱进行化合物定性鉴别要求。由于五氯苯酚和内标五氯苯酚-13C6存在相同质量数的母离子m/z268.8、270.8,为避免干扰定量,五氯苯酚-13C6选择m/z272.8/272.8离子对的峰面积参与计算,其余离子作为定性离子。优化后的质谱参数见表1。
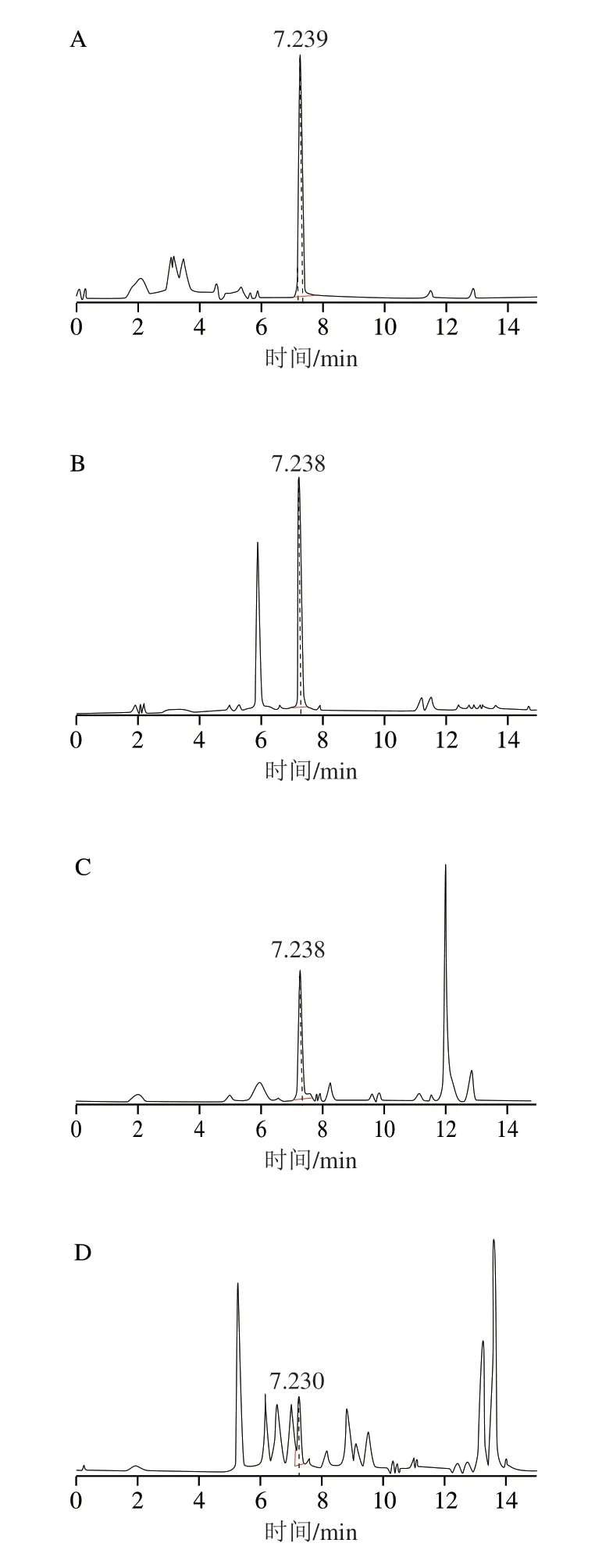
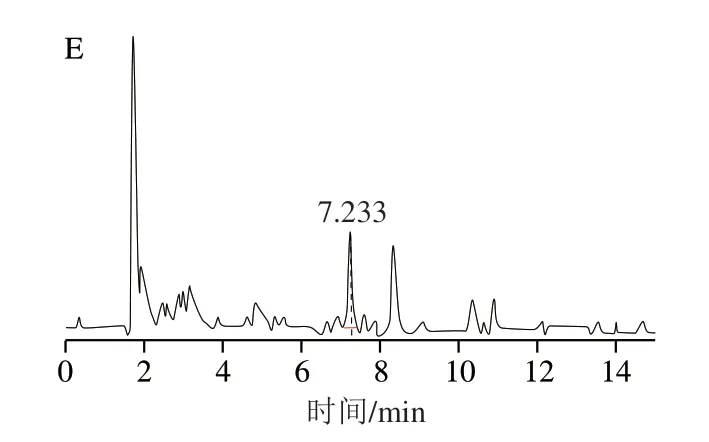
图3 基质匹配标准品(10 μg/L)的提取离子色谱图Fig.3 Extracted ion chromatogram of matrix matching standard solution (10 μg/L)
2.2 前处理方法选择与优化
2.2.1 提取条件优化
五氯苯酚含酚羟基呈酸性,其pKa值为4.93,在酸性条件下呈分子态,易溶于甲醇、乙腈等有机溶剂;在碱性条件下呈离子态,溶于甲醇、乙腈,更易溶于水[27],因此,利用五氯苯酚与五氯苯酚钠可相互转化的性质可提高萃取回收率。由于有机试剂不能溶解奶粉样品,无法形成分散性好的溶液,因此,只能萃取样品表面的五氯苯酚,无法有效萃取奶粉颗粒内部的五氯苯酚,导致检测结果不准确。本实验先以5 倍于奶粉质量的水体积充分溶解奶粉,破坏奶粉颗粒,释放奶粉中可能存在的待测化合物,然后通过酸水解法或碱水解法使可能以结合态形式存在的待测化合物转化为游离态,再进一步用有机试剂提取,使检测结果更准确。甲醇或乙腈均可作为提取试剂和蛋白沉淀剂,但乙腈的萃取回收率和蛋白沉淀效果优于甲醇,因此,本实验选择乙腈作为提取试剂和蛋白沉淀剂。
为避免同位素稀释法经内标折算后不能体现方法的回收率差异,除特殊说明外,本实验涉及的回收率比较均采用基质匹配外标法定量,以此确定最佳的实验条件,最终形成最优的同位素稀释样品前处理方法。
采用空白奶粉样品添加五氯苯酚5 µg/kg,比较酸水解法和碱水解法的回收率差异。酸水解法是用甲酸替代氢氧化钾或氢氧化钠溶液,其余步骤按1.3.3节操作;碱水解法完全按1.3.3节操作。结果表明,碱水解法比酸水解法回收率高约25%~35%,且重复性更好。其原因可能是部分五氯苯酚与奶粉中含有羧基(—COOH)或氨基(—NH2)的物质相互作用[28],形成了结合态,碱水解法可以将结合态、分子态等形式存在的待测化合物充分转化为易溶于水的五氯苯酚钠,有利于充分提取,回收率更高,重复性更好;酸水解法对结合态存在的待测化合物作用不明显,回收率偏低。因此,本实验选择碱水解法。
2.2.2 QuEChERS方法优化
QuEChERS法[29]萃取与固相萃取法相比,更简单、更高效、成本更低、重复性更好,同时具备萃取和初步净化样品作用,避免了固相萃取法步骤繁琐[30]、耗时长、堵塞柱子以及重复性不稳定等缺点,本实验优先选择QuEChERS法萃取,适用于大批量样品快速检测。
QuEChERS萃取常用的盐析试剂有无水硫酸镁、无水硫酸钠、乙酸钠、氯化钠等。在优化的实验条件下,比较无水硫酸镁、无水硫酸钠、乙酸钠、氯化钠对五氯苯酚萃取回收率的影响,以基质匹配外标法定量计算回收率,结果表明,无水硫酸镁作盐析试剂时,回收率最高。进一步比较无水硫酸镁添加量为1、2、3、4 g对回收率的影响。结果表明,当溶解奶粉的水与无水硫酸镁添加量比例为5∶1(mL/g)时,回收率最佳;当无水硫酸镁添加量超过该比例时,回收率有所下降,这可能是由于过量无水硫酸镁加入瞬间局部水分被迅速吸收,形成的颗粒物吸附五氯苯酚。
多次萃取可提高目标化合物的回收率,但前处理耗时长,需要消耗更多有机试剂。本实验使用同位素稀释内标法检测,仅需QuEChERS法萃取一次,回收率达到90%以上,操作简单、显著缩短样品前处理时间,有利于大批量样品快速检测。
2.2.3 样品净化
奶粉样品含有大量蛋白质、约16%脂肪以及约1%~3%磷脂。QuEChERS法同时起到萃取和去除无机盐、水溶性杂质等净化作用,但脂肪和磷脂也会被乙腈提取出来,这些杂质对五氯苯酚检测起基质抑制作用,需进一步净化。Captiva EMR-Lipid脂质去除净化柱[31]可同时去除乙腈提取液中脂肪和磷脂,有效降低基质抑制,与GB 23200.92—2016的MAX固相萃取柱净化相比,整个净化过程省略了活化、淋洗、洗脱等步骤,简化净化流程,直接收集流出液即完成净化操作,显著提高前处理效率,且样品加标绝对回收率比GB 23200.92—2016高约10%~15%,因此,选择采用Captiva EMR-Lipid脂质去除净化柱对样品提取液作进一步净化。
用空白基质提取液配制相同质量浓度的标准溶液,分别用尼龙66(材质为聚己二酰己二胺)和聚四氟乙烯材质的有机系针式滤头过滤,比较不同材质滤头对五氯苯酚的吸附作用。结果表明,尼龙66有机系针式滤头对五氯苯酚有吸附,五氯苯酚损失约30%~35%;聚四氟乙烯有机系针式滤头对五氯苯酚无吸附。其原因可能是尼龙66滤膜材质的胺基(—NH—)与五氯苯酚的酚羟基结合,使部分五氯苯酚保留在滤膜上,导致五氯苯酚损失,但将过滤后的滤液用同一个滤头再过滤一次,损失率下降至10%左右,可能是由于再次过滤能将保留在滤膜上的五氯苯酚洗脱下来;聚四氟乙烯不存在与五氯苯酚发生反应的基团,所以五氯苯酚无损失。因此,选择使用PTFE材质的有机系针式滤头过滤。
2.3 方法学考察
2.3.1 基质效应
除不加同位素内标外,按照优化的前处理方法对添加五氯苯酚3 μg/kg的奶粉样品进行6 个平行测定,制得样品待测液,考察基质效应。分别用乙腈、甲醇、空白基质提取液配制标准工作曲线,分别对样品待测液进行外标法定量,计算平均回收率,见表2。结果表明,以乙腈、甲醇配制的标准工作曲线定量的平均回收率分别为33%、25%;以空白基质提取液配制的标准工作曲线定量(基质匹配外标法定量)的回收率为63%;表明存在较强的基质抑制作用。为降低或消除基质抑制作用,本实验采用空白基质提取液与同位素稀释内标法相结合配制标准工作曲线进行定量,平均回收率为90%,有效降低基质抑制作用,使定量结果更加准确、可靠。由于五氯苯酚未能碎裂形成子离子碎片,实际样品的提取离子色谱图显示杂峰较多(图4),采用同位素稀释内标法可提高定性鉴别准确度。
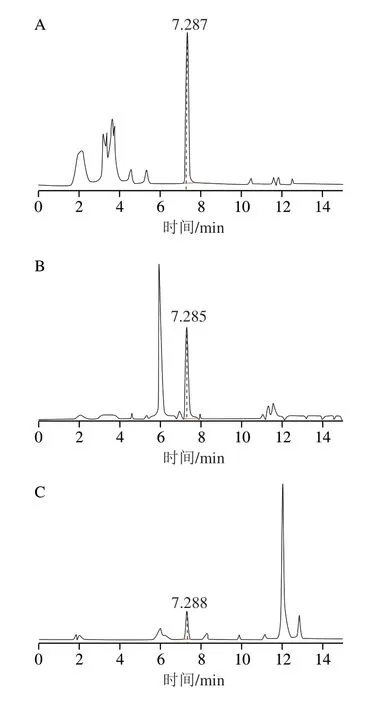
图4 空白奶粉样品添加15.0 μg/kg标准品的提取离子色谱图Fig.4 Extracted ion chromatogram of spiked blank sample at 15.0 μg/kg

表2 标准曲线配制方法对回收率的影响Table 2 Influence of standard curve preparation methods on PCP recovery
2.3.2 线性关系、检出限和定量限
五氯苯酚的空白基质提取液-同位素稀释内标标准工作曲线在质量浓度0.2~150 μg/L范围内,具有良好的线性关系,线性方程为y=0.24256x+0.04470,相关系数r=0.9960。以不含五氯苯酚的奶粉样品添加标准品的方式考察方法检出限和定量限,分别以定量离子3 倍信噪比和10 倍信噪比响应值对应的含量作为方法检出限和定量限,方法检出限和定量限分别为0.5、1.5 μg/kg。在1.3.5节和1.3.6节条件下测定,获得的基质匹配标准品(10 μg/L)的提取离子色谱图(图3)。
2.3.3 回收率和精密度
在2 g(精确至0.01 g)不含五氯苯酚的奶粉样品中分别添加质量浓度为0.1 μg/mL五氯苯酚标准溶液30、60 μL,1 μg/mL五氯苯酚标准溶液30 μL(添加水平分别相当于样品中五氯苯酚含量为1.5、3.0、15.0 μg/kg),然后在每个样品中添加100 μL质量浓度为0.5 μg/mL的五氯苯酚-13C6标准溶液,每个添加水平平行测定6 次,空白基质提取液-同位素稀释内标法定量,考察方法回收率和精密度,结果见表3,平均回收率为90.3%~119.2%,相对标准偏差(relative standard deviation,RSD)为5.8%~7.5%,回收率和精密度均符合GB/T 27404—2008附录F之F.1回收率和F.3精密度要求,满足奶粉中五氯苯酚残留量检测要求。1.3.5节和1.3.6节条件下测定,获得的空白奶粉样品添加15.0 μg/kg标准品的提取离子色谱图。
2.4 实际样品测定
采用建立的方法对45 批奶粉样品(婴幼儿配方奶粉1 段15 批次,2段10 批次,3段10 批次,中老年奶粉10 批次)进行检测,均未检出五氯苯酚。
3 结论
本实验建立QuEChERS萃取,Captiva EMR-Lipid脂质去除净化柱净化,基质匹配-同位素稀释内标法结合LC-MS/MS测定奶粉中五氯苯酚的分析方法。在水浴加热条件下,采用碱水解法将奶粉中可能以结合态、分子态形式存在的待测化合物充分转化为易溶于水的五氯苯酚钠,在乙腈存在条件下,用甲酸将五氯苯酚钠转化为不溶于水、易溶于乙腈的五氯苯酚,再以无水硫酸镁为盐析试剂的QuEChERS法萃取,用Captiva EMR-Lipid脂质去除净化柱对样品提取液作进一步净化,净化液与水按1∶1比例混合后,用LC-MS/MS测定,以基质匹配-同位数稀释内标标准工作曲线法定量,本方法具有操作简单、快速、回收率高、准确可靠等优点,弥补了奶粉中五氯苯酚残留量检测方法缺失,为开展相关风险监测提供技术支持。
