非钠盐替代对薏米淀粉-肌原纤维蛋白复合凝胶特性的影响及风味分析
2023-09-13冯雅梅蔡茜茜伍久林黄建联汪少芸
陈 旭,冯雅梅,蔡茜茜,伍久林,黄建联,汪少芸,
(1.福州大学生物科学与工程学院,福建 福州 350108;2.福州海洋研究院海洋食品研发中心,福建 福州 350108;3.福建省冷冻调理水产品加工重点实验室,福建 厦门 361022;4.安井食品集团股份有限公司,福建 厦门 361022)
肌原纤维蛋白(myofibrillar protein,MP)是肌肉中具有重要生物学功能的盐溶性蛋白质,其热诱导凝胶特性是影响凝胶类肉糜制品品质的决定因素。相比于其他肉糜类凝胶,鱼糜凝胶性能往往较差,通过添加不同多糖,如淀粉、亲水胶体、膳食纤维等形成复合凝胶,可改善鱼糜凝胶特性[1]。薏米俗称“药王米”,具有免疫调节、降血糖、抗炎等功效,再加上其药食同源性的特点,使薏米的研究与开发备受关注,其中薏米淀粉(coix seed starch,CSS)占薏米质量的60%左右[2]。CSS作为一种新型的小颗粒淀粉资源,由于颗粒的结构、直链和支链淀粉含量、溶胀特性、糊化特性等特性,使其在工业应用中发挥独特的作用[3]。NaCl是生产以盐溶MP凝胶为基础的鱼糜产品的必要条件,但考虑到Na+摄入过多会导致高血压、心血管疾病等健康问题,因此采取降低NaCl含量策略以改善鱼糜产品的健康特性[4]。但在加工过程中,直接降低NaCl含量可能导致鱼糜凝胶的劣化。为了在低钠盐条件下仍能保持鱼糜凝胶特性,可用一些对人体有益的阳离子来替代部分Na+,如利用K+、Mg2+、Ca2+等,以维持或改善鱼糜的凝胶性质,使鱼糜产品更适合食用。因此,本研究旨在探究CaCl2、MgCl2和KCl替代NaCl后,其对低钠盐CSS-MP复合凝胶特性的影响,以期为开发低钠盐复合鱼糜凝胶制品提供理论参考。
1 材料与方法
1.1 材料与试剂
冷冻真鲷鱼为福建省水产研究所提供。CSS为实验室提取制备。
氯化钠、氯化钙、氯化镁、氯化钾、十二水合磷酸氢二钠、二水合磷酸二氢钠、氢氧化钠、五水合硫酸铜、乙二胺四乙酸 西陇科学有限公司;过硫酸铵 中国医药集团有限公司。
1.2 仪器与设备
HH-S6数显恒温水浴锅 河南金博仪器制造有限公司;FJ 300-SH高速分散均质机 上海沪析实业有限公司;WSD-3A色差计 北京康光光学仪器有限公司;LYNX6000高速离心机、Multiskan FC多功能酶标仪德国Thermo Fisher Scientific公司;MCR302旋转流变仪奥地利安东帕有限公司;Fluoromax-4荧光光谱仪HORIBA科学仪器事业部;TS-5000Z电子舌 日本Insent公司;PEN3.5电子鼻 德国AIRSENSE公司。
1.3 方法
1.3.1 MP的提取
参考陈旭等[4]方法。以鱼肉-缓冲液料液比1∶4(g/mL)混合(缓冲液含0.1 mol/L NaCl、10 mmol/L 磷酸盐、1 mmol/L乙二醇双(2-氨基乙基醚)四乙酸、2 mmol/L MgCl2,pH 7.0)。用均质机均质分散60 s并于4 ℃、6000×g离心,收集沉淀。重复上述操作3 次。再将得到的沉淀悬浮于0.1 mol/L NaCl溶液中均质、离心洗涤3 次后即得实验用MP。所有操作过程均在低温(0~4 ℃)进行。最终获得的MP于4 ℃贮存备用,48 h内用完。利用双缩脲法测定MP浓度。
1.3.2 CSS的提取
参考Cardoso等[5]的方法提取,利用冷冻干燥机进行冻干,得实验用CSS。
1.3.3 低钠盐CSS-MP复合凝胶的制备
取上述提取的MP,在CaCl2、MgCl2和KCl最佳添加量的单因素研究基础之上[6],分别用添加不同量的氯盐配制成对照组(3% NaCl)、CaCl2替代组(2.0% NaCl+1.0%CaCl2)、MgCl2替代组(2.5% NaCl+0.5% MgCl2)、KCl替代组(1.5% NaCl+1.5% KCl),并将各组MP质量浓度固定为120 mg/mL,即为不同盐离子含量的MP溶液。再分别向对照组和不同氯盐替代组添加4% CSS,充分搅拌均匀后,即得低钠盐CSS-MP复合溶胶。将复合溶胶置于25 mL的烧杯中并在80 ℃水浴30 min形成凝胶,之后立即置于冰水浴中冷却至室温(24~26 ℃),在4 ℃放置12 h后,再进行指标检测。
1.3.4 凝胶强度的测定
参考Zhuang Xinbo等[7]的方法测定。将CSS-MP复合凝胶切割成边长为2 cm左右的正方体。测试参数:直径0.5 cm的圆柱型探头,测前速率2.0 mm/s,测中速率1.0 mm/s,测后速率2.0 mm/s,触发力5 g。以最大触发力作为凝胶强度值。
1.3.5 持水力的测定
参考Yang Kun等[8]用离心法测定。将复合凝胶置于50 mL离心管中,称量为m1。4 ℃、6000×g离心30 min,将离心管倒转,用滤纸吸去残留水,称量为m2。记录空离心管质量m0。持水力按式(1)计算:
1.3.6 流变学特性测定
参考Zhou Tiantian等[9]的方法。设置流变仪为振荡模式,使用50 mm平行板,将低钠盐CSS-MP复合溶胶样品分别置于上下板间距为1 mm的空隙中,硅油覆盖在板的边缘。测试频率为1 Hz,应变为2%。以恒定的升降温速率进行动态温度梯度扫描测试,记录样品升温-恒温-降温全过程的储能模量(G’)和损耗模量(G”)的变化。
1.3.7 表面疏水性的测定
根据结合的疏水发色团溴酚蓝(bromophenol blue,BPB)含量确定MP的表面疏水性[10]。参考陈旭等[4]样品处理方法,用含有不同浓度的氯盐溶液等比例稀释CSS-MP复合溶液。取1 mL稀释后的样液与0.2 mL BPB(1 mg/mL)混合后旋涡振荡10 min。6000×g离心15 min后取上清液,稀释10 倍,通过595 nm紫外扫描分光光度计检测BPB结合情况确定MP的表面疏水性。按式(2)计算:
1.3.8 巯基含量的测定
参考陈旭等[4]方法。取0.5 mL的样液(MP质量浓度为5 mg/mL),加入4.5 mL缓冲液(含8 mol/L尿素、0.01 mol/L乙二胺四乙酸、0.1 mol/L磷酸二氢钠)和100 µL Ellman试剂(0.01 mol/L 5,5’-二硫代双(2-硝基苯甲酸)、0.01 mol/L磷酸二氢钠)。充分混合反应,于波长412 nm处测定吸光度。除使用无尿素缓冲液外,活性巯基含量的测定方法如上所述。巯基含量按式(3)计算:
式中:A412nm为样品在412 nm处的吸光度;D为稀释倍数;C为MP质量浓度/(mg/mL);13600为摩尔消光系数(L/(mol·cm))。
1.3.9 同步荧光光谱分析
参照Pan Xingren等[11]的方法,将MP溶液稀释为1 mg/mL,然后使用荧光光谱仪进行测定。激发波长为295 nm,狭缝宽为2.5 nm,波长扫描范围为300~450 nm。设置激发波长和发射波长的波长差Δλ为15 nm和60 nm。
1.3.10 扫描电子显微镜分析
参考Wang Limei等[12]方法,凝胶样品用3%戊二醛溶液固定24 h,磷酸盐缓冲液漂洗3 次,然后用35%、50%、75%、85%、95%和100%乙醇溶液进行梯度脱水,再利用冷冻干燥机对凝胶样品进行冻干。将冻干样品镀上一层金,置于扫描电子显微镜台上观察。
1.3.11 感官评分
参考宋春勇[13]和任佳怿等[14]方法,选择在校的食品专业学生对凝胶样品进行感官评分。评价指标包括色泽、气味、滋味和组织形态。
1.3.12 电子鼻分析
参考陈小冬等[15]方法,用分析天平称量10.0 g凝胶样品装入容量为30 mL的顶空瓶中,在室温下静置平衡1 h后,进行电子鼻分析。
1.3.13 电子舌分析
参考杨峰等[16]方法,取30.0 g凝胶样品,加入200 mL去离子水,用高速均质机匀浆5 min,之后于4 ℃,8000×g离心15 min,取上清液过滤成无沉淀无油液体,收集滤液进行电子舌检测分析。
1.4 数据处理
采用IBM SPSS Statistics 20对结果进行统计分析,通过Duncan多重范围检验进行方差分析确定均值之间的差异显著性,结果以表示,P<0.05,差异显著,采用Origin 2018软件进行作图。
2 结果与分析
2.1 凝胶强度和持水力的测定结果
如图1所示,与对照组的凝胶强度179.8相比,CaCl2、MgCl2和KCl替代组的凝胶强度分别降低至178.4、164.8和172.3。相比之下,含有1.0% CaCl2的复合凝胶表现出较好的凝胶强度,与对照组相比无显著差异。这可能与低浓度NaCl不利于MP的展开有关,因为低钠盐会抑制肌球蛋白从致密结构中溶出,并且Ca2+、Mg2+、K+的存在可能导致MP的水结合能力较弱,不利于蛋白质与蛋白质、蛋白质-多糖之间的相互作用,最终影响了蛋白质的结合性能,降低了CSS-MP复合凝胶的质地特性[17]。Ge Ge等[18]发现当KCl取代量为25%时,凝胶强度显著增强(P<0.05),而当KCl取代量为50%时,凝胶强度降低,表明低浓度K+能促进MP的展开,而过高浓度的K+则会对凝胶强度产生不利影响。S—S键和疏水相互作用有助于形成稳定、不可逆、规则的凝胶网络。然而,不同盐离子引起过度的相互作用会导致蛋白质聚集,阻碍肌球蛋白的交联,使凝胶强度降低。虽然有文献报道Ca2+会导致蛋白质结构发生改变,对MP的凝胶强度产生消极影响[19],但适量的Ca2+替代Na+对MP的凝胶强度影响不显著。
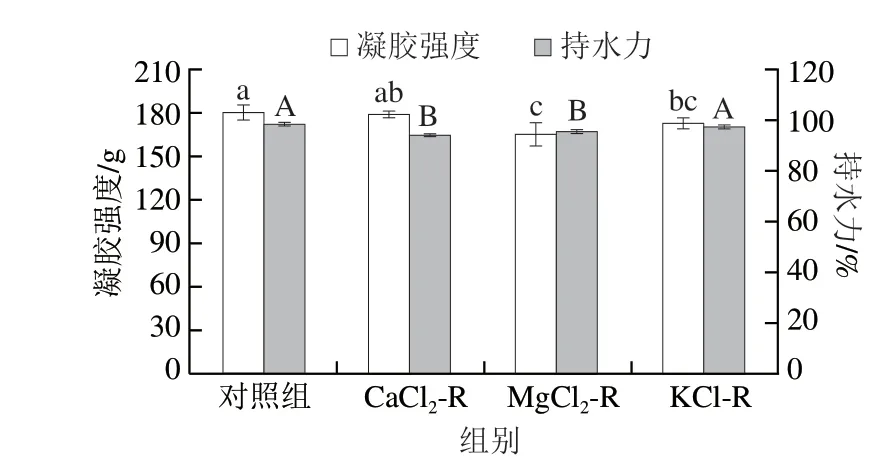
图1 氯盐对低钠盐CSS-MP复合凝胶强度和持水力的影响Fig.1 Effect of different chloride salts on the strength and WHC of low sodium CSS-MP composite gel
低钠盐条件下复合凝胶的持水力均有所降低,与凝胶强度具有相似的变化趋势,说明凝胶强度与持水力密切相关。与KCl替代组相比,CaCl2替代组和MgCl2替代组持水力显著低于对照组(P<0.05)。这与Zheng Jiabo等[20]的研究结果类似。由于盐离子与蛋白质的强结合作用,NaCl可激活蛋白质,对于MP凝胶的持水能力有着重要的作用,而Mg2+和Ca2+的存在阻止了Cl-渗透到蛋白质分子中,对蛋白质的持水能力产生负面影响[19-21]。此外,不同盐对MP构象的影响不同,如K+比Na+具有更弱的电场和更低的静电作用,这可能导致肌球蛋白的溶解度和总蛋白的理化性质不同[22],最终影响了蛋白凝胶的持水能力。
2.2 流变学特性分析
G’值表示黏弹性材料在变形过程中的存储能量,反映了试样的弹性特性[23]。热诱导MP凝胶网络的形成是一个多步骤的过程,包括蛋白质变性或天然蛋白质空间结构的部分展开,然后通过形成二硫键或非共价键的相互作用进行聚集,包括静电、氢键和疏水相互作用等[24]。由图2可知,在25~80 ℃的升温阶段,CaCl2和MgCl2替代组与对照组的凝胶行为不同。对照组的G’值最初增长缓慢,在38.4 ℃时达到峰值,随后迅速下降到49.7 ℃时的最小值,这与疏水相互作用和二硫键的形成有关。进一步加热至80 ℃后,G’值又迅速增加,而CaCl2和MgCl2替代组则相反,在50~80 ℃的加热过程中,G’显著下降(P<0.05)。G’的增加表明MP凝胶化或弹性蛋白网络开始形成,对照组、CaCl2、MgCl2、KCl替代组在32.1、30.5、31.6 ℃和31.2 ℃时开始形成凝胶。在升温阶段,与Na+和K+相比,Ca2+和Mg2+的存在大大降低了G’,这可能是由于不同盐离子对MP溶解性的差异,而KCl渗透可以增强G’,因为它的扩散速度比其他盐更快[22]。另外,盐离子也会影响蛋白质分子间的静电相互作用,从而影响热成胶过程中蛋白质-蛋白质、淀粉-蛋白质之间的相互作用,导致流变学性质的变化[25]。在恒温(80 ℃)和降温阶段(80~25 ℃),大量氢键的形成加强了凝胶网络,不同处理组的G’显著升高,最终CaCl2替代组复合凝胶的流变特性明显优于对照组和MgCl2、KCl替代组。原因可能是在CSS-MP复合凝胶体系中,Ca2+的添加有利于在已形成的凝胶网络基础上,进一步促进蛋白聚集交联,使凝胶网络结构变得更加致密有序。这与前面观察到的凝胶质构特性趋势一致。

图2 氯盐对低钠盐CSS-MP复合凝胶G’的影响Fig.2 Effect of different chloride salts on the storage modulus (G’) of low sodium CSS-MP composite gel
2.3 氯盐对低钠盐CSS-MP复合凝胶表面疏水性的影响
如图3所示,不同氯盐部分替代NaCl对CSS-MP复合凝胶表面疏水性有显著的影响(P<0.05)。CaCl2替代组和MgCl2替代组的表面疏水性显著高于对照组,而KCl替代组的表面疏水性显著低于对照组(P<0.05)。二价金属离子会导致蛋白质结构发生改变,促进蛋白分子链的伸展,使包埋在蛋白质内部的疏水性基团暴露于分子表面,因而增大了蛋白质表面疏水性[26]。但经过KCl的替代后表面疏水性下降,原因可能是K+使蛋白质内部疏水基团的卷曲度发生改变,促进了MP的聚集。不同氯盐与MP分子侧链形成“盐桥”,促进蛋白分子的展开,使得疏水性氨基酸暴露,基团暴露程度的不同可能会对CSS与MP的相互作用产生影响,进而引起复合体系在热诱导过程中发生分子聚集作用,最终引起CSS-MP复合凝胶功能特性的改变。
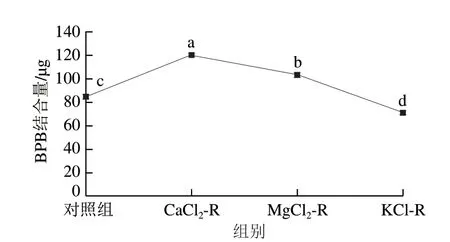
图3 氯盐对低钠盐CSS-MP复合凝胶表面疏水性的影响Fig.3 Effect of different chloride salts on the surface hydrophobicity of low sodium CSS-MP composite gel
2.4 氯盐对低钠盐CSS-MP复合凝胶巯基含量的影响
巯基对于蛋白质空间结构的稳定性有重要作用。如图4所示,与对照组相比,CaCl2替代组和MgCl2替代组的总巯基含量显著降低(P<0.05),KCl替代组的总巯基含量无显著差异。总巯基明显减少,说明Ca2+和Mg2+的加入使未展开的蛋白质重新排列并与其他分子相互作用,这一结果表明,CaCl2和MgCl2的替代有助于CSS和MP相互作用形成二硫键。陈立德[27]研究也表明Mg2+和Ca2+的添加有利于促进猪肉MP热诱导成胶时二硫键的生成。但不同氯盐替代NaCl后,复合凝胶的活性巯基含量均显著下降(P<0.05)。活性巯基含量的减少主要是由于蛋白质表面活性基团的嵌入,或通过生成二硫键将暴露的分子间基团氧化所致[28],这与Zhang Ziye等[29]的研究结果类似。

图4 氯盐对低钠盐CSS-MP复合凝胶巯基含量的影响Fig.4 Effect of different chloride salts on sulfhydryl group content of low sodium CSS-MP composite gel
2.5 同步荧光光谱分析
同步荧光光谱已被广泛应用于揭示蛋白质配体相互作用,利用同步荧光光谱提供的信息可以反映色氨酸残基(Trp)和酪氨酸残基(Tyr)周围微环境的变化[30]。如图5所示,不同氯盐替代NaCl后均发生了荧光猝灭现象,其中KCl替代组,CaCl2替代组和MgCl2替代组的同步荧光强度依次降低,说明疏水分子与MP的结合导致了发色团在溶液环境中的暴露更大,荧光强度降低[31]。并且在Δλ=60 nm时,Trp残基的发射峰表现出轻微的蓝移,最大荧光发射峰从对照组的348 nm到CaCl2替代组的344 nm,MgCl2替代组的343 nm和KCl替代组的349 nm,这表明Ca2+、Mg2+、K+的加入,使Tyr和Trp残基周围微环境的极性降低,疏水性增强,这与表面疏水性测定结果一致。此外,Trp残基的荧光强度要强于Tyr残基,这表明Trp残基对低钠盐复合凝胶中MP猝灭固有荧光的贡献更大[32]。同步荧光结果表明,CSS可能主要通过疏水相互作用与MP蛋白分子形成复合物,而CaCl2、MgCl2和KCl的替代在一定程度上影响两者的相互作用,进而影响蛋白质结构,最终增强MP的热稳定性。

图5 氯盐对低钠盐CSS-MP复合凝胶同步荧光的影响Fig.5 Effect of different chloride salts on synchronous fluorescence spectrum of low sodium CSS-MP composite gel
2.6 低钠盐对CSS-MP复合凝胶微观结构的影响
放大低钠盐CSS-MP复合凝胶2000 倍和20000 倍的扫描电镜图像如图6所示。添加3% NaCl的对照组复合凝胶表面呈现致密的结构,孔隙和丝状结构相对均匀,整体表现出明显的三维凝胶网络,这与文献报道的MP通过热诱导凝胶化形成结构良好、高度相互连接的三维蛋白质网络结构相符合[33]。在低钠盐CSS-MP复合凝胶体系中,以CaCl2、MgCl2和KCl部分替代NaCl后,凝胶的网络结构发生了显著的变化。当复合凝胶中的NaCl被1.0%的CaCl2部分取代后,其凝胶结构较为松弛,凝胶网络结构呈雪花状,通过细丝交联在一起,其结构较为致密,促使CaCl2替代组的凝胶强度与对照组相当。对于MgCl2替代组,在图6E、F可以观察到,凝胶表面部分呈片状结构,相邻层被细丝附着,且内部结构出现了大小不一的孔洞,凝胶结构变得松散。观察图6G、H,KCl部分替代NaCl后,复合凝胶中蛋白质聚集,呈不均匀、不规则孔隙结构,内部还存在较大的团聚体。不同氯盐的替代引起凝胶结构的变化可能与MP和不同盐离子交联程度不同从而导致蛋白质-淀粉之间的反应不均匀有关。CaCl2、MgCl2和KCl的替代,使复合凝胶呈现出更无序、更聚集的结构,导致凝胶质量下降。但对于CaCl2替代组而言,致密孔洞的形成也导致该替代组的凝胶质量较好,可能由于CaCl2的存在刺激了MP与CSS颗粒的相互作用,这有助于结构的均匀性。
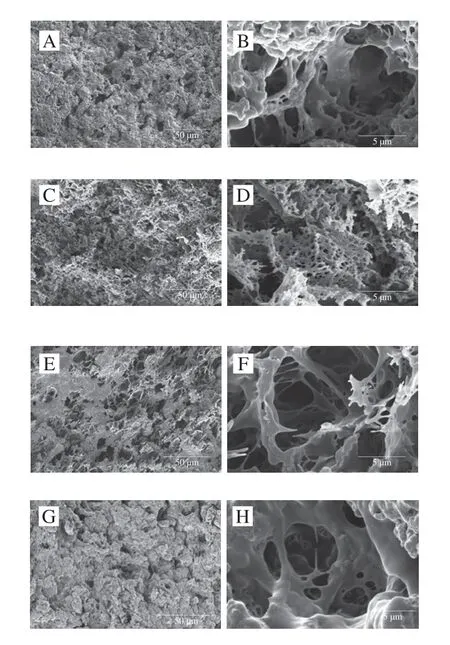
图6 氯盐对低钠盐CSS-MP复合凝胶微观结构的影响Fig.6 Effect of different chloride salts on the microstructure of CSS-MP gel
2.7 低钠盐CSS-MP复合凝胶感官评分
如表1所示,与对照组相比,在色泽上,CaCl2替代组和KCl替代组复合凝胶的评分有所增加,但无显著差异;在气味上,不同氯盐替代组的评分均显著高于对照组(P<0.05);在滋味上,CaCl2替代组和KCl替代组的评分显著低于对照组(P<0.05);在组织形态上,MgCl2替代组评分显著低于对照组(P<0.05),CaCl2替代组和KCl替代组无显著差异。综合各指标的得分情况,从整体看,CaCl2、MgCl2和KCl替代组与对照组的感官评定总分没有显著差异。通过感官评分的结果可以得出,在一定浓度范围内,用CaCl2、MgCl2和KCl替代部分NaCl对低钠盐CSS-MP复合凝胶的感官特性不会有太大影响,总体上在消费者的可接受范围内。

表1 低钠盐CSS-MP复合凝胶感官评分结果Table 1 Sensory evaluation results of low sodium CSS-MP composite gel
2.8 电子鼻分析
采用金属电子鼻传感器对低钠盐CSS-MP复合凝胶的挥发性成分进行检测。雷达图中主要涉及10 种传感器W1C(芳香成分、苯类)、W3C(芳香成分灵敏、氨类)、W5C(短链烷烃芳香成分)、W1S(甲基类)、W2S(对醇类、醛酮类)、W3S(长链烷烃类)、W5S(氮氧化合物类)、W6S(氢化物)、W1W(硫化物)、W2W(芳香成分、有机硫化物)响应值的变化。由图7可知,对照组和CaCl2、MgCl2和KCl替代组复合凝胶的风味轮廓相似,说明各处理组中对凝胶样品主体风味特征贡献较大的化合物种类基本相同。W1W、W1S、W2W和W2S这4 种类型的传感器对低钠盐CSS-MP复合凝胶的响应值较高,而W3C、W5C和W6S这3 种类型的传感器对凝胶的响应值较低,并且与对照组相比,以0.5% MgCl2替代NaCl后的复合凝胶对W1W传感器的响应值明显提高,表明低钠盐CSS-MP复合凝胶中的挥发性风味物质主要为硫化物成分、甲基类、醇类和醛酮类,其中MgCl2的添加更是提高了硫化物的含量。
对低钠盐CSS-MP复合凝胶电子鼻响应信号进行主成分分析(principal component analysis,PCA),结果如图8所示。PC1贡献率为71.6%,PC2贡献率为23.9%,2 种成分的贡献率之和超过95%,说明这2 个PC能够较好反映低钠盐CSS-MP复合凝胶的总体风味特征。从图8对照组和不同氯盐替代组之间的距离可以看出,CaCl2替代组与对照组几乎重合,说明2 组样品的气味差异较小。这可能是由于Ca2+有利于促进蛋白聚集交联,也可能由于Ca2+存在刺激了MP与CSS颗粒的相互作用,形成更加致密均匀的凝胶网络结构,不利于气味释放,因此表现出CaCl2替代组与对照组的气味差异较小。
2.9 电子舌分析
采用电子舌系统对低钠盐CSS-MP复合凝胶的甜味、酸味、咸味、苦味、涩味、鲜味、涩味回味、苦味回味和丰富性进行检测。所有数据均是以人工唾液(参比溶液)为标准的绝对输出值,以基准溶液的输出为“0”,即各项指标的无味点均表示为0,除了酸味和咸味的无味点为负值(分别为-13和-6),无味点以下的指标可以认为是该物质没有味道。由图9可知,对照组和不同氯盐替代组的甜味、苦味回味、涩味回味和丰富性均接近于无味点。与添加了3% NaCl的对照组相比,CaCl2的替代产生了酸味,但减少了复合凝胶的苦味,而MgCl2和KCl的替代无明显差异。此外,CaCl2和MgCl2的替代提高了复合凝胶的鲜味和咸味,而KCl的替代使这2 种味道显著减弱(P<0.05)。以上结果说明1.0% CaCl2和0.5% MgCl2的替代可达到与3% NaCl相似的咸味感知,并且在一定程度上还能起到增鲜提味的作用。

图9 低钠盐CSS-MP复合凝胶的电子舌雷达图Fig.9 Electronic tongue radar charts of low sodium CSS-MP composite gel
3 结论
基于钙镁钾盐替代的低钠盐CSS-MP复合凝胶中,CaCl2替代组的凝胶特性优于其他氯盐替代组。然而,与KCl替代组比,CaCl2替代组和MgCl2替代组表现出较弱的持水力。在感官特性方面,1.0% CaCl2和0.5% MgCl2的替代可达到与3% NaCl相似的咸味感知,综合感官评分结果显示3 种氯盐以一定比例替代NaCl对低钠盐CSS-MP复合凝胶的感官特性没有显著影响。
