叶酸联合二甲双胍对多囊卵巢综合征合并代谢综合征血清指标的影响
2023-09-13娜迪拉卢雪玲
娜迪拉,李 凤,魏 巍,卢雪玲
新疆医科大学第七附属医院内分泌科, 乌鲁木齐 830028
多囊卵巢综合征(polycystic ovary syndrome,PCOS)是一种以雄激素水平过高为主要生化或临床表现、并以持续性无排卵和卵巢多囊样改变为主要特征的妇科内分泌疾病,患者常伴有肥胖和胰岛素抵抗(insulin resistance,IR)[1]。代谢综合征(metabolic syndrome,MS)作为一种代谢紊乱性疾病,与PCOS发病人群部分重叠。研究发现,多种肝细胞因子与糖脂代谢紊乱相关疾病的发病有关,血管生成素样蛋白(angiopoietin-like protein,Angptl)-2、Angptl-4作为肝脏分泌的多功能糖蛋白被证实与PCOS及MS的发生有关[2-3]。二甲双胍是目前治疗PCOS常用的胰岛素增敏剂,已被证实能够减轻PCOS患者的IR而发挥治疗作用[4]。叶酸具有保护血管内皮细胞和预防心脑血管疾病等作用,对肥胖成年人具有增强胰岛素敏感性及改善糖代谢异常等作用[5]。本研究对PCOS合并MS患者采用叶酸联合二甲双胍治疗,观察其对患者血清Angptl-2、Angptl-4及微炎症状态等指标的影响,为临床治疗PCOS及MS提供参考。
1 一般资料
选取收治的PCOS合并MS患者180例为研究对象。
纳入标准:①PCOS诊断符合《妇产科学》(第9版)[1]中相关诊断标准;②MS诊断符合中华医学会糖尿病学分会提出的诊断标准[6];③无其他内科合并症,如甲状腺、肾上腺等脏器的疾病;④无肝、肾功能障碍及高泌乳素血症等;⑤入组前3个月内未接受激素类药物的治疗;⑥患者自愿参与研究且签署知情同意书。
排除标准:①其他疾病诱发的高雄激素血症,如库欣综合征、分泌雄激素的肿瘤等;②合并恶性肿瘤者;③合并严重感染性疾病者;④合并严重心脑血管疾病者;⑤无完整卵巢或子宫者;⑥近3个月内使用对糖脂代谢及炎症因子有影响的药物者。
将入组患者用随机数字表法分为对照组与观察组,每组90例。2组患者的年龄、体质量指数(body mass index,BMI)、月经初潮年龄、病程及PCOS家族史等一般资料比较,差异无统计学意义(P>0.05),见表1。本次研究的设计符合《赫尔辛基宣言》并获得医院伦理委员会审批通过。

表1 2组患者一般资料的比较
2 方法
2.1 治疗方法
2组患者均给予调整生活方式的指导,肥胖及糖代谢异常者鼓励控制饮食和适量运动。对照组患者于月经周期第5天开始给予炔雌醇环丙孕酮片[规格为2 mg醋酸环丙孕酮+0.035 mg炔雌醇,拜耳医药保健有限公司广州分公司]治疗,每日1片,每晚睡前口服,连续服用21 d后停用为1个疗程,撤退性出血第5日开始进入下一个疗程。同时给予盐酸二甲双胍片(规格为0.25 g,石家庄以岭药业股份有限公司)口服,早餐及晚餐前各1片(0.5 mg),连续服用3个月经周期。观察组在对照组治疗的基础上,给予叶酸片(规格为5 mg,常州制药厂有限公司)口服,每次5 mg,每日1次,连续服用3个月经周期。
2.2 观察指标
2组患者于治疗前及治疗3个月经周期后月经来潮第2~5日,早晨采集空腹肘静脉血10 mL,分为2管。一管抗凝血立即送至生化室,以3 000 r·min-1离心10 min,分离血浆,用葡萄糖氧化酶法测定空腹血糖(fasting plasma glucose,FPG);另一管室温静置1 h后,以3 000 r·min-1离心10 min,分离血清,用于其他生化指标的检测。用葡萄糖氧化酶法检测总胆固醇(total cholesterol,TC),用甘油磷酸氧化酶法检测三酰甘油(triglyceride,TG),用计算法测算低密度脂蛋白(low density lipid protein-cholesterol,LDL-C)和高密度脂蛋白(high density lipid protein-cholesterol,HDL-C),用化学发光法检测空腹胰岛素(fasting insulin,FINS),用稳态模型法计算稳态模型胰岛素抵抗指数(homeostasis model assessment of insulin resistance,HOMA-IR)。HOMA-IR=(FPG×FINS)/22.5。用放射免疫法检测内分泌指标雌二醇(estradiol,E2)、睾酮(testosterone,T)、卵泡刺激素(follicle stimulating hormone,FSH)、促黄体生成素(luteinizing hormone,LH),计算LH/FSH值。用酶联免疫吸附试验检测血清Angptl-2、Angptl-4和各项炎症指标,包括肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、超敏C-反应蛋白(high-sensitivity C-reactive protein,hs-CRP)和白细胞介素-6(interleukin-6,IL-6)。用放射免疫法检测血浆同型半胱氨酸(homocysteine,Hcy)。用台式血压计测量静息状态下的收缩压(systolic blood pressure,SBP)和舒张压(diastolic blood pressure,DBP)。测量体质量、身高、腰围(waistline,W)和臀围(hip,H),计算BMI和腰臀比(waist-hip ratio,WHR)。BMI=体质量/身高2。WHR=腰围/臀围。
2.3 统计学方法

3 结果
3.1 生殖激素水平的比较
治疗前,2组E2、T、FSH、LH和LH/FSH值比较,差异无统计学意义(P>0.05)。治疗后,2组E2、FSH水平比较,差异无统计学意义(P>0.05),T、LH及LH/FSH值均下降,且观察组低于对照组(P<0.05)。结果见表2。

表2 2组生殖激素水平的比较
3.2 人体测量指标及血压的比较
治疗前,2组患者的BMI、WHR、SBP及DBP比较,差异无统计学意义(P>0.05)。治疗后,2组患者的SBP和DBP比较差异无统计学意义(P>0.05),观察组的BMI和WHR低于对照组(P<0.05)。结果见表3。
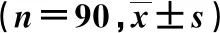
表3 2组人体测量指标及血压的比较
3.3 糖代谢指标的比较
治疗前,2组患者的FBG、FINS和HOMA-IR比较,差异无统计学意义(P>0.05);治疗后,2组患者的FBG、FINS和HOMA-IR均降低(P<0.05),观察组的FINS和HOMA-IR低于对照组(P<0.05),2组的FBG比较差异无统计学意义(P>0.05)。结果见表4。

表4 2组糖代谢指标的比较
3.4 血脂指标的比较
治疗前,2组患者的TC、TG、LDL-C、HDL-C和TG/HDL-C值比较,差异均无统计学意义(P>0.05);治疗后,2组患者的TC、TG、LDL-C、HDL-C和TG/HDL-C值均下降,观察组的TC、LDL-C和TG/HDL-C值均低于对照组(P<0.05),但2组TG和HDL-C水平比较差异无统计学意义(P>0.05)。结果见表5。
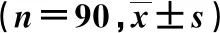
表5 2组血脂指标的比较
3.5 血清Angptl-2、Angptl-4及Hcy水平的比较
治疗前,2组患者的血清Angptl-2、Angptl-4和血浆Hcy水平比较,差异均无统计学意义(P>0.05)。治疗后,2组患者的血清Angptl-2水平均下降,且观察组低于对照组(P<0.05);2组Angptl-4的水平均升高,且观察组高于对照组(P<0.05)。观察组血浆Hcy显著降低,而对照组有所升高,2组间比较差异有统计学意义(P<0.05)。结果见表6。

表6 2组血清Angptl-2、Angptl-4及Hcy水平的比较
3.6 血清炎症因子的比较
治疗前,2组患者的血清hs-CRP、TNF-α和IL-6水平比较,差异均无统计学意义(P>0.05)。治疗后,2组患者血清hs-CRP、TNF-α和IL-6的水平均下降,且观察组低于对照组(P<0.05)。结果见表7。

表7 2组血清炎症因子的比较
3.7 不良反应发生情况的比较
用药期间,观察组出现1例轻度恶心、1例轻度头晕,不良反应发生率为2.22%;对照组出现1例轻度头晕、1例嗜睡、1例恶心,不良反应发生率为3.33%。2组不良反应发生率比较,差异无统计学意义(χ2=0.002,P=0.962)。
4 讨论
PCOS作为一种内分泌紊乱性疾病,临床主要采用口服避孕药、环丙孕酮进行治疗。本研究采用炔雌醇与环丙孕酮复合制剂调节月经周期和抗雄激素治疗,其可抑制子宫内膜过度增生,并与双氢睾酮竞争性结合雄激素受体,从而促进睾酮的清除,还可抑制下丘脑释放促性腺激素,从而缓解高雄激素血症及伴随症状[7]。PCOS患者常合并高胰岛素血症及IR,尤其是合并MS的PCOS患者往往还伴发肥胖、脂代谢紊乱等,激活炎症因子的表达,使PCOS病情加重[8]。
二甲双胍也被应用于PCOS的治疗,其能够抑制肝糖输出,提高组织对胰岛素的敏感性及对葡萄糖的利用率,从而缓解高胰岛素血症及IR,随着IR的改善,患者的排卵功能也会改善,二甲双胍可与炔雌醇环丙孕酮发挥协同作用,提高促排卵治疗的效果[9]。PCOS患者存在明显的Hcy水平升高,高Hcy血症可能与PCOS患者心血管并发症的发生有关[10]。二甲双胍治疗PCOS可能影响患者对维生素B12和叶酸的吸收,从而导致Hcy水平的升高,故PCOS患者常伴有Hcy升高的现象[11]。冯婉琴等[12]的研究结果显示,亚甲基四氢叶酸还原酶基因多态性与PCOS的发生密切相关,给叶酸利用能力较差者补充叶酸有利于改善其高胰岛素血症或IR,对PCOS的治疗具有辅助意义。叶酸能够减轻糖尿病小鼠的炎症及氧化应激反应,下调Hcy的水平,增强胰岛素受体的敏感性,对靶器官起保护作用[13]。本研究中,对照组常规应用炔雌醇环丙孕酮与二甲双胍治疗,观察组在对照组治疗的基础上加用叶酸片,结果显示,2组患者的FBG、FINS和HOMA-IR均下降,且观察组FINS和HOMA-IR的降幅更大(P<0.05)。关于二甲双胍与叶酸联合应用治疗PCOS合并MS使IR进一步降低的机制尚不明确,分析其原因,可能是由于患者体内缺乏叶酸,加之Hcy处于高表达状态,单独使用二甲双胍对IR的改善不理想,而口服叶酸片可外源性补充叶酸并下调Hcy,故可进一步降低患者的IR。观察组BMI、WHR、TC、LDL-C和TG/HDL-C值的降幅均较对照组更大(P<0.05),且Hcy的水平明显下降(P<0.05)。可能由于补充叶酸后,叶酸在体内形成四氢叶酸(tetrahydrofolate,THFA),而THFA能够作为甲基供体促进Hcy的再甲基化并重新合成甲硫酸,使Hcy的水平下降,随着Hcy水平的降低,Hcy对细胞内3-羟基-3-甲基戊二酰辅酶A还原酶(3-hydroxy-3-methylglutaryl coenzyme-A reductase,HMGCR)的活性刺激作用降低,有利于胆固醇的排泄并抑制其合成量的异常增加,还可促进胆固醇转化为胆汁酸,下调胆固醇水平,发挥调脂作用[14]。
研究表明,PCOS患者和MS患者均普遍存在亚临床炎症状态,炎症反应可参与IR的发生和发展,当PCOS合并MS时患者的炎症反应及IR均更明显。Angptl-2是与脂肪组织相关的促炎因子,研究表明,循环系统中Angptl-2的水平与IR、肥胖及炎症反应关系紧密,其过表达可诱导脂肪组织相关炎症细胞因子的释放、加速脂肪分化等,从而参与肥胖、IR及MS的发生与发展过程[15]。Angptl-4也是Angptl家族成员之一,不同于Angptl-2,Angptl-4以糖基化、寡聚体及多种亚型的形式分布于体内,参与机体血管生成、糖脂代谢以及细胞分化等生理过程,被证实与肥胖、糖脂代谢紊乱及炎症反应密切相关[16]。研究表明,Angptl-2与Angptl-4间可能存在拮抗作用,两者平衡失调可能引起糖脂代谢紊乱,并可参与肥胖及炎症反应,加重PCOS病情[17]。hs-CRP、TNF-α及IL-6均是经典慢性炎症因子,已被证实在PCOS患者中明显升高,尤其是在合并MS的患者中其水平的升高更为明显,可通过多途径、多机制影响IR[18]。本研究中,治疗后2组患者Angptl-2、Hcy、hs-CRP、TNF-α和IL-6的水平均有不同程度的下降,Angptl-4有所升高,而观察组各指标的改善情况均明显优于对照组(P<0.05)。表明二甲双胍可在一定程度上降低PCOS患者慢性炎症反应的水平,而与叶酸联用可进一步控制慢性炎症,调节Angptl-2与Angptl-4的平衡,从而发挥对PCOS的治疗作用,这与王永玲等[19]、唐侨飞等[20]的报道基本相符。内分泌指标检测结果显示,2组治疗前、后E2和FSH水平虽未见明显差异,但观察组的T、LH及LH/FSH值下降得更为明显且更接近正常水平,表明叶酸联合二甲双胍能够更好地改善PCOS患者的内分泌紊乱,这与其改善IR及慢性炎症、调节血脂、调节Angptl-2与Angptl-4的平衡、下调Hcy水平等作用有关。
综上所述,叶酸联合二甲双胍治疗PCOS合并MS能够有效缓解患者的肥胖、糖脂代谢紊乱及慢性炎症反应,下调Hcy的水平,调节Angptl-2与Angptl-4的平衡,重建内分泌系统平衡,且无明显不良反应,具有一定的临床推广价值。
