从磷化盘条酸洗废液中制取三氯化铁的试验研究
2023-09-13李洪瑞侯成林王昌鑫刘璇曹放任翠娟王博恒
李洪瑞,侯成林,王昌鑫,刘璇,曹放,任翠娟,王博恒
北方工程设计研究院有限公司,河北 石家庄 050000
某金属制品公司主要从事磷化盘条的生产加工和销售,在酸洗除锈工段产生大量酸洗废液,其中含有高浓度游离酸(盐酸)、氯化亚铁等化合物,属于危险废物。传统的废酸处理方法为中和法[1-2],即采用废碱液或成品碱进行中和,经固液分离后排入厂内污水站或园区污水厂作进一步处理,该过程产生的大量污泥仍属危废,外运处置费用高。因此,对酸洗废液进行资源化利用是当前研究的主要方向。鉴于这种酸洗废液含有高浓度氯化亚铁,可将其氧化为三氯化铁,制成污水处理净水剂,工艺相对简单且成本较低[3-6]。
本文通过采用不同氧化剂直接氧化、催化氧化等方式[7]对酸洗废液进行资源化利用研究,并考察不同反应条件对氧化结果的影响,最终确定最佳的氧化工艺,并按标准《水处理剂 聚氯化铁》(HG/T 4672-2014)对成品进行评价。
1 实验
1.1 试验水质
试验用酸洗废液呈灰黑色,含三价铁1.1%~1.6%、二价铁7.8%~10.5%和游离酸(以HCl 计)6.5%~9.0%。
1.2 试剂和仪器
主要试剂有过氧化氢(质量分数30%)、次氯酸钠(有效氯含量10%)、盐酸、硫酸、硫代硫酸钠、淀粉、碘化钾、硝酸银、亚硝酸钠、磷酸、重铬酸钾、二苯胺磺酸钠、氟化钾、氢氧化钠、酚酞指示液等,均为分析纯。
主要仪器包括磁力搅拌器,烧杯、量筒等玻璃器皿,以及自制催化氧化反应器(有机玻璃材质,有3 层填料,有效反应容积2 L)。
1.3 测试指标及方法
根据标准《水处理剂 氯化铁》(GB/T 4482-2018)检测亚铁离子、铁离子和游离酸(以HCl 计)的含量。按HG/T 4762-2014 标准,以碱度滴定法测盐基度。
1.4 成品指标要求
根据HG/T 4672-2014 标准,作为水处理剂用的氯化铁中Fe3+的质量分数应不低于8.0%,Fe2+的质量分数不大于0.2%,盐基度不低于5.0%。
2 结果与讨论
2.1 过氧化氢氧化对酸洗废液中各指标转化率的影响
以过氧化氢为氧化剂,在反应时间、反应温度、搅拌转速等条件相同的情况下对酸洗废液进行氧化,分析不同过氧化氢投加量下酸洗废液中亚铁离子的转化率。
量取50 mL 酸洗废液倒入250 mL 锥形瓶中(底部有转子),然后置于磁力搅拌器中,设定一定的转速,令锥形瓶中的废液匀速转动且不溅起。
分别在锥形瓶中投加不同量的30%过氧化氢,反应30 min 后关闭磁力搅拌器,取锥形瓶内溶液分别测定Fe2+、Fe3+和游离酸的含量,结果见图1。
由图1 可知,过氧化氢的用量对亚铁离子的转化率有重要影响。随着过氧化氢投加量的增加,废酸中亚铁离子的质量分数急剧降低,同时游离酸含量降低,三价铁离子的质量分数升高。当过氧化氢的投加量为41.2%时,二价铁的质量分数降到了0.01%,游离酸含量降至0.08%,三价铁的质量分数增大到了11.28%,其中二价铁和三价铁的质量分数均达到了标准的要求。继续增大过氧化氢的投加量,各项指标变化趋势相同,但变化幅度很小,因此41.2%为过氧化氢的临界投加点,此时的酸液经过聚合反应后可作为液态水处理剂来使用。
试验所用废酸中Fe2+含量为0.083 6 g/mL,50 mL 废酸中Fe2+含量为4.18 g。临界投加点所用30%过氧化氢为35 mL,因此每克Fe2+对应投加8.37 mL 过氧化氢(质量分数30%),Fe2+的质量分数即可降至0.01%以下,实现完全达标。
2.2 次氯酸钠氧化对酸洗废液中各指标转化率的影响
反应条件同2.1 节,将30%过氧化氢改为次氯酸钠,在不同的投加量下反应30 min 后测定Fe2+、游离酸和Fe3+的含量,结果见图2。随着次氯酸钠投加量的增加,废酸中亚铁离子的质量分数降低并呈一定的线性关系,同时游离酸含量降低,三价铁离子的质量分数升高。当次氯酸钠的投加量为44.4%时,二价铁的质量分数降到0.19%,游离酸含量降至0.14%,三价铁的质量分数增大到11.11%,其中二价铁和三价铁的质量分数均达到了标准的要求。继续加大次氯酸钠的投加量,各项指标变化趋势相同,但变化幅度很小。因此,次氯酸钠的临界投加点为44.4%,此时的酸液经过聚合反应后可作为液体氯化铁水处理剂来使用。
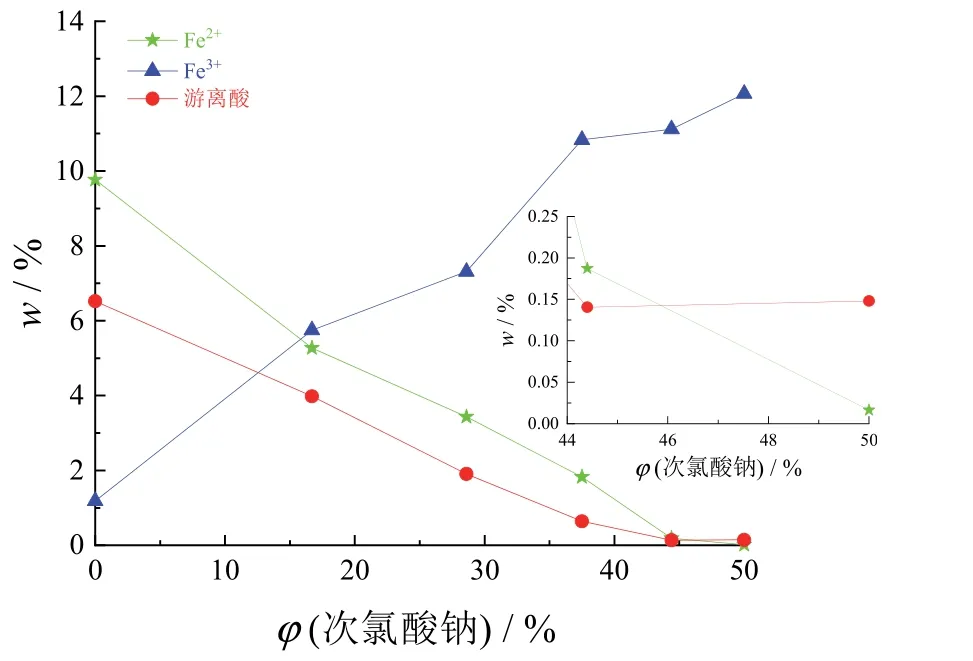
图2 Fe2+、Fe3+及游离酸质量分数随次氯酸钠投加量的变化Figure 2 Variations of mass fractions of Fe2+, Fe3+, and free acid with dosage of sodium hypochlorite
50 mL 废酸中含有4.18 g 的Fe2+,临界投加点所用次氯酸钠为40 mL,因此每克Fe2+对应投加9.57 mL 次氯酸钠(有效氯含量10%),Fe2+的质量分数即可降至0.01%以下,实现完全达标。
2.3 循环喷淋催化氧化对酸洗废液中各指标转化率的影响
强氧化剂直接氧化反应快,但投加量巨大,在真正实际工程中的处理费用难以接受,因此寻求低成本、工艺简单实用的处理方法是盐酸酸洗废液资源化的重要方向。循环喷淋催化氧化法是在常温常压下,利用催化剂亚硝酸钠催化氧气将二价铁离子氧化为三价铁离子[8],其反应如式(1)[9]所示。
当催化剂亚硝酸钠投加到酸洗废液中,会迅速发生反应(2)、(3)和(4),生成的NO 经过式(5)所示反应被O2氧化为NO2,反应混合气体为棕黄色。气相中的NO2在废盐酸中发生式(6)所示的反应。在气液接触过程中,Fe2+被氧化为Fe3+,NO2被还原为NO,然后循环往复,最终二价铁全部被氧化为三价铁。
循环喷淋催化氧化试验采用如图3 所示的氧化塔,底部设氧气接口、催化剂投加口及放空、取样口等,顶部设有混合气排放口、压力表接口等。

图3 循环喷淋催化氧化塔示意图Figure 3 Schematic diagram of circulating spray catalytic oxidation tower
试验时,在反应器内投加2 L 酸洗废液,在容器底部通入氧气(流量为2 L/min),采用循环泵将废酸液从底部泵入反应器顶部喷头处,将20%的亚硝酸钠溶液(相当于3.6 mol/L)分批次投加到反应容器内(每小时投加一次,每次10 mL),使得废酸液中二价铁与催化剂亚硝酸钠产生的二氧化氮发生气液接触反应,反应后的混合气体通过反应器顶部排气口排出,经两级氢氧化钠溶液吸收后排放。常温下反应6 h,每小时取样一次,分别测定Fe2+、Fe3+及游离酸的含量。
2.3.1 不同催化剂投加点对二价铁转化率的影响
试验伊始,首先确定催化剂的投加点。在装置设计时,虽然催化剂投加口设在底部,但上部废液进口处也可投加催化剂。于是考察了催化剂投加位置对结果的影响。由图4 可知:在上部投加催化剂时,溶液中仍含有较多的Fe2+,说明氧化反应不完全。这是因为从上部投加时,距离反应器顶部排气口较近,投加过程中产生的棕黄色二氧化氮大部分未能进入溶液内部,只与上表面溶液发生反应,导致催化剂未得到充分利用,Fe2+转化率低。底部投加催化剂时,在氧气的压力推动下,产生的二氧化氮能充分与溶液进行接触,反应速率高,二价铁至三价铁的转化率高,反应相对彻底。因此,采取催化剂底部投加的方式更有利于反应的进行。

图4 催化剂投加位置对处理效果的影响Figure 4 Effects of different catalyst feeding positions on treatment effectiveness
2.3.2 反应时间的影响
采用底部均匀投加的方式进行循环喷淋催化氧化试验,酸洗废液中Fe2+、Fe3+和游离酸的含量变化见图5。
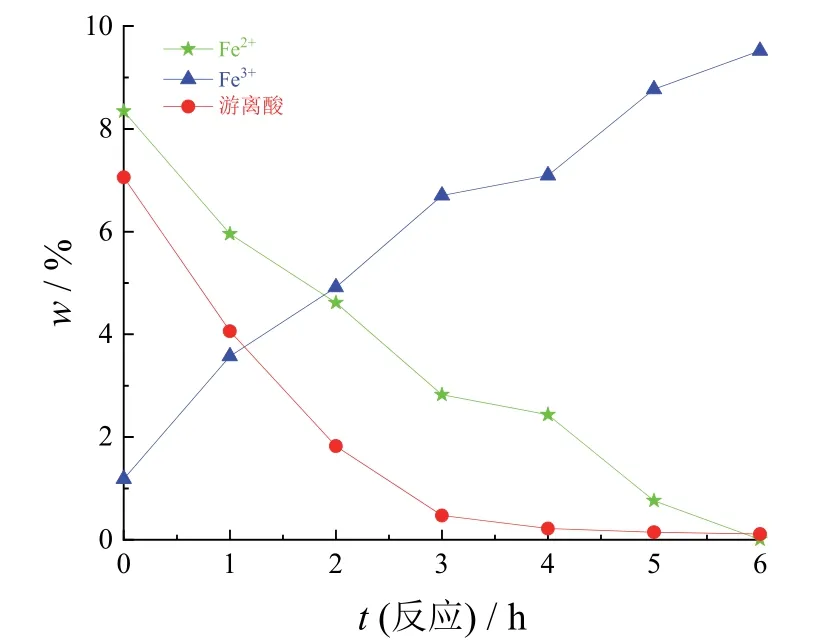
图5 采用循环喷淋催化氧化塔时Fe2+、Fe3+及游离酸的质量分数随反应时间的变化Figure 5 Variations of mass fractions of Fe2+, Fe3+, and free acid with reaction time in circulating spray catalytic oxidation tower
由图5 可见,随着反应时间的延长,Fe2+和游离酸的含量逐渐降低,Fe3+的含量逐渐升高。在反应6 h 后,Fe2+的质量分数已经从最初的8.343%降至0.007%,Fe3+的质量分数从最初的1.184%升高至9.522%,游离酸质量分数降低至0.11%。
经过催化氧化反应6 h 后,酸洗废液中Fe2+和Fe3+的转化规律如图6 所示。
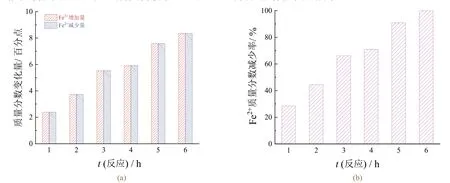
图6 二价铁和三价铁离子的转化规律Figure 6 Transformation laws of ferrous and ferric ions
从图6a 可以看出,与反应前的酸洗废液相比,随着催化氧化反应的进行,各时段内Fe2+质量分数的降低值与Fe3+的质量分数的升高值保持一致。这进一步说明在废盐酸溶液中,Fe2+通过亚硝酸钠的催化作用,已经被氧化为Fe3+。
从图6b 则可以看出,与反应前的废盐酸相比,二价铁的质量分数减少率随着反应时间的延长而逐步增大,催化氧化6 h 后二价铁的质量分数减少率高达99.92%,说明此时二价铁已经几乎完全被氧化为三价铁。
2.3.3 废盐酸感官特征的变化
催化氧化反应之前,磷化盘条酸洗废液呈现很深的墨绿色。反应发生后的3 h 之内,溶液依然呈现墨绿色;3 h 以后,溶液逐渐呈现棕红色;5 h 后,溶液呈现出明显的棕黄色。
众所周知,三价铁离子在溶液中会显黄色,二价铁离子则显浅绿色。废盐酸颜色的变化也可以间接证明溶液中Fe3+含量在逐渐升高,Fe2+含量在逐渐降低,据此可以判断催化氧化反应的程度。
2.4 聚合反应试验
通过以上氧化试验可知,虽然二价铁达到了标准要求,但由于没有加碱,检不出盐基度。为保证氧化后废液的稳定性[10],需要对其盐基度进行调整。
取氧化后的液体100 mL,分别加入不同体积分数的氢氧化钠溶液(30%液碱),搅拌反应30 min 后测盐基度,结果见表1。样品1 原来的三价铁浓度低,故加入液碱后虽然盐基度达标,但是混合后三价铁的质量分数低于8%,不符合要求;样品2-4 原来的三价铁质量分数在10%以上,因此加入液碱后的三价铁质量分数可以满足标准的要求,并且随着加入液碱量的增多,盐基度呈上升趋势,液碱(质量分数30%)投加的体积分数至少要在10%以上才能保证盐基度达标。

表1 调盐基度的测试结果Table 1 Test results of basicity adjustment
3 结论与存在的问题
1) 过氧化氢和次氯酸钠对酸洗废水中的亚铁离子都有很好的氧化作用。针对本研究中的酸洗废水,当每克Fe2+投加8.37 mL 过氧化氢(质量分数30%),或者投加9.57 mL 次氯酸钠(有效氯含量10%),搅拌反应30 min 后废液中二价铁离子和游离酸的质量分数可以达到水处理剂聚氯化铁成品的要求。
2) 循环喷淋催化氧化工艺对钢件酸洗废盐酸中的Fe2+具有很好的氧化效果,在氧气流量2 L/min 和亚硝酸钠投加量0.018 mol/L,常温催化氧化6 h 后,废盐酸中的Fe2+(质量浓度0.083 6 g/mL)已经有99.92%转化为Fe3+,再通过投加液碱调节盐基度,即可得到聚氯化铁成品,其中二价铁离子、三价铁离子和游离酸的质量分数达到了标准《水处理剂 聚氯化铁》(HG/T 4672-2014)的要求。
3) 强氧化剂氧化法及循环喷淋氧化法均对磷化盘条酸洗废液中的二价铁有很好的去除效果,但强氧化剂氧化法的药剂投加量大,按体积比将近1∶1 投药才能氧化彻底,运行费用高,而循环喷淋催化氧化法的药剂投加量小,氧气及亚硝酸钠易得且价格便宜,反应产生的氮氧化物可通过废酸储池循环利用一部分,另一部分通过两级碱液吸收达标后排放,故在实际工程中建议采用催化氧化法对酸洗废液进行资源化利用处理,制成的三氯化铁可作为净水剂出售。
