基于UHPLC-Q-Exactive Orbitrap HRMS技术分析黄芪汤颗粒的化学成分与小鼠口服后的入血成分
2023-09-08李荣胜黄思红尹艺晓蒋式骊慕永平陈佳美
张 清,李荣胜,2,黄思红,沈 沁,尹艺晓,蒋式骊,慕永平,陈佳美,刘 平,刘 伟,2
1.上海中医药大学附属曙光医院肝病研究所,肝肾疾病病证教育部重点实验室,上海市中医临床重点实验室(上海 201203);2.上海中医药大学附属曙光医院药学部国家中医药管理局中药制剂三级实验室(上海 201203);3.上海中医药大学附属曙光医院宝山分院儿科(上海 201900)
黄芪汤始载于宋代典籍《太平惠民和剂局方》,由黄芪和甘草两味药材按6∶1 比例组成,又称黄芪六一汤。黄芪甘温,具有益气健脾、托毒生肌之功;甘草甘平,有补中益气、调和诸药之效。两药相须为用,可平补气血、安和五脏,对于中焦虚损的诸多病症疗效显著[1-2]。该方的临床应用和基础研究主要涉及慢性肝病(乙型肝炎、胆汁淤积、肝纤维化、肝硬化等)和2型糖尿病[2-3]。黄芪汤的药理研究主要集中于慢性肝病,其能够上调肝组织成骨蛋白和促激蛋白膜结合抑制因子同源物(BAMBI)表达[4],下调血小板内皮细胞黏附分子(CD)31 和血管性血友病因子(vWF)的表达,减轻肝窦内皮细胞毛细血管化的程度,进而发挥抗肝纤维化作用[5]。中药复方化学成分复杂,在体内可能发挥协同作用,但目前尚未见开展黄芪汤颗粒化学成分系统研究的报道,且尚未有黄芪汤颗粒灌胃小鼠后入血原型及代谢产物的研究报道。故此,本研究借助超高效液相串联四极杆-静电场轨道阱高分辨质谱(UHPLC-QExactive Orbitrap HRMS)分析技术,采用正、负离子模式扫描,根据化合物保留时间、相对分子质量、二级碎片离子等信息,结合对照品比对、文献报道等方式,快速、系统地开展黄芪汤的化学成分与入血成分研究,以期为黄芪汤药效物质基础研究、复方质量控制及临床合理应用等提供部分科学依据和参考。
1 材料与方法
1.1 材料
1.1.1 动物 健康雄性C57/BL6J 小鼠9 只,体质量20~22 g,由北京维通利华实验动物技术有限公司上海分公司提供。动物生产合格证号:SCXK(沪)2022-0007。动物使用许可证号:SYXK(沪)2022-0018。动物饲养于上海中医药大学动物房,饲养室温度为25 ℃,相对湿度为40%~70%,光照周期明、暗各12 h。本动物实验通过上海中医药大学实验动物伦理委员会批准(批准号:PZSHUTCM210709019)。
1.1.2 药物与试剂 黄芪皂苷Ⅲ、染料木苷、奎宁酸、阿魏酸,大连美仑生物技术有限公司(批号分别为A0122AS、J0218AS、MB6731、M1102AS);异黄芪皂苷Ⅰ、异黄芪皂苷Ⅱ、黄芪皂苷Ⅱ、毛蕊异黄酮苷、甘草苷、黄芪紫檀烷、大豆皂苷Bb、绿原酸、原儿茶酸,成都普瑞法科技开发有限公司(批号分别为BP1719、BP1630、BP0211、BP0306、BP0874、PRF20010802、PRF21030441、PRF7102045、PRF10061151);环黄芪醇,上海源叶生物科技有限公司(批号:C14J9Q65733);甘草酸、隐绿原酸,上海融禾医药科技发展有限公司(批号分别为150206、15020603);异甘草苷、甘草素、异甘草素、咖啡酸、芒柄花素、毛蕊异黄酮、黄芪甲苷I、芒柄花苷、柚皮素、夏佛塔苷、异夏佛塔苷、芹糖异甘草苷、芹糖甘草苷、异佛来心苷,上海诗丹德标准技术服务有限公司(批号分别为ST04480120、ST07000120、ST09620120、8066、3524、9314、10618、9453、9165、ST07760120、ST04950120、ST18930105、ST04390120、STC9740105)。以上对照品质量分数均≥98%。甲醇、乙腈、甲酸为高效液相色谱(HPLC)级,美国Thermo Fisher Scientific 公司;实验用水为超纯水,由Milli-Q 超纯水处理系统制得;其他试剂均为分析纯。
黄芪汤委托江苏江阴天江药业有限公司制作成颗粒剂(批号:2208305),每袋4.0 g(每克颗粒剂相当于2.92 g生药)。
1.1.3 主要仪器 UHPLC-Q-Exactive Orbitrap HRMS分析仪及超高效液相色谱仪(Dionex Ultimate 3000型),美国Thermo Fisher Scientific 公司;Acquity UPLC BEH C18色谱柱(100 mm×2.1 mm,1.7 μm),美国Waters公司;Milli-Q 超纯水处理系统,美国Millipore 公司;BP211D电子分析天平,德国Sartorius公司。
1.2 色谱质谱检测方法
1.2.1 色谱分析 采用Dionex Ultimate 3000 仪器,甲醇-0.1%甲酸水溶液为流动相梯度洗脱。洗脱程序:0~2 min,4%甲醇;2~6 min,4%~12%甲醇;6~38 min,12%~70%甲醇;38~38.5 min,70%甲醇;38.5~39 min,70%~95%甲醇;39~43 min,95%甲醇;43~45 min,4%甲醇。流速0.3 mL/min,柱温40 ℃,进样量5 μL。
1.2.2 质谱分析 采用UHPLC-Q-Exactive Orbitrap HRMS 分析仪进行质谱分析。加热离子源(H-ESI),辅助气流量13 arb,辅助加热器温度300 ℃,离子传输管温度320 ℃,自动增益控制(AGC)为1×106,射频水平(S-lens)50。电喷雾电离负离子模式(ESI-):鞘气(N2)流量35 arb,喷雾电压2.5 kV;电喷雾电离正离子模式(ESI+):鞘气(N2)流量35 arb,喷雾电压3.5 kV。扫描方式采用同时正负离子一级全扫描/二级全扫描(Full MS/dd-MS2)模式,其中包括1 次一级全扫描(分辨率为70 000 FWHM)和1 次数据依赖的二级扫描(分辨率为17 500 FWHM)2 个事件,正、负离子扫描范围均为m/z100~1 500,碰撞能梯度为10 V、20 V、40 V。
1.3 对照品溶液的制备 精密称取各对照品约1.00 mg,加入甲醇配制成1.00 g/L 的单一对照品储备液。精密量取储备液适量,加入20%甲醇水溶液稀释成浓度为1 mg/L的混合溶液。
1.4 供试品溶液的制备 取黄芪汤颗粒1 g(相当于生药2.92 g),精密称定,加水50 mL,超声1 h 使其溶解。取上述提取溶液适量,采用20%甲醇稀释,获得按生药量计算为10 g/L 的稀释溶液,摇匀,经0.22 μm 微孔滤膜滤过后即得供试品溶液。
1.5 血清样本的制备 给药前将小鼠禁食12 h,自由饮水。将小鼠随机分为空白组(3 只)和黄芪汤颗粒组(6 只),空白组灌胃超纯水,黄芪汤颗粒组按照生药含量7.32 g/kg 灌胃黄芪汤颗粒提取液(按65 kg 体质量成人等效剂量换算而得),分别在给药后1 h 和3 h 时各处理3 只,摘眼球取血,置于4 ℃箱过夜;4 500 r/min、4 ℃离心15 min,获取血清。
1.6 血清样品处理 取200 μL血清样品,加入1 000 μL甲醇沉淀蛋白,12 000 r/min、4 ℃离心10 min,取上清液960 μL 至1.5 mL EP 管,温和37 ℃氮气流吹干;加80 μL 20%甲醇水溶液复溶,12 000 r/min、离心10 min,取上清液进样分析。
1.7 检测与分析 按“1.2”项下色谱、质谱条件分别对对照品混合溶液、黄芪汤颗粒供试品及小鼠血清样品进行数据采集和结果分析。依据高分辨质谱提供的准分子离子和加荷离子等信息提取到相对分子量和质谱离子峰,经Xcalibur 3.0 软件在允许误差范围内(±10×10-6)拟合计算出可能的元素组成,再结合对照品、参考文献等提供的二级质谱离子碎片信息比对,进一步鉴定出黄芪汤颗粒所含的化学成分。
2 结果
2.1 黄芪汤颗粒中化学成分鉴定 基于“1.2”项下色谱、质谱条件优化后,对黄芪汤颗粒及小鼠血清样品进行数据采集和定性分析。在正、负离子同时扫描模式下,从黄芪汤颗粒中共鉴定出167 种化学成分,包括89种黄酮类、65 种皂苷类、9 种有机酸类以及4 种其他类化合物,其中30 种化学成分经对照品比对确证,包括奎尼酸、咖啡酸、原儿茶酸等。黄芪汤颗粒提取液正、负离子模式总离子流图(TIC)见图1,黄芪汤颗粒化学成分及小鼠口服给药后血清中鉴定的原型成分结果见表1[6-10](见本文二维码中)。
2.1.1 黄酮类成分的质谱裂解表征 黄酮类化合物是黄芪汤颗粒的主要成分,故进一步研究黄芪汤颗粒所含的黄酮类化合物的质谱裂解规律。黄酮类化合物在电喷雾质谱(E S I - M S)中,易脱去糖基、丢失中性碎片-O、-CO、-H2O、-CO2,易发生逆狄尔斯-阿德尔反应(RDA)裂解[11]。
以化合物15(异甘草苷)和化合物40(芒柄花苷)的裂解途径为例,阐明黄酮类化合物可能的裂解规律。在负离子扫描模式下,异甘草苷产生[M-H]-准分子离子峰(m/z417.119 8),化学式为C21H22O9(误差为3.140 ppm)。在其ESI-MS2质谱图中检测到有m/z255.066 4[M-HC6H10O5]-和m/z297.077 0[M-H-C6O3]-两个离子碎片。m/z255.066 4[M-H-C6H10O5]-再依次丢失-C9H10、-O基团,产生m/z180.005 5[M-H-C9H10]-和m/z148.015 5[MH-O]-离子碎片;而m/z297.077 0[M-H-C6O3]-依次丢失-C7H4O3、-C7H4O 碎片,产生m/z119.044 8[M-HC7H4O3]-和m/z153.018 2[M-H-C7H4O]-离子碎片,其中m/z153.018 2 丢失-O,产生m/z135.007 5[M-H-O]-离子碎片。芒柄花苷ESI-MS 模式下在加HCOOH 情况下有较高的离子响应信号,产生m/z475.123 5[M+HCOOHH]-准分子离子峰,在丢失-CHOOH 情况下得到m/z429.115 8[M-H-HCOOH]-,经软件拟合化学元素组成为C23H23O11(误差为3.498 ppm),在其ESI-MS2质谱图中检测到有m/z348.878 7[M-H-C5H4O]-和m/z267.066 6[MH-C6H10O5]-两个离子碎片。m/z348.878 7[M-HC5H4O]-离子碎片再丢失-C11H6O4基团产生m/z148.187 1[M-H-C11H6O4]-离子碎片;m/z267.066 6[M-H-C6H10O5]-依次丢失-C9H4O3、-CH2,产生m/z252.042 8[M-H-CH2]-和m/z107.880 8[M-H-C9H4O3]-离子碎片。化合物15 和化合物40 裂解途径符合黄酮类化合物的裂解规律,与对照品和数据库裂解途径一致,最终确定化合物为异甘草苷(C21H22O9)与芒柄花苷(C22H22O9)。相应质谱裂解途径见图2。
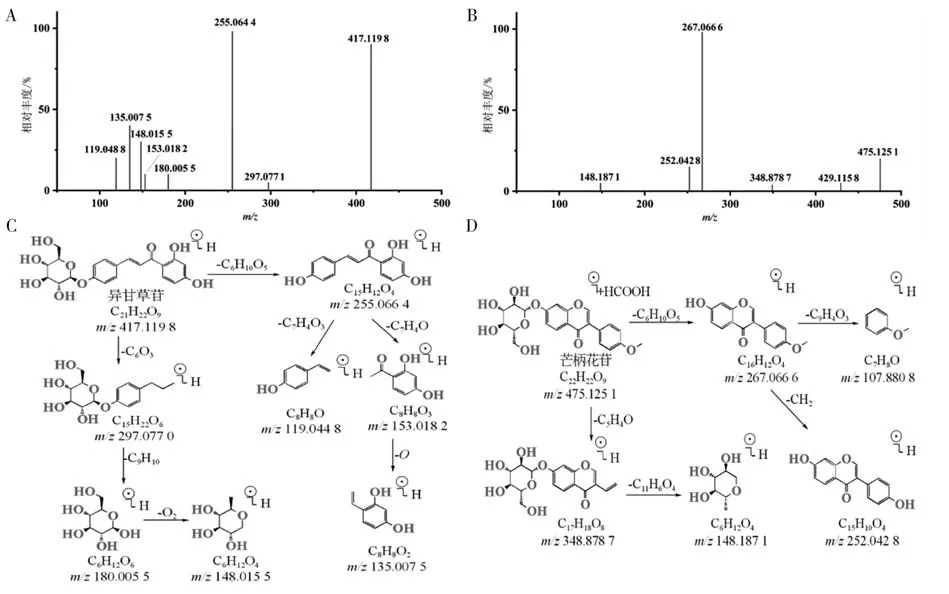
图2 异甘草苷与芒柄花苷的质谱图(A、B)和推测裂解规律图(C、D)
2.1.2 皂苷类成分的质谱裂解表征 皂苷类成分是存在于黄芪和甘草药材中的另一类重要成分。黄芪皂苷和甘草酸均属于三萜皂苷类,是苷类中结构比较复杂的化合物。该类化合物由苷元连接糖苷类组成,在质谱条件下易发生脱Glu、连续脱H2O、丢CO 及Aglcone等基团。
以化合物116(甘草酸)和化合物139(黄芪甲苷)为例,阐明该类化合物可能的裂解路径。甘草酸在负离子模式下检测到m/z821.398 0[M-H]-准分子离子信号,经软件拟合可能的元素组成为C42H62O16(误差为3.686×10-6),ESI-MS2质谱图中检测到有m/z733.913 8[M-H-C-CO2]-和m/z351.057 5[M-H-C29H42O5]-离子碎片。两个离子碎片分别丢失-C7H10O9、-C6H18O11基团,产生m/z113.023 0[M-H-C7H10O9]-和m/z300.369 3[M-HC6H18O11]-离子碎片,其中m/z300.369 3 丢失C19H30O11基团产生m/z193.035 0[M-H-C19H30O11]-离子碎片。黄芪甲苷在负离子加-HCOOH 情况下有较高的响应,经软件拟合元素组成可能为C42H69O16(误差为3.602×10-6),在其ESI-MS2质谱图中检测到m/z783.451 0[M-HCOOH]-离子碎片。该离子碎片依次丢失-C9H16O7、-C7H10O4、-C5H16O3、-C6H14基团,产生m/z548.460 7 [M-HC9H16O7]-、m/z548.460 7[M-H-C7H10O4]-、m/z548.460 7[M-H-C5H16O3]-以及m/z548.460 7 [M-H-C6H14]-离子碎片。化合物116 和化合物139 裂解途径符合黄酮类化合物的裂解规律,与对照品裂解途径一致,最终确定化合物为甘草酸(C42H62O16)与黄芪甲苷(C41H68O14)。相应质谱裂解途径见图3。

图3 甘草酸与黄芪甲苷的质谱图(A、B)和推测裂解规律图(C、D)
2.2 小鼠入血成分及代谢产物鉴定 基于“2.1”项下鉴定结果,针对黄芪汤颗粒的化学成分及其可能产生的代谢产物,对小鼠血浆样本的检测结果进行提取分析,结合保留时间及二级碎片离子信息,发现小鼠灌胃黄芪汤颗粒后,血浆样本中可检出60 种原型成分和43种代谢产物。43 种代谢产物中黄酮类33 种,皂苷类10种;主要代谢途径为糖基化(+C6H10O5)、氧化(+O)、去饱和(-H2)、脱水(-H2O)、甲基化(+CH3)、乙酰化(+C2H2O)、硫酸化(+SO3)以及葡萄糖醛酸化(+C7H12O7)等反应。黄芪汤颗粒入血原型成分见表1(见本文二维码中),代谢产物成分见表2(见本文二维码中),灌胃给药后小鼠血清样品中鉴定出的代谢产物离子峰见图4。
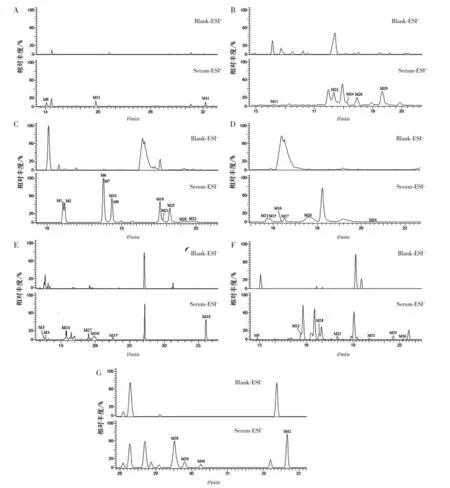
图4 小鼠空白血清与含药血清中提取的代谢产物离子流图
2.2.1 黄酮类化合物代谢产物 本实验检测到黄酮类原型成分有异甘草素、异甘草苷、甘草苷、甘草素、毛蕊异黄酮、柚皮素、芒柄花素。以黄酮类成分异甘草苷代谢产物M1、M3 以及异甘草素代谢产物M31、M21 的详细代谢过程为例,分析该类化合物代谢产物可能的路径。结果显示,该类化合物在小鼠血清中易发生甲基化、硫酸化以及葡萄糖醛酸化等类型反应。
M1在保留时间为11.06 min时,提取到m/z593.150 1[M-H]-的离子峰,经软件拟合其分子式为C27H30O15(误差为3.884×10-6),是异甘草苷的一个代谢产物,较异甘草苷m/z417.118 0[M-H]-增加-C6H8O6,符合葡萄糖醛酸化产物。M3 在保留时间为12.64 min 时提取到m/z497.077 0[M-H]-离子峰,该峰较异甘草苷的理论相对分子质量增加-SO3,经软件拟合其分子式为C21H22O12S(误差为4.379×10-6),为异甘草苷甲基化产物。其他特征离子碎片m/z255.066 1、m/z148.160 1、m/z135.007 4与异甘草苷的离子碎片相似,且与文献报道的情况一致,因此推断M1 是异甘草苷葡萄糖醛酸化产物,M3 是异甘草苷甲基化产物。
M31 在保留时间为19.75 min 时,提取到m/z271.096 5[M+H]+离子峰,经软件拟合其分子式为C16H14O4(误差为-0.426×10-6),与异甘草素的理论相对分子质量相差-CH3,该离子碎片峰为异甘草素甲基化代谢产物。M32 在保留时间为19.84 min 时,提取到m/z337.039 5[M-H]-离子峰,经软件拟合其分子式为C15H14O7S(误差为-2.054×10-6)与异甘草素的理论相对分子质量相比增加+SO3,该离子碎片峰为异甘草素硫酸化代谢产物。其他特征离子碎片m/z255.066 0、m/z148.010 1、m/z135.007 7 与异甘草素的离子碎片相似。因此,推断M31 是异甘草素甲基化代谢产物,M32 是异甘草素硫酸化代谢产物。
同理,其他黄酮类化合物在准分子离子碎片上同样发生葡萄糖醛酸化、硫酸化,部分代谢产物在二级裂解碎片上发生水合、氧化或者去饱和后发生甲基化。推测的异甘草苷(A)和异甘草素(B)代谢产物途径见图5。

图5 异甘草苷(A)、异甘草素(B)以及甘草酸(C)、黄芪甲苷(D)代谢途径
2.2.2 皂苷类化合物代谢产物 本研究中皂苷类原型成分有甘草酸和黄芪甲苷,以皂苷类成分甘草酸代谢产物M38~M40 和黄芪甲苷代谢产物M11、M33、M35、M36、M42、M43 的详细代谢过程为例,分析该类化合物代谢产物可能的路径。结果显示,该类化合物在体内易发生水合后葡萄糖醛酸化或硫酸化,部分代谢产物在准分子离子碎片脱掉糖苷后发生水合、氧化后易硫酸化或乙酰基化。
M38、M39、M40 分别在保留时间为29.55 min、29.82 min和30.27 min时,提取到m/z471.311 1[M-H]-3个离子信号,经软件拟合其分子式为C29H44O5(误差为1.208×10-6、2.502×10-6和1.653×10-6),与甘草酸的理论相对分子质量相比,可发现是甘草酸水解两分子葡萄糖醛酸并氧化后的代谢产物。M41 在保留时间为32.27 min 时,提取到m/z455.352 0[M-H]-离子信号,经软件拟合其分子式为C30H46O3(误差为0.238×10-6),与甘草酸的理论相对分子量相比是甘草酸水解两分子葡萄糖醛酸丢失-O的代谢产物,经与对照品和文献比对一致[12],上述产生的代谢产物符合甘草酸的代谢路径。
M11在保留时间为15.61 min时提取到m/z717.351 4[M+H]+离子碎片,其拟合分子式为C36H62O12S(误差为-0.249×10-6),与黄芪甲苷的理论分子质量相比,为丢失-C6H10O5后水合、硫酸化的代谢产物。M33、M35、M36分别在保留时间20.27 min、21.59 min、22.23 min 时提取到m/z747.362 0[M-H]-的3 个离子碎片峰,经软件拟合其化学式为C36H60O14S(误差为-6.053×10-6、-3.765×10-6和-7.270×10-6),与黄芪甲苷的理论分子量相比,为丢失-C5H8O4后经氧化、硫酸化的代谢产物。M42 在保留时间为32.66 min 时提取到m/z681.330 3[M-H]-离子碎片峰,经软件拟合分子式为C35H54O11S(误差为-9.481 ×10-6),与黄芪甲苷的理论分子质量相比,为丢失-C6H10O6后经还原、硫酸化的代谢产物。M43 在相对保留时间为40.15 min 时提取m/z677.425 9[M-H]-离子碎片峰,经软件拟合其化学式为C38H62O11(误差为4.112×10-6);此与黄芪甲苷的相对理论分子质量相比,为丢失-C5H8O5后经水合、乙酰基化的代谢产物,与对照品和文献比对一致[13]。上述产生的代谢产物符合黄芪甲苷的代谢路径。甘草酸(C)和黄芪甲苷(D)代谢产物途径见图5。
3 讨论
化学成分极为复杂是中药复方的主要特征之一,理化性能分析、HPLC、气相色谱(GC)等方法常用于复方中含量较高成分的分析。对于口服复方后入血成分及其代谢产物,由于受到机体自身因素(如代谢酶的参与、内源性成分的干扰、成分含量较低等)影响,导致其分析十分困难。近年来,液质联用技术在中药复方化学成分、代谢产物鉴定等方面的应用极大推进了中药复方化学成分及体内暴露成分的解析,进一步促进了中药复方药效物质相关研究的进展[14]。
本研究采用UHPLC-Q-Exactive Orbitrap HRMS 技术分析黄芪汤所含的化学成分,并完成小鼠灌胃后原型成分和入血成分、代谢产物的快速鉴定。从黄芪汤颗粒中共鉴定出167 种化学成分,包括89 种黄酮类、65种皂苷类、9 种有机酸类以及4 种其他类化合物;小鼠在灌胃后的血清中检测到60 种原型成分和43 种代谢产物成分。目前针对黄芪汤的研究主要集中于对慢性肝病、糖尿病等疾病干预的药效作用。已有研究[15-18]阐明了黄芪汤、黄芪总苷、黄芪甲苷、甘草酸对肝纤维化的部分作用机制,然而黄芪汤化学成分十分复杂,其中可能存在其他的成分也具有抗纤维化的作用。因此,本实验采用UHPLC-Q-Exactive Orbitrap HRMS 技术分析鉴定黄芪汤颗粒的化学成分及主要入血成分,发现黄芪和甘草中均有种类丰富的皂苷类与黄酮类成分,结合对照品、MassBank 等数据库及文献中提供信息的比对,可以对化合物进行鉴定。同类型化合物含有相似的化学结构,在化合物质谱裂解过程中会产生相似的裂解碎片,利用该性质可进一步提高鉴定化合物的准确性和合理性。值得关注的是以峰面积作为参照,甘草苷、甘草素、黄芪甲苷、甘草酸、毛蕊异黄酮、芒柄花素、芒柄花苷等成分在黄芪汤和小鼠血清中都有较好的响应,这些成分有望成为黄芪汤质量控制的指标。本次研究还发现黄芪汤体内代谢产物多以Ⅱ相代谢物为主,主要包括甲基化、葡萄糖醛酸化及硫酸化产物,这可能与天然产物的化学性质有关。后续课题组将结合本次实验结果,进一步探讨相关化合物在体内的相互转化关系。
值得一提的是,本研究中复方化学成分与入血成分仅为定性分析,后续仍需要进行定量分析与全面的体内代谢过程研究,同时结合体内外药效评价模型,开展更为深入的药效物质基础及作用机制研究,以阐明黄芪汤的药效物质基础,进而为该方的科学合理应用及相关的新药研发提供实验依据。
