地塞米松玻璃体内植入剂早期联合康柏西普在抗血管内皮生长因子治疗反应不佳糖尿病性黄斑水肿中的应用△
2023-08-31邓爱萍方成彦宁秋艳
邓爱萍 田 润 熊 成 李 妍 方成彦 宁秋艳
糖尿病视网膜病变(DR)是糖尿病重要的微血管并发症,而糖尿病性黄斑水肿(DME)可发生在DR的任何阶段,是糖尿病患者视力受损的主要原因[1]。目前针对DME的治疗方式较多[2]。药物治疗包括抗血管内皮生长因子(VEGF)药物、 糖皮质激素,新型药物,如白细胞介素抑制剂、铑激酶抑制剂及神经保护剂等也有研究应用于DME治疗。手术有玻璃体切割术联合内界膜剥出[3]、传统激光格栅光凝及微脉冲激光[4]等多种治疗方法。近年来,抗VEGF药物逐步成为DME治疗中的一线治疗方案[5]。但随着研究的不断深入,越来越多的研究表明,约1/3的DME患者对抗VEGF治疗反应不佳[6-7]。反应不佳的原因较多,可能由于个体DME发病机制中以炎症因素为主导,亦可能受患者个体差异影响,如年龄、血糖或血压控制等不同因素的共同作用[8]。
长期持续的黄斑水肿可导致黄斑功能不可逆性损伤,尽早、有效且持续性维持DME患者的黄斑结构为治疗的最终目标,目前一线治疗方案抗VEGF单药对于部分患者仍不能满足该目标。对于难治性DME的定义,以及换药或联合治疗的推荐[9]往往在抗VEGF治疗三针后评估及开展。该方法对于抗VEGF应答不佳的患者可能使其错过早期控制DME的时机,增加不必要的经济负担及注射风险。因此,本研究回顾性分析采用早期联合治疗方案在该类患者中的应用疗效及安全性数据,旨在探讨早期联合方案的可行性,现将结果报告如下。
1 资料与方法
1.1 一般资料
回顾性研究。选择2018年8月至2022年3月于云南大学附属医院检查确诊的DME患者50例50眼纳入研究。其中男27例27眼,女23例23眼;年龄(45.0±9.5)岁。纳入标准:(1)2型糖尿病,血糖控制良好,糖化血红蛋白≤10.0%,DR分期为Ⅱ~Ⅳ期;(2)有累及中心凹的DME,并导致患者视力下降;(3)黄斑中心凹视网膜厚度(CMT)≥300 μm;(4)无影响眼底检查的屈光间质混浊及瞳孔缩小;(5)FFA检查无黄斑缺血及其他原因引起的黄斑水肿;(6)随访期间未行全视网膜激光光凝治疗;(7)患者配合度以及依从性良好,随访时间≥12个月;(8)注射康柏西普治疗2周后,水肿消退少于30%,或视力改善小于5个字母或下降者。排除标准:(1)合并其他黄斑病变,如黄斑前膜、黄斑裂孔等,或其他原因引起的黄斑水肿,如葡萄膜炎、视网膜中央静脉阻塞等;(2)合并糖尿病视神经病变;(3)既往3个月内目标眼曾行激光光凝治疗或抗VEGF药物治疗,6个月内曾行曲安奈德药物治疗;(4)目标眼既往有玻璃体视网膜手术病史;(5)目标眼有青光眼病史或高眼压症;(6)全身情况不允许FFA检查,如患有哮喘、严重高血压等,或其他原因不能配合相关检查;(7)失访及数据丢失。所有患者均获知情并签署书面知情同意书。
1.2 方法
1.2.1 分组
以患者入组序列号分组,单号患者分为单药治疗组(单药组)(25例),双号患者分为联合治疗组(联合组)(25例),单药组男14例,女11例;年龄(41.0±5.6)岁。联合组男13例,女12例;年龄(43.0±3.4)岁。治疗前2组患眼最佳矫正视力(BCVA)、CMT比较,差异均无统计学意义(均为P>0.05)。两组患者基线资料见表1。
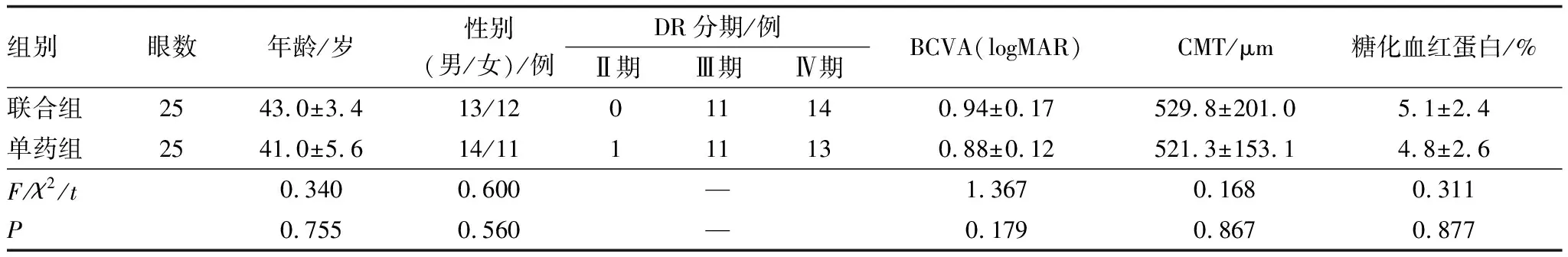
表1 联合组和单药组DME患者基线资料
1.2.2 干预方法
单药组患眼治疗方案为每个月1次抗VEGF治疗,共4次,之后改为2个月1次,共3次治疗至观察终点48周。联合组首针抗VEGF治疗2周后行地塞米松玻璃体内植入剂(IDI)注射,2周后继续每个月1次抗VEGF治疗,共4次,之后改为2个月1次,共3次治疗至观察终点48周。治疗及随访方案见图1。

图1 联合组和单药组患者治疗及随访方案
1.2.3 药物注射流程
在无菌层流手术室按常规无菌操作准备。以1 mL注射器抽取10 g·L-1抗VEGF药物(康柏西普)0.05 mL(含康柏西普0.5 mg),于颞上或鼻上方距角巩膜缘3.5~4.0 mm处垂直于巩膜面穿刺注射。注射完毕后予妥布霉素地塞米松眼膏涂眼后包封。注射前及注射后第2天监测患眼眼压。术前及术后3 d患者滴5 g·L-1左氧氟沙星滴眼液,每天4次。在无菌层流手术室按常规无菌操作准备,将IDI的安全阀拔出,于颞下或鼻下方角膜缘后3.5~4.0 mm处睫状体平坦部垂直于眼球壁进针,使硅胶套与结膜接触,明确安全情况下按动给药器开关进行给药操作,置入1枚IDI(0.7 mg)。术毕予妥布霉素地塞米松眼膏涂眼后包封。注射前及注射后第2天监测患眼眼压。术前及术后3 d患者滴5 g·L-1左氧氟沙星滴眼液,每天4次。
1.2.4 观察指标
对比观察2组患者干预前及干预后4周、8周、12周、20周、24周、32周、40周及48周的BCVA、CMT及术后不良反应事件发生情况。BCVA结果转换为logMAR视力后进行统计分析,数值越小,BCVA 越好。通过德国海德堡OCT扫描仪采集患者同部位黄斑区视网膜断层图像并测量CMT,CMT测量3次取平均值。不良反应事件记录项目包括高眼压、白内障、视网膜脱离及眼内炎。
1.3 统计学处理
采用SPSS 21.0 统计学软件进行统计分析,计数资料组间比较采用χ2检验;计量资料以均数±标准差表示,组间比较采用单因素方差分析,采用重复测量方差分析对治疗前后不同时间点各项指标进行分析,采用LSD-t检验行进一步两两比较。检验水准:α=0.05。
2 结果
2.1 BCVA结果
干预后第4周,单药组和联合组患眼BCVA较基线均有不同程度提升。第8周开始,联合组患眼BCVA较单药组显著提高,差异有统计学差异(P<0.05)。联合组患眼在视力提升上的优势持续到第24周。48周时,联合组患眼BCVA较单药组仍有显著提高,BCVA差异有统计学差异(P<0.05)(表2)。
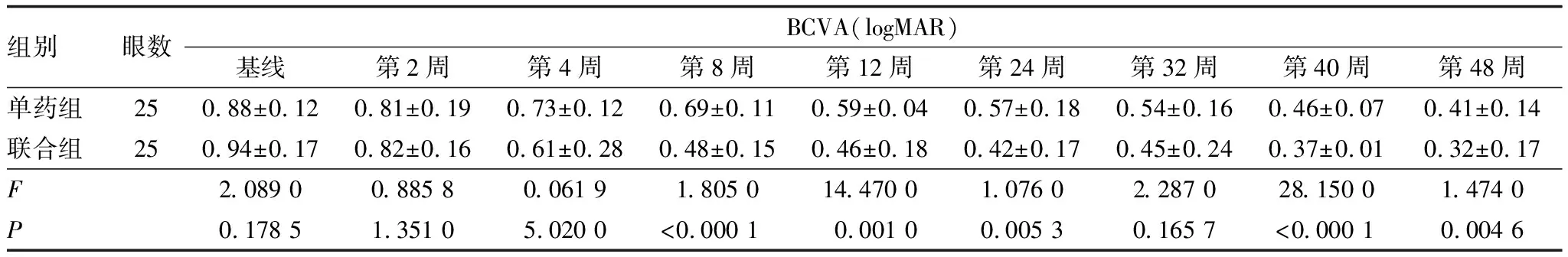
表2 两组DME患者不同时间点BCVA比较
2.2 CMT结果
干预后第4周,联合组患眼CMT降低,与单药组比较,差异有统计学意义(P<0.05)。从第4周开始,第4周、第8周、第12周、第24周、第32周、第40周及第48周7个时间点,联合组患眼CMT较单药组均较低,差异均有统计学意义(均为P<0.05)(表3)。

表3 两组DME患者不同时间点CMT比较
2.3 不良反应事件发生情况
联合组患眼高眼压发生率为24%(6眼), 单药组为8%(2眼),差异有统计学意义(P<0.05)。联合组患眼高眼压发生在注药后1~2个月,均可用降眼压药物控制至正常范围;单药组患眼高眼压发生在注药后1~2 d,未予药物治疗。2组患眼均未出现视野缺损及神经纤维层厚度改变。联合组患眼白内障发展2眼,单药组1眼,3例(3眼)均为高龄患者(>65岁),其白内障发展均未达到需要手术干预的程度。2组患眼均未出现眼内炎、视网膜脱离、玻璃体积血等并发症。
3 讨论
玻璃体内注射抗VEGF药物是目前治疗DME最常用的手段之一。然而,一项纳入712例中国DME患者的研究显示,接受连续3个月玻璃体内注射康柏西普 (0.5 mg)治疗后,41.3%的DME患者治疗反应欠佳[10]。此类DME患者虽经多次玻璃体内注射抗VEGF药物治疗,但黄斑水肿仍持续存在,同时,多次玻璃体内注射的长期安全性并不明确[11]。
针对抗VEGF应答不佳的持续性DME患者的治疗方案目前尚未有统一标准。但有回顾性研究表明,1针抗VEGF治疗后1个月,如果CMT下降<25%,可预测后续抗VEGF治疗不应答[12]。基于此,1针抗VEGF应答不佳可作为抗VEGF治疗预后较差的重要预测因素。所以,针对抗VEGF治疗应答不佳的持续性DME患者,尽早转换治疗方案十分必要。本研究中,治疗2周后开始行早期评估,凡水肿改善和/或视力评估不理想者,尽早行治疗方案的优化。关于应答不佳的标准,本研究参考2020年中国台湾DME治疗专家共识[13],结合临床实际及当地医保政策,制定为较符合国情的水肿消退少于30%,视力改善小于5个字母或下降者。
炎性反应在DME的发生过程中起重要作用。研究发现,DME患者房水中IL-6的水平较正常对照组显著升高,IL-6与DME的严重程度及VEGF水平呈正相关,炎症介质与VEGF共同导致DME患者眼内炎症反应加重、视网膜血管内皮细胞渗漏及视力下降[14]。因此,抗VEGF和抗炎在DME的治疗过程中可能起互补作用,在机制上有很高的可行性和合理性。
关于抗VEGF和抗炎的联合治疗,近些年国外陆续已有报道。Maturi等[15]研究显示,24周时联合治疗组的视网膜厚度发生了显著降低;但值得关注的是,联合治疗组和雷珠单抗组患者的平均BCVA差异无统计学意义。视网膜厚度改变与本研究结果相似,本研究中,从第4周开始CMT发生显著降低,直到第48周,联合组患眼CMT较单药组仍较低,差异有统计学意义(P<0.05)。但与Maturi等[15]研究不同的是,本研究第8周开始,联合组 BCVA(logMAR)较单药组出现显著性提高(P<0.05),且视力提升可维持至48周,持续起效。造成这一结果的原因可能是,Maturi等[15]的研究使用IDI的时间较晚,地塞米松的药效可能发生在光感受器死亡后。因此,即使可有效降低水肿,但未获得相应的视力改善。这一猜测也与本研究的设计相符,即尽早进行抗炎的干预治疗,可获得更好的视力改善。另一项关于联合治疗的研究[16]显示,与基线检查时相比,单独接受抗VEGF治疗的患眼在12个月或24个月时没有显著改善视力或降低CMT,从抗VEGF治疗转向联合类固醇治疗后,患眼开始显示出显著的功能和解剖学优势。与Maturi等[15]的研究不同,该研究[16]显示,早期(3个月)的联合治疗可较单药治疗获得更好的视力提升和解剖学改善;值得一提的是,该研究[16]不仅限于难治性DME患者,所有DME在早期进行联合治疗均可获得更好的视力预后。与该研究[16]不同,本研究将抗VEGF单药治疗反应较好的患者排除,仅针对反应不佳的预期难治性DME患者进行比较。本研究结果显示,对于抗VEGF治疗应答不佳的DME患者,选择IDI和康柏西普早期(2周)联合的治疗方案,其效果在视力改善和解剖学改善两个方面均优于单药治疗。其中,解剖学改善从第4周开始出现统计学差异,解剖学改善与视力提升均可持续到48周。联合治疗方案结果提示,尽早行联合治疗,不仅可快速获得视力提升,其结果也可维持长达48周。这提示临床中遇到此类持续性DME患者,可尽早行联合IDI治疗,以获得更快更好的视力提升。
在安全性方面,本研究主要通过术后不良反应进行评价。在高眼压方面,有研究观察玻璃体内注射雷珠单抗、阿柏西普及IDI(傲迪适)3种不同药物后短期(术前、术后即刻及术后30 min、1 h、2 h、1 d)眼压变化发现,玻璃体内注射0.1 mL雷珠单抗或阿柏西普可引起暂时性眼压升高,均可自行降至正常,0.7 mg傲迪适玻璃体内注射引起的暂时性眼压升高不明显[17]。这与本研究结果单药组在注药早期发生一过性高眼压情况一致,考虑为眼内容物短期增加所导致的一过性变化,且均能自行恢复,本研究抗VEGF药物注射量为0.05 mL,较前述研究不同,因此发生术后一过性高眼压比例较低。联合组在后期抗VEGF治疗中也有一过性眼压增高情况,但与单药组比较差异没有统计学意义。有研究显示,IDI发生眼压增高的比率为28.5%,且平均在注药后2个月达到峰值,4个月后可恢复到基线水平[18-19]。本研究联合组高眼压发生率为24%,发生时间在注药后1~2个月,均可用药物控制至正常范围,且未引起视力下降、视野缺损及神经纤维层厚度改变。眼压正常后距离IDI后3个月均可停用药物,与前述研究结果类似。亦提示对于IDI联合治疗的患者需密切观察眼压变化并及时给予药物控制,避免发生不可逆性病变。其次,在白内障方面,有研究显示,基线时有晶状体眼晶状体变性(皮质、 核或后囊膜混浊)的患者为85%,在使用IDI第1年后,白内障相关并发症的发生率增加,如皮质、核或后囊膜混浊加重,超3/4的白内障手术在研究的18~39个月进行[20]。Reid等[21]研究表明,接受多次注射的患者,其白内障形成的风险更高。本研究联合组白内障发展2例,单药组1例,3例患者均为高龄患者(>65岁),其白内障发展程度均未达需手术干预程度,可能与观察时间不足有关。两组患眼均未有发生其他严重并发症如视网膜脱离及眼内炎等。鉴于以上不良反应的研究,本研究在治疗期间密切观察患者眼压变化,整体评价其具有良好的安全性。
4 结论
IDI早期联合康柏西普可快速缓解抗VEGF治疗反应不佳DME患眼黄斑水肿,获得更好的持续性视力改善,其效果优于康柏西普单药。联合治疗需关注患者眼压增高的可能,尤其在注射后1~2个月为发生高峰期。本研究不足之处为本研究是回顾性分析,加之样本量较少,纳入标准及随访标准等还存在一定的不足,研究结果仍有待于进一步的多中心、大样本的分析研究佐证。
