有氧运动对慢性非细菌性前列腺炎大鼠血清环氧化酶-2和前列腺素E2表达的影响
2023-08-28李章春孙海波党荣敏胡先运
李章春,孙海波△,刘 萍,宁 燕,党荣敏,秦 萍,胡先运
1.黔南民族医学高等专科学校,贵州都匀 558000;2.贵州医科大学,贵州贵阳 550004
慢性非细菌性前列腺炎(CAP)是男性泌尿科的常见病和多发病,全世界发病率为3%~16%,我国发病率高达17.2%~24.6%[1-3]。由于CAP发病机制还未十分明确,常用的抗菌药物、α1-受体阻滞剂等药物治疗效果并不理想,且长期服用该类药物又易出现不同程度的不良反应,对患者的生活质量造成严重的影响[4]。CAP发病机制研究发现,氧化应激反应在其发生与发展过程中发挥了重要的作用,环氧化酶-2(COX-2)、前列腺素E2(PGE2)水平的升高能进一步加剧患者的疼痛[5-6]。随着CAP治疗研究的不断发展,运动疗法能够缓解CAP的炎症作用已被证实[7-8],有氧运动的抗氧化、降低氧化损伤作用,为CAP运动疗法研究提供了新的思路。为此,本研究通过观察CAP大鼠血清COX-2、PGE2表达,探讨有氧运动对CAP辅助治疗的作用机制。现报道如下。
1 材料与方法
1.1标本来源 SPF级SD雄性大鼠,体重200~220 g,长沙市天勤生物技术有限公司提供,许可证号:SCXK(湘)2019-0013。SPF级SD雄性大鼠随机分为正常对照大鼠(正常组)、CAP模型对照大鼠(模型组)、有氧运动大鼠(运动组),每组10只大鼠,喂养3 d后开始模型制备。
1.2试剂与药物 大鼠COX-2、PGE2、IL-6、IL-8和肿瘤坏死因子-α(TNF-α) 酶联免疫吸附试验试剂盒,购自武汉纯度生物科技有限公司;消痔灵注射液,购自吉林集安益盛药业股份有限公司,国药准字Z22026175。
1.3方法
1.3.1模型制备 采用乙醚进行大鼠麻醉,后仰位置于消毒毛巾上,于下腹部正中位进行常规消毒等处理后行2 cm左右切口,找到并提起膀胱,将准备好的25%消痔灵注射液以每侧0.1 mL的剂量分别注入两侧的前列腺背叶内,逐层进行缝合,模型制备时间7 d[9],7 d后运动组开始进行游泳有氧运动。
1.3.2运动条件及方法 泳池材质:塑料;规格:宽、长、高依次为70 cm×120 cm×60 cm;水深:约50 cm;水温:33~36 ℃;运动方法[10]:游泳运动采用无负重形式,第1天游泳时间为35 min,第2天起每天增加5 min,直至50 min,此后每天进行一次50 min的游泳运动,每周休息1 d,游泳运动6 d,共持续4周,模型组和正常组不进行游泳运动,自由进食和饮水。每次运动结束后迅速捞起大鼠,用干毛巾将其身体擦干。
1.3.3实验取材 末次游泳结束2 h后,对每组大鼠进行称重并记录,股动脉取血,经常规静置、离心后,取上清液待测备用;处死大鼠后,于操作台剪下前列腺及膀胱,剔除膀胱和脂肪,小心剥离前列腺组织,后滤纸吸干并进行称重记录,取部分前列腺组织置于4%的多聚甲醛中固定。
1.3.4指标检测 采用酶联免疫吸附试验法检测大鼠血清COX-2、PGE2表达和IL-6、IL-8和TNF-α水平,酶标仪型号:mindrady MR-96A。
1.3.5白细胞计数和卵磷脂小体计数方法 依据文献[11]方法,取大鼠相同部位的部分前列腺组织采用电子天平称重,以4 μL/mg加入0.9%无菌NaCl溶液比例充分研磨至匀浆液,吸取20 μL匀浆液加0.38 mL白细胞稀释液进行混匀(稀释20倍),在白细胞计数池中滴10 μL混合液,静置2~3 min,显微镜下对四角4个大方格内的白细胞总数进行计数(白细胞计数/mL=计数区白细胞总数/20×106/mL);另取10 μL匀浆液,进行卵磷脂小体密度观察,卵磷脂小体计数方法同白细胞计数方法。
1.3.6大鼠前列腺组织病理评分方法 0分为前列腺组织内均匀分布粉红色分泌物,结构正常无明显炎性改变;1分为前列腺组织轻度水肿且腔内粉红色分泌物减少;2分为前列腺组织内水肿和炎细胞浸润明显,出现局灶性坏死的腺上皮面积<1/3;3分为前列腺组织内水肿和炎细胞浸润明显,1/3<出现局灶性坏死的腺上皮面积<1/2;4分为前列腺组织内高度水肿,炎细胞浸润明显,出现局灶性坏死的腺上皮面积>1/2[12]。
1.3.7标本处理 取出经甲醛固定备用的前列腺组织,经常规的组织脱水、浸蜡、切片等处理后,进行HE染色,光镜下观察组织病理学改变。

2 结 果
2.1各组大鼠血清IL-6、IL-8、TNF-α水平比较 与正常组比较,运动组和模型组大鼠血清IL-6、IL-8、TNF-α水平升高,差异有统计学意义(P<0.05);与模型组比较,运动组大鼠血清IL-6、IL-8、TNF-α水平降低,差异有统计学意义(P<0.05)。见表1。
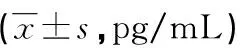
表1 各组大鼠血清IL-6、IL-8、TNF-α水平比较
2.2各组大鼠血清COX-2、PGE2表达比较 与正常组比较,运动组和模型组大鼠血清COX-2、PGE2表达升高,差异有统计学意义(P<0.05);与模型组比较,运动组大鼠血清COX-2、PGE2表达降低,差异有统计学意义(P<0.05)。见表2。

表2 各组大鼠血清COX-2、PGE2表达比较
2.3COX-2、PGE2表达与IL-6、IL-8、TNF-α水平相关性分析 相关性分析显示,CAP大鼠血清内COX-2、PGE2表达与IL-6、IL-8、TNF-α水平呈正相关(P<0.01),COX-2与PGE2也呈正相关(P<0.01)。见表3 。

表3 COX-2、PGE2表达与IL-6、IL-8、TNF-α水平相关性分析
2.4各组大鼠前列腺组织内白细胞计数和卵磷脂小体计数比较 与正常组比较,运动组和模型组大鼠前列腺组织内白细胞计数均升高,卵磷脂小体计数均降低,差异有统计学意义(P<0.05);与模型组比较,运动组白细胞计数降低,卵磷脂小体计数上升,差异有统计学意义(P<0.05)。见表4。
表4 各组大鼠前列腺组织内白细胞计数和卵磷脂小体计数比较个/mL)
2.5不同组别大鼠前列腺组织病理评分比较 与正常组比较,运动组和模型组大鼠前列腺组织病理评分的平均计分升高,差异有统计学意义(P<0.05);与模型组比较,运动组大鼠前列腺组织病理评分的平均计分降低,差异有统计学意义(P<0.05)。见表5。
表5 不同组别大鼠前列腺组织病理评分比较
2.6有氧运动对CAP大鼠前列腺组织病理学改变的影响 通过显微镜观察各组大鼠前列腺组织,检测结果显示,正常组大鼠前列腺组织病理学检查未见异常(图1);模型组大鼠前列腺组织则呈现明显的慢性炎症改变,镜下可见腺体上皮细胞增生明显,周围间质明显纤维化,层次增加,大量淋巴细胞等慢性炎症细胞浸润,间质内毛细血管扩张,红细胞增加(图2);与模型组比较,运动组大鼠前列腺组织慢性炎症病理改变减轻,可见腺体上皮细胞增生数量、间质纤维化程度及慢性炎症细胞浸润现象均明显减轻(图3)。

图1 正常组大鼠前列腺组织病理切片(HE染色,×100)
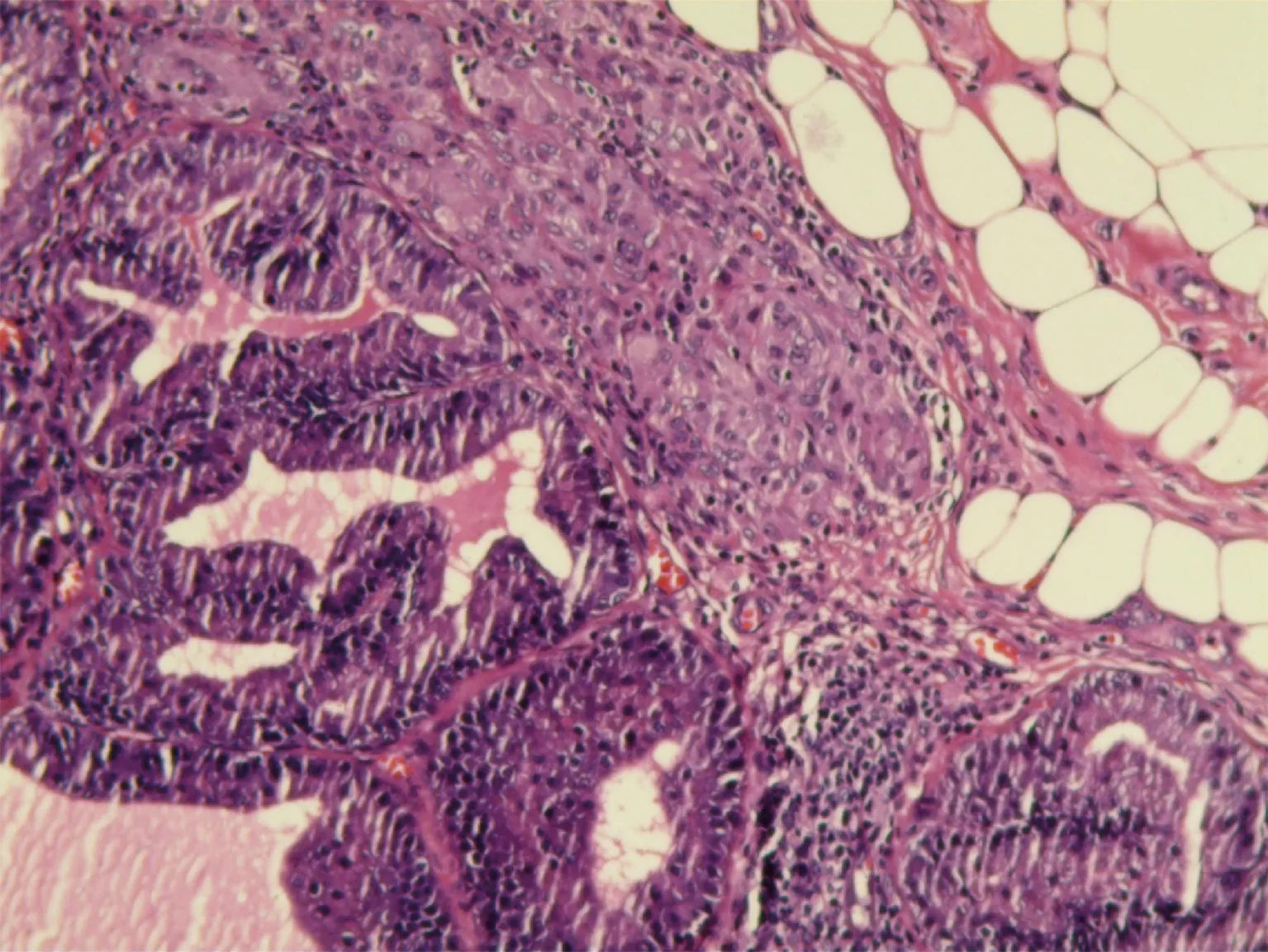
图2 模型组大鼠前列腺组织病理切片(HE染色,×100)

图3 运动组大鼠前列腺组织病理切片(HE染色,×100)
3 讨 论
《中国健康管理与健康产业发展报告(2018)》发布数据显示[13],慢性病已严重威胁我国居民身心健康。为进一步提高全民健康水平,国务院办公厅已印发《中国防治慢性病中长期规划(2017-2025年)》,倡导通过开展健步走、适量运动等形式提升全民健康素质[14],更是通过颁布《“健康中国2030”规划纲要》文件,把全民健康上升到国家战略层面,呼吁加强“体医融合”,要在慢性病的预防和康复过程中发挥科学健身的积极作用[15]。2019年,国务院又颁发了《关于实施健康中国行动的意见》,再次强调推动形成体医结合的疾病管理和健康服务模式,为不同人群提供针对性的运动健身方案[16]。可见,发挥科学运动在疾病管理中的重要作用已上升到国家层面。CAP发病机制研究发现,不良生活习惯、久坐等是其重要的诱因之一[1]。有研究均已证实,有氧运动能够通过降低CAP患者或动物模型体内的细胞因子水平,对CAP起到缓解作用[7,10]。本研究结果显示,与正常组比较,运动组和模型组大鼠血清IL-6、IL-8、TNF-α水平升高,差异有统计学意义(P<0.05);与模型组比较,运动组大鼠血清IL-6、IL-8、TNF-α水平降低,差异有统计学意义(P<0.05),表明有氧运动能够降低CAP大鼠血清细胞因子水平。本研究结果还发现,与模型组比较,运动组大鼠血清COX-2、PGE2表达降低,差异有统计学意义(P<0.05)。
环氧化酶(COX)也被称为前列腺素内氧化酶还原酶,能够调节前列腺素(PG)的生成,在炎症反应过程中发挥重要作用,与组织疼痛关系密切。COX-2是COX的诱导型酶,通常情况下在内脏组织中无表达或低水平表达,但受到肿瘤、细胞因子等因素刺激能够在短期内快速升高[17]。有研究发现,COX-2表达与CAP的关系密切,CAP大鼠COX-2表达显著高于正常大鼠,并可能参与了大鼠神经疼痛的形成,可以作为CAP治疗和预后的一个重要诊断[18-19]。有研究证实,CAP患者前列腺液内COX-2存在高表达,通过抑制COX-2表达能够缓解患者疼痛,改善排尿等症状[20]。本研究结果显示,与正常组比较,运动组和模型组大鼠血清COX-2、PGE2表达升高,差异有统计学意义(P<0.05);与模型组比较,运动组大鼠血清COX-2、PGE2表达降低,差异有统计学意义(P<0.05),表明有氧运动能够降低CAP大鼠血清COX-2表达。原因可能为:一方面有氧运动能够降低CAP大鼠血清细胞因子水平,而COX-2表达与TNF-α、IL-6、IL-8水平呈显著正相关(P<0.01),这些细胞因子水平的降低可能下调了COX-2表达;另一方面长期有规律的有氧运动能够提高机体抗氧化酶的水平,进而对COX-2表达发挥下调作用[21-22]。
PG是一种脂肪酸衍生物,在人体体液和组织中有着广泛的分布,在疼痛、炎症反应、肿瘤等方面具有重要作用,PGE2为其家族中重要的一员,是肿瘤和感染的重要介质,也是维持内环境稳定的重要因子[23]。PGE2的表达受COX-2的调控和影响,抑制COX-2的表达能够下调PGE2的合成。有研究表明,降低PGE2、细胞因子等表达能够改善CAP大鼠前列腺组织病理学改变[24]。本研究结果发现,与模型组比较,运动组大鼠血清PGE2表达降低,差异有统计学意义(P<0.05)。病理观察显示,相比较模型组,运动组大鼠前列腺组织慢性炎症细胞浸润现象明显减轻,表明有氧运动能够对CAP大鼠前列腺组织炎症起到缓解作用,其作用机制可能是有氧运动降低TNF-α、IL-6、IL-8水平和COX-2表达,通过COX-2-PGE2通路作用,进而对PGE2的表达产生抑制。有研究证实,规律性的身体活动能够对病理状态或多种生理变化发挥抗氧化及抗炎作用[25]。
综上所述,本研究认为长期有规律的有氧运动能够抑制CAP大鼠血清COX-2、PGE2的表达,COX-2-PGE2通路在疾病的形成和发展过程中发挥了重要作用,而有氧运动对其影响还处于探索阶段,还需进一步开展广泛而深入的研究。
