PPOS方案用于卵巢高反应患者的效果评价
2023-08-21李力男王明磊张晓磊陈永乾吴华颖
李力男,王明磊,张晓磊,陈永乾,吴华颖
卵巢高反应是指在控制性卵巢刺激(controlled ovarian stimulation,COS)中出现对外源性促性腺激素(gonadotropin,Gn)异常敏感,表现为大量卵泡募集、发育及雌激素的明显增高[1]。卵巢高反应患者在COS中易发生早发黄体生成素(luteinizing hormone,LH)峰及卵巢过度刺激综合征(ovarian hyperstimulation syndrome,OHSS)[2],不但可能影响胚胎质量和子宫内膜容受性,而且OHSS加重了患者的心理、经济负担[3-4]。拮抗剂方案通过垂体非降调节方式,通过药物、扳机选择,在一定程度上降低了OHSS的发生率,是目前卵巢高反应的常用促排卵方案[5]。高孕激素下促排卵(progestin-primed ovarian stimulation,PPOS)方案通过大剂量孕激素抑制LH增加,达到卵泡募集作用,在不同卵巢储备功能的不孕患者中取得了良好的效果[6-7]。本研究旨在比较应用拮抗剂方案和PPOS方案对卵巢高反应患者的促排卵效果及妊娠结局影响,为卵巢高反应患者方案选择提供依据。
1 资料和方法
1.1 研究对象
回顾性分析2021年1月至2022年12月在哈尔滨医科大学附属第一医院生殖医学科行体外受精(in vitro fertilization,IVF)/卵细胞浆内单精子注射(intracytoplasmic sperm injection,ICSI)的158例卵巢高反应患者的临床资料,根据不同促排卵方案分为两组,PPOS组:应用PPOS方案73例,拮抗剂组:应用拮抗剂方案85例。
纳入标准[1]:① 患者年龄<40岁;② 在COS中发育卵泡数>20个,和/或获卵数>15 个;③ 抗苗勒管激素(anti-Müllerian hormone,AMH)>8 ng/mL;④ 体质量指数(body mass index,BMI)<28 kg/m2;⑤ 新鲜周期促排卵后行全胚冷冻,择期行冻融胚胎移植。排除标准:① 染色体异常;② 生殖系统发育异常;③ 中重度子宫内膜异位症、腺肌病;④ 子宫内膜病变;⑤ 合并其他内外科疾病,不适宜妊娠者,以及合并其他引起雌激素增高疾病。本研究经医院伦理委员会批准,患者知情并签署同意书。
1.2 促排卵方案
所有患者月经出血第2~4天就诊,行超声检查和性激素测定,进入促排卵周期。根据基础窦卵泡数(AFC)水平、基础激素水平、年龄、BMI、AMH确定Gn(果纳芬,瑞士默克雪兰诺公司)起始剂量,起始剂量为100~150 IU/d。PPOS方案口服安宫黄体酮(醋酸甲羟孕酮,浙江仙琚制药)10 mg/d直至人绒毛膜促性腺激素(human chorionic gonadotropin,hCG)日。拮抗剂方案根据LH水平和卵泡大小采用灵活方案加用醋酸西曲瑞克(思则凯,瑞士默克雪兰诺公司)0.25 mg/d直至hCG日。经阴道超声监测卵泡发育情况,测定血清E2、LH、孕激素(progesterone,P)水平,调整促排卵用药剂量。当2~3个优势卵泡≥18 mm,注射醋酸曲谱瑞林(达必佳,辉灵制药有限公司)0.2 mg,36 h后经阴道超声下取卵,胚胎培养后全胚冷冻。
1.3 冻融胚胎移植方案
冷冻移植内膜准备方案采用替代周期,月经出血2~4 d口服戊酸雌二醇(补佳乐,德国拜耳公司) 6~8 mg/d,6~8 d后行超声检查,根据内膜厚度调整雌激素剂量,当内膜厚度≥8 mm,转化内膜,加用地屈孕酮(达芙通,荷兰苏威制药有限公司)40 mg/d,黄体酮阴道缓释凝胶(雪诺酮,瑞士默克雪兰诺公司)90 mg/d。移植1~2枚卵裂期胚胎,移植后14 d验孕,hCG≥50 mIU/mL为生化妊娠,补佳乐逐渐减量。生化妊娠后21 d行超声检查,超声下见妊囊及胎心搏动为临床妊娠,达芙通减量并维持至妊娠12周,雪诺酮维持至妊娠10周。
1.4 观察指标
评估两组患者一般资料:年龄、不孕年限、不孕类型、BMI、AMH、基础AFC、基础性激素。促排卵情况:Gn用量、Gn天数、早发LH峰率(LH≥10 U/L,且 LH 水平超过基线值2.5倍)、OHSS发生率、既往IVF失败情况、优势卵泡数(hCG日直径>14 mm)。胚胎情况:获卵数、MII数、2PN数、2PN卵裂数、可移植胚胎数、优质胚胎数、2PN受精率、MII卵率、2PN卵裂率、优胚率、受精方式。妊娠情况:生化妊娠率、胚胎种植率、临床妊娠率、累计妊娠率[8](指一次促排卵后获得的胚胎经过冷冻移植后获得临床妊娠,不包括尚未获得临床妊娠且仍有冷冻胚胎者)、早期流产率、异位妊娠率。
1.5 统计学方法
2 结果
2.1 两组一般资料比较
两组患者年龄、不孕年限、不孕类型、BMI、AMH、基础AFC,基础E2、基础LH、基础卵泡刺激素(follicle-stimulating hormone,FSH)、基础P水平差异无统计学意义(P>0.05)。详见下页表1。

表1 两组一般资料比较
2.2 两组促排卵情况及胚胎情况比较
PPOS组Gn用量、Gn时间、早发LH峰率、OHSS发生率明显低于拮抗剂组,差异有统计学意义(P<0.05)。PPOS组既往IVF失败率高于拮抗剂组,差异有统计学意义(P<0.05)。PPOS组MII卵率、2PN卵裂率高于拮抗剂组,差异有统计学意义(P<0.05)。两组获卵数、MII数、2PN数、2PN卵裂数、可移植胚胎数、优质胚胎数、2PN受精率、优胚率、受精方式比较,差异无统计学意义(P>0.05)。详见表2。

表2 两组促排卵情况及胚胎情况比较
2.3 两组妊娠情况比较
PPOS组首次冷冻移植63例,32例获得临床妊娠,拮抗剂组首次冷冻移植73例,39例获得临床妊娠。两组间生化妊娠率、胚胎种植率、临床妊娠率、累计妊娠率、早期流产率、异位妊娠率差异无统计学意义(P>0.05)。详见表3。
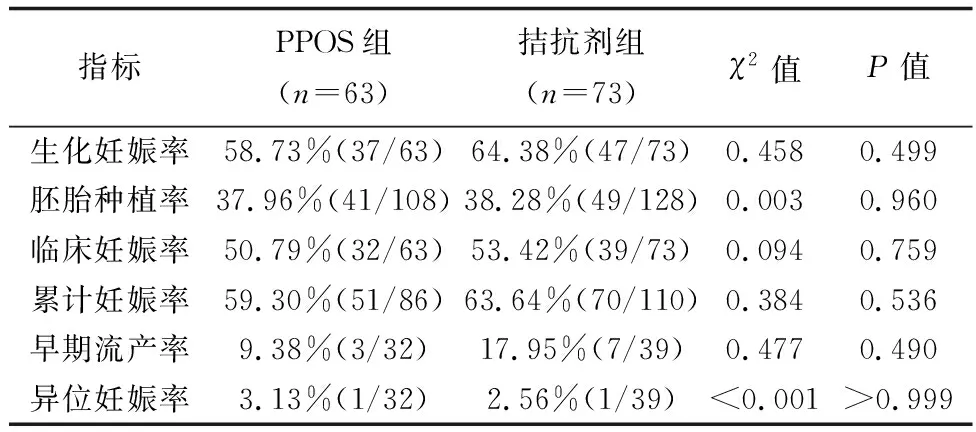
表3 两组妊娠情况比较
3 讨论
卵巢高反应患者卵泡期可能表现出早发LH峰,卵泡生成过程中高水平的LH可能过早激活减数分裂过程并损害卵母细胞,导致细胞凋亡。LH的过度分泌还可能促进卵泡中的颗粒细胞过早黄素化和卵泡闭锁,卵母细胞过早成熟,会损害卵母细胞和胚胎的质量[9-10]。由于多卵泡发育,卵巢体积增大,雌二醇水平升高,易诱发OHSS。PPOS方案2015年由Kuang等[11]提出,通过口服孕激素,作为促性腺激素释放激素(gonadotropin-releasing hormone,GnRH)类似物的替代品,在卵泡期早期,利用高水平孕激素负反馈的作用,从而抑制LH过早升高。拮抗剂方案通过促性腺激素释放激素拮抗剂抑制早发LH水平升高。两种方案在一定程度上都能抑制LH早发。本研究采用GnRH激动剂扳机,不但能够促进卵子成熟,避免应用hCG,减少OHSS发生。所有患者采用全胚冷冻,冷冻移植也避免了新鲜周期妊娠导致的卵巢过度刺激症状加重。
本研究发现PPOS方案与拮抗剂方案相比,Gn时间短、剂量少,PPOS方案口服孕激素用药更为简单,花费更少,患者经济负担小。Chen等[12]研究显示过高的LH与卵母细胞和胚胎质量的显著下降有关,导致多囊卵巢综合征女性的妊娠率降低和流产率升高。PPOS方案与拮抗剂方案相比,能更有效地抑制早发LH峰发生,减少由于LH过高对于卵子的不利影响,这与Wang等[13]研究结果一致。Xiao等[14]研究提出PPOS组与拮抗剂组相比,轻中度OHSS发生率更低。本研究中PPOS方案无OHSS发生,与拮抗剂方案相比,更有效地降低了OHSS发生率。
Carter等[15]提出,在培养基中添加孕激素不影响胚胎在体外发育至囊胚。Wang等[16]研究表明PPOS 组的活产缺陷发生率 (1.52%) 与短方案组 (1.63%) 相似,PPOS方案不增加新生儿先天畸形发生风险,证明了PPOS方案应用的安全性。Xiao等[14]研究表明卵巢高反应患者应用PPOS方案与拮抗剂方案相比,着床率、临床妊娠率、流产率相似。本研究PPOS方案应用高剂量孕激素促排卵,并未影响卵子和胚胎质量,通过冷冻移植能够获得与拮抗剂相似的妊娠结局,证明了PPOS方案对于卵巢高反应患者的有效性和安全性。
本研究还有其他几点发现:① PPOS组MII卵率、2PN卵裂率明显高于拮抗剂方案组,这可能是与PPOS组不易出现异常LH有关,更有利于卵子发育。② 尽管PPOS组在获卵数、可移植胚胎数均优于拮抗剂组,生化妊娠率、临床妊娠率略低于拮抗剂组,但差异均无统计学意义。这可能与PPOS组既往失败次数更多相关,也可能是由于样本量小导致。③ 本研究为回顾性研究,纳入样本量较少,由于随访时间不足,并未随访活产率及新生儿畸形率,在后续研究中,还需进一步扩大样本量,完善实验设计,开展随机对照研究,更系统全面地比较不同方案的应用价值。
综上所述,对于卵巢高反应患者,应用PPOS方案,花费更少,能够抑制早发LH峰,避免OHSS发生,并且获得与拮抗剂方案相似的胚胎质量和妊娠结局。但目前PPOS方案不是正常卵巢功能和卵巢高反应患者的主流方案,由于高孕激素水平影响子宫内膜容受性,导致子宫内膜种植床提前关闭,不能新鲜周期移植,而拮抗剂可以进行新鲜周期移植,缩短妊娠时间,减少冷冻胚胎风险。因此对于促排前评估OHSS发生高风险者、既往IVF-ET失败者,可以考虑应用PPOS方案,为卵巢高反应患者促排卵提供一种新的选择。
