铜阳极泥脱铜渣中铅的高效浸出试验研究
2023-08-05王佳寅南君芳李斌川陈建设刘奎仁
王佳寅,韩 庆,南君芳,李斌川,陈建设,刘奎仁
(1.东北大学 有色金属资源循环利用沈阳市重点试验室,辽宁 沈阳 110819;2.东北大学 冶金学院,辽宁 沈阳 110819;3.国投金城冶金有限责任公司,河南 灵宝 472500)
铜阳极泥是铜电解精炼的副产品之一,其中含有Au、Ag等有价金属,具有一定回收价值[1-2]。其处理工艺主要包括传统火法、卡尔多炉、全湿法、半湿法和选冶联合法等[3]。其中,铜阳极泥半湿法处理工艺因具有成本低、污染小等优点[4],相比其他方法应用更广泛,其主要流程为硫酸化焙烧脱硒—酸浸脱铜—氯化分金—亚钠分银—金银还原与精炼[5]。
脱铜渣是铜阳极泥经过硫酸化焙烧和酸浸脱铜2个工序所产生的重要中间产物之一,通常含有大量贱金属化合物[6-8],其中PbSO4质量分数可达20%[9]。在提取贵金属过程中,Pb2+进入溶液会形成PbO覆盖在Au、Ag表面,对Au、Ag溶解起到抑制作用,阻碍其浸出[10];在后续氯化金离子的还原过程中,铅等杂质会干扰其还原电位,对还原过程产生不利影响[11];此外,脱铜渣中大量的PbSO4极易导致所得金属产品中铅含量超标[12]。目前,有关铜阳极泥脱铜渣湿法脱铅的研究鲜见报道。
湿法提铅方法主要有碱浸法、氯盐法和碳酸盐转化—酸浸法。碱浸法脱铅存在碱度要求高、浸出过程选择性差、浸出液黏度较大且成分复杂等问题[13-14],不利于脱铜渣中有价金属的富集;用碳酸盐转化—酸浸法从金矿焙烧酸浸渣中脱铅,铅转化率与浸出率分别可达97%和83%[15-16],但该工艺流程复杂,酸浸过程选择性较差,不适用于脱铜渣中铅的脱除;采用NaCl-HCl体系对阳极泥脱铜渣进行二段脱铅,脱铅率较高,金浸出率也能得到大幅提升,但该体系选择性较差,浸出液成分复杂,有价金属分离困难[17]。因此,探寻一种选择性强、浸出效果好的高效浸出剂对脱铜渣脱铅具有重要意义。
乙二胺四乙酸二钠(EDTA-2Na)是常用的螯合剂之一,其性质稳定且无氧化还原性,多用于鉴定金属离子和改善土壤中重金属超标问题[18]。脱铜渣中多数有价金属主要以单质、金属氧化物或其他复杂化合物形式存在,铅则主要以简单离子化合物PbSO4形式存在,溶液中EDTA有效配体极易与重金属阳离子螯合,且EDTA-2Na对Pb2+具有较强的螯合作用。试验研究了用以EDTA-2Na从脱铜渣中浸出PbSO4,考察了EDTA-2Na用量、浸出时间、浸出温度、溶液pH和液固体积质量比对Pb浸出率的影响,并探讨了浸出动力学。
1 试验部分
1.1 试验原料、试剂与设备
脱铜渣:来自某黄金冶炼厂阳极泥处理过程,破碎球磨至过100目筛,其主要化学成分见表1,脱铜渣XRD分析结果如图1所示。脱铜渣中Pb的存在形式主要为PbSO4,Te的主要存在形式为碱溶性TeO2和Ag2Te,渣中还存在少量微溶于水的Ag2SO4,为避免其进入溶液,需加入少量NaCl,使Ag富集于渣中。
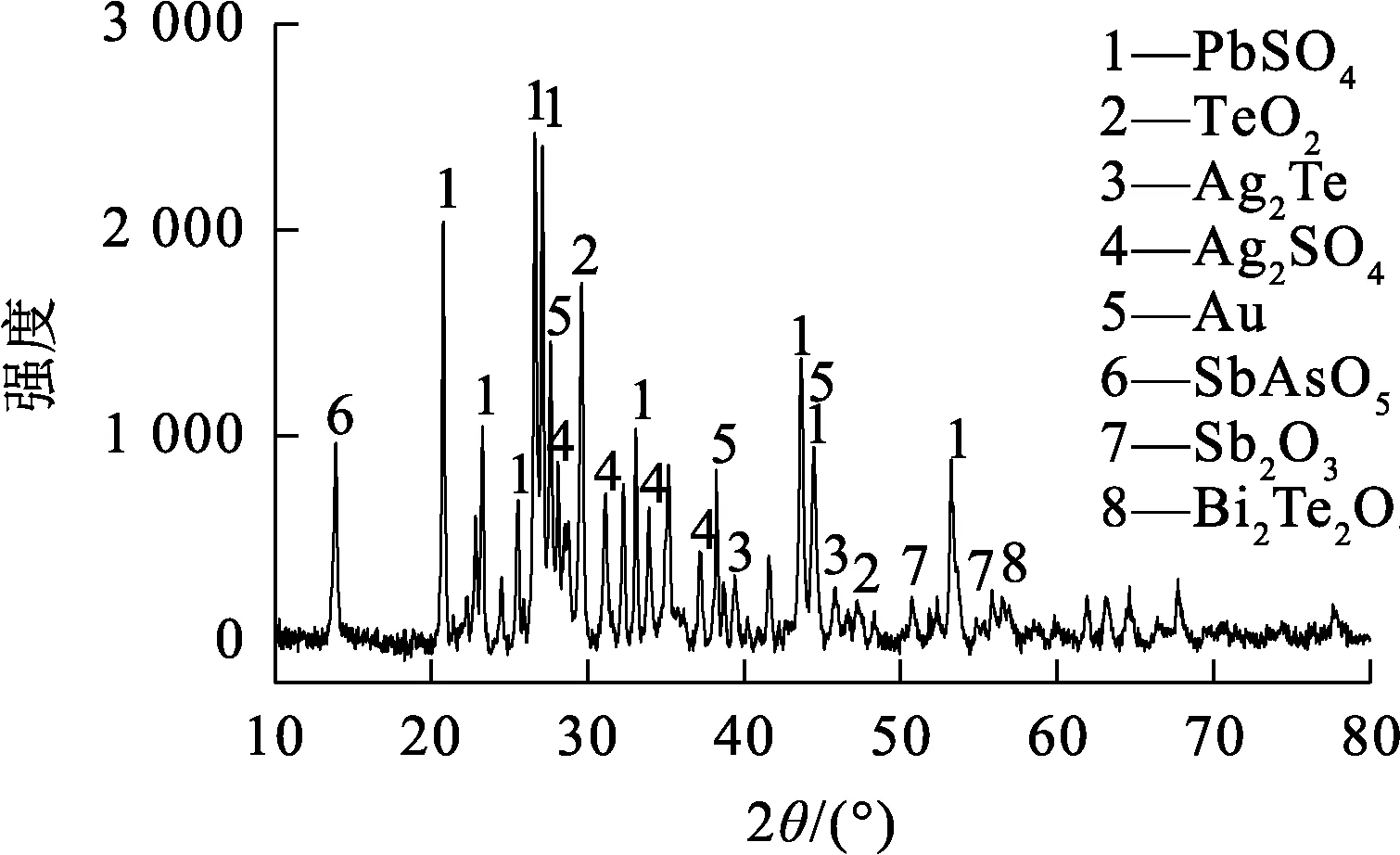
图1 脱铜渣的XRD图谱

表1 脱铜渣的主要成分 %
试验试剂:乙二胺四乙酸二钠、氢氧化钠、盐酸、九水硫化钠,均为分析纯,国药集团化学试剂有限公司。
试验设备:PHS-25型电位-pH计,上海仪电科学仪器股份有限公司;DF101S型集热式磁力搅拌器,巩义市予华仪器有限责任公司;DZF-6050型真空干燥箱,上海精宏实验设备有限公司;SHB-Ⅲ型循环水式多用真空泵,南京科尔仪器设备有限公司;UPT-Ⅱ型优普纯水机,四川优普超纯科技有限公司;D8 ADVANCE型X射线衍射仪(XRD),德国布鲁克公司;AL104型电子天平,上海沪粤明科学仪器有限公司;FMS36型ICP-OES光谱仪,德国斯派克分析仪器公司。
1.2 试验原理
脱铜渣中Pb的主要物相为PbSO4。EDTA与Pb的配合物稳定性常数的对数(lgKf)为18.04[19],配合比例为1∶1,而PbSO4溶度积常数的负对数(-lgKsp)为7.80,前者远大于后者,说明EDTA-Pb的稳定性高于PbSO4,即PbSO4可溶解于EDTA-2Na溶液。另外,脱铜渣中微溶的Ag2SO4也会进入溶液,加入适量NaCl,反应生成AgCl沉淀,将Ag富集到渣中,涉及的主要化学反应如下:

(1)

(2)
1.3 试验方法
试验在300 mL烧杯中进行,向烘干后的烧杯中按设定浸出剂用量和液固体积质量比依次加入EDTA-2Na、去离子水、NaCl。将烧杯置于集热式磁力搅拌器内(400 r/min,±0.1 ℃)开始升温,用NaOH和HCl调溶液pH,同时使用pH计进行监测。待pH与温度达到预定值后,将脱铜渣加入到烧杯中,开启搅拌并计时,搅拌过程中调pH在设定值范围内。每隔一定时间过滤少量溶液,量取定量溶液经王水消解,稀释至一定浓度范围送检,按照式(3)计算Pb浸出率。试验结束后进行抽滤,滤渣经去离子水洗涤之后密封保存,向滤液中加入与铅物质的量等量的Na2S进行硫化沉铅,沉铅后过滤收集滤液密封备用。
(3)
式中:x—铅浸出率,%;ρt—浸出t时间时溶液中铅质量浓度,g/L;V0—初始溶液体积,L;m—脱铜渣质量,g;w—脱铜渣中铅质量分数,%。
2 试验结果与讨论
2.1 n(EDTA)/n(Pb)对脱铜渣中Pb浸出率的影响
试验条件:溶液pH=5,浸出时间120 min,液固体积质量比4/1,浸出温度为323 K。n(EDTA)/n(Pb)对脱铜渣中Pb浸出率的影响试验结果如图2所示。可以看出:随n(EDTA)/n(Pb)增大,脱铜渣中Pb浸出率升高,当n(EDTA)/n(Pb)为2/1时,Pb浸出率可达99%。EDTA配体与Pb2+按1/1进行螯合,但脱铜渣中含有大量可溶性金属离子(Cu2+、Bi3+等),这些离子可与Pb2+发生配位竞争而进入溶液,故需加入足量EDTA以确保Pb的螯合浸出效果。因此,确定适宜的n(EDTA)/n(Pb)为2/1,即EDTA浓度为0.351 mol/L。
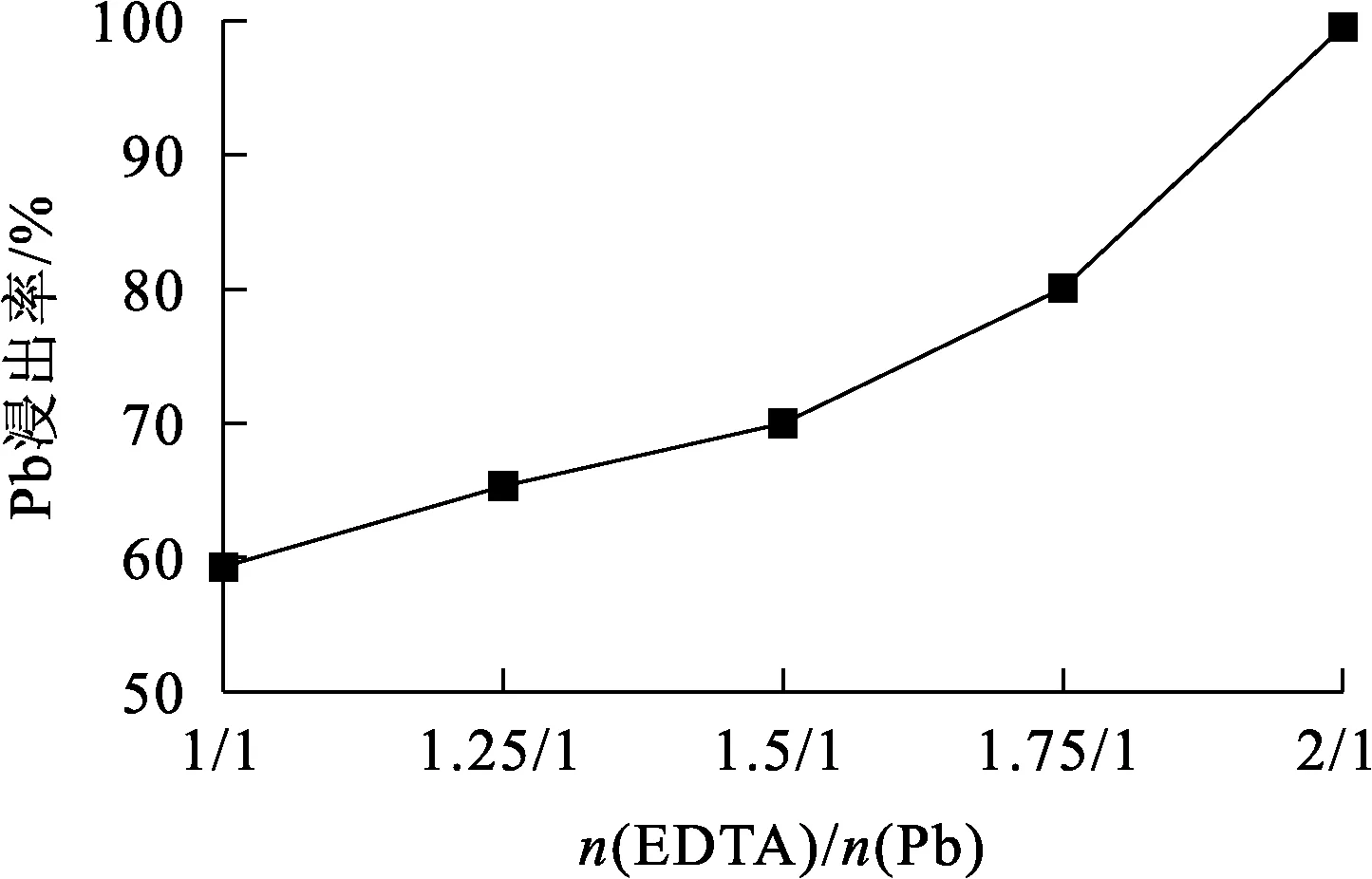
图2 n(EDTA)/n(Pb)对脱铜渣中Pb浸出率的影响
2.2 溶液pH对脱铜渣中Pb浸出率的影响
试验条件:n(EDTA)/n(Pb)=2/1,浸出时间120 min,液固体积质量比4/1,浸出温度323 K。溶液pH对脱铜渣中Pb浸出率的影响试验结果如图3所示。
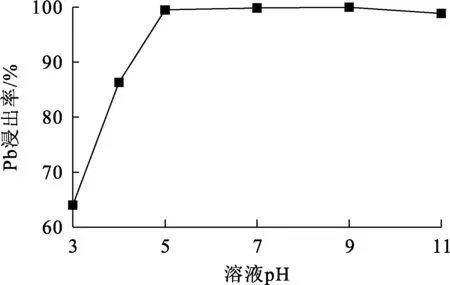
图3 溶液pH对脱铜渣中Pb浸出率的影响
由图3看出:pH<5时,随pH升高,脱铜渣中Pb浸出率快速升高;pH升至5时,Pb浸出率接近100%。这是因为在不同pH条件下,EDTA-2Na(记作Na2H2Y)在溶液中的存在形式变化较大:pH较低时,溶液中大量H+与Na2H2Y配体结合,形成不具有螯合作用的H4Y,导致EDTA-2Na溶液的螯合浸出能力大幅降低;pH=5时,溶液中EDTA的有效配体主要为H2Y2-、HY3-和Y4-,其可与Pb2+按1∶1比例进行螯合,达到浸出Pb的目的。因此,确定适宜溶液pH为5。
2.3 液固体积质量比对脱铜渣中Pb浸出率的影响
试验条件:n(EDTA)/n(Pb)=2/1,浸出时间120 min,溶液pH=5,浸出温度323 K。液固体积质量比对脱铜渣中Pb浸出率的影响试验结果如图4所示。
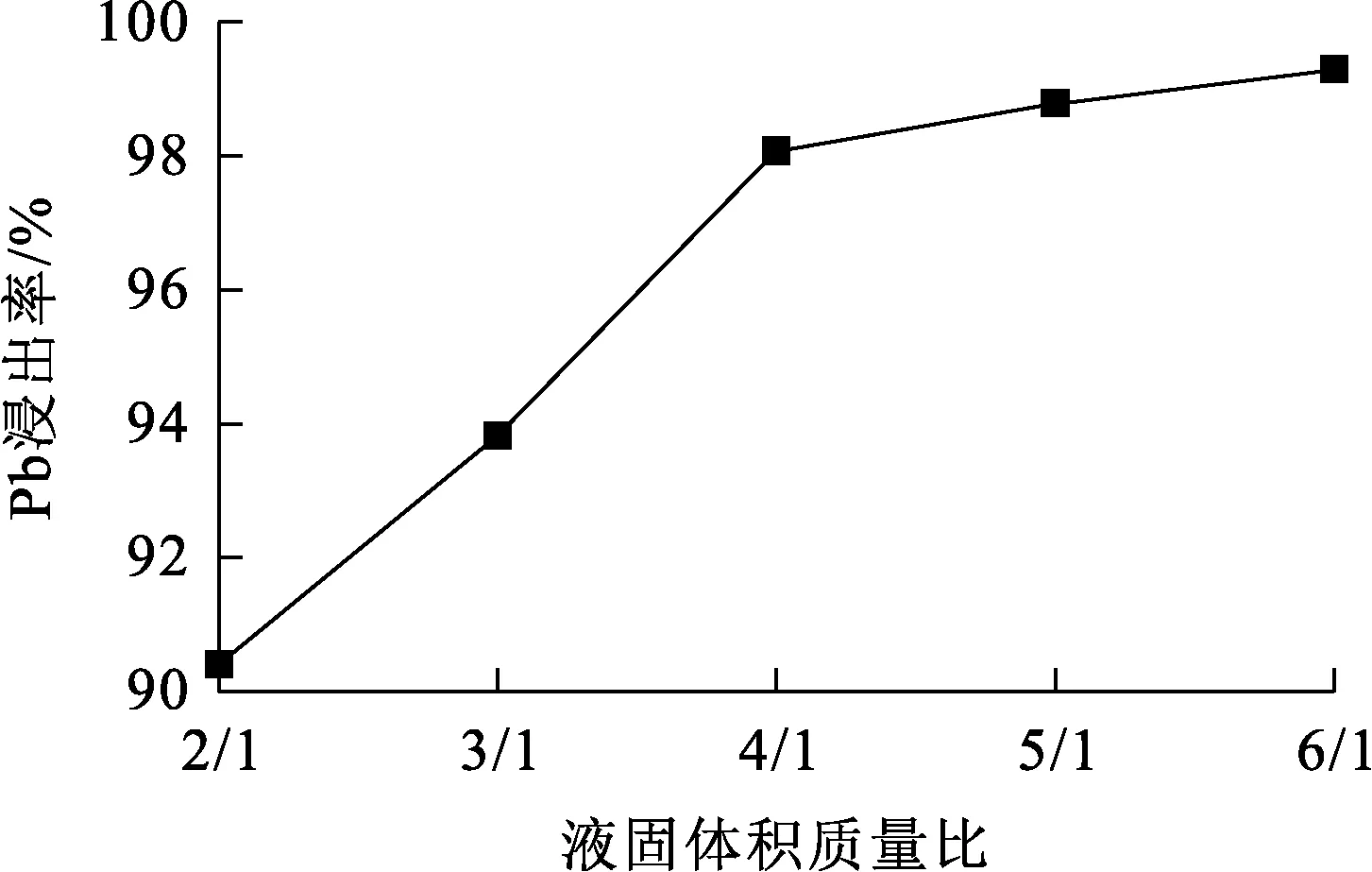
图4 液固体积质量比对脱铜渣中Pb浸出率的影响
由图4看出,随液固体积质量比增大,脱铜渣中Pb浸出率呈上升趋势:液固体积质量比增至4/1时,Pb浸出率达拐点;之后随液固体积质量比进一步增大,Pb浸出率升幅变缓。因此,确定适宜的液固体积质量比为4/1。
2.4 浸出时间对脱铜渣中Pb浸出率的影响
试验条件:溶液pH=5,n(EDTA)/n(Pb)=2/1,液固体积质量比4/1,浸出温度323 K。浸出时间对脱铜渣中Pb浸出率的影响试验结果如图5所示。
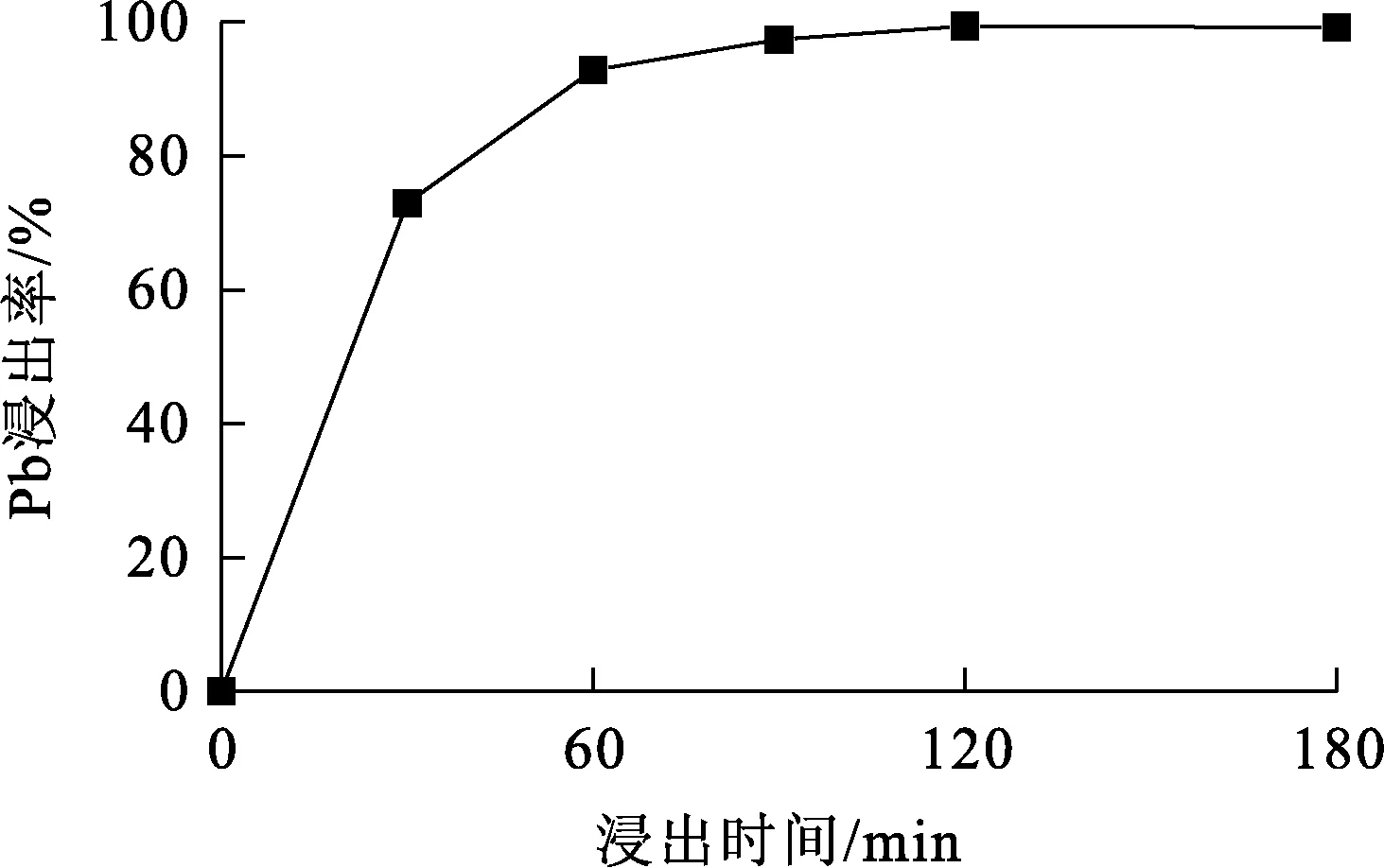
图5 浸出时间对脱铜渣中Pb浸出率的影响
由图5看出:随浸出时间延长,脱铜渣中Pb浸出率升高;浸出120 min时,Pb浸出率可达99%;继续延长浸出时间,Pb浸出率不变。因此,确定适宜浸出时间为120 min。
2.5 温度对脱铜渣中Pb浸出率的影响
试验条件:溶液pH=5,n(EDTA)/n(Pb)=2/1,浸出时间为120 min,液固体积质量比4/1。温度对脱铜渣中Pb浸出率的影响试验结果如图6所示。
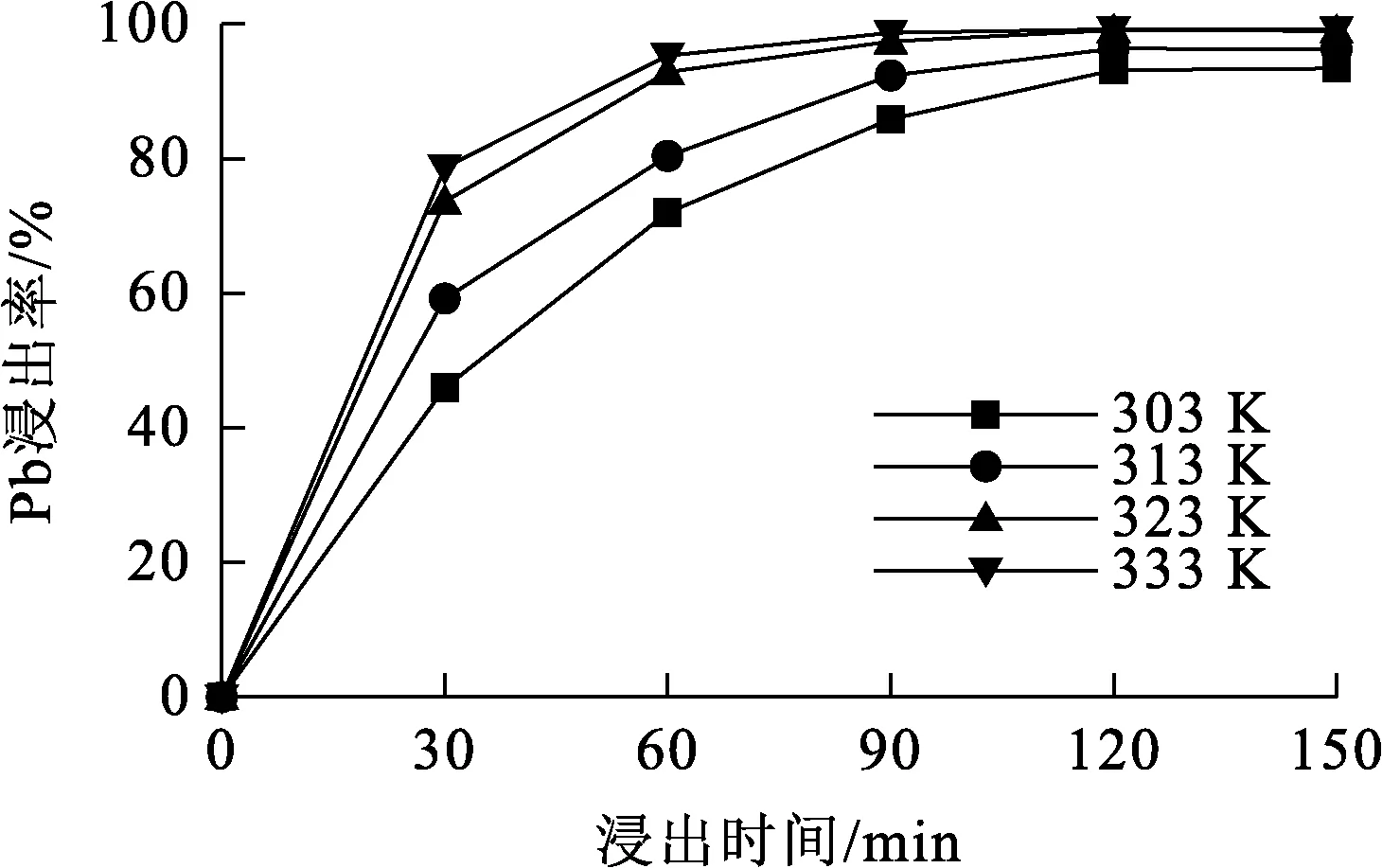
图6 温度对脱铜渣中Pb浸出率的影响
由图6看出:浸出温度为303 K,脱铜渣中Pb浸出率约为93%,随浸出温度升高,Pb浸出率有所升高;温度升至323 K时,Pb浸出率达99%左右,温度继续升高,Pb浸出率变化不大。因此,确定适宜的浸出温度为323 K。
2.6 验证试验
综合上述结果,确定最佳浸出条件为:n(EDTA)/n(Pb)=2/1,溶液pH=5,液固体积质量比4/1,浸出温度323 K,浸出时间120 min。在该条件下重复进行3次验证试验,结果见表2。
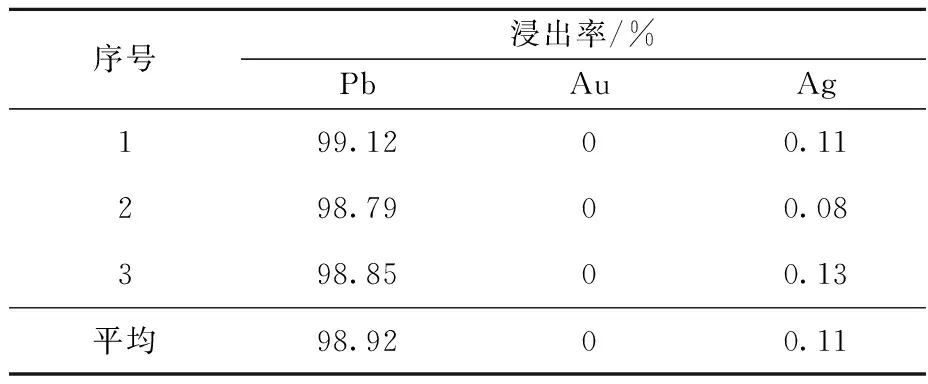
表2 验证试验结果
由表2看出:在最佳浸出条件下,Pb浸出率可稳定在99%左右;贵金属Au和Ag损失很小,可进一步加以富集。
2.7 浸出动力学分析
浸出过程是发生在固-液非均相体系中的复杂反应,由于原料颗粒足够细小,可以将其认为是一个致密的细小球型颗粒,且浸出过后仍然残留有固相颗粒,因此浸出过程符合典型的未反应核收缩模型(缩核模型)特征[20-23]。在该模型中,浸出过程主要受以下步骤影响:(内、外)扩散、界面化学反应、扩散与界面化学反应混合作用。式(4)~(7)分别描述了反应速率受液相边界层外扩散控制、固相产物层内扩散控制、界面化学反应控制和混合控制的浸出动力学规律。
x=kt;
(4)
(5)
(6)
(7)
式中:x—脱铜渣中Pb浸出率,%;t—反应时间,min;k—反应速率常数,min-1。
在排除液相边界层外扩散控制(式(4))的前提下,根据式(5)~(7)对图6中的数据进行拟合,结果分别如图7~9所示。
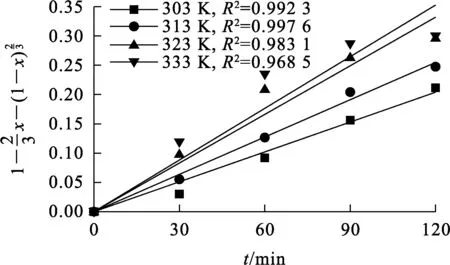
图7 不同温度下对浸出时间t的拟合曲线
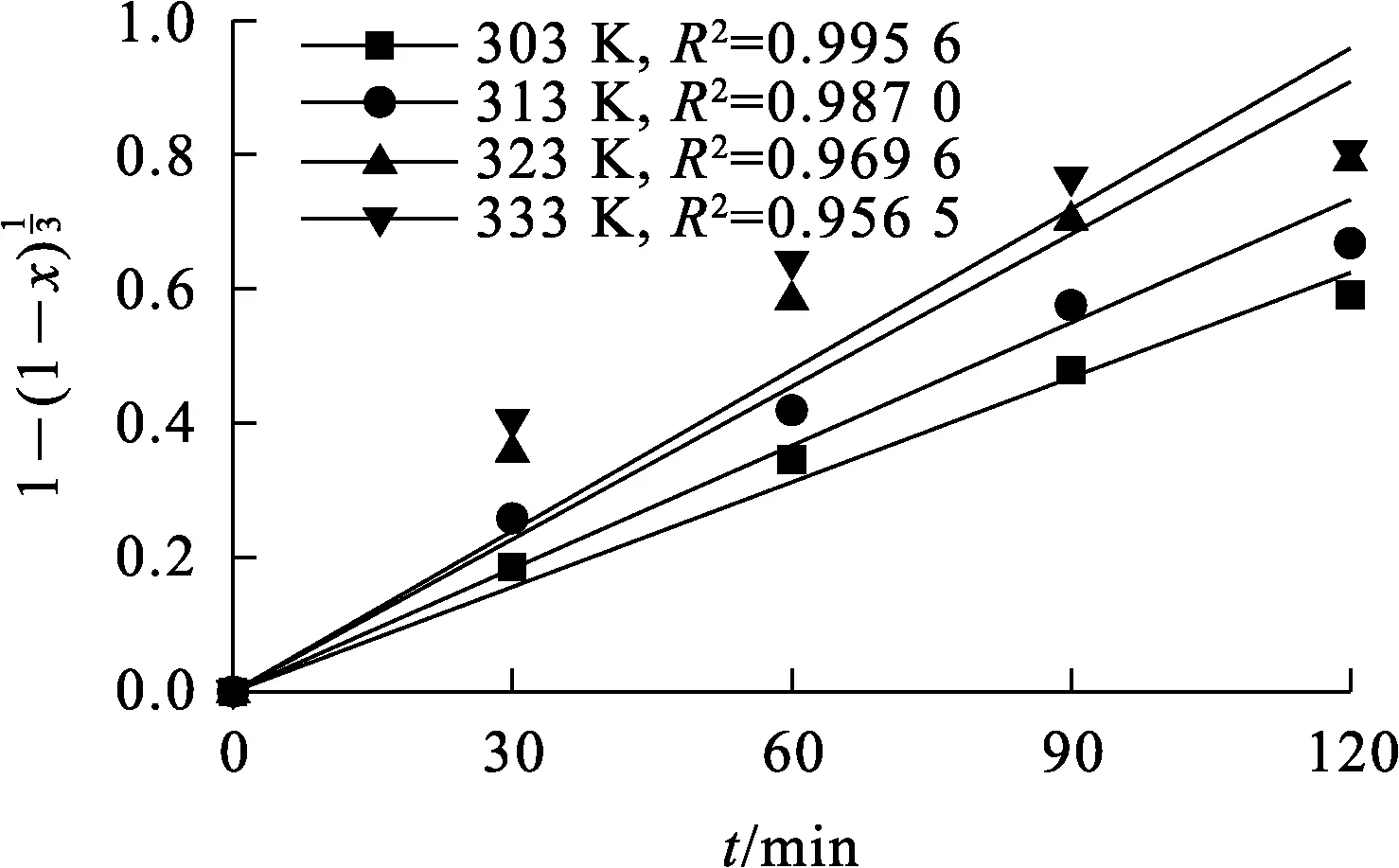
图8 不同温度下对浸出时间t的拟合曲线
由上述拟合结果可知:图9中数据拟合的相关系数均大于0.98,表明该浸出过程受扩散与化学反应混合控制。采用Arrhenius方程(式(8))对不同温度下速率常数k进行拟合,结果如图10所示,计算可得该浸出反应表观活化能为17.93 kJ/mol。
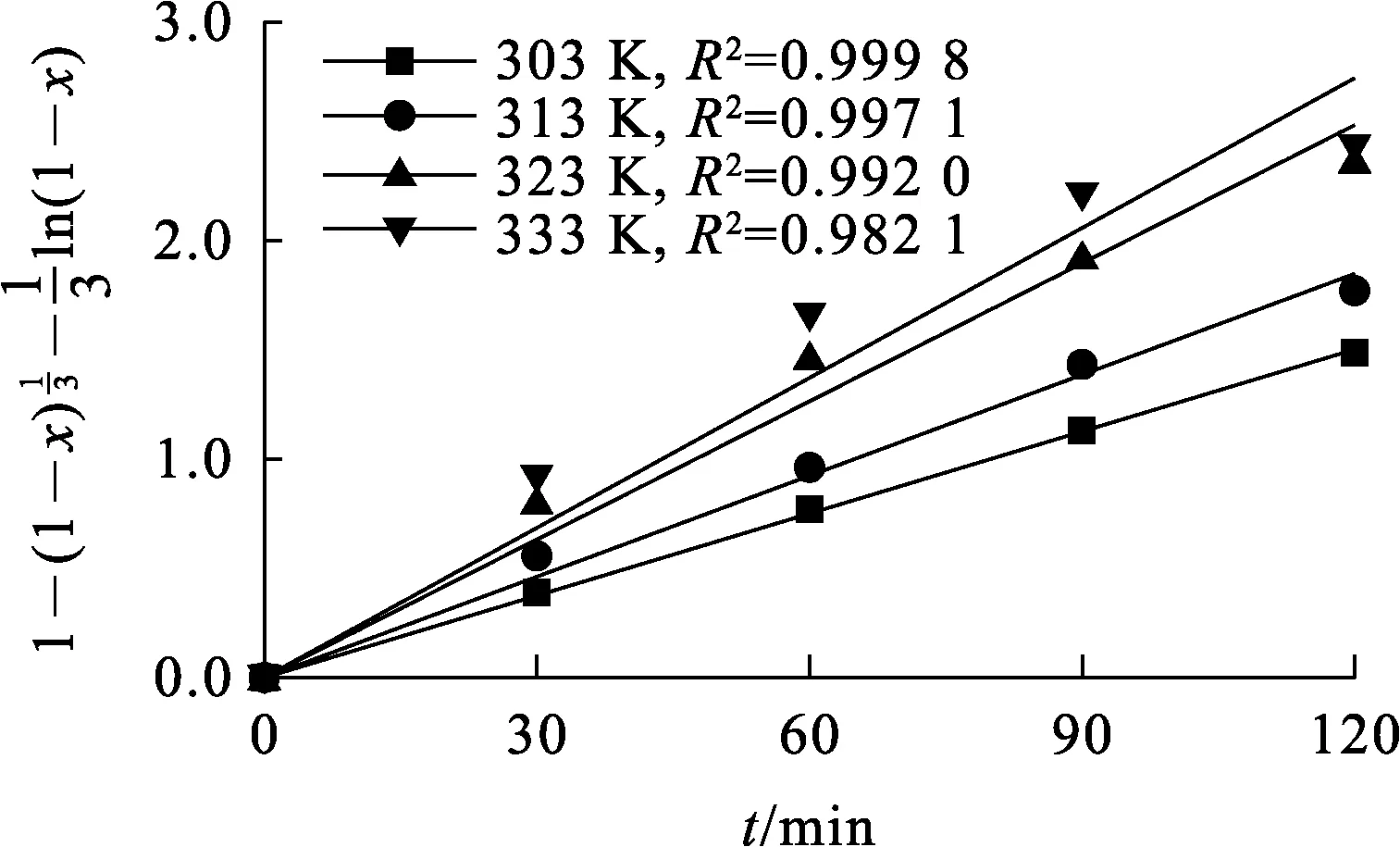
图9 不同温度下对浸出时间t的拟合曲线
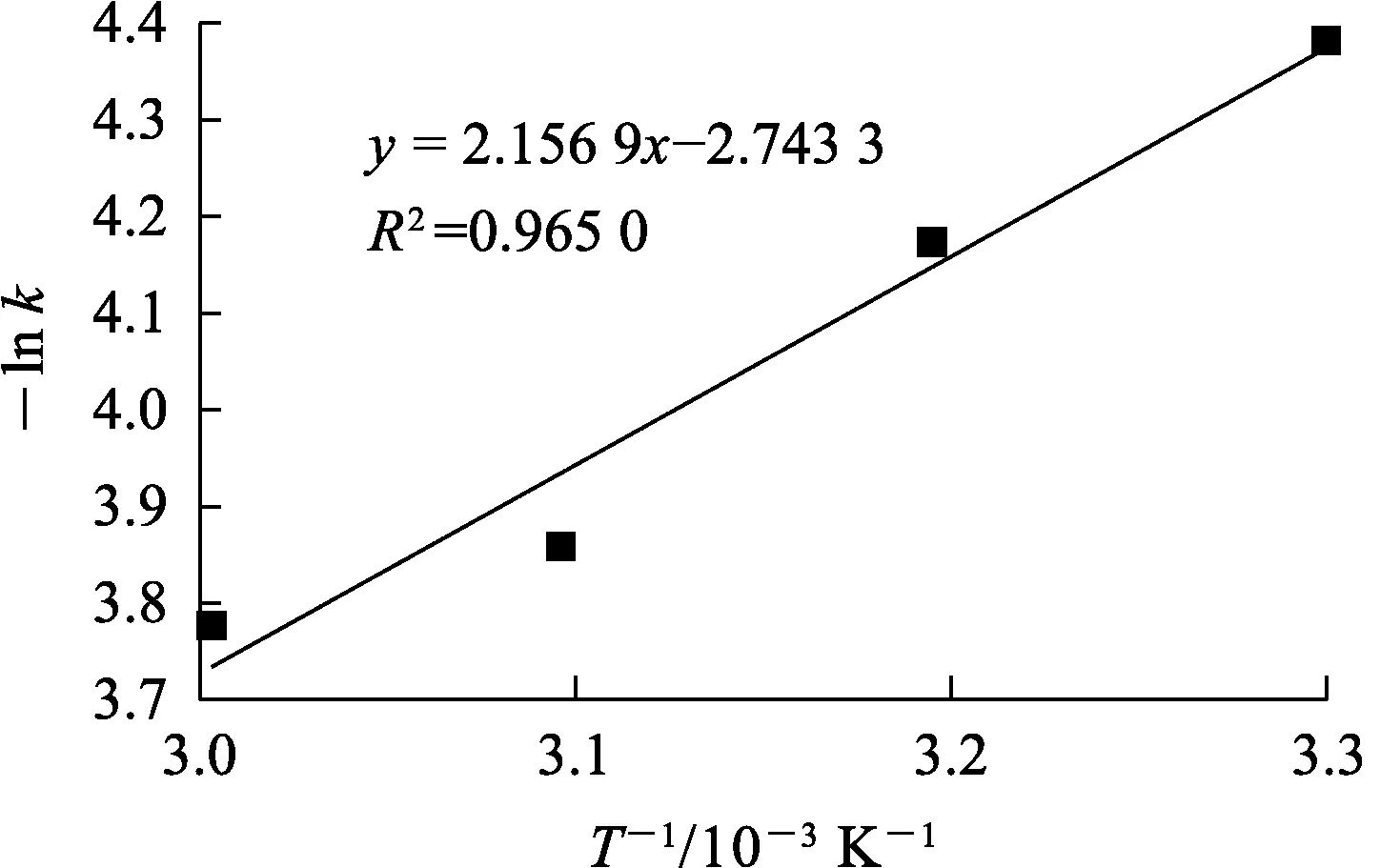
图10 -ln k与T-1的关系曲线
(8)
式中:k—化学反应速率常数,min-1;A—频率因子,min-1;R—理想气体常数,8.314 J/(mol·K);Ea—表观活化能,kJ/mol。
3 结论
采用乙二胺四乙酸二钠(EDTA-2Na)从铜阳极泥脱铜渣中浸出铅是可行的。在pH=5、n(EDTA)/n(Pb)=2/1、液固体积质量比4/1、浸出温度323 K、浸出时间120 min最优条件下,铅浸出率可达99%,且渣中贵金属基本不损失,可实现脱铜渣中铅元素的高效浸出。浸出过程符合未反应核收缩模型,受扩散与化学反应混合控制,表观活化能为17.93 kJ/mol。该法选择性较强,浸出效果较好,浸出效率高,后续浸出液可经沉铅后回收再利用,可为铜阳极泥半湿法工艺脱铅提供了一种新途径。
