超高效液相色谱-串联质谱法测定动物源性食品中的13 种利尿剂
2023-08-05任晓伟范力欣何亮娜马俊美
任晓伟,范力欣,何亮娜,孙 磊,马俊美
(河北省食品安全重点实验室,国家市场监管重点实验室(特殊食品监管技术),特殊食品安全与健康河北省工程研究中心,河北省食品检验研究院,河北 石家庄 050000)
利尿剂是作用于肾脏,增加电解质和水排出的能够产生利尿作用的一类药物[1],在临床上广泛应用于利尿消肿、降压和脑水肿等治疗[2-5]。利尿剂因为具有很强的排尿能力在需要快速减肥才能达到某一体质量类别的运动中经常被滥用。利尿剂还可以作为掩蔽剂增加尿量,从而稀释一些违禁兴奋剂的浓度,使这些违禁兴奋剂的检测变得更加困难。例如呋塞米和布美他尼等高效利尿剂可使尿液中兴奋剂的浓度降低4~5 倍[6]。此外,碳酸酐酶抑制剂组的利尿剂会导致尿液呈碱性,从而抑制碱性兴奋剂的排泄,导致兴奋剂的阴性分析[6-9]。1988年汉城奥运会期间,4 名运动员的利尿剂速尿检测呈阳性。1988年另一种引起广泛关注的利尿剂丙磺舒,它能有效减少合成类固醇和抗生素的排泄,使尿液中的类固醇浓度降低至原来的十分之一。因此在使用丙磺舒后对合成类固醇和抗生素的准确分析难度较大。自1988年,国际奥委会禁止在冬季和夏季奥运会上使用不同种类的利尿剂。另外,利尿剂还被应用到动物饲养当中,用于治疗奶牛乳房炎,或者是改善禽蛋蛋白比例等[10]。这会使利尿剂在动物体内存在残留。运动员误食这些食品后不仅会对身体健康产生负面影响,也会造成尿检阳性事件。所以开发出一种灵敏、简捷的检验食品中违禁利尿剂的分析技术手段刻不容缓。
由于动物源性食品中利尿剂的微量存在和显著的基质效应,前处理过程在仪器分析之前至关重要。为了获得更好的分析准确度,需要去除样品基质中的干扰。在以往的一些研究中,利尿剂的净化方法主要是液-液萃取(liquid-liquid extraction,LLE)和常规的固相萃取(solid phase extraction,SPE)[11-14]。这些方法往往需要较长的提取时间,大量的溶剂和繁杂的后续步骤。本实验中使用PRiME HLB通过式固相萃取柱净化。PRiME HLB通过式固相萃取柱是近年来发展起来的一种直通型SPE固相萃取柱[15-18]。它将提取、浓缩、净化融为一体,不仅能有效去除样品基质中的脂肪和磷脂类化合物等杂质,而且使用前无需活化和平衡[19]。直通型SPE固相萃取柱既精简了实验的前处理过程,又提高了分析准确度。
目前,利尿剂的检测主要针对人及动物的尿样、保健品和饲料等样品,方法有薄层色谱(thin-layer chromatography,TLC)法[20]、循环伏安法[21]、胶束液相色谱法[22]、液相色谱(liquid chromatography,LC)法[23-24]、液相色谱-质谱(liquid chromatography-mass spectrometry,LC-MS)法[25-28]、气相色谱-质谱(gas chromatography-mass spectrometry,GC-MS)法[29-30]等。其中LC-MS和GC-MS是两种比较常见的方法。但是在使用GC-MS法对利尿剂进行分析时,为提高利尿剂的挥发性,在GC-MS分析前需要对样品进行甲基化或硅烷化等衍生化处理[16]。而衍生化处理包含许多实验步骤,前处理过程比较复杂。超高效液相色谱-串联质谱(ultrahigh performance liquid chromatography-tandem mass spectrometry,UPLC-MS/MS)不仅不用衍生化的处理,而且灵敏度高、准确度好、应用广泛。因此,本实验开发出了一种直通型SPE联合内标法检测13 种利尿剂的新型UPLC-MS/MS方法。该方法简单高效、精密度好、重复性好和特异性强,适用于动物源性食品中13 种利尿剂的批量、准确检测。
1 材料与方法
1.1 材料与试剂
鸡蛋、牛奶、鸡肉和猪肉食品样品来源于本地农贸市场,均未检出实验中涉及的13 种利尿剂。
氨苯蝶啶、螺内酯、坎利酮、乙酰唑胺、4-氨基-6-氯苯-1,3-二磺酰胺、氯噻嗪、氢氯噻嗪、氯噻酮、呋塞米、苄氟噻嗪、托拉塞米、坎利酮-D6、氢氯噻嗪-13C-D2、呋塞米-D5、乙酰唑胺-D3、氯噻酮-D4、苄氟噻嗪-D5、氨苯蝶啶-D5、氯噻嗪-13C15N2、丙磺舒-D14、4-氨基-6-氯苯-1,3-二磺酰胺-N2、托拉塞米-D7标准物质(纯度大于95%)天津ALTA科技有限公司;丙磺舒标准物质(纯度>95%)CATO Research Chemicals公司;托伐普坦、托伐普坦-D7标准物质(纯度>95%)加拿大 TLC PharmaChem有限公司;乙腈、甲醇、正己烷(均为色谱纯)美国Millipore公司;甲酸(色谱纯)美国Sigma公司;乙酸铵(纯度98%)上海麦克林生化科技有限公司;超纯水 屈臣氏商标有限公司;Oasis PRiME HLB固相萃取柱(200 mg/6 mL)美国Waters公司。
1.2 仪器与设备
TSQ Quantiva UPLC-MS/MS仪 美国Thermo公司;Elmasonic P300H超声波清洗器 德国Elma公司;3-18KS离心机 美国Sigma公司;Multi Reax振荡器 德国Heidolph公司;N-EVAP 112氮吹仪 美国Organomation 公司;ME204E/02电子分析天平(感量0.00001 g)Mettler Toledo国际贸易(上海)有限公司。
1.3 方法
1.3.1 标准品溶液的配制
1.3.1.1 标准贮存液、内标贮存液
准确称取13 种利尿剂标准品和12 种利尿剂内标标准品,分别使用甲醇配制为0.1 mg/mL的利尿剂标准贮存液和内标贮存液(氨苯蝶啶和氨苯蝶啶-D5标准品需先用甲酸溶解,再用甲醇稀释并定容)。于-20 ℃避光贮存,有效期6 个月。
1.3.1.2 混合标准工作液
准确量取氯噻嗪、氢氯噻嗪、苄氟噻嗪、坎利酮和托拉塞米的外标贮存液(1.3.1.1节)各1 mL,氯噻酮、乙酰唑胺、呋塞米、螺内酯、4-氨基-6-氯苯-1,3-二磺酰胺、氨苯蝶啶、丙磺舒和托伐普坦的外标贮存液(1.3.1.1节)各2.5 mL,到同一100 mL容量瓶中,甲醇定容。混合外标工作液中氯噻嗪、氢氯噻嗪、苄氟噻嗪、坎利酮和托拉塞米的质量浓度为1 µg/mL;氯噻酮、乙酰唑胺、呋塞米、螺内酯、4-氨基-6-氯苯-1,3-二磺酰胺、氨苯蝶啶、丙磺舒和托伐普坦的质量浓度为 2.5 µg/mL。4 ℃以下避光贮存,有效期1 个月。
1.3.1.3 混合内标工作液
量取12 种利尿剂内标贮存液(1.3.1.1节)各1 mL,到同一100 mL容量瓶中,甲醇定容。混合内标工作液中12 种利尿剂内标质量浓度为1 µg/mL。4 ℃以下避光贮存,有效期1 个月。
1.3.2 样品前处理1.3.2.1 试样制备
取鸡蛋、鸡肉和猪肉试样约200 g(鸡蛋需去壳),用匀浆机充分匀浆均匀,放入洁净聚乙烯瓶中,于4 ℃冷藏密封保存。取牛奶试样搅拌均匀,装入洁净聚乙烯瓶中,于4 ℃冷藏密封保存。
1.3.2.2 提取
准确称取均质后试样2 g于(精确至0.01g)50 mL塑料离心管中,添加1 µg/mL的12 种利尿剂混合内标工作液(1.3.1.3节)40 µL,加入10 mL 90%乙腈溶液(对于猪、牛、羊、禽类食品)/乙腈(对于蛋、奶类食品),于旋涡振荡器上剧烈振荡2 min,超声15 min,4 ℃、8000 r/min离心5 min。加入3 mL正己烷溶液(乙腈饱和),低速涡旋10 s,4 ℃、8000 r/min离心3 min,取乙腈层待净化。
1.3.2.3 净化
取上述提取液5 mL过PRiME HLB固相萃取柱,以不大于1 mL/min的速率通过固相萃取柱,用带有刻度的玻璃试管准确接收流出的样液,并用1 mL的90%乙腈-甲醇溶液淋洗过柱,接收全部液体。洗脱液于40 ℃氮气吹至近干。加入1 mL乙腈-水(1∶1,V/V)溶液溶解残渣,过0.22 µm微孔滤膜,待测。
1.3.3 样品检测
1.3.3.1 色谱条件色谱柱:ACQUITY HSS T3色谱柱(100 mm× 2.1 mm,1.8 μm);柱温:30 ℃;进样量:5 μL;流速:0.3 mL/min;流动相:流动相和梯度洗脱条件见表1。
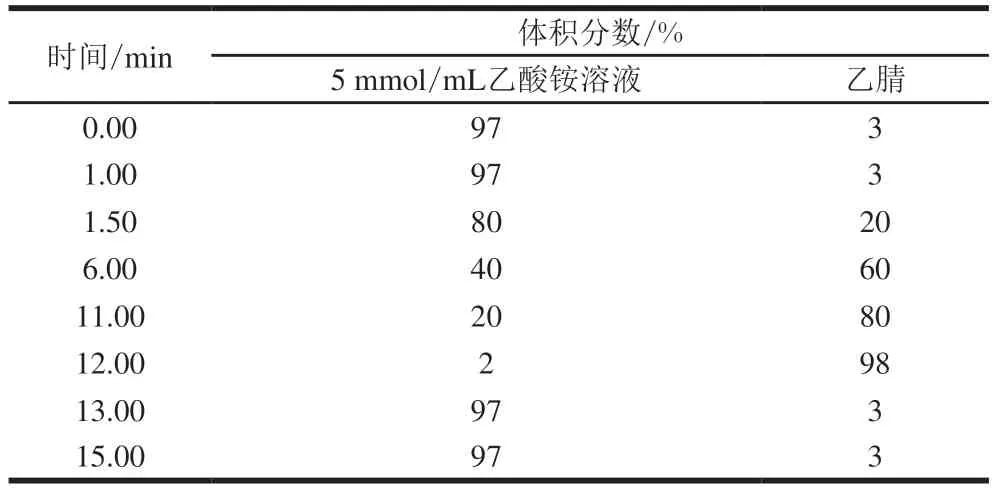
表1 梯度洗脱条件Table 1 Gradient elution conditions
1.3.3.2 质谱条件
电喷雾(electrospray ion source,ESI)离子源;离子化电压+3500 V/-2500 V;离子传输管温度342 ℃;加热温度358 ℃;鞘气(N2):35 arb;辅助气(N2):10 arb;13 种利尿剂及其内标物的其他质谱参数见表2、3。
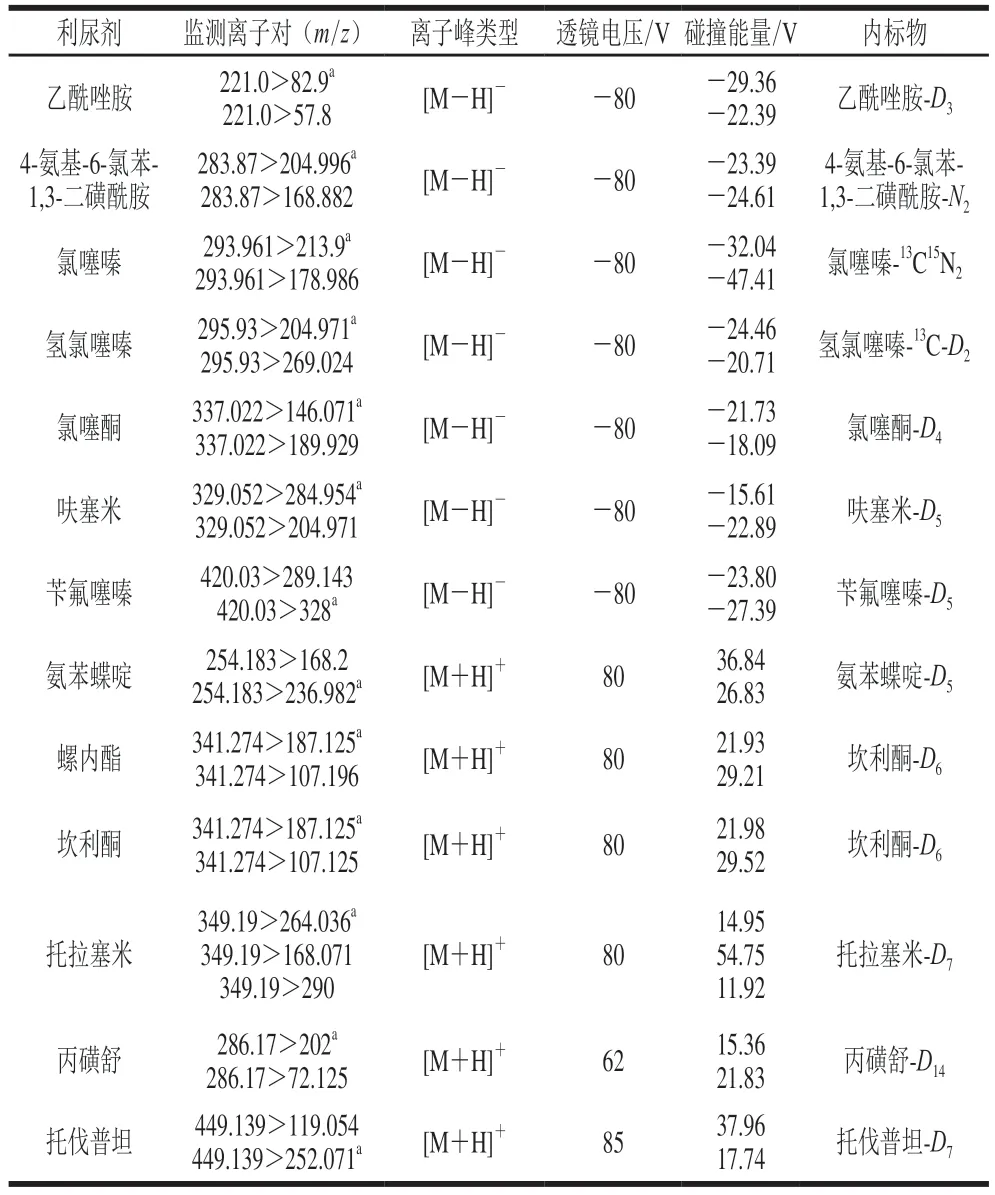
表2 13 种利尿剂的MRM参数和内标物Table 2 MRM parameters and internal standards of 13 diuretics
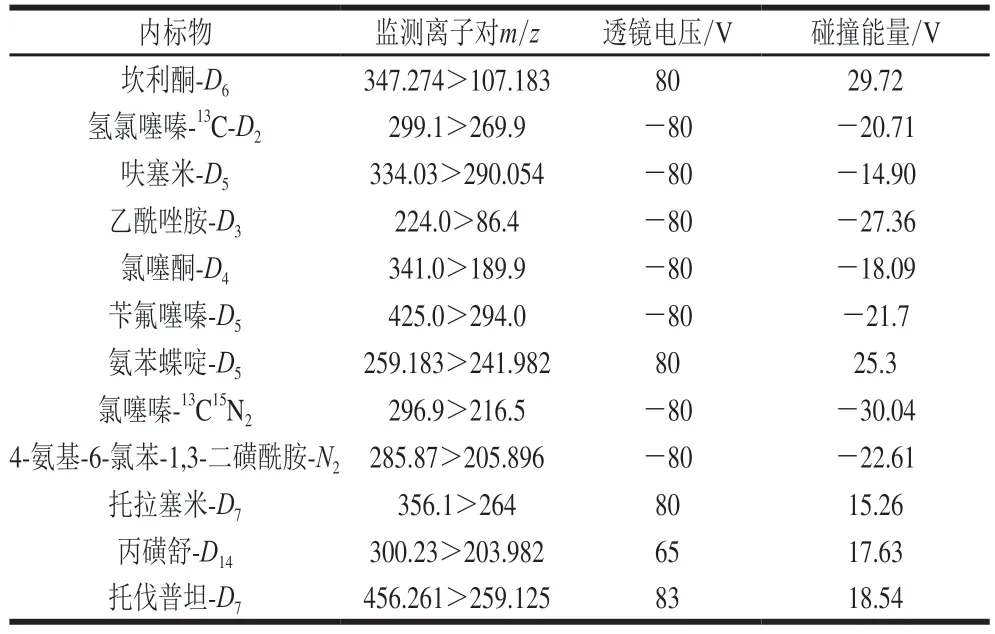
表3 12 种利尿剂内标物的MRM参数Table 3 MRM parameters of 12 internal standards of diuretics
2 结果与分析
2.1 前处理条件的优化
甲醇和乙腈是动物源性食品中常用的有机提取试剂,考察甲醇和乙腈对13 种利尿剂的提取效果。结果显示:用乙腈时响应值普遍更高,13 种利尿剂的回收率更好(图1)。据报道,乙腈具有蛋白质沉淀效果好、相容性好、脂溶性低等优点,被广泛应用于食品中有毒有害物质的提取[31-32]。但是,当使用甲醇或乙腈提取时,肌肉组织容易聚集导致提取溶剂不能充足的渗入样品,而使用有机试剂的水溶液就能有效避免肌肉组织的这种聚集。因此,本研究还对比乙腈、90%乙腈溶液和80%乙腈溶液对肌肉组织中利尿剂的提取效果。结果显示:对于猪、牛、羊、禽类使用90%乙腈溶液提取效果更好(图2)。对于猪、牛、羊、禽类食品,最佳提取溶剂为90%乙腈溶液;对于鸡蛋和牛奶类食品,最佳提取溶剂是乙腈。另外,动物源性食品中基质复杂。进样前进行净化处理是很有必要的。本研究采用PRiME HLB通过式固相萃取柱净化,省去了常规SPE的分析操作步骤(活化、淋洗和调整pH值)。该操作能有效分离出动物源性食品中富含的磷脂类化合物和脂肪等物质,提高分析灵敏度。由图3可见,经PRiME HLB通过式固相萃取柱净化后的鸡肉样品,以基质成分的强度估算,基质成分明显减少。
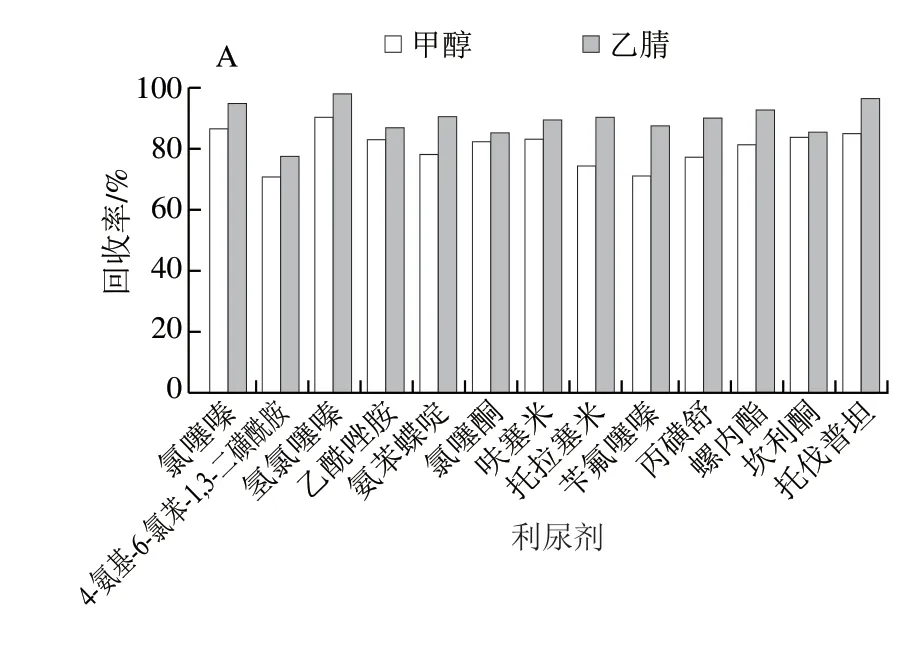
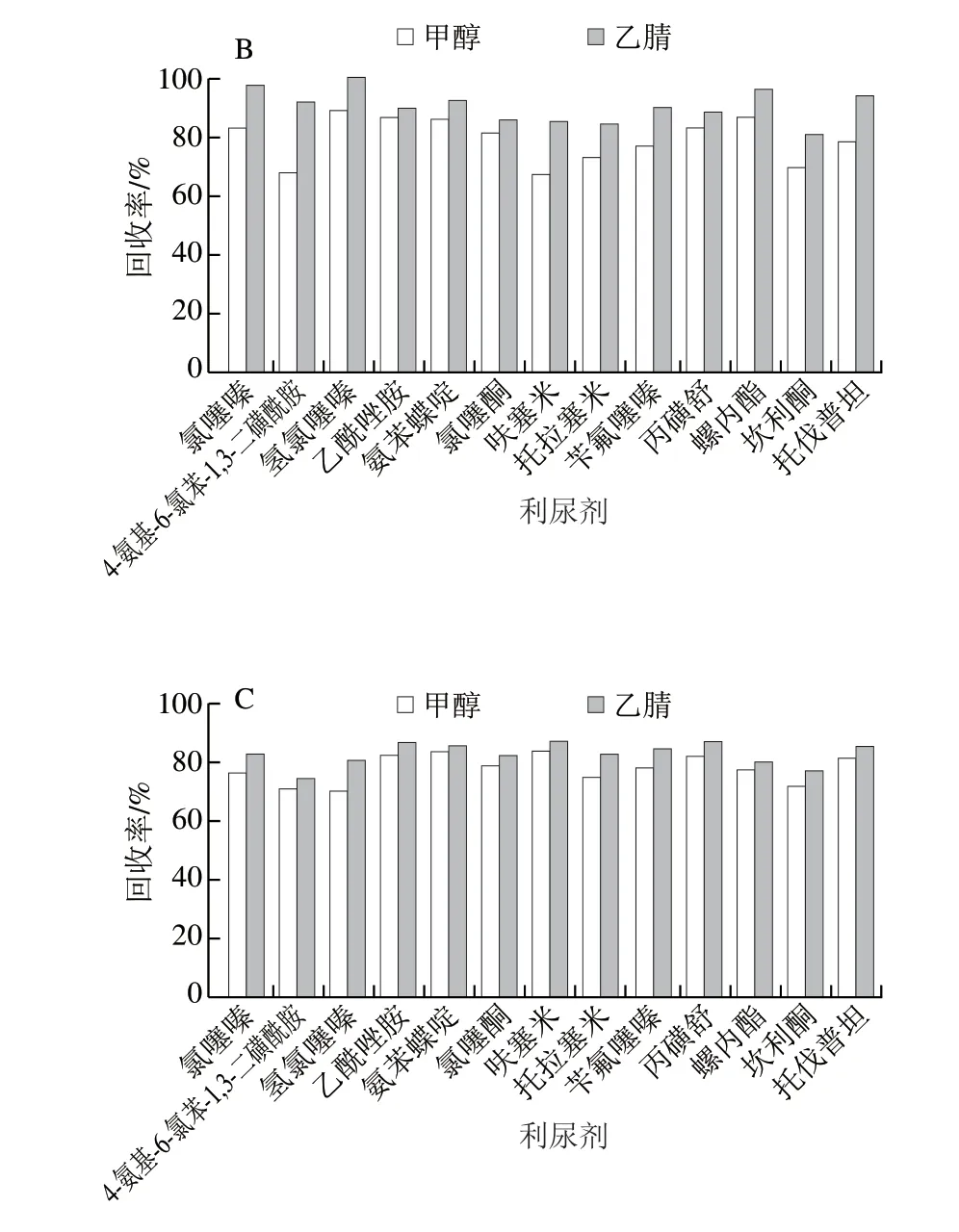
图1 甲醇和乙腈对13 种利尿剂回收率的影响Fig.1 Effects of methanol and acetonitrile on recoveries of 13 diuretics
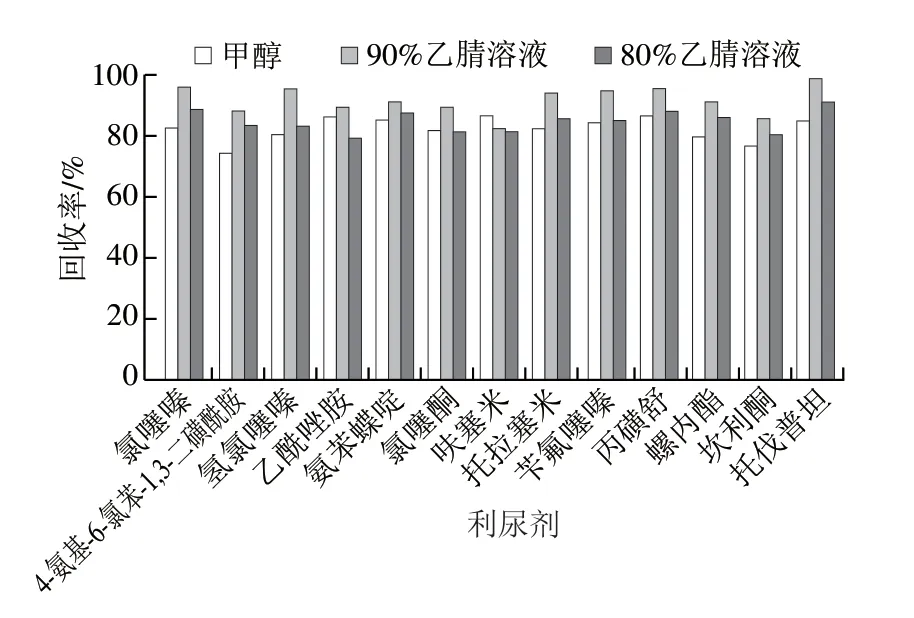
图2 乙腈、90%乙腈溶液和80%乙腈溶液在肌肉中对 13 种利尿剂回收率的影响Fig.2 Effects of acetonitrile,90% acetonitrile solution and 80% acetonitrile solution on recoveries of 13 diuretics from muscle
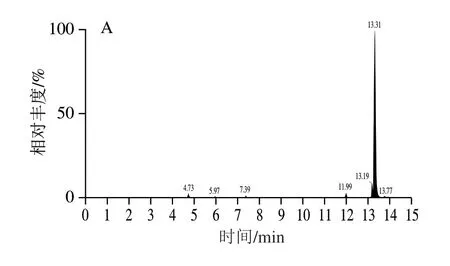
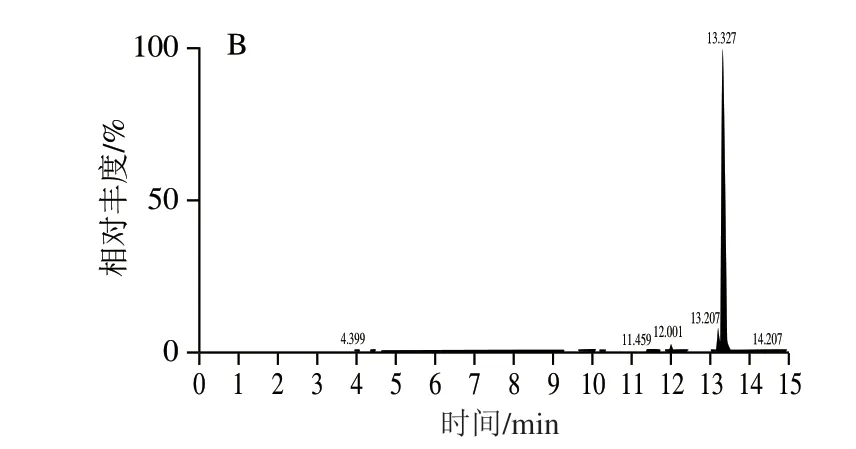
图3 未经PRiME HLB净化(A)和经PRiME HLB净化(B)的 空白鸡肉样品的总离子流图比较Fig.3 Total ion current chromatograms of blank chicken sample before (A) and after (B) purification on PRiME HLB column
2.2 基质效应评价
基质效应会抑制或增强被分析物的信号,导致定量结果的不准确和仪器寿命缩短。在本研究中,采用基质和溶剂所绘标准曲线的斜率比值评价基质效应对实验结果的影响程度。当斜率比值大于1.2或小于0.8时,基质效应就会影响分析结果[33]。为有效消除基质效应对分析结果造成的影响,本实验选用鸡肉作为基质对比无内标和有内标时13 种利尿剂的基质效应。如表4所示,在不使用内标时仅有7 种利尿剂无显著的基质效应。而使用内标后13 种利尿剂的斜率比值均在0.8~1.2之间,基质效应对分析结果的影响可以忽略。这一结果证实了内标法可以消除基质效应造成的定量结果偏差,提高检测方法的稳定性和精准性。
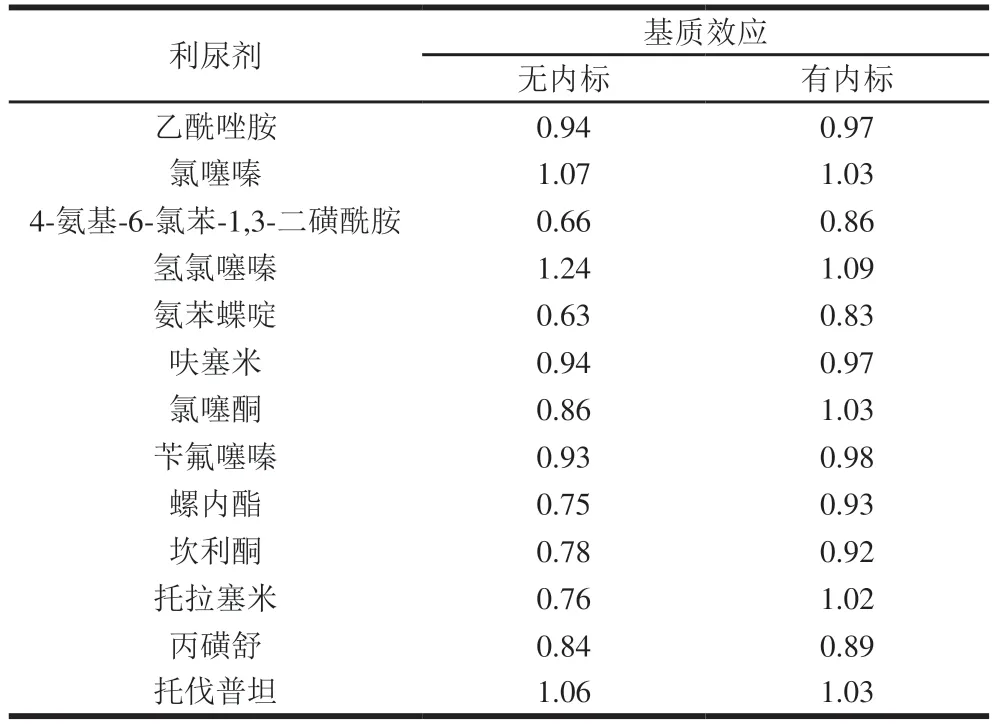
表4 无内标和有内标时13 种利尿剂的基质效应Table 4 Matrix effects of 13 diuretics in the absence and presence of internal standard
2.3 色谱条件的优化
本研究测验多个液相色谱参数对13 种利尿剂及其内标物分离效果的影响。对比Waters XBridge BEH C18柱(2.1 mm×100 mm,2.5 μm)和ACQUITY HSS T3柱(100 mm×2.1 mm,1.8 μm)的分离性能,结果显示,ACQUITY HSS T3色谱柱在峰形、分辨率、保留时间等方面表现更好;流动相的组成对分析物的电离和质谱的检测灵敏度都有一定的影响,乙腈是一种常用的流动相,具有很强的洗脱能力,乙酸铵可以有效的改善色谱峰的峰形,因此,本研究的流动相采用乙腈和乙酸铵溶液,同时使用梯度洗脱对目标化合物进行有效分离。图4显示了13 种利尿剂优化后的SRM谱图。
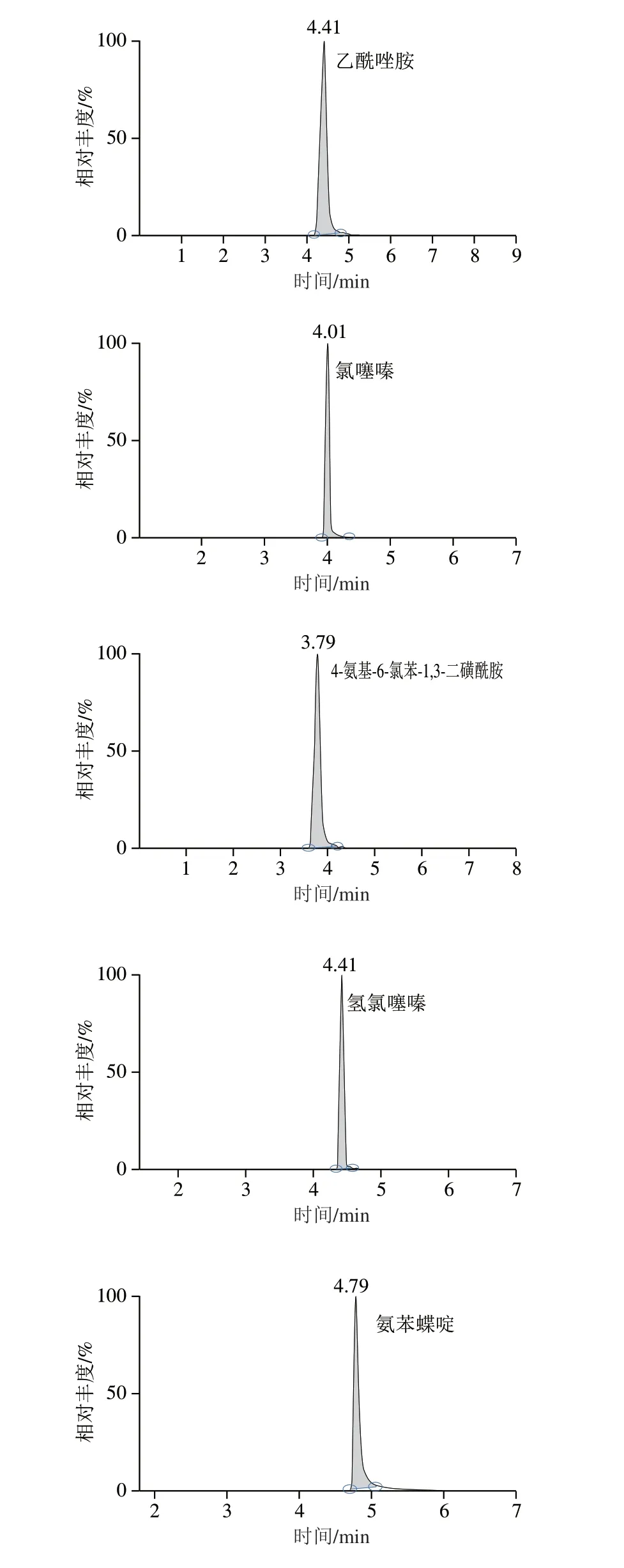
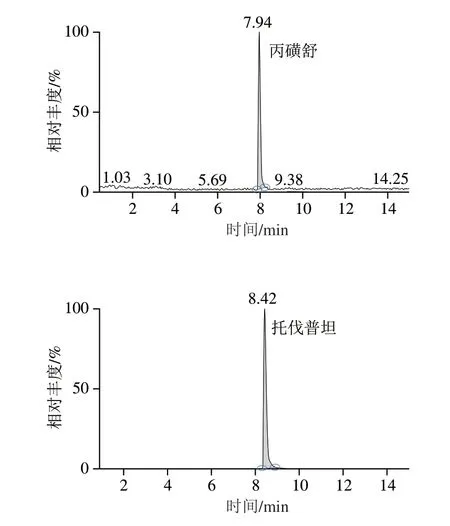
图4 13 种利尿剂的提取离子色谱图Fig.4 Extracted ion chromatograms of 13 diuretics
2.4 质谱条件的优化
将13 种利尿剂及其内标物的标准溶液注入质谱,从结构上分析,有的化合物容易带正电荷,即正离子电离信号响应强;有的化合物容易带负电荷,即负离子电离信号响应强。因此,母离子扫描使用ESI+/ESI-模式。其中在正模式下,质子化的分子[M+H]+作为基峰;在负模式下,去质子化的分子[M-H]-作为基峰。在这种条件下,对相应的母离子峰实施后续的子离子扫描,得到它们各自的子离子,并挑选2 对响应值高的子离子进行二级质谱参数优化。优化后的相关参数见表2、3。
2.5 线性关系考察和方法定量限
使用利尿剂混合标准工作液(1.3.1.2节)以及内标工作液(1.3.1.3节)通过50%乙腈溶液配制成混合标准系列溶液。其中氯噻嗪、氢氯噻嗪、苄氟噻嗪、坎利酮和托拉塞米的质量浓度为2、5、10、20 ng/mL和 50 ng/mL;氯噻酮、乙酰唑胺、呋塞米、螺内酯、4-氨基-6-氯苯-1,3-二磺酰胺、氨苯蝶啶、丙磺舒和托伐普坦质量浓度为5、12.5、25、50 ng/mL和125 ng/mL;内标溶液的质量浓度为20 ng/mL。现用现配,后对配制的标准系列溶液进行数据分析。
使用内标法对供试品溶液中的利尿剂进行数据分析,其中内标法采用以各个利尿剂质量浓度为X轴,以各个利尿剂对其内标物的峰面积的比值为Y轴。测定数据 见表5。
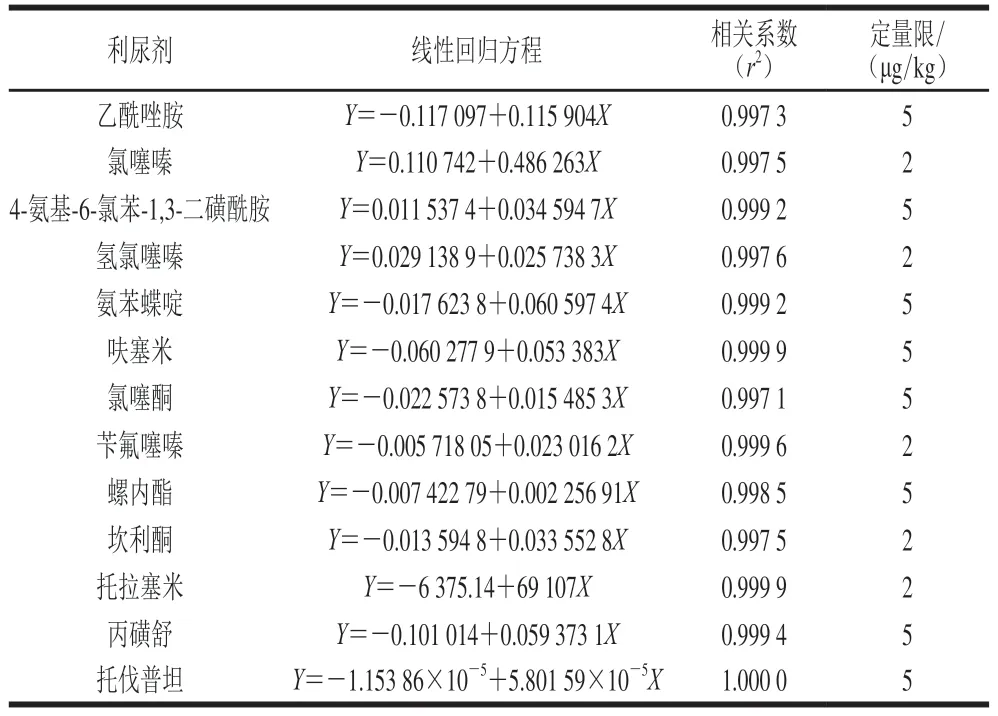
表5 13 种利尿剂的线性关系和定量限Table 5 Calibration equations and LOQs of 13 diuretics
2.6 回收率和精密度实验结果
实验选取猪肉、鸡肉、鸡蛋和牛奶4 种空白基质进行精密度和准确度的实验,在每种空白基质中分别加入相应量的13 种利尿剂混合标准工作液以及混合内标工作液制成一定浓度的质控样本:高、中和低浓度水平,每个水平独立检测6 次。如表6所示,在猪肉中,加标回收率为68.8%~115.9%以内,相对标准偏差(relative standard deviation,RSD)为0.47%~9.5%。在鸡肉中,加标回收率在73.0%~116.6%以内,RSD为0.51%~9.3%。在鸡蛋中加标回收率为68.3%~117.9%,RSD 为0.59%~8.7%。在牛奶中加标回收率为69.9%~118.0%,RSD为0.72%~6.6%。
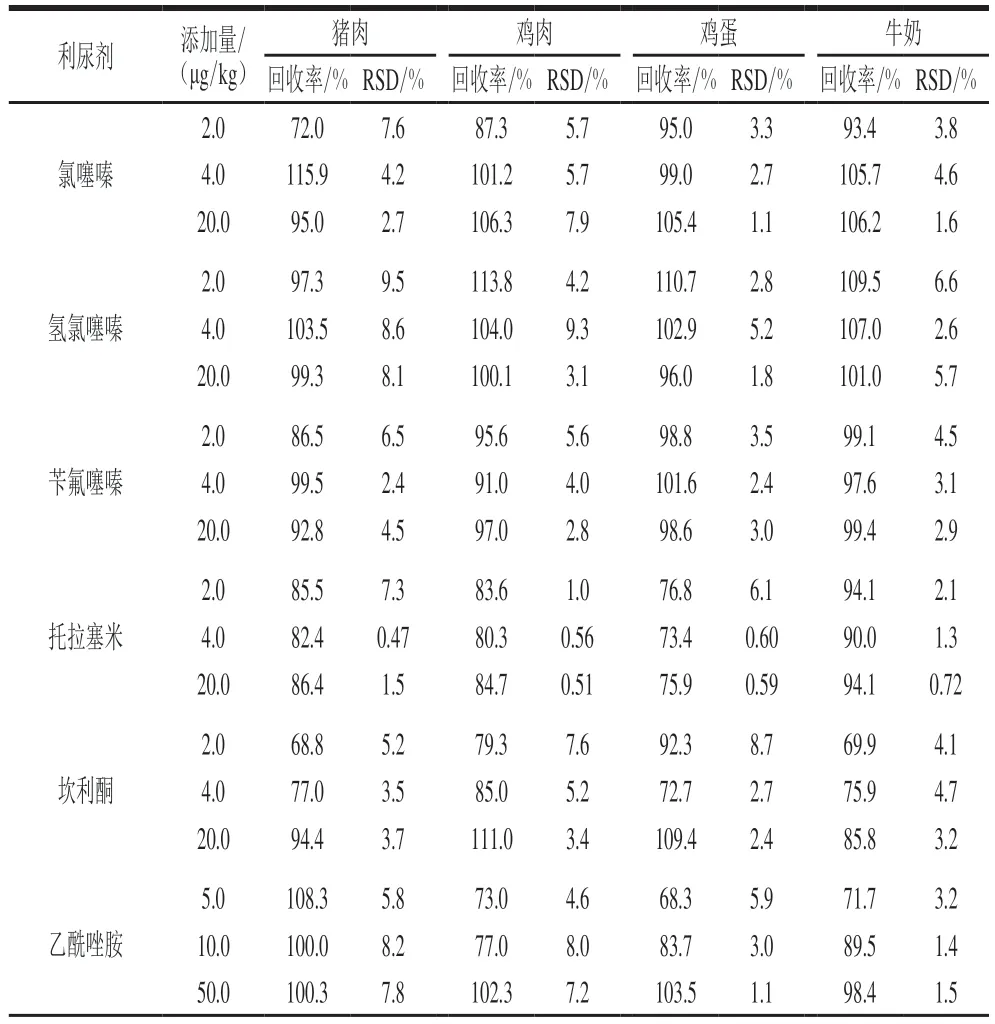
表6 13 种利尿剂的回收率和RSD(n=6)Table 6 Recoveries and RSDs of 13 diuretics from spiked real samples (n =6)
3 结论
本实验成功地开发了一种通过式SPE-UPLC-MS/MS同时检测肉、蛋、奶食品中13 种利尿剂的新型方法。采用乙腈或90%乙腈溶液为提取试剂,有效提取样品中13 种利尿剂,采用PRiME HLB柱净化后,有效去除了样品中的杂质,同时使用同位素内标法在一定程度上排除了基质效应对结果的干扰。该方法简单、高效,实现了对动物源性食品中13 种利尿剂的精确定量分析。本方法不仅可以作为一种执法监督和检查手段,为动物源性食品中的利尿剂的检测提供依据,也可以作为其他方法的辅助手段,为其他研究人员提供技术支持。
