腹腔镜与开腹胃癌根治术患者术后肠黏膜屏障、免疫与氧化应激反应的变化比较
2023-06-25胡金伟何新阳
胡金伟 何新阳


【摘要】 目的:探究腹腔鏡与开腹胃癌根治术患者术后肠黏膜屏障、免疫与氧化应激反应的变化。方法:选取2020年6月-2022年10月安徽医科大学附属省立医院收治的80例胃癌患者,根据随机数字表法将其分为A组和B组,每组40例。A组进行开腹胃癌根治术,B组则进行腹腔镜胃癌根治术。比较两组术前及术后1、3、7 d的肠黏膜屏障指标[二胺氧化酶(DAO)、D-乳酸(D-LAC)及内毒素(ET)]、免疫指标[T淋巴细胞亚群(CD3+、CD4+、CD8+)及免疫球蛋白(IgA、IgM、IgG)]与氧化应激反应指标[总抗氧化能力(TAC)、超氧化物歧化酶(SOD)、丙二醛(MDA)]。结果:术前,两组肠黏膜屏障指标、免疫指标与氧化应激反应指标比较,差异均无统计学意义(P>0.05);术后1、3、7 d,B组DAO、D-LAC、ET、CD8+、MDA均低于A组,B组CD3+、CD4+、IgA、IgM、IgG、TAC、SOD均高于A组,差异均有统计学意义(P<0.05)。结论:腹腔镜胃癌根治术患者术后肠黏膜屏障、免疫与氧化应激反应指标均优于开腹胃癌根治术,因此在胃癌患者中的应用价值相对更高。
【关键词】 腹腔镜胃癌根治术 开腹胃癌根治术 肠黏膜屏障 氧化应激反应
Comparison on the Change of Postoperative Intestinal Mucosal Barrier, Immunity and Oxidative Stress Response in Patients with Laparoscopic and Open Radical Gastrectomy/HU Jinwei, HE Xinyang. //Medical Innovation of China, 2023, 20(12): 0-026
[Abstract] Objective: To investigate the change of postoperative intestinal mucosal barrier,immunity and oxidative stress response of patients with laparoscopic and open radical gastrectomy. Method: A total of 80 patients with gastric cancer in Anhui Medical University Affiliated Provincial Hospital from June 2020 to October 2022 were selected, they were divided into group A and group B according to random number table method, with 40 cases in each group. The group A was treated with open radical gastrectomy, the group B was treated with laparoscopic radical gastrectomy. Then the intestinal mucosal barrier indexes [diamine oxidase (DAO), D-lactic acid (D-LAC), endotoxin (ET)], immunity indexes [T lymphocyte subsets (CD3+, CD4+, CD8+) and immunoglobulins (IgA, IgM, IgG)] and oxidative stress response indexes[total antioxidant capacity (TAC), superoxide dismutase (SOD), malondialdehyde (MDA)] before operation and at 1, 3, 7 d after the operation were compared between the two groups. Result: Before operation, there were no significant differences in intestinal mucosal barrier indexes, immune indexes and oxidative stress response indexes between the two groups (P>0.05); 1, 3 and 7 d after operation, DAO, D-LAC, ET, CD8+ and MDA in group B were lower than those in group A, while CD3+, CD4+, IgA, IgM, IgG, TAC and SOD in group B were higher than those in group A, the differences were statistically significant (P<0.05). Conclusion: The change amplitude of laparoscopic radical gastrectomy are relatively better than those of patients with open radical gastrectomy, so its application value in patients with gastric cancer is relatively higher.
[Key words] Laparoscopic radical gastrectomy Open radical gastrectomy Intestinal mucosal barrier Oxidative stress response
First-author's address: Anhui Medical University Affiliated Provincial Hospital, Hefei 230001, China
doi:10.3969/j.issn.1674-4985.2023.12.006
胃癌根治术是临床中治疗胃癌的有效方式,因此临床中关于胃癌根治术各方面的研究是重点。而腹腔镜胃癌根治术作为微创治疗方式,其临床应用率持续提升,相关研究不断增多,涉及面也不断扩宽[1-2]。肠黏膜屏障作为消化系统手术患者中研究较多的方面,其在胃癌根治术患者中的研究可见,但是在不同术式中的变化波动研究仍不足。另外,机体免疫与氧化应激作为受手术及创伤程度影响较大的方面,其对于手术患者的手术创伤程度与术后恢复效果、速度均有一定的价值[3-5]。本研究现比较腹腔镜与开腹胃癌根治术患者术后肠黏膜屏障、免疫与氧化应激反应的变化情况,现报道如下。
1 资料与方法
1.1 一般资料 选取2020年6月-2022年10月安徽医科大学附属省立医院收治的80例胃癌患者。纳入标准:(1)年龄20~75岁;(2)符合胃癌根治术手术指征。排除标准:(1)合并高血压、糖尿病或其他慢性基础疾病;(2)3个月内手术史或创伤史;(3)放化疗史;(4)合并代谢性或免疫性疾病。根据随机数字表法将患者分为A组和B组,每组40例。本研究经医院医学伦理学委员会批准,患者均知情同意本研究。
1.2 方法 A组进行开腹胃癌根治术,对患者进行常规的术前检查,全麻后于上腹部正中做手术切口,入腹后常规探查,将网膜囊切除,清除淋巴结,切除病灶,切除范围在病灶边缘3~5 cm处,而位于胃窦处者则切除远端2/3胃组织,后期常规处理。B组则进行腹腔镜胃癌根治术,建立二氧化碳气腹,维持压力12~15 mmHg,对患者进行常规的术前检查,全麻后,脐孔处放置镜头,左腋前线肋缘下、右腋前线肋缘下、脐左5 cm偏上及右锁骨中线平脐上做手术戳孔,入腹后常規探查,将病灶切除,进行淋巴结清扫及消化道重建等。两组的其他治疗均相同。
1.3 观察指标及判定标准 比较两组术前及术后1、3、7 d的肠黏膜屏障指标[二胺氧化酶(DAO)、D-乳酸(D-LAC)及内毒素(ET)]、免疫指标
[T淋巴细胞亚群(CD3+、CD4+、CD8+)及免疫球蛋白(IgA、IgM、IgG)]与氧化应激反应指标[总抗氧化能力(TAC)、超氧化物歧化酶(SOD)及丙二醛(MDA)]。(1)血清指标:于术前及术后1、3、7 d分别采集两组空腹静脉血5.0 mL,将其采用医用离心机按照3 000 r/min的速度离心5 min后,取血清进行肠黏膜屏障指标(DAO、D-LAC及ET)、免疫球蛋白(IgA、IgM及IgG)与氧化应激反应指标(TAC、SOD及MDA)的检测,采用全自动生化仪及酶联免疫法试剂盒进行检测。(2)T淋巴细胞亚群:于术前及术后1、3、7 d分别采集两组的空腹静脉血4.0 mL,将其采用流式细胞仪进行CD3+、CD4+及CD8+等指标的检测。上述方面由两名检验科工作人员操作检测。
1.4 统计学处理 数据检验软件为SPSS 23.0,计量资料用(x±s)表示,比较采用t检验;计数资料以率(%)表示,比较采用字2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组一般资料比较 A组男23例,女17例;年龄39~74岁,平均(53.91±7.93)岁;疾病分期:Ⅰ期5例,Ⅱ期25例,Ⅲ期10例;ASA分级:Ⅰ级12例,Ⅱ级28例。B组男22例,女18例;年龄40~74岁,平均(53.93±7.79)岁;疾病分期:Ⅰ期3例,Ⅱ期26例,Ⅲ期11例;ASA分级:Ⅰ级11例,Ⅱ级29例。两组一般资料比较,差异均无统计学意义(P>0.05),具有可比性。
2.2 两组术前及术后1、3、7 d的肠黏膜屏障指标比较 术前,两组DAO、D-LAC、ET比较,差异均无统计学意义(P>0.05);术后1、3、7 d,B组DAO、D-LAC、ET均低于A组,差异均有统计学意义(P<0.05)。见表1。
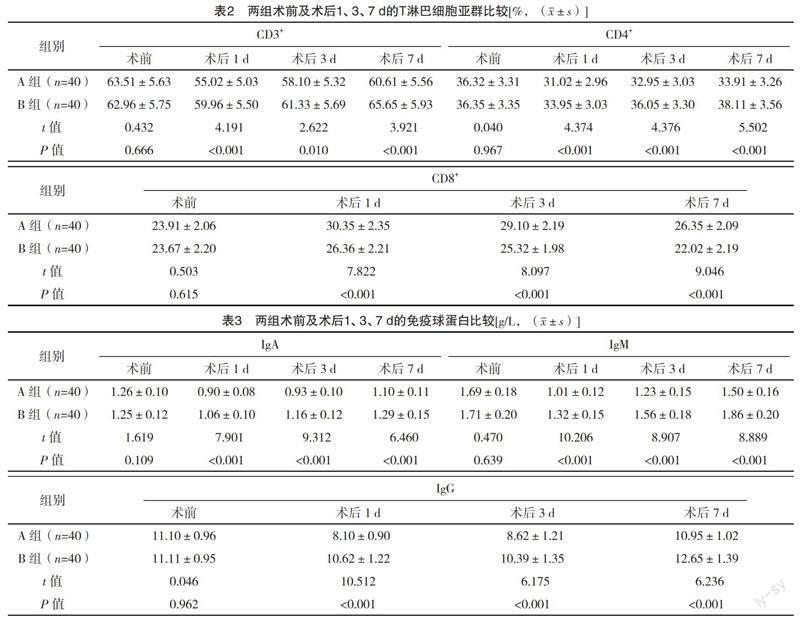
2.3 两组术前及术后1、3、7 d的T淋巴细胞亚群比较 术前,两组CD3+、CD4+、CD8+水平比较,差异均无统计学意义(P>0.05);术后1、3、7 d,B组CD8+均低于A组,CD3+、CD4+均高于A组,差异均有统计学意义(P<0.05)。见表2。
2.4 两组术前及术后1、3、7 d的免疫球蛋白比
较 术前,两组IgA、IgM、IgG水平比较,差异均无统计学意义(P>0.05);术后1、3、7 d,B组IgA、IgM、IgG水平均高于A组,差异均有统计学意义(P<0.05)。见表3。
2.5 两组术前及术后1、3、7 d的氧化应激反应指标比较 术前,两组TAC、SOD、MDA比较,差异均无统计学意义(P>0.05);术后1、3、7 d,B组MDA均低于A组,TAC、SOD均高于A组,差异均有统计学意义(P<0.05)。见表4。
3 讨论
胃癌根治术的临床研究多见,而随着微创技术的应用,腹腔镜胃癌根治术的临床应用率持续提升,与之相关的各方面研究不断扩宽。而腹腔镜手术除具有较小的手术创伤外,其对机体其他多方面也可造成较大影响[6-7]。而本类手术作为消化系统手术治疗方式,其对消化系统的影响相对更为突出,因此关于消化系统方面的变化研究意义与需求均较高。肠黏膜屏障作为有效反映肠道屏障防御体系的指标,其在手术患者,尤其是消化系统手术患者中的评估意义与需求较高[8-10],而DAO、D-LAC及ET作为临床常见的相关指标,其在本类患者中的监测意义较高,当上述指标异常升高时,说明肠黏膜屏障处于受损的状态,对其监测有助于了解肠道系统受到影响的程度及恢复效果。T淋巴细胞亚群及免疫球蛋白作为有效反映机体免疫状态的指标,其在手术患者中的变化波动也有较高的监测意义,对于了解患者的免疫应激及术后恢复均有积极的作用[11-12]。另外,氧化应激指标中的TAC、SOD及MDA等在反映手术损伤程度及修复效果等多方面均有积极的作用,当TAC及SOD降低,MDA升高时,说明机体抗氧化损伤能力受损,不利于患者的术后机体恢复,因此对于不同手术胃癌患者的监测价值较高[13-15]。
本研究结果显示,术后1、3、7 d,腹腔镜胃癌根治术患者的肠黏膜屏障指标(DAO、D-LAC及ET)、免疫指标[T淋巴细胞亚群(CD3+、CD4+、CD8+)及免疫球蛋白(IgA、IgM、IgG)]与氧化应激反应指标(TAC、SOD及MDA)均优于开腹手术,说明腹腔镜手术对患者上述方面的影响更小,同时术后恢复均相对更快,因此进一步肯定了腹腔镜胃癌根治术在本类患者中的可取性。分析原因,腹腔镜手术对机体损伤较小,对机体造成的不良应激相对更小[16-17],胃肠系统方面受到的不良影响更小,表现为肠黏膜屏障指标的波动相对更小,而机体免疫应激与损伤修复方面的表现也更为轻微[18-20],故较为全面地肯定了腹腔镜胃癌根治术的应用价值。
综上所述,腹腔镜胃癌根治术患者术后肠黏膜屏障、免疫与氧化应激反应指标均优于开腹胃癌根治术,因此在胃癌患者中的应用价值相对更高。
参考文献
[1]孙宏建.腹腔镜辅助D2根治性全胃切除术联合细胞免疫对胃癌患者肿瘤标志物水平的影响[J].吉林医学,2022,43(3):674-676.
[2]顾飞腾,黄秀凤.腹腔镜下胃癌根治术治疗进展期胃癌患者的近期疗效及对免疫功能与远期预后的影响[J].医疗装备,2022,35(22):82-85.
[3]沙鑫.腹腔镜辅助D2根治术治疗胃癌患者疗效及胃泌素族水平的影响[J].黑龙江医药,2022,35(5):1187-1189.
[4]冯伟静,曾伟,周雪涛,等.腹腔镜下远端早期胃癌根治术治疗效果及其血清肿瘤标志物的变化[J].临床和实验医学杂志,2022,21(5):501-505.
[5]王俊增,宋尉官.腹腔镜辅助胃癌根治术治疗进展期胃癌患者的临床疗效及对肠道功能的影响[J].中国现代药物应用,2022,16(17):32-35.
[6] JIAO J,LIU S,CHEN C,et al.Comparative study of laparoscopic radical gastrectomy and open radical gastrectomy[J].J Minim Access Surg,2020,16(1):41-46.
[7]劉紫朦,赵传稳,余昌达,等.腹腔镜辅助胃癌根治术对胃癌患者机体应激反应及免疫功能的影响[J].中国医学创新,2022,19(23):65-68.
[8]罗东明,钟倩,陈德伦,等.早期肠内营养支持对胃癌术后患者肠黏膜屏障功能保护的研究进展[J/OL].中华普外科手术学杂志:电子版,2022,16(6):700-702.http://qikan.cqvip.com/Qikan/Article/Detail?id=7108498579.
[9]赵煜辉,甘建雄,李可嘉.通腑活血汤联合谷氨酰胺对胃癌根治术后患者氧化应激和肠黏膜屏障功能的影响[J].中国肿瘤临床与康复,2019,26(6):727-730.
[10] YEN H H,YEH C C,LAI I R.Laparoscopic versus open distal gastrectomy for elderly patients with advanced gastric cancer: a retrospective comparative study[J].World J Surg Oncol,2022,20(1):355.
[11] METERE A,GRAVES C E,PIETRAFORTE D,et al.The effect of sleeve gastrectomy on oxidative stress in obesity[J].Biomedicines,2020,8(6):168.
[12]宋学民,徐君毅,以敏,等.达芬奇手术机器人系统对胃癌根治性切除术患者胃肠功能恢复及免疫功能的影响[J].中国医学装备,2022,19(7):89-93.
[13]何小霞,李宝钏.腹腔镜与开腹根治术对进展期胃癌患者机体炎症反应、免疫功能及疼痛因子的影响[J].中国现代医学杂志,2021,31(6):23-26.
[14]沈乃营,郭栋,何盟国,等.腹腔镜胃癌根治术对术后恢复及血浆氧化应激水平的影响[J].中国现代普通外科进展,2019,22(3):228-230,234.
[15]谭玉成,徐建庆.腹腔镜根治术对胃癌患者肿瘤标志物及氧化应激水平的影响[J].陕西医学杂志,2021,50(8):969-972.
[16] MUADDI H,HAFID M E,CHOI W J,et al.Clinical outcomes of robotic surgery compared to conventional surgical approaches (laparoscopic or open): a systematic overview of reviews[J].Ann Surg,2021,273(3):467-473.
[17]高野,李凤岩,王恩慈.腹腔镜与开腹根治手术下胃癌患者的氧化应激、血清炎症因子及感染状况分析[J].中国现代医生,2020,58(22):55-58.
[18]李正凯,阮雁捷,郭冠军,等.盐酸羟考酮在大鼠胃癌根治术中的超前镇痛效果评价及对应激反应的影响[J].实用癌症杂志,2022,37(12):1920-1925.
[19]孟庆.腹腔镜下胃癌根治术与传统开腹手术治疗进展期胃癌的疗效比较[J].中国现代药物应用,2022,16(8):1-3.
[20]梁含理.腹腔镜辅助小切口胃癌根治术治疗进展期胃癌的疗效及对患者术后恢复的影响[J].当代医学,2022,28(18):128-130.
(收稿日期:2023-03-06) (本文编辑:张明澜)
