基于高质量研究系统评价中草药治疗轻度中度阿尔茨海默病患者的有效性与安全性
2023-06-23王威第五永长王登坤杨谦苟于瑞刘奇周源
王威 第五永长 王登坤 杨谦 苟于瑞 刘奇 周源
摘要 目的:系統评价中草药治疗轻度至中度阿尔茨海默病(AD)患者的有效性与安全性。方法:检索Cochrane图书馆、EMbase、PubMed、Medline、国家知识基础设施数据库(CNKI)等数据库,时间从建库至2020年1月18日。根据Cochrane工具评价文献的质量,排除没有提到随机与盲法的研究。采用RevMan5.3分析中草药治疗AD的疗效,通过计算Cochrane手册中的公式计算观察组与对照组的阿尔茨海默病评定量表(ADAS-Cog)、临床痴呆评定量表(CDR)和简易精神状态检查(MMSE)的效应值,对效应值进行Meta分析,分组描述其差异。结果:共纳入8项高质量的随机对照研究,国内外研究各4项,共582例患者,观察组与对照组每组291例。Meta分析结果显示2组异质性较高,通过亚组分析组间异质性降低,中草药治疗轻度中度AD可改善ADAS-cog评分,且优于安慰剂组(MD=-1.80,95%CI为-3.37~0.23,I2=0%,P=0.84)与多奈哌齐组(MD=-12.07,95%CI为-12.71~11.43,I2=53%,P=0.12,);MMSE评分也优于多奈哌齐(MD=-0.73,95%CI为-0.12~1.58,I2=0%,P=0.57);CDR评分也有改善,安慰剂组MD=-2.63,95%CI为-3.24~2.02,I2=42%,P=0.19;多奈哌齐组MD=-0.27,95%CI为-0.81~0.27,I2=75%,P=0.05。结论:中草药制剂与提取物都能够改善轻度至中度AD患者的认知能力ADAS-cog,MMSE与综合能力CDR,在改善认知能力方面优于多奈哌齐且不良反应发生率比多奈哌齐低,安全性较高,可供临床参考。
关键词 中草药;中药;阿尔茨海默病;系统评价;Meta分析
Efficacy and Safety of Chinese Herbal Medicine in the Treatment of Mild to Moderate Alzheimer′s Disease Based on High-quality Research:A Systematic Review
WANG Wei1,DIWU Yongchang2,WANG Dengkun1,YANG Qian1,GOU Yurui1,LIU Qi2,ZHOU Yuan2
(1 The First Clinical School of Shaanxi University of Chinese Medicine,Xianyang 712000,China; 2 Department of Clinical Medicine,Shaanxi University of Traditional Chinese Medicine,Xianyang 712000,China)
Abstract Objective:To systematically review the efficacy and safety of Chinese herbal medicine in the treatment of patients with mild to moderate Alzheimer′s disease(AD).Methods:Cochrane Library,EMbase,PubMed,Medline,CNKI,and other databases were searched from database inception to January 18,2020.According to the Cochrane risk of bias tool,the quality of the literature was evaluated,and studies that did not mention randomization and blinding were excluded.RevMan5.3 was used to analyze the efficacy of Chinese herbal medicine in the treatment of AD.The effect values of the Alzheimer′s Disease Assessment Scale-Cognitive Subscale(ADAS-Cog),Clinical Dementia Rating(CDR),and Mini-Mental State Examination(MMSE) of the treatment group and the control group were calculated according to the formulas in the Cochrane Handbook.The effect values underwent Meta-analysis and the differences were described by groups.Results:Eight high-quality randomized controlled trials(RCTs) were included,including four Chinese trials and four foreign ones,with 582 patients involved,including 291 in the treatment group and 291 in the control group.The Meta-analysis results showed that the heterogeneity of the two groups was high,and the heterogeneity between the groups was reduced by subgroup analysis.In the treatment of mild to moderate AD,Chinese herbal medicine could improve the ADAS-Cog score,which was superior to the placebo group(MD=-1.80,95%CI -3.37 to 0.23,I2=0%,P=0.84) and the donepezil group(MD=-12.07,95%CI -12.71 to 11.43,I2=53%,P=0.12).In terms of MMSE score improvement,Chinese herbal medicine was superior to donepezil(MD=-0.73,95%CI -0.12 to 1.58,I2=0%,P=0.57).In terms of CDR score improvement,Chinese herbal medicine was superior to placebo(MD=-2.63,95%CI -3.24 to 2.02,I2=42%,P=0.19) and donepezil(MD=-0.27,95%CI -0.81 to 0.27,I2=75%,P=0.05).Conclusion:Chinese herbal medicine preparations and extracts can improve the cognitive ability(ADAS-Cog and MMSE) and comprehensive ability(CDR) of patients with mild to moderate AD.They are superior to donepezil in improving cognitive ability with a lower incidence of adverse reactions than donepezil and higher safety,which can be used for clinical references.
Keywords Chinese herbal medicine; Chinese medicine; Alzheimer′s disease; Systematic review; Meta-analysis
中图分类号:R282;R749.1文献标识码:Adoi:10.3969/j.issn.1673-7202.2023.01.016
阿尔茨海默病(Alzheimer′s Disease,AD)是老年痴呆的主要原因,也是老年人群的第5大死因,其特征是记忆力减退和进行性神经认知功能障碍。全世界大约5 000万痴呆症患者,每年新增病例1 000万,其中AD占痴呆总患病人数的60%~70%[1]。尽管与AD发病机制相关的一系列假说得到了发展,但仍未有确凿的证据能够完全解释其发病的原因[2]。目前可用的药物治疗相对不足,迫切需要开发和实施新的疗法[3]。AD属于中医的“呆证”范畴,轻度AD的中医证候主要表现为髓海渐空、脾肾两虚、气血不足等,中度AD以痰浊蒙窍、瘀阻脑络、心肝火旺为主[4]。在临床上复合证候也比较常见,如髓空痰浊证[5]。通过基础研究许多中草药的药理作用也逐渐浮出水面[6],其作用机制可能是通过激活多信号通路对人海马神经起到促进作用,但疗效尚无定论[7]。由于安全性的担忧导致中草药在国际上的认可度和接受度较低[8]。本研究通过整合国内外高质量的临床研究文献,系统评价了中草药治疗轻度至中度AD患者疗效与安全性。
1 资料与方法
1.1 资料来源 使用中国生物医学文献数据库(China Biology Medicine disc,CBM),国家知识基础设施数据库(China National Knowledge Infrastructure,CNKI),中国学术期刊数据库(China Science Periodical Database,CSPD)中文科技期刊数据库(Chinese Citation Database,CCD),Cochrane Library数据库、EMbase数据库、PubMed、Medline等中英文数据库检索AD临床随机对照试验(Randomized Controlled Trial,RCT)。检索时间从建库至2021年1月18日。检索词:1)中草药,中药,Chinese Herbal Medcine等;2)阿尔茨海默病,阿尔兹海默病,老年痴呆,Alzheimer disease,dementia等;3)临床试验、安慰剂、随机、双盲、对照等。
1.2 纳入标准 符合2011年美国国立老化研究所和阿尔茨海默病协会制定的AD诊断标准,2013年美国精神障碍诊断与统计手册(DSM-Ⅵ)等;觀察组包括:任何形式的草药、草药制剂、草药提取物,不限制剂量、使用频率、剂型、疗程等。对照组可以是安慰剂、中药或西药,不限制给药方式和剂量。包含所有研究中草药治疗AD患者的RCT,不限制研究背景、出版语言、持续时间等。
1.3 排除标准 未提到具体的盲法与随机方法的研究;排除观察组或对照组的简易精神状态检查(Mini Mental Status Examination,MMSE)基线平均得分低于10分的研究,因为参与者低于10分通常被归类为重度AD;配合辅助治疗,如其他非中草药辅助性药物、针灸等研究;数据缺失的研究;研究对象包括轻度认知障碍(Mild Cognitive Impairment,MCI)、血管性痴呆(Vascular Dementia,VD)与重度痴呆的研究。
1.4 纳入标准 按照PRISMA声明(Preferred Reporting Items For Systematic Reviews and Meta-analyses Statement)的文献筛选流程图[9]。剔除明显不符的文献,阅读文献的标题摘要,根据纳入排标准阅读全文评估符合标准的研究。提取符合纳入标准的数据,包括第一作者,标题,发表年份,样本量,干预措施,诊断标准,研究持续时间,对照措施,数据信息(基线、治疗结束、随访),参与者平均年龄,脱落人数,结局指标,受教育年限,不良反应等。2名研究者独立提取数据,当原始文献的数据出现不完整和明显偏差时,需联系原作者,进一步获取准确信息,最后交叉核对,如有不同意见,由第三方评价者进行审核。
1.5 偏倚风险评估 根据Cochrane Handbook 5.2.0提供的文献评价标准[10],对所纳入的研究进行方法学质量评价,包括:随机序列的产生、分配隐藏、对研究者和研究对象设盲、对结局评价者设盲、结局资料的完整性、选择性报告、其他可能影响结果真实性的因素等7方面因素。质量评价仍由2名研究者独立进行交叉检查,任何异议将与第3名研究者讨论并进行裁决,最终达成一致意见。
1.6 阿尔茨海默病评定量表-认知部分(Alzheimer′s Disease Assessment Scale-Cognitive Subscale,ADAS-cog)评分 6项研究以ADAS-cog作为评估工具[11,13,15-18],其中2项研究提到了基线与终点的具体数据[11,13],4项研究给出了效应值(终点Mean±SD-基线Mean±SD)[15-18],通过其中1项研究中给出的基线、终点与效应值的SD[13],计算出观察组Corr=0.89,对照组Corr=0.84。根据Cochrane Handbook 5.2.0提供的换算公式,计算出2项研究的效应值;对效应值进行Meta分析,发现异质性较高(P<0.000 01,I2=98%)使用亚组分析,根据不同的干预措施分为奈哌齐组和安慰剂组后,中草药对比多奈哌齐组的异质性基本消失(P=0.12,I2=53%),对比安慰剂组中有一项研究异质性较高[17],分析其原因可能与给药途径有关,其采用口服药物治疗,而同组其他两项研究采用静脉滴注治疗,将其剔除后组间异质性消失(P=0.84,I2=0%)。
1.7 MMSE评分 4项研究将MMSE作为评估工具,以多奈哌齐作为对照组[11-14],通过分析效应值,发现组间异质性较大,剔除异质性较高的1项研究后异质性消失(P=0.57,I2=0%)[12],分析异质性原因与数据不完整有关,且没有报告脱落人数,导致研究结果有明显的异质性。
1.8 临床痴呆评定量表(Clinical Dementia Rating,CDR)评分 5项研究以CDR作为结局指标,评价了中草药治疗轻度中度AD患者的综合能力[12,15-18]。
1.9 数据分析 采用Cochrane协作网提供的RevMan 5.3统计软件进行分析。连续型资料采用加权均方差(Weighted Mean Difference,WMD)表示,二分类资料采用相对风险比(Risk Ratio,RR)和95%CI表示。若无明显异质性(P>0.1,I2<50%),以固定效应模型计算合并效应量;若存在异质性(P<0.1,I2>50%),则以随机效应模型计算合并效应量,并进行亚组分析,寻找异质性来源;若异质性过大,则仅做描述性分析。对于不完整数据进行意向性治疗分析(Intention-to-Treat Analysis,ITT Analysis)以验证证据的可靠性。
2 结果
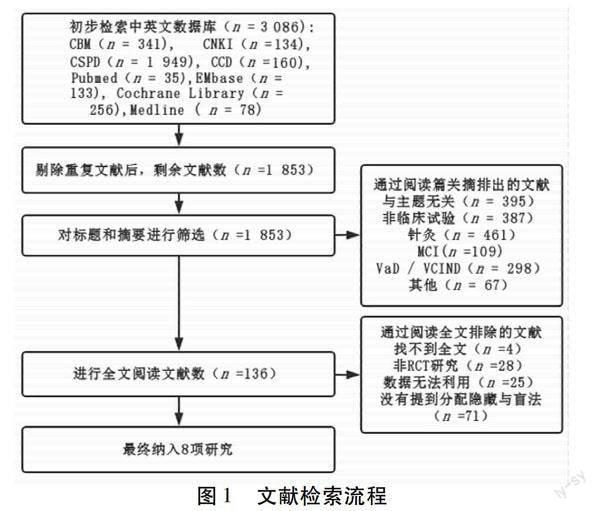
2.1 文献检索结果 根据检索策略,初步检索文献3 086篇,经剔重后剩余1 853篇文献,经阅读文献题目、摘要、关键词后剩余136篇文献;阅读全文后4篇没有找到全文,28篇非RCT研究,数据无法利用25篇,没有提到分配隐藏与盲法71篇,最终纳入15篇文献进行数据分析。见图1。
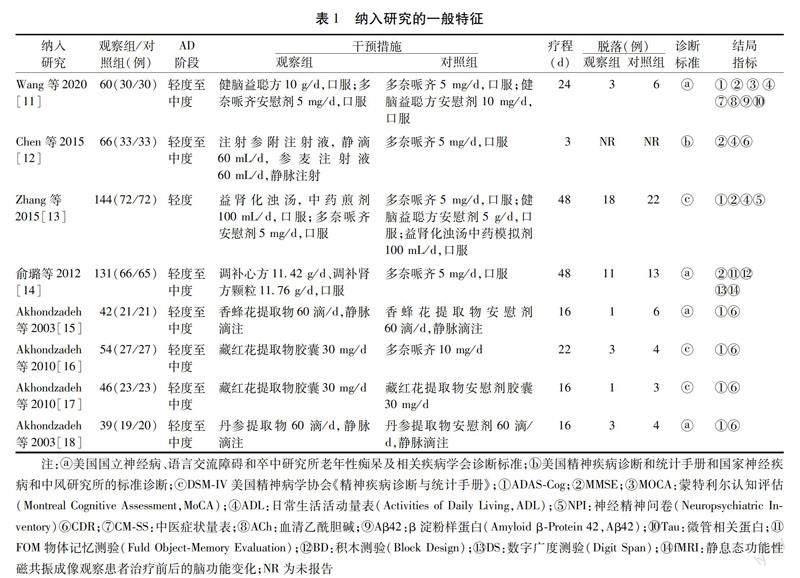
2.2 纳入研究的一般特征 共纳入8项研究[11-18],4项研究在国内进行[11-14],4项研究在国外进行[15-18],共包括582例患者(观察组:291例,对照组:291例)。1项研究[12]对受试者进行12个月的随访,5项研究[12-14,16-17]对报告了患者的受教育年限,7项研究[11,13-18]报告了脱落人数与具体脱落原因。观察组中有3项研究[11,13-14]使用中草药复方,5项研究[12,15-18]使用单味种草药提取物;对照组中5项研究[11-14,16]使用多奈哌齐,3项研究[15,17-18]使用安慰剂。见表1。
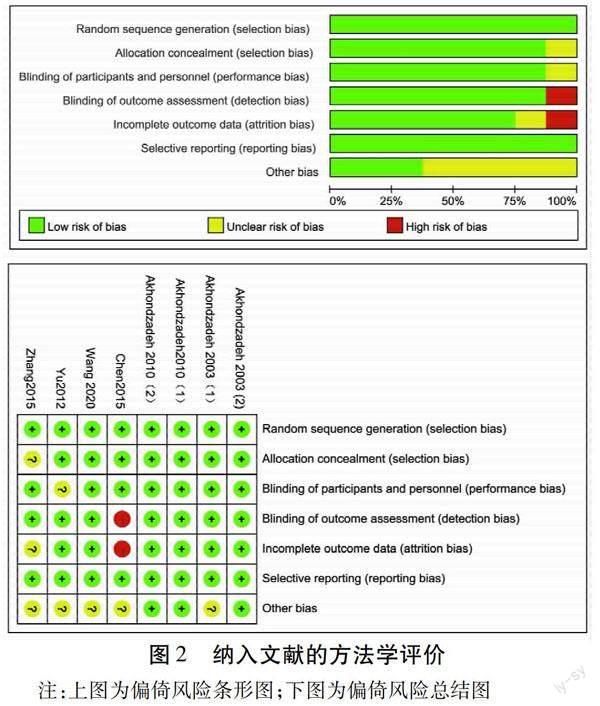
2.3 纳入研究的质量评价 所纳入的8项研究均质量相对较高,所有研究都阐述了具体的随机方法、分配隐藏、具体的盲法与不良反应,均无选择性报告研究结果。7项双盲研究结果数据完整,1项单盲研究未对研究者施盲,且未报告脱落人数,可能存在偏倚[12]。见图2。
2.4 ADAS-cog评分 结果显示中草药组优于安慰剂组(MD=-12.07,95%CI为-12.71~-11.43,P<0.000 01),明显优于多奈哌齐组(MD=-1.80,95%CI为-3.37~-0.23,P=0.02),提示中草药对轻度至中度AD的认知能力有改善作用且优于多奈哌齐。见图3。
2.5 MMSE评分 结果显示,中草药组与多奈哌齐组在MMSE评分评定认知功能障碍上差异无统计学意义(MD=-0.73,95%CI为-0.12~1.58,P=0.09)。见图4。
2.6 CDR评分 通过对计算出的效应值的Meta分析发现组间组异质性较高(P<0.000 01,I2=96%),进行亚组分析后异质性降低,中草药对比安慰剂、多奈哌齐2个亚组的异质性分别为P=0.19,I2=42%;P=0.05,I2=75%。两亚组Meta分析结果显示,中草药组对于改善CDR评分优于安慰剂(MD=-2.63,95%CI为-3.24~-2.02,P<0.000 01),与多奈哌齐组比较差异无统计学意义(MD=-0.27,95%CI为-0.81~0.27,P=0.32)。见图5。
2.7 不良事件 在8项研究中,没有严重不良事件的报道,只报告了轻度不良事件,观察组主要表现为胃肠道反应、兴奋、头晕、打喷嚏、便秘等,对照组主要表现为失眠、恶心、呕吐、头晕、疲劳等。对照组出现不良反应人数多于观察组,出现不良反应后均没有暂停试验,也没有进行药物干预,受试者不良反应自行好转。以多奈哌齐作为对照组的5项研究[11-14,16]的不良反应,中草药不良反应发生率为16%(30/183),多奈哌齐为42%(77/182),但组间差异无统计学意义(P=0.06)。见图6。
3 讨论
到目前为止,AD的治疗仍然是一个大難题,西药胆碱酯酶抑制剂如多奈哌齐通常用于治疗轻度至中度AD,但五年以上远期疗效如何还需进一步求证[19]。谷氨酸受体阻滞剂如美金刚,轻度、中度、重度3个阶段的AD皆可治疗,但肾功能不全的患者慎用,临床上也通常将两类药物联合使用[20]。中药制剂治疗老年痴呆有着悠久的历史,用于治疗轻度至中度AD具有很大的潜力[21],可以延缓Aβ沉积物和牛磺酸,调节胆碱能神经递质的代谢等[22],且不良反应相对较低。但大多数中药治疗AD的研究的临床研究设计并不严谨,本研究的优点在于所纳入的文献的质量相对较高,方法学设计较为合理。
在中医整体观念与西方精准医学的激烈碰撞下,中草药的药理研究应运而生。各种草药提取物、化学物质等正在进行临床研究,研究表明中草药提取物对AD具有潜在的治疗作用[23]。纳入的研究除了中药制剂外还包括藏红花提取物,丹参提取物等,此外人参提取物能有效改善AD患者的认知能力[24]。许多在基础研究阶段的中草药提取物也展现出了很大的潜力,如石菖蒲提取物β-细辛可以抑制β淀粉样蛋白(Amyloid β-protein,Aβ),并且这种作用可能通过促进AD细胞模型中的自噬而发生[25];还可以有效地促进PINK1-Parkin介导的线粒体吞噬,从而改善Aβ1-42所致AD大鼠的学习记忆能力[26]。何首乌也有治疗AD的治疗潜力,其主要成分之一2,3,5,4′-四羟基二苯乙烯-2-O-β-D-葡萄糖苷在果蝇和人细胞中也表现出相似的抗Aβ42细胞毒性的保护活性[27]。此外还有益智仁、远志、丹参等药物的提取物质同样能够改善认知能力。
目前,已有4个不同版本的AD中医证候诊断标准,其中医证候特征都不外乎虚实2种,轻度AD以为虚证为主,中度AD以实证为主,临床多见虚实夹杂。除了上文中提到的6种中医证候外,临床中遇到的很多患者并不局限于单一证候上,会伴随很多兼证,如肾虚髓空、髓空痰浊、肾虚血瘀、脾肾两虚夹痰浊等,因此准确合理地辨证施治将事半功倍。所纳入的8项研究有3项[11,13-14]使用的是中草药复方,分别为健脑益聪方(肾虚兼血瘀)、调补心身方(心肾两虚)和益肾化浊汤(肾虚兼痰浊)。5项研究[12,15-18]使用中草药提取物,其中人参、附子、麦冬、香蜂花主虚,藏红花、丹参主瘀。通过分析发现中药制剂与提取物在改善认知能力与综合能力方面不相上下,对于AD患者都具有一定的疗效,且相对于多奈哌齐都具有较小的不良反应。目前在常用于治疗AD的中草药复方中还没有发现香蜂花的踪迹,如果将其加入中草药复方中可能会与其他药物起到相辅相成的作用;相反在使用单味中草药提取物时考虑到不同的中医证候运用不同的提取物,抑或是根据不同的中医证候将中草药提取物联合在一起使用,临床疗效也许会更显著。
研究局限性:由于纳入研究的患者是轻度至中度AD,基线数值差异较大,虽然对其进行了换算,弥补了基线数据差异大的缺陷,但将计算出的效应值进行Meta分析时异质性相对较高。不同的中医证候之间的用药及疗效存在差异,中草药复方与单味中草药提取物的疗效以及不同的给药途径同样也存在差异。患者的教育水平、年龄和性别等因素会影响量表的评分。此外还有许多主观因素干扰,这些因素限制了证据的力量。需要更多高质量的、大样本的、有明确的客观结局指标(如:生物标志物,影像学检查等)的临床研究来进一步深入探讨中草药治疗轻度至中度AD的疗效。
结果表明,中草药复方与提取物都能够有效改善轻度至中度AD患者的认知能力与综合能力,在改善认知能力方面优于多奈哌齐,且不良反应发生率明显比多奈哌齐低,安全性很高,可供临床参考。
利益冲突声明:本文无任何利益冲突。
参考文献
[1]世界卫生组织.痴呆症[EB/OL].[2020.9.21](2021.1.15).https://www.who.int/zh/news-room/fact-sheets/detail/dementia.
[2]BEHL C.The search for novel targets in Alzheimer′s disease-The 90s redux[J].Prog Mol Biol Transl Sci,2021,177:123-135.
[3]BRIGGS R,KENNELLY SP,O′NEILL D.Drug treatments in Alzheimer′s disease[J].Clin Med(Lond),2016,16(3):247-253.
[4]田金洲,时晶.阿尔茨海默病的中医诊疗共识[J].中国中西医结合杂志,2018,38(5):523-529.
[5]芦锰,周雨慧,李晓宁,等.基于数据挖掘中医药治疗阿尔茨海默病用药规律研究[J].中国中药杂志,2021,46(6):1558-1563.
[6]WANG ZY,LIU JG,LI H,et al.Pharmacological effects of active components of chinese herbal medicine in the treatment of Alzheimer′s disease:a review[J].Am J Chin Med,2016,44(8):1525-1541.
[7]YANG WT,ZHENG XW,CHEN S,et al.Chinese herbal medicine for Alzheimer′s disease:Clinical evidence and possible mechanism of neurogenesis[J].Biochem Pharmacol,2017,141:143-155.
[8]PEI H,MA L,CAO Y,et al.Traditional Chinese medicine for Alzheimer′s disease and other cognitive impairment:a review[J].Am J Chin Med,2020,48(3):487-511.
[9]MOHER D,SHAMSEER L,CLARKE M,et al.Preferred reporting items for systematic review and meta-analysis protocols(PRISMA-P) 2015 statement[J].Syst Rev,2015,4(1):1.
[10]HIGGINS JP,ALTMAN DG,GTZSCHE PC,et al.The Cochrane Collaboration′s tool for assessing risk of bias in randomised trials[J].BMJ,2011,343:d5928.
[11]WANG HC,LIU NY,ZHANG S,et al.Clinical experience in treatment of Alzheimer′s disease with Jiannao Yizhi Formula(健腦益智方) and routine western medicine[J].中国结合医学杂志(英文版),2020,26(3):212-218.
[12]CHEN S,YAO X,LIANG Y,et al.Alzheimer′s disease treated with combined therapy based on nourishing marrow and reinforcing Qi[J].J Tradit Chin Med,2015,35(3):255-259.
[13]ZHANG Y,LIN C,ZHANG L,et al.Cognitive improvement during treatment for mild Alzheimer′s disease with a Chinese herbal formula:a randomized controlled trial[J].PLoS One,2015,10(6):e0130353.
[14]俞璐,林水淼,周如倩,等.中医辨证治疗轻中度阿尔茨海默病的随机对照试验[J].中西医结合学报,2012,10(7):766-776.
[15]AKHONDZADEH S,NOROOZIAN M,MOHAMMADI M,et al.Melissa officinalis extract in the treatment of patients with mild to moderate Alzheimer′s disease:a double blind,randomised,placebo controlled trial[J].J Neurol Neurosurg Psychiatry,2003,74(7):863-866.
[16]AKHONDZADEH S,SHAFIEE SABET M,HARIRCHIAN MH,et al.A 22-week,multicenter,randomized,double-blind controlled trial of Crocus sativus in the treatment of mild-to-moderate Alzheimer′s disease[J].Psychopharmacology(Berl),2010,207(4):637-643.
[17]AKHONDZADEH S,SABET MS,HARIRCHIAN MH,et al.Saffron in the treatment of patients with mild to moderate Alzheimer′s disease:a 16-week,randomized and placebo-controlled trial[J].J Clin Pharm Ther,2010,35(5):581-588.
[18]AKHONDZADEH S,NOROOZIAN M,MOHAMMADI M,et al.Salvia officinalis extract in the treatment of patients with mild to moderate Alzheimer′s disease:a double blind,randomized and placebo-controlled trial[J].J Clin Pharm Ther,2003,28(1):53-59.
[19]贾建平.中国痴呆与认知障碍诊治指南[M].北京:人民卫生出版社,2015:47-48.
[20]田金洲.中国痴呆诊疗指南[M].北京:人民卫生出版社,2017:210-212.
[21]ZHANG Y,NOH K,SONG W.Chinese herbal medicines on cognitive function and activity of daily living in senior adults with Alzheimer′s disease:a systematic review and meta-analysis[J].Integr Med Res,2019,8(2):92-100.
[22]牛天童,刘广志.中药对阿尔茨海默病鼠模型作用机制的研究进展[J].中国医药,2021,16(12):1903-1906.
[23]CHEN SY,GAO Y,SUN JY,et al.Traditional Chinese medicine:role in reducing β-amyloid,apoptosis,autophagy,neuroinflammation,oxidative stress,and mitochondrial dysfunction of Alzheimer′s disease[J].Front Pharmacol,2020,11:497.
[24]LEE ST,CHU K,SIM JY,et al.Panax ginseng enhances cognitive performance in Alzheimer disease[J].Alzheimer Dis Assoc Disord,2008,22(3):222-226.
[25]WANG N,WANG H,LI L,et al.β-asarone inhibits amyloid-β by promoting autophagy in a cell model of Alzheimer′s disease[J].Front Pharmacol,2019,10:1529.
[26]HAN Y,WANG N,KANG J,et al.β-Asarone improves learning and memory in Aβ1-42-induced Alzheimer′s disease rats by regulating PINK1-Parkin-mediated mitophagy[J].Metab Brain Dis,2020,35(7):1109-1117.
[27]LIU QF,LEE JH,KIM YM,et al.In vivo screening of traditional medicinal plants for neuroprotective activity against Aβ42 cytotoxicity by using drosophila models of Alzheimer′s disease[J].Biol Pharm Bull,2015,38(12):1891-1901.
(2021-03-03收稿 本文编辑:张雄杰)
基金項目:国家自然科学基金项目(82074503);陕西省“专项支持计划”技术创新领导工程项目(陕组通字2018-33号);陕西省自然科学基础研究计划-重大项目(2017ZDJC-15);陕西中医药大学学科创新团队项目(2019-QN05)作者简介:王威(1993.05—),男,硕士研究生在读,研究方向:中医内科学老年病,E-mail:615134464@qq.com通信作者:第五永长(1971.07—),男,博士后,主任医师,教授,博士研究生导师,研究方向:神经退行性疾病的中医药防治,E-mail:diwuyongchang@126.com
