利用乳液静电纺丝法制备具有稳定芯壳结构的PLGA/DEX 电纺纤维
2023-06-21王倩茜王凯戎龚雨薇张华林
王倩茜, 王凯戎, 龚雨薇, 张华林
(宁夏医科大学口腔医学院,银川 750004)
药物递送系统是将生物活性物质和各种载体材料结合起来用以靶向输送药物的系统,此方法既可以保持生长因子的稳定性,又能够很好地控制药物释放,因此其在药物控释、缓释等领域具有较好应用前景[1]。传统的溶液静电纺丝技术制备的纳米纤维通常是单轴结构,采用这种方法制备的载药纳米纤维在释放初期容易产生药物突释的现象。而且当搭载物为生物活性大分子时,由于聚合物溶液会直接与生物活性大分子接触,会对其分子结构造成破坏,从而破坏蛋白的生物活性[2],乳液静电纺丝技术能够很好地克服这些不足。乳液静电纺丝技术与传统的溶液静电纺丝技术的原理类似,区别在于用乳液取代之前所用的均一透明的纺丝溶液来进行静电纺丝,就可以制备出具有稳定芯壳结构的电纺纤维[3]。根据连续相和分散相不同,乳液可分为油包水型乳液(W/O)和水包油型乳液(O/W)两种类型。油包水型乳液可将水溶性的生物活性大分子或药物包裹在纤维的芯层,在电纺前及电纺过程中,药物或活性因子等一直位于纤维的芯层而未与壳层的有机溶剂接触,这样药物就可以避免受到外界环境和有机溶剂的影响而失去活性。这种包覆结构还避免了传统的溶液静电纺丝带来的药物分散不均和突释等问题[4-6]。本研究将聚乳酸-羟基乙酸共聚物[poly(lactic-co-glycolic acid)PLGA]作为壳层、葡聚糖(dextran,DEX)作为芯层,通过改变油相溶剂的成分、水相溶液的浓度以及水油体积比来调整乳液水相与油相间的相容性、黏度比以及界面张力,以制备具有稳定芯壳结构的电纺纤维并优化相关的工艺参数,为利用乳液静电纺丝法制备以PLGA/DEX 为载体的载药纤维膜奠定实验基础。
1 材料与方法
1.1 试剂
PLGA(PLA∶PGA = 75∶25,济南岱罡生物科技有限公司);三氯甲烷(CHCl3)、N,N-二甲基甲酰胺(DMF)、三氟乙醇(TFE,分析纯,徐州天鸿化工贸易有限公司);PBS(美国HyClone 公司);DEX(美国Sigma-ALdrich 公司)。
1.2 仪器
恒温干燥箱(DHJ-9030,上海一恒科技有限公司);电子天平(ME204E,瑞士METTLER 公司);超声振荡器(KQ-100,昆山超声仪器有限公司);静电纺丝仪(SS-2535,北京永康乐业科技发展有限公司);透射电子显微镜(TEM,JEM-3010,日本JEOL 公司);扫描电子显微镜(SEM,JSM-6510,日本JEOL 公司)。
1.3 电纺液的配制
将PLGA 溶解于按一定比例混合的CHCl3、TFE 及DMF 的有机溶剂中,分别获得PLGA 溶液O-1 和O-2 作为壳层溶液(即油相,其中O-1为0.15 g·mL-1的PLGA 溶液,溶剂为DMF 和CHCl3,体积比为1∶3;O-2 为0.15 g·mL-1的PLGA 溶液,溶剂为CHCl3、TFE、DMF,体积比为65∶10∶25)。将3 种含不同浓度DEX 的水溶液作为芯层溶液W-1、W-2、W-3(即水相,其中W-1 为0.5 g·mL-1的DEX 溶液;W-2 为0.2 g·mL-1的DEX 溶液;W-3 为0.15 g·mL-1的DEX 溶液),各溶液均在常温下配制,静置并排除气泡后待用。
利用上述壳层溶液O-1、O-2 和芯层溶液W-1、W-2、W-3 配制成以下6 组电纺液S1~S6。S1:将O-1 作为油相溶液,W-1 作为水相溶液,按水油体积比1∶20 的比例,将W-1 逐滴加入O-1 中,并利用超声振荡器以及磁力搅拌器将其充分混合均匀,制备成S1 号电纺液;S2:将O-2作为油相溶液,W-1 作为水相溶液,按水油体积比1∶20 的比例,将W-1 逐滴加入O-2 中,并利用超声振荡器以及磁力搅拌器将其充分混合均匀,制备成S2 号电纺液;S3:将O-1 作为油相溶液,W-2 作为水相溶液,按水油体积比1∶20 的比例,将W-2 逐滴加入O-1 中,并利用超声振荡器以及磁力搅拌器将其充分混合均匀,制备成S3号电纺液;S4:将O-1 作为油相溶液,W-2 作为水相溶液,按水油体积比1∶15 的比例,将W-2 逐滴加入O-1 中,并利用超声振荡器以及磁力搅拌器将其充分混合均匀,制备成S4 号电纺液;S5:将O-1 作为油相溶液,W-3 作为水相溶液,按水油体积比1∶10 的比例,将W-3 逐滴加入O-1中,并利用超声振荡器以及磁力搅拌器将其充分混合均匀,制备成S5 号电纺液;S6:将O-1 作为油相溶液,W-3 作为水相溶液,按水油体积比1∶13 的比例,将W-3 逐滴加入O-1 中,并利用超声振荡器以及磁力搅拌器将其充分混合均匀,制备成S6 号电纺液。将上述电纺液配制成功后静置,观察并比较6 组电纺液的乳液体系是否稳定、两相溶液的相容性以及界面张力是否适当,以优选出乳液性质最稳定的电纺液。
1.4 乳液静电纺丝法制备PLGA/DEX 纳米纤维
将6 组电纺液分别载入静电纺丝设备的注射装置中(2.5 mL 注射器,内径为0.5 mm 的金属针头)并将其固定于螺旋推注器上,螺旋推注器的速度为0.2 mm·min-1,接收距离为15 cm,电纺时将高压电源与金属喷头相连,在14 kV 的电压下分别对6 组纺丝液进行电纺,电纺时间为90 min,观察并比较各组电纺液的纺丝过程是否稳定以及制备的PLGA/ DEX 纳米纤维膜是否均匀。
1.5 扫描电镜观察
利用SEM 观察6 组PLGA/ DEX 纤维膜的表面形貌。利用Smile View 软件检测6 组PLGA/DEX 纤维的直径。
1.6 透射电镜观察
利用铜网接取6 组PLGA/ DEX 电纺纤维,于TEM 下观察其是否具有稳定的芯壳结构。
2 结果
2.1 电纺液的稳定性
将制备的6 组电纺液静置观察,可发现S1电纺液由于水相浓度过高,导致界面张力过大,两相相容性很差,水相以较大的液滴悬浮于油相溶液上层,无法形成微小的液滴悬浮于油相中,因此S1 乳液不能作为合格的乳液静电纺丝液制备纳米纤维。由于TFE 能与水和有机溶剂相混溶,S2 电纺液引入TFE 后,水相溶液与油相溶液的界面张力减小,与S1 相比,其两相的相容性有所改善,但仍存在部分较大的液滴漂浮于油相的上层,乳液体系仍不稳定的情况。与S1、S2 相比,S3 电纺液的界面张力小,两相的相容性更好,能够形成乳液体系,但静置半小时后,乳液存在轻微破乳现象,即水相的小液滴逐渐凝聚成团,形成大液滴,使水油两相分离,虽较S1、S2 更稳定,但乳液的稳定程度仍不够理想。S4 与S3 水油两相的成分相同,仅调整了水油体积比例,初期能够形成乳液,半小时后观察,也存在轻微破乳现象;S5 电纺液,降低了水相溶液的浓度,水油两相之间相容性较好,水相分散成微小的液滴悬浮于油相溶液中,静置半小时后观察,乳液出现分层;S6 与S5 水油两相的成分相同,仅调整了水油体积比,通过搅拌振荡后能够形成稳定的乳液,静置30 min 后,乳液性质未发生改变,见图1。

图1 6 组电纺液的稳定性大体观察图
2.2 乳液静电纺丝过程的稳定性
6 组不同的电纺液由于水相浓度不同、水油体积比例不同,使电纺液的可纺性也不尽相同。在电纺过程中,S1 纺丝液的油相具有良好的可纺性,但水相溶液黏度大,无法分散成微小的液滴被油相包裹带出,而是聚集成大的液滴从针头处喷溅出来,影响了电纺的稳定性;S2 纺丝液引入TFE 后,电纺效果没有明显改善,仍有大的液滴从针头处喷溅出来,无法完成稳定电纺;S3 纺丝液在电纺初期,能够进行稳定的电纺,但在电纺后期,纺丝液存在破乳现象,水油易分离,偶尔有少量液滴聚集从针头喷出,整体电纺较稳定;S4 与S3 相比,调整了水油体积比后,电纺过程中无明显差别,同样后期存在破乳现象,偶有液滴从喷头处喷出,整体电纺较稳定;S5 纺丝液在电纺过程中,初期能够进行稳定的电纺,但在电纺后期,纺丝液出现分层现象,纺丝过程不稳定;S6 与S5 纺丝液成分相同,仅调整了水油体积比,纺丝液性质稳定,可纺性好,整个电纺过程中未发生破乳现象,喷头处也无液滴喷出,纺丝过程稳定,见图2。

图2 6 组电纺液纺丝过程
2.3 纤维膜大体观察
S1 电纺液在电纺过程中有大的液滴从针头处喷溅出来,使其制备的纳米纤维膜表面呈颗粒状,不均匀;与S1 相比,S2 电纺液的电纺过程没有明显改善,仍有少数大的液滴从针头处喷溅出来,制备的纳米纤维膜仍呈颗粒状,但较S1 均匀;S3 电纺液在电纺初期能够进行稳定的电纺,但在电纺后期,有少数小液滴从针头处喷溅出来,制备的纳米纤维膜整体较均匀;S4、S5 电纺液的电纺过程与S3 无明显区别,制备的纳米纤维膜整体较均匀;S6 电纺液的电纺过程稳定,无液滴从针头处喷溅出来,其制备的纳米纤维膜较光滑、均匀,见图3。

图3 6 组PLGA/ DEX 纳米纤维膜实物图
2.4 SEM 结果
6 组电纺液电纺后均能形成表面光滑且无明显串珠状结构的纤维,纤维交织成网。由于S1 电纺液中水相溶液浓度最大,纺丝液的黏度也最大,电纺过程不稳定,导致电纺后的纳米纤维直径差异较大,直径为0.15~0.45 μm,平均直径为(0.24±0.06)μm;S2 电纺液通过改变油相溶剂的成分,适当减小两相的界面张力,与S1 相比,电纺过程没有明显改善,电纺后的纳米纤维直径差异仍较大,为0.1~0.6 μm,平均直径为(0.31±0.09)μm;S3 电纺液中水相溶液浓度降低,纺丝液的黏度也随之降低,电纺初期较稳定,但在电纺后期纺丝液出现破乳现象,电纺过程不稳定,纳米纤维直径为0.15~0.50 μm,平均直径为(0.29±0.06)μm;与S3 相比,S4 电纺液降低水油两相体积比后,电纺过程无明显差别,电纺后的纳米纤维直径为0.35~0.75 μm,平均直径为(0.49±0.08)μm;S5 电纺液初期能够进行稳定电纺,电纺后期纺丝液出现分层现象,电纺过程不稳定,电纺后的纳米纤维直径为0.1~0.7 μm,平均直径为(0.39±0.13)μm;S6 电纺液的电纺过程整体稳定,电纺后的纳米纤维直径分布较均匀,为0.20~0.45 μm,平均直径为(0.32±0.04)μm,见图4、图5。

图4 6 组电纺液电纺后PLGA/DEX 纤维的SEM 图
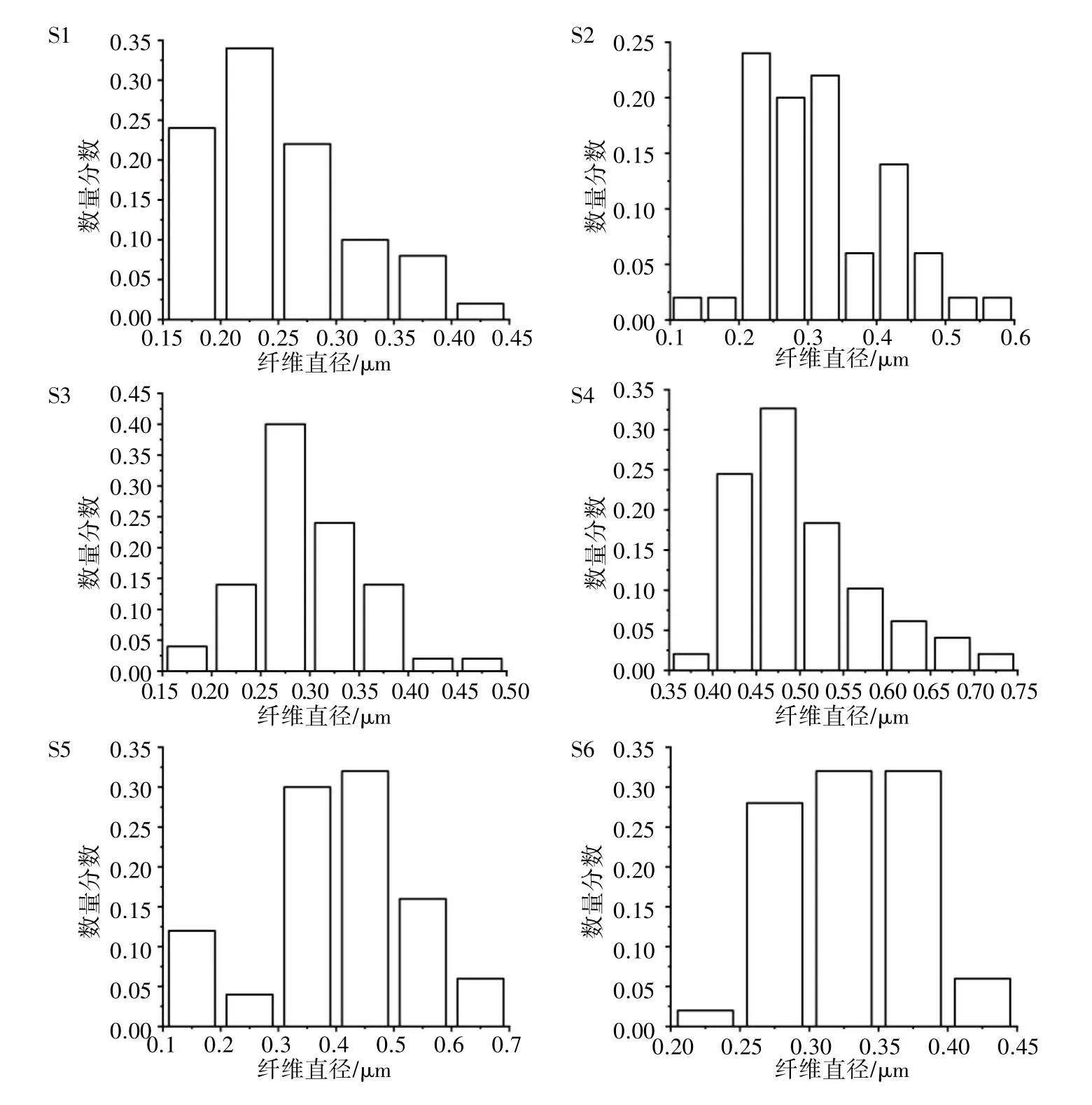
图5 6 组电纺液电纺后PLGA/DEX 纤维的直径分布图
2.5 TEM 结果
S1 电纺后,仅有极其微量的水相溶液被油相包裹,无法形成稳定的芯层,且包裹量极小。S2加入TFE 后,纺丝液的搭载能力有所提升,与S1相比,芯层物质较多,但仍无法形成理想的芯壳结构。调整水相浓度后,S3 能够形成芯壳结构的纳米纤维,但水相溶液不只存在于芯层,壳层中也散在分布着未完全溶解的DEX 颗粒。增大水油体积比后,仍然可以形成稳定的芯壳结构,但S4 纤维壳层较S3 电纺纤维的壳层散在分布的DEX 颗粒更多。S5 和S6 纺丝液将水相溶液的浓度减小后,DEX 在水相中溶解更均匀,壳层无散在的DEX 颗粒,均能够形成稳定的芯壳结构,见图6。

图6 6 组电纺液电纺后PLGA/DEX 纤维的TEM 图(bar=200 nm)
3 讨论
影响静电纺丝纤维形貌的参数有很多,主要包括电纺设备自身参数(如电纺时电压、针头与接收器的距离、液体推进速度等)、纺丝液性质(如聚合物种类、纺丝液黏度、溶液和溶剂的稳定性)以及电纺环境(温度、湿度等)[7]。利用乳液电纺技术制备纳米纤维,除了以上电纺本身的影响因素以外,乳液的稳定性对于获得具有芯壳结构的纳米纤维也十分关键。其中,水相和油相溶液间的相容性、黏度比以及界面张力都对乳液稳定性有很大影响[8]。制备具有稳定的芯壳结构的纳米纤维使其具有更高的载药量及更好的控释、缓释效果,在递送特殊药物方面具有重要意义[9-10]。
乳液的性质主要由乳液的稳定性、黏度及其电导率决定[11-12]。本研究通过改变油相溶剂的成分、水油体积比以及水相的浓度来改善乳液的性质,以达到形成稳定芯壳结构的目的。理想的静电纺丝液要求其具有良好的可纺性,在适当的电纺参数下,可纺性好的电纺液能够形成粗细均匀、形貌良好的电纺纤维,相反,可纺性差的电纺液纺丝过程不稳定,无法得到性质稳定的电纺纳米纤维。高聚物溶剂的电导率是电纺纤维形貌的重要影响因素之一,由于CHCl3的电导率较低,将其作为静电纺丝的单一溶剂时,得到的纳米纤维存在大量串珠,纤维形貌不良,不是静电纺丝的良溶剂[13]。引入DMF 后,使CHCl3∶DMF 按3∶1比例混溶作为高聚物的有机溶剂,能够制备出形貌良好的电纺纳米纤维[14],是乳液电纺理想的壳层溶剂。S1 电纺液由于水相浓度过高,使得两相界面张力过大,且黏度过高,导致难以形成稳定的乳液电纺液。S2 与S1 相比,水相溶液浓度不变时,适当引入TFE 后,通过电纺过程以及电镜结果发现,由于TFE 具有既能与水混溶,也能作为有机溶剂的性质,一定程度上减小了芯层溶液与壳层溶液的界面张力,增大了两相的相容性,相容性提升后,S2 较S1 芯层搭载物质更多,证明两相之间的相容性越好,纳米纤维的搭载能力就会越高。但由于DEX 浓度过高,两相界面张力过大,无法形成稳定的电纺液,使得DEX 溶液以液滴的形式从纺丝针头喷出,并且容易堵塞电纺喷头,中断电纺过程。
纺丝液黏度是影响其可纺性的重要因素之一[12,15-16]。与同轴电纺相似,乳液电纺过程中,壳层需要有一定的黏度来克服两相之间的界面张力,将水相的小液滴牵引拉长,形成芯壳结构的纳米纤维,并且适当的黏度能够保证壳层溶液的表面张力与电场力相平衡,以形成稳定的复合Taylor 锥。但芯层的水溶液黏度不宜过大也不宜过小,黏度过高,无法被油相溶液牵拉形成稳定的复合喷射流;黏度过低,电纺的稳定性下降,不能形成稳定喷射流。因此,水相溶液的黏度需要在适当的范围内才能得到不间断芯壳结构的纳米纤维。调整水相溶液的浓度可以有效改善其黏度。本研究结果显示,水相的黏度随着浓度的降低而降低,两相的相容性则随着黏度降低而升高。与S1、S2 相比,当DEX 浓度从0.5 g·mL-1降低到0.2 g·mL-1和0.15 g·mL-1时,S3、S4、S5、S6 电纺液的黏度随之降低,纺丝液的性质变得更稳定,能够形成稳定的芯壳结构。但当DEX 浓度为0.2 g·mL-1时,水相黏度依然较大,一些黏度大的液滴不能被牵拉成芯层,混合在壳层被带出,形成壳层的颗粒状结构。继续降低芯层浓度为0.15 g·mL-1后,水相黏度适当,两相溶液相容性好,电纺液性质稳定,能够制备出具有明显芯壳结构的纳米纤维材料。
乳液的水油体积比也是影响纤维芯壳结构的重要因素之一[17]。水相体积比过高时,电纺液的可纺性下降,电纺时以乳液液滴的形式从针头喷出,使电纺喷射流不稳定;水相体积比过小时,水溶液的小液滴彼此间距离较远,无法形成稳定连续的芯壳结构。因此,合理的水油体积比对于制备具有连续芯壳结构的纳米纤维十分重要,并且可以通过控制水油体积比来调整壳层的厚度,以控制药物的释放速度。在本研究中发现,改变乳液的水油比对纤维直径和形貌影响非常巨大。在DEX 浓度不变时,增大水相在乳液电纺液中的体积比,纤维中搭载的药物增多,芯层直径增大,壳层直径减小。在DEX 浓度为0.15 g·mL-1时,形成的电纺纤维形貌结构较好,并且根据S5与S6 电纺液的水油体积比不同,显示壳层的厚度不同,考虑到水相体积比越高,纺丝液的稳定性越差,壳层越薄,可认为与水油体积比为1∶10时相比,水油体积比为1∶13 的电纺液更稳定,更容易得到壳层厚度适宜的具有稳定芯壳结构的电纺纤维。
乳液电纺的影响因素复杂多样,电纺纤维的最终形貌是多种因素相互作用的结果,要想得到理想的具有芯壳结构的纳米纤维,需要对各因素进行调整优化。除去本研究中提到的电导率、黏度以及水油比以外,电纺速度、电压值、接收距离、电纺温度湿度等也对纤维形貌结构有重要的影响。本研究重点研究了纺丝液性质对电纺稳定性以及纤维形貌的影响,其他因素对电纺过程以及纤维形貌结构的影响有待进一步探究。
水油两相的黏度对电纺纤维的形貌影响巨大。当水相溶液浓度过高时,导致其黏度过大,两相界面张力大,不利于壳层溶液将其牵引拉出,不能形成稳定连续的芯壳结构纳米纤维。适度降低水相浓度,黏度也随之降低,两相的相容性提高,乳液趋于稳定。水油两相的体积比是纤维芯壳结构以及形貌尺寸的重要因素。适宜的水油体积比形成的乳液,其性质更稳定,可纺性更好。也可通过调整水油体积比来调整壳层的厚度,以控制药物的释放。将浓度为0.15 g·mL-1的PLGA(溶剂为DMF 和CHCl3,体积比为1∶3)作为油相溶液,浓度为0.15 g·mL-1的DEX 作为水相溶液,水油体积比为1∶13 时配制的乳液静电纺丝液性质最稳定,将该纺丝液在速度为0.2 mm·min-1、接收距离为15 cm、电压为14 kV 的条件下进行电纺能够得到具有稳定芯壳结构的电纺纳米纤维。
