血清SP-A 水平联合肺部超声评分对新生儿呼吸窘迫综合征的评估价值
2023-06-17潘华廖欢钟桂福刘锋罗孝华
潘华,廖欢,钟桂福,刘锋,罗孝华
赣州市妇幼保健院,江西 赣州 341099
新生儿呼吸窘迫综合征(NRDS)病情危重,发病较急,如不尽早诊断与治疗,会导致患儿窒息或病死,严重威胁新生儿生命安全[1]。肺部超声因其操作简单、无辐射、可重复操作等优势被广泛用于肺部疾病诊断中,效果显著[2]。目前,临床已逐渐采用量化手段来进行肺部超声检查,双肺12 区评分是通过对双肺12 个区域量化评分来显示双肺病变情况,更具科学性、可靠性[3]。血清肺表面活性蛋白(SP-A)已被证实在肺实质及间质性损伤疾病中具有显著表达,与肺部疾病进展和预后密切相关[4]。基于此,本研究旨在探究血清SP-A 联合肺部超声评分在新生儿NRDS 严重程度及预后的评估价值,以期为临床早期诊断疾病和评估预后提供参考。
1 资料与方法
1.1 一般资料
本研究经赣州市妇幼保健院医学伦理委员会批准[2021 审(082)号],选择2021 年8 月至2022年3 月赣州市妇幼保健院收治的90 例NRDS 新生儿作为NRDS 组,并选择同期健康新生儿45 例作为对照组。对照组男24 例,女21 例;顺产20 例,剖宫产25 例。NRDS 组男47 例,女43 例;顺产42 例,剖宫产48 例。比较两组一般资料(P>0.05),有可比性。
1.2 纳排标准
(1)纳入标准:①NRDS 诊断符合《实用新生儿学》[5]中相关标准;②NRDS 新生儿于出生24 h内入院;③均为单胎;④患儿家长均签知情同意书。(2)排除标准:①合并肺出血、心力衰竭者;②心源性肺水肿;③入院前已接受肺表面活性物质治疗者;④染色体异常、先天性畸形患儿。
1.3 方法
1.3.1血清SP-A 检测抽取对照组及NRDS 组新生儿外周肘静脉血2 mL,以2 000 r/min 的速度离心10 min,将上清液转移至小型离心管中,冰箱-80℃保存集中送检。采用酶联免疫吸附法检测血清SP-A 水平,试剂盒厂家为北京兰博利德商贸有限公司。
1.3.2肺部12 区超声检查所有新生儿均采用迈瑞M9 便携式彩色多普勒超声进行肺部超声检查,凸阵探头:3~5 MHz,线阵探头:8~12 MHz。在新生儿安静状态下,协助其取仰卧、侧卧、俯卧体位,根据胸骨旁线、腋前线及后线、后正中线、双乳头连线把双侧肺部各分为6 个区域,依次用超声从上到下、从左到右对这12 个区域进行扫查,查看有无胸膜线异常、A 线消失、肺实质、弥漫性肺水肿等,并保存声像图。
肺部超声评分标准[6],0 分:肺实变;1 分:有大量融合B 线(瀑布征);2 分:有大量B 线且部分融合;3 分:B 线散在分布,且界限分明;4 分:平滑A 线或孤立B 线<3 条。每个区域0~4 分,12 个区域总分为0~48 分,得分越低,肺部损伤越严重。
1.3.3NRDS 病情严重程度评估方法参考《实用新生儿学》对NRDS 病情严重程度进行分级,Ⅰ级:X 线胸片检查示双肺透亮度降低,有细小颗粒且均呈散在分布,可见网状阴影;Ⅱ级:病变延伸至肺野中外带部位,有支气管充气征表现;Ⅲ级:双肺野透亮度显著降低,膈缘、心缘有模糊影;Ⅳ级可见明显枯枝状支气管充气征,整个肺野表现为白肺状。其中Ⅰ级为轻度组,Ⅱ~Ⅲ级为中度组,Ⅳ级为重度组。
1.3.4预后评估方法按出院时临床结局可将NRDS新生儿分为预后良好组、预后不良组。预后良好:经治疗后出院时NRDS 呼吸道症状减轻或消失,生命体征平稳,胸片检查结果基本正常,脱离呼吸机及氧疗。预后不良:经治疗后效果不理想无法脱离呼吸机,合并严重的并发症或家属因预后、经济等因素放弃治疗或生命体征消失,宣布临床死亡。
1.4 统计学方法
采用SPSS 23.0 统计学软件,以例(%)表示计数资料,采用χ2检验;采用表示计量资料,两组间以t检验,多组间用单因素方差检验,采用logistic 回归分析NRDS 新生儿预后不良的危险因素。绘制受试者工作曲线(ROC)曲线并计算曲线下面积(AUC)值,评估血清SP-A 水平联合肺超声评分对NRDS 新生儿病情严重程度及预后的价值,AUC 值>0.9 表示评估价值较高,0.71~0.90 表示有一定评估价值,0.5~0.7 表示评估价值较差。检验水准α=0.05。
2 结果
2.1 血清SP-A、肺部超声评分
NRDS 组血清SP-A 水平高于对照组,肺部超声评分低于对照组(P<0.05)。见表1。
表1 两组血清SP-A、肺部超声评分比较()

表1 两组血清SP-A、肺部超声评分比较()
2.2 不同病情程度的NRDS 患儿血清SP-A、肺部超声评分
中、重度组血清SP-A 水平高于轻度组,肺超声评分低于轻度组(P<0.05);重度组血清SP-A 水平高于中度组,肺超声评分低于中度组(P<0.05)。见表2。
表2 不同病情程度的NRDS患儿血清SP-A、肺部超声评分比较()

表2 不同病情程度的NRDS患儿血清SP-A、肺部超声评分比较()
注:与轻度组比较,aP<0.05;与中度组比较,bP<0.05。
2.3 NRDS 新生儿预后结局的危险因素logistic 回归分析
胎龄、母体妊娠期糖尿病、血清SP-A 水平、肺部超声评分与NRDS新生儿预后不良的发生有关,差异有统计学意义(P<0.05)。见表3。
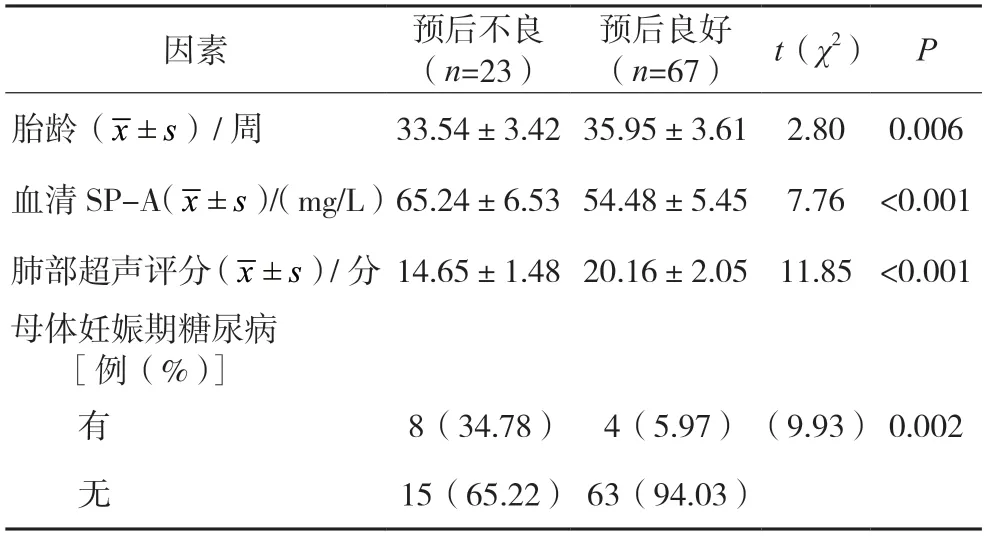
表3 NRDS新生儿预后结局的危险因素分析
将胎龄、血清SP-A 水平、肺部超声评分(均为连续变量)和母体妊娠期糖尿病(1=有,0=无)作为自变量,将NRDS 新生儿预后结局作为因变量(1=预后不良,0=预后良好)。经logistic 回归分析显示,母体有妊娠期糖尿病、血清SP-A 水平较高为NRDS 新生儿预后不良的危险因素(OR>1,P<0.05);胎龄较高、肺超声评分较高为NRDS 新生儿预后不良的保护因素(OR<1,P<0.05)。见表4。
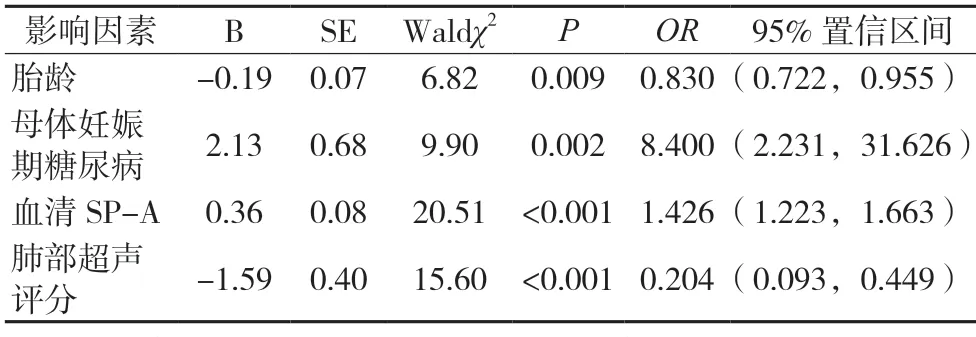
表4 NRDS新生儿预后结局的危险因素logistic回归分析
2.4 血清SP-A 水平联合肺超声评分评估NRDS新生儿病情严重程度及预后价值的ROC 曲线
将血清SP-A 水平、肺部超声评分作为检验变量,将NRDS 新生儿病情严重程度(1=轻度,2=中度,3=重度)及预后状况(1=预后不良,0=预后良好)作为状态变量,绘制ROC 曲线(见图1,2)。结果显示,血清SP-A 水平联合肺超声评分评估NRDS 新生儿病情严重程度及预后的AUC 为0.913、0.896,评估价值较单一检测高。见表5,6。

图1 血清SP-A水平联合肺超声评分评估NRDS新生儿病情严重程度ROC曲线图
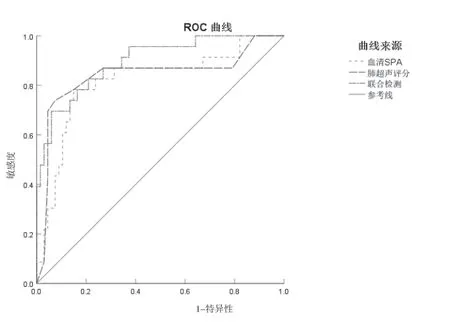
图2 血清SP-A水平联合肺超声评分评估NRDS新生儿预后的ROC曲线图

表5 血清SP-A水平联合肺超声评分评估NRDS新生儿病情严重程度ROC曲线分析

表6 血清SP-A水平联合肺超声评分评估NRDS新生儿预后的ROC曲线分析
3 讨论
NRDS 因肺表面活性物质缺乏所致,在新生儿中具有较高的发病率、致死率。X 线片为检查该疾病的常用方式,但X 线有辐射性,易对新生儿造成辐射损伤,不宜重复使用,且X 线检查也会加重患儿家属的心理负担,引发医患纠纷,需寻求更加安全、有效的诊断方式。
本研究将肺部超声、血清SP-A 检查用于NRDS 新生儿临床诊断中,结果显示,NRDS 组血清SP-A 水平高于对照组,肺部超声评分低于对照组,且随着病情程度增加,NRDS 新生儿的血清SP-A 水平逐渐升高,肺超声评分逐渐降低,且预后不良组血清SP-A 水平高于预后良好组,肺部超声评分低于预后良好组,说明血清SP-A 水平、肺部超声评分与NRDS 新生儿病情严重程度及预后密切相关。肺部超声主要通过检查肺泡及间质内水含量变化所产生的超声伪影来评估患儿的肺部病变情况,具有无辐射、可床旁检查、可重复的优点,且胎儿分娩后可立即行肺部超声检查,安全性更高[7]。但单纯的肺部超声检查也会存在漏诊风险,近年来临床多通过肺部超声评分来量化超声检查结果,以便提高肺超声检查的可靠性。双肺12 区评分是以新生儿的腋前、后线为基准线,将双肺分为12 个区域,以不同的分值来表示不同区域肺部组织病变情况,可有效避免肺内局部病灶遗漏的发生,结合肺实变累及区域进行病情程度的判断效果更显著[8]。
SP-A 为肺表面活性物质的主要蛋白成分,NRDS 发生后,患儿肺内大量漏出的血浆蛋白及分泌的肺内弹性蛋白酶能分解出SP-A,而SP-A 可经受损的肺泡毛细血管进入血液循环中,导致血清SP-A 水平升高,且血清SP-A 升高会降低肺表面活性物质合成量,加重肺上皮功能损伤,进而导致患儿病情加重,造成预后不良[9-10]。因此,血清SP-A 水平与NRDS 新生儿病情严重程度、预后密切相关。本研究logistic 回归分析结果显示,母体有妊娠期糖尿病、胎龄较低、血清SP-A 水平较高、肺超声评分较低为NRDS 新生儿预后不良的危险因素,进一步证实上述结论。但因研究者精力有限,未对母体妊娠期糖尿病、胎龄与NRDS 新生儿预后的关系进行详细分析,这是本研究的局限性,未来可对此展开深入探究。此外,本研究绘制ROC 曲线,结果显示,血清SP-A 水平联合肺超声评分评估NRDS 新生儿病情严重程度及预后的AUC 为0.913、0.896,较单一检测的评估价值高,说明血清SP-A水平、肺部超声评分联合检测可提升NRDS 新生儿病情程度及预后的评估价值。
综上所述,血清SP-A 水平、肺部超声评分与NRDS 新生儿病情严重程度及预后密切相关,联合检测可提升NRDS 新生儿病情程度及预后的评估价值。
