吉西他滨膀胱灌注对非肌层浸润性膀胱癌TURBT 术后复发及免疫功能的影响
2023-06-17熊毅
熊毅
瑞金市人民医院,江西 瑞金 342500
非肌层浸润性膀胱癌是指癌细胞仅局限在黏膜与黏膜下层,未在上皮内浸润性生长。经尿道膀胱肿瘤电切术(TURBT)是治疗非肌层浸润性膀胱癌的主要手段,但该术式破坏肿瘤层次,病灶切除不彻底,若术后不及时采取进一步的防治措施,术后种植、转移风险高[1]。膀胱灌注化疗是降低膀胱癌术后复发风险的重要措施,对促进良性预后尤为关键,但不同药物作用机制不同,带来的整体效益也不尽相同[2-3]。吉西他滨注射液属嘧啶类抗肿瘤药物,主要通过抑制DNA 合成、癌细胞增殖,加速癌细胞凋亡[4]。本研究将吉西他滨用于患者TURBT 术后膀胱灌注,观察患者免疫功能及术后复发风险。
1 资料与方法
1.1 一般资料
选自瑞金市人民医院2018 年1 月至2021 年12月期间收治的60 例非肌层浸润性膀胱癌患者,按随机数字表法分为两组。对照组30 例,其中男性23 例,女性7 例;年龄(52.36±2.24)岁,年龄范围40~67 岁;肿瘤单发20 例,多发10 例;肿瘤长径<3 cm 10 例,≥3 cm 20 例;病理学分级:G1 7例,G2 15 例,G3 8 例;病灶位置:膀胱三角区19例,膀胱侧壁9 例,膀胱顶壁2 例。研究组30 例,其中男性24 例,女性6 例;年龄(52.39±2.27)岁,年龄范围40~70 岁;肿瘤单发21 例,多发9 例;肿瘤长径<3 cm 12 例,≥3 cm 18 例;病理学分级:G1 9 例,G2 15 例,G3 6 例;病灶位置:膀胱三角区19 例,膀胱侧壁9 例,膀胱顶壁2 例。两组上述基线资料对比(P>0.05)有可比性。本次研究内容均得到瑞金市人民医院医学伦理委员会审批。
1.2 纳排标准
纳入标准:非肌层浸润性膀胱癌符合《膀胱癌患者诊疗指南》[5]中内容,且经病理组织学确诊;均行TURBT;纳入对象或其近亲属均知情并签署知情同意书。排除标准:伴心肝肾等器质性病变;过敏体质;伴其他恶性肿瘤;伴严重血尿不能承受灌注治疗;合并精神疾患或正在服用抗精神病类药物。
1.3 方法
1.3.1 研究组 术后24 h 行注射用盐酸吉西他滨(LILLY FRANCE,注册证号HJ20160225,规格:1.0 g)灌注,吉西他滨1 000 mg+生理盐水50 mL,患者排尿后,无菌操作下将混合溶液经一次性导尿管注入膀胱,保持2 h 后排出,期间嘱患者30 min 更换体位一次,平卧、俯卧、左右侧卧,确保注射液与膀胱各壁接触。
1.3.2 对照组 术后24 h 行注射用盐酸表柔比星[辉瑞制药(无锡)有限公司,国药准字H20000497,规格:50 mg]膀胱灌注,表柔比星注射液40 mg+生理盐水50 mL,灌注时间、方式等均与研究组相同。
1.4 观察指标
(1)血清因子,采用酶联免疫吸附法检测治疗前、治疗结束时血清重组人Dickkopf 蛋白1(DKK1)、可溶性血管细胞黏附分子-1(sVCAM-1)、血管内皮因子(VEGF)。(2)免疫功能,间接酶联免疫吸附法及流式细胞术(美国BeckmaIl coulter 流式细胞仪,型号:Cytoflex S,BECKMAN COULTER)检测治疗前、治疗结束后淋巴细胞[CD3+、自然杀伤细胞(NK 细胞)、CD4+/CD8+]及免疫球蛋白(IgA、IgG、IgM)水平。(3)不良反应,对比两组患者治疗期间有无发生如下症状:尿路刺激征(主要表现为尿急、尿频、尿痛),肉眼血尿,尿道狭窄(主要表现为尿频、尿急、排尿时间延长、尿液分叉等)及肝肾功能损害(经临床实验室血常规相关检查评估)。(4)复发率,患者均完成8 个月随访,每2 个月进行一次膀胱镜检查,若镜下发现肿物,留取并送病理科检查,确认是否复发。随访截止时间2022 年8 月31 日。
1.5 统计学方法
2 结果
2.1 血清因子比较
治疗前,两组血清因子DKK1、sVCAM-1、VEGF表达对比,差异无统计学意义(P>0.05),治疗结束时,研究组血清DKK1、sVCAM-1、VEGF 表达低于对照组(P<0.05)。见表1。
表1 两组血清因子比较() ng/L
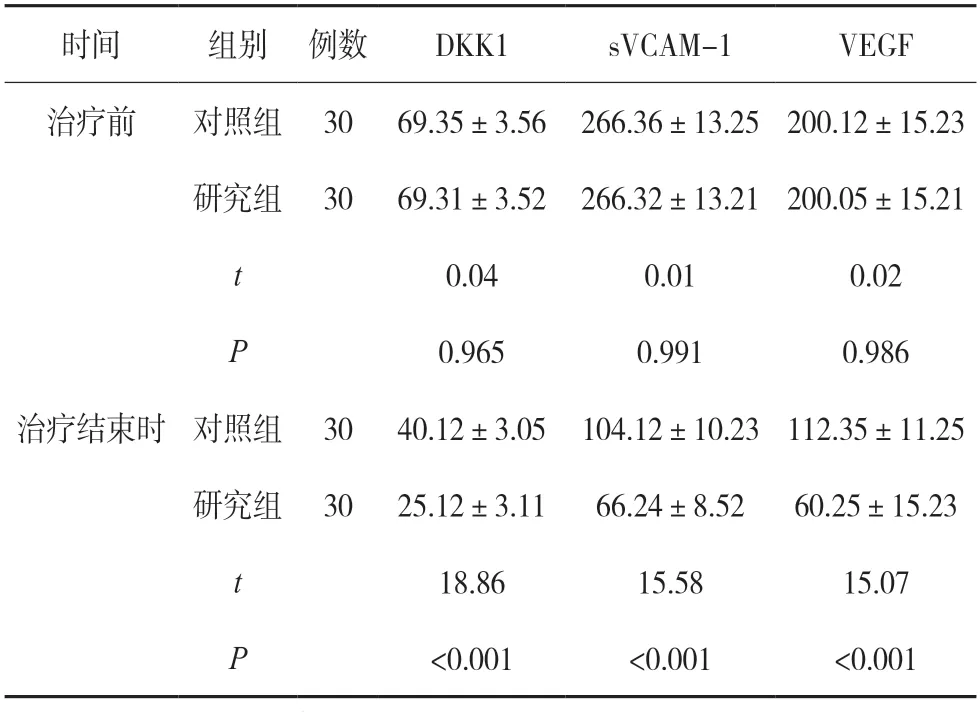
表1 两组血清因子比较() ng/L
2.2 免疫功能比较
治疗前,两组血清IgA、IgG、IgM、CD3+、CD8+、CD4+/CD8+表达对比(P>0.05),治疗结束时,研究组上述IgA、IgG、IgM、CD3+、CD4+/CD8+高于对照组,CD8+表达低于对照组(P<0.05)。见表2。
表2 两组免疫功能比较()

表2 两组免疫功能比较()
2.3 不良反应
两组患者不良反应总发生率对比,差异无统计学意义(P>0.05)。见表3。
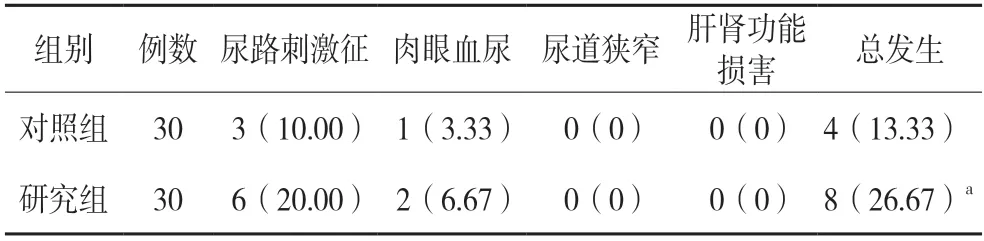
表3 两组不良反应比较[例(%)]
2.4 复发率比较
随访期间,研究组复发1例,复发率3.33%(1/30),对照组复发3 例,复发率10.00%(3/30),研究组复发率低于对照组,差异无统计学意义(χ2=0.27,P=0.605)。
3 讨论
TURBT 术可中断病灶细胞对机体的侵蚀,保护机体免疫功能,虽通过局部切除病灶可获取一定治疗效果,但术后仍存在复发风险,这可能与机体免疫力低下、病灶残留有关[6]。故术后联合有效的干预措施,对降低术后复发风险十分有必要。
恶病质、疾病进展、预后等与机体免疫状态密切相关,疾病原因导致机体长时间高耗能,癌细胞增殖、种植等导致免疫功能下降,癌细胞逃避免疫应答、监测,引发不良预后[7-10]。本研究结果显示,两组IgA、IgG、IgM、CD3+、CD4+/CD8+表达均升高,CD8+表达下降,且研究组上述IgA、IgG、IgM、CD3+、CD4+/CD8+高于对照组,CD8+表达低于对照组,提示患者术后给予吉西他滨膀胱灌注利于增强患者术后免疫功能。吉西他滨主要经抑制癌细胞DNA 合成,诱导并加速其凋亡,具体表现为:(1)降低脱氧胞苷激酶活性,促进吉西他滨向活性的三磷酸转化;(2)进入集体后的代谢物,抑制细胞DNA 合成并阻断细胞周期,继而抑制癌细胞增殖,诱导凋亡进程;(3)分子量大,无法透过膀胱黏膜,无法吸收至全身系统,不良反应小;(4)脂溶性好,利于渗透癌细胞,利于短时间内达到稳态血药浓度,加速癌细胞凋亡[11-13]。DKK1 与VEGF均是肿瘤标志物,高表达提示新生血管形成,利于促进癌细胞增殖;sVCAM-1 具备黏附因子活性,利于调节细胞之间作用,上述指标表达情况直接反应术后癌病灶残留及药物歼灭癌病灶情况[14-15]。本研究结果还显示,治疗结束时,研究组血清DKK1、sVCAM-1、VEGF 表达低于对照组,提示术后联合吉西他滨膀胱灌注,利于抑制癌细胞活性、复制。原因可能与膀胱灌注利于药物与病灶直接接触,局部药物浓度高,抑制残留癌细胞增殖,加速凋亡有关[15]。两组患者不良反应总发生率对比,差异无统计学意义,提示将吉西他滨注射液膀胱灌注用于非肌层浸润性膀胱癌患者TURBT 术后治疗中,安全可靠,可在临床相关患者治疗中开展。两组复发率对比差异无统计学意义,原因可能与研究纳入样本少、术后随访时间短有关,希望未来开展大样本、延长随访周期的相关研究。
综上所述,非肌层浸润性膀胱癌患者TURBT 术后联合吉西他滨膀胱灌注对增强机体免疫功能,降低复发风险均有一定成效,且安全性理想,建议在临床非肌层浸润性膀胱癌患者术后联合治疗中开展。
