塞来昔布在EGFR-TKI 耐药性晚期NSCLC 中对PD-1 抑制剂的免疫增敏作用
2023-06-17胡晟钊陈颖犁黄绍芳黄仕鹏
胡晟钊,陈颖犁,黄绍芳,黄仕鹏
1.南昌大学第一附属医院,江西 南昌 330006;2.江西省儿童医院,江西 南昌 330006
非小细胞肺癌(NSCLC)严重影响人类生命健康,大部分患者在得到明确诊断时已处于中晚期,无法进行手术治疗[1]。一项调查[2-3]显示,50%左右的晚期NSCLC 患者出现表皮细胞生长因子突变(EGFR),临床针对这类患者通常采用EGFR-酪氨酸激酶抑制剂(EGFR-TKI)进行治疗,取得了一定的效果,患者生存率得到明显提升。然而经EGFRTKIs 治疗后的晚期NSCLC 患者大都出现耐药,对患者预后造成不良影响[4]。故探究可有效改善NSCLC晚期患者EGFR-TKI 耐药后的新治疗策略尤为重要。程序性死亡分子-1(PD-1)是治疗NSCLC 患者的五大常用手段之一,然而其对发生EGFR 突变阳性的晚期NSCLC 患者基本没有效果[5]。有研究[6]证实,塞来昔布是一种安全性较高的“增敏剂”,其可有效增强PD-1 抑制剂联合化疗的临床疗效。基于上述背景,本研究旨在探究塞来昔布在EGFR-TKI 耐药性晚期NSCLC 中对PD-1 抑制剂的免疫增敏作用。
1 资料与方法
1.1 一般资料
选择2020 年12 月至2022 年1 月在南昌大学第一附属医院呼吸科进行治疗的晚期NSCLC 患者82 例,纳入标准:(1)年龄18~70 岁;(2)与《中国临床肿瘤学会原发性肺癌诊疗指南(2018 年版)》[7]中诊断标准一致;(3)经CT 或MRI 等影像学检查后发现可评估的病灶;(4)既往通过EGFRTKI 治疗后出现耐药,且存在EGFR 突变阳性及T790M 突变阴性;(5)患者或近亲属均签订知情同意书;(6)经南昌大学第一附属医院医学伦理委员会审批通过。排除标准:(1)中医证型与体力状态(ECOG)评分为3~5 分;(2)有高血压、冠心病、糖尿病者;(3)近3 个月内参与其他药物实验者;(4)预计生存期不足3 个月者;(5)对塞来昔布等相关药物过敏者。按随机数字表法将82 例NSCLC 患者分为对照组(n=41)、治疗组(n=41),其中对照组男性21 例,女性20 例,年龄(56.78±6.24)岁;治疗组男性22 例,女性19 例,年龄(57.78±7.45)岁;两组一般资料相比差异无统计学意义(P>0.05)。
1.2 方法
对照组采用TPC 治疗方案,第1 天予以特瑞普利单抗注射液240 mg 静脉滴注,注射用培美曲塞二钠500 mg/m2静脉滴注,卡铂注射液AUC=4-5,静脉滴注。21 d 为1 周期。治疗组在对照组基础上采用塞来昔布胶囊(Pfizer Pharmaceuticals LLC,国药准字J20140072,规格:200 mg)200 mg/次,每天2 次,21 d 为1 周期。
1.3 观察指标
1.3.1临床疗效根据《实体瘤疗效评价标准》[8]对两组疗效进行评价,包括完全缓解(CR,病灶完全消失4 周及以上);部分缓解(PR,病灶体积较基线缩小>50%,时间≥4 周);疾病稳定(SD,病灶体积较基线缩小25%~50%,时间≥4 周);疾病进展(PD,不符合以上标准);CR 和PR 患者所占比例定义为客观有效率。
1.3.2EGFR 突变检测取两组淋巴结活检组织,并送至病理科进行EGFR 及T790M 突变检测。
1.3.3环氧化酶2(COX-2)蛋白检测取两组淋巴结活检组织采用免疫组化法检测其中COX-2 蛋白表达,以胞浆、胞膜出现棕黄色颗粒为阳性。
1.3.4毒副作用参照药物毒副反应判定标准(NCICTC)(2.0 版)分度标准[9],对治疗过程中出现的毒副作用进行分级,并比较两组严重毒副作用发生率。
1.4 统计学方法
数据分析采用SPSS 21.0,符合正态分布及方差齐性的计量资料采用表示,两组间比较以独立样本t检验;计数资料以例(%)表示,两组间比较以χ2检验;P<0.05 为差异有统计学意义。
2 结果
2.1 两组临床疗效分析
治疗组PR 例数21 例,治疗有效率为51.22%,对照组PR 例数8 例,治疗有效率19.51%,两组相比差异有统计学意义(P<0.05)。见表1。
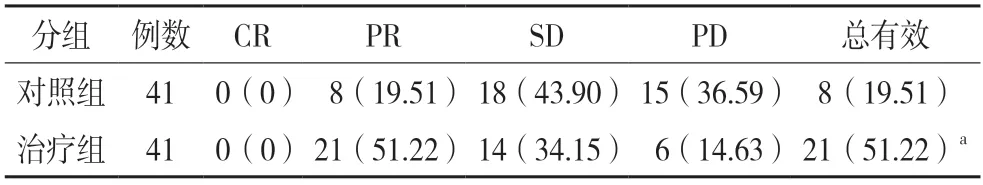
表1 两组临床疗效对比[例(%)]
2.2 两组表皮生长因子受体-T790M(EGFR-T790M)突变情况分析
治疗组EGFR-T790M 突变率为19.51%(8/41),对照组EGFR-T790M 突变率为65.85%(27/41),两组相比差异有统计学意义(P<0.05)。见表2。
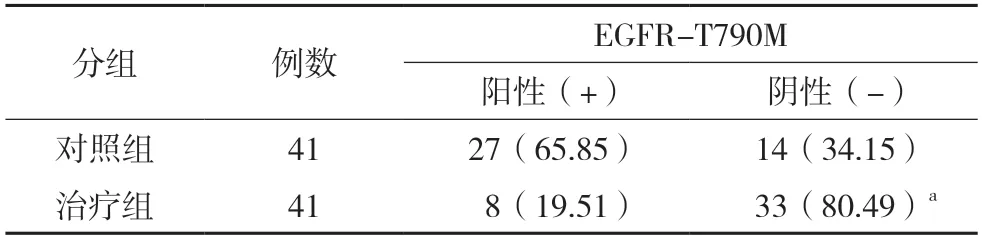
表2 两组EGFR-T790M突变率对比[例(%)]
2.3 两组COX-2 蛋白表达比较
治疗组COX-2 阳性表达率为24.39%(10/41),对照组COX-2 阳性表达率为60.98%(25/41),两组相比差异有统计学意义(P<0.05)。见表3。

表3 两组COX-2蛋白表达比较[例(%)]
2.4 两组毒副作用发生率比较
治疗组毒副作用发生率为24.39%(10/41),对照组毒副作用发生率为34.15%(14/41),两组相比差异无统计学意义(P>0.05)。见表4。
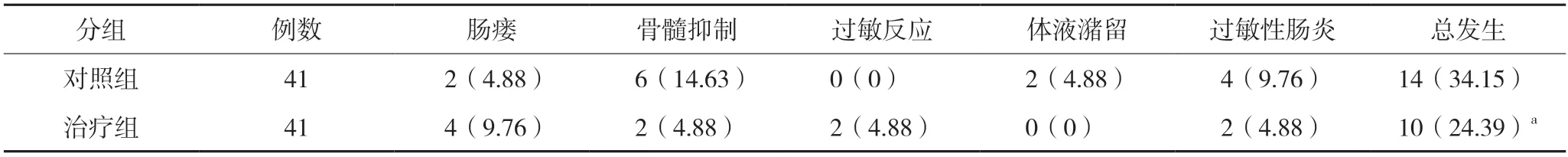
表4 两组毒副作用发生率比较[例(%)]
3 讨论
报道[10-12]显示,将EGFR-TKI 作为一线治疗方案的NSCLC 患者客观缓解率及中位无进展生存期得到明显提升,其生活质量亦随之改善。然而患者出现耐药进而引发疾病进展,且目前尚未形成统一有效的后续治疗策略[13]。PD-1 抑制剂是一种免疫检测点抑制剂,其在治疗NSCLC 方面具有重要作用,然而针对EGFR-TKI 耐药的晚期NSCLC 患者,PD-1 联合EGFR-TKI 治疗的方案效果极差,被称为免疫治疗的“冷肿瘤”[14]。故探究一种可有效增强PD-1 联合EGFR-TKI 临床疗效的方法尤为重要。
塞来昔布是一种选择性COX-2 抑制剂,其可阻断肿瘤血管生成并诱导细胞周期发生变化,最终增强放疗敏感性[15]。王阳等[16]研究显示,塞来昔布有利于病情转归,其在减少降低病灶大小并提高患者生活质量方面具有重要价值。何慧娟、胡伟[17]报道证实,塞来昔布可作为辅助治疗手段应用于其他实体瘤治疗,在提高放射线对肿瘤病灶细胞生长抑制方面具有重要作用。Chen 等[18]通过COX-2 抑制剂塞来昔布治疗胰腺癌患者发现,该药物可有效增强吉西他滨对胰腺癌的化疗敏感性,可发挥更好的抗癌作用。Choe 等[19]研究证实,塞来昔布联合吉非替尼治疗头颈部鳞癌患者,可明显提高头颈部鳞癌对多西他赛的化疗敏感性。除此之外,有学者[20]表明,塞来昔布联合PD-1单克隆抗体治疗黑色素瘤患者,可发挥协同抗肿瘤作用,说明COX-2 抑制剂塞来昔布可作为肿瘤患者免疫治疗的有用辅助剂。本研究结果显示,经塞来昔布治疗后,治疗组患者总有效率明显优于对照组,说明塞来昔布可有效提高NSCLC 患者临床疗效。除此之外我们对两组淋巴结活检组织中EGFR-T790M 突变状态进行检测,发现治疗组EGFR-T790M 突变率明显低于对照组,提示塞来昔布可在一定程度上改善NSCLC 晚期患者EGFRT790M 突变状态。
肺腺癌细胞中COX-2 表达明显上调,可导致细胞凋亡受阻并诱导肿瘤血管生成,同时亦可抑制机体免疫并促进肿瘤侵袭及转移,最终诱导肿瘤进展[20]。研究[21]显示,通过COX-2 抑制剂塞来昔布联合PD-1 治疗乳腺癌荷瘤小鼠可明显提高肿瘤抑制率及生存率。我们对两组淋巴结活检组织中COX 表达情况进行检测,发现治疗组COX-2 阳性表达率明显低于对照组,以上研究结果证实,塞来昔布可作为“增敏剂”提高NSCLC 晚期患者PD-1抑制剂联合化疗的临床疗效。
塞来昔布可明显提高NSCLC 患者出现化疗敏感性,增强其临床疗效,且可改善EGFR-T790M突变状态,为改善化疗方案,减少化疗药物毒性提供理论依据,并为临床治疗晚期NSCLC 患者提供一种新的思路。然而本研究样本量较少,研究周期较短,且研究对象受药物敏感性及耐受性影响较大,结果可能存在一定的偏倚,故在日后的研究中我们将进一步扩大样本量展开深入研究。
