红花高效液相色谱指纹图谱分析及含量测定
2023-06-17李强程艳芹苗青刘旭
李强 程艳芹 苗青 刘旭
红花为菊科植物红花(Carthamus tinctorious L.)的干燥管状花,又名次红、红蓝花、红花菜、红花草等,味辛性温,归心、肝经,具有活血通经、散瘀止痛的功效。中药红花已有4 000 多年的历史,分布较广,在很多国家均有栽培,原产于埃及,在我国也多有栽培,主产于新疆、河南、湖南、四川、云南等地[1,2]。红花是现代中药制剂的常用药材,在中医药领域应用广泛,在临床上治疗冠心病、心绞痛效果较好,其有增强心肌收缩、轻度兴奋心脏、降低冠脉阻力、增加冠脉流量的作用[3]。红花中的羟基红花黄色素A 具有提高动物缺氧的耐受力,并能使冠脉扩张,增加冠脉流量,对血管平滑肌细胞的增殖具有抑制作用。目前,红花中已分离鉴定的化学成分有60 多种,主要分为黄酮类、木脂素类、多炔类等,成分十分复杂,其中羟基红花黄色素A 是红花的主要有效成分[4,5]。文献资料中对红花药材的相关研究多以标志性成分羟基红花黄色素A 单一指标为考察对象,不足以全面地反映红花药材的质量。因此,建立有效的红花药材质量评价方法,确保红花药材质量稳定,直接关系到红花相关药品和临床处方的疗效。本实验采用高效液相色谱(HPLC)方法,建立红花药材的指纹图谱,同时对羟基红花黄色素A、山奈酚、槲皮素3 种成分的含量进行研究分析,为进一步考察不同产地红花药材的质量状况提供图谱信息,为其质量评价提供新的参考和借鉴。
1 材料与方法
1.1 药品和试剂甲醇(色谱纯,天津市四友精细化学品有限公司,批号:Q/BSYZ01-2017);磷酸(分析纯,莱阳市康德化工有限公司,批号:201901);灭菌注射用水(山东齐都药业有限公司,批号:2A20112009);羟基红花黄色素A、槲皮素、山奈酚(中国食品药品检定研究院,批号依次为:BZP0382、BZP0083、BZP0129);红花药材来源见表1。

表1 红花药材来源
1.2 仪器和设备液相色谱仪LC-2030 型(日本岛津制作所);超声波仪SY2200-SB2200 型(上海必能信超声有限公司);电子天平YP202N 型(上海精密科学仪器有限公司);电子天平DV215CD 型(美国奥豪斯公司);循环水真空泵SHZ-DⅢ型(巩义市予华仪器有限责任公司);电热恒温水箱HH-W21-420 型(余姚市亚星仪器仪表有限公司)。
1.3 色谱条件色谱柱:Inertsil ODS-SP(4.6mm×150 mm,5μm);通过对比流动相[甲醇-0.4%磷酸溶液、乙腈-0.4%磷酸溶液、甲醇-水(每100ml 水中含1ml pH=6.0 的醋酸-醋酸铵缓冲溶液)]、检测波长(全波长扫描)及柱温(25℃、30℃、35℃)等色谱条件,经过图谱分析后筛选出流动相:甲醇-0.4%磷酸溶液,检测波长:254nm,进样量:10μl;柱温:30℃为最优检测条件,所得色谱峰分离度良好,无拖尾现象。流动相梯度洗脱程序[6]见表2。

表2 流动相梯度洗脱程序
1.4 供试品溶液的制备分别考察2 种提取方法(超声波提取和加热回流提取)、3 种提取溶剂(纯甲醇、75%甲醇、60%甲醇)、超声波提取时间(20min、40min、60min)对羟基红花黄色素A、槲皮素、山奈酚3 种指标成分含量测定的影响,结果表明以75%甲醇为提取溶剂超声波提取40min,所得的有效成分含量较高且操作简便。按照以上方法精密称量红花药材(编号S1)粉末0.4g,置于具塞锥形瓶中,用移液管精密称定75%的甲醇50ml 加入,超声提取(功率300W,频率50kHz)40min,放冷,再称定质量,用75%甲醇补足减失的质量,摇匀,滤过,再用0.45μm 的有机微孔滤膜滤过,取续滤液,即得。
1.5 混合对照品溶液的制备精密称取羟基红花黄色素A、槲皮素和山奈酚对照品分别为17.8mg、1.9mg、1.8mg,置同一100ml 容量瓶中,加甲醇,超声(功率:300W,频率:50kHz)溶解,放冷,定容,制成每1ml 含羟基红花黄色素A 0.178mg、槲皮素0.019mg、山奈酚0.018mg 的混合对照品溶液,备用。
1.6 单个对照品溶液的制备精密称取羟基红花黄色素A、槲皮素、山奈酚对照品药物适量,分别于不同的10ml 容量瓶中加适量甲醇摇匀,超声溶解,放冷,甲醇定容,得到羟基红花黄色素A、槲皮素、山奈酚质量浓度分别为1.484mg/ml、0.412mg/ml、0.432mg/ml 的单个对照品溶液,备用。
1.7 指纹图谱的建立
1.7.1 精密度试验 取相同的红花供试品溶液(编号S1),按照规定的色谱条件,连续进样6 次并记录所得色谱图,以羟基红花黄色素A 峰为参照样,计算各共有峰相对峰面积和相对保留时间,如果所得RSD 值均小于2%,则表明仪器精密度良好。
1.7.2 稳定性试验 取相同的红花供试品溶液(编号S1),按照规定的色谱条件,在0、3、6、9、12、24h 分别进样分析并记录所得色谱图,以羟基红花黄色素A 峰为参照样,计算各共有峰相对峰面积和相对保留时间,如果所得RSD 值均小于2%,则表明红花供试品溶液在24h 内稳定性良好。
1.7.3 重复性试验 取相同批次的红花样品6 份(编号S1),分别配置供试品溶液后按照规定的色谱条件进样分析并记录所得色谱图,以羟基红花黄色素A 峰为参照样,计算各共有峰相对峰面积和相对保留时间,如果所得RSD 值均小于2%,则表明重复性良好。
1.7.4 指纹图谱的测定及相似度分析[7]取6 批不同产地的红花样品按照1.4 方法制成供试品溶液,按照规定的色谱条件进样分析并记录65min 色谱图。取混合对照品溶液,按照规定的色谱条件进样分析并记录65min 色谱图。分别取3 种对照品溶液,按照规定的色谱条件进样分析并记录65min 色谱图。对6 批不同产地红花药材指纹图谱利用“中国色谱指纹图谱相似度评价系统(2012 版)”进行相似度分析。
1.8 含量测定
1.8.1 系统适用性试验 取红花供试品和混合对照品溶液,按照规定的色谱条件进样分析并记录65min 色谱图。
1.8.2 线性关系考察 取相同的红花混合对照品溶液,分别精密吸取10、15、20、25、30、35μl 进样分析并记录65min 色谱图,测出羟基红花黄色素A、槲皮素、山奈酚的峰面积,以对照品溶液进样量作自变量X,以生物碱相应峰面积作因变量Y 做线性回归分析。
1.8.3 加样回收率试验 精密称取同一批红花样品(编号S3)9 份,各0.5g,置于平底烧瓶中,按3 个浓度梯度分别加入羟基红花黄色素A、槲皮素、山奈酚对照品,测定加样回收率。
1.8.4 样品测定 取红花样品制成的供试品溶液,按照规定的色谱条件进样分析并记录65min 色谱图,计算样品中羟基红花黄色素A、槲皮素、山奈酚含量。
2 结果
2.1 指纹图谱的测定结果对比指纹图谱,除溶剂峰外共确定10 个共有峰,经过进样剖析单个对照品后获得的色谱图,确定其中3 个色谱峰,分别为羟基红花黄色素A、槲皮素、山奈酚。见图1、2。6批不同红花药材样品中共有峰相对保留时间及峰面积见表3、4。

图1 红花药材指纹图谱

图2 红花混合对照品

表3 6 批红花药材样品中共有峰相对保留时间

表4 6 批红花药材样品中共有峰相对峰面积
2.2 指纹图谱相似度分析6 批红花药材与对照图谱(SR)相似度分别为0.976、0.922、0.953、0.981、0.943、0.992。提示6 种不同产地的红花药品指纹图谱差异较小。见图3。
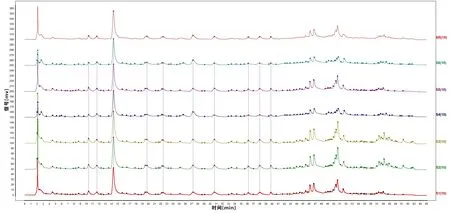
图3 6 批红花药材指纹图谱
2.3 各试验结果及样品测定系统适用性试验分析结果表明,3 种成分的分离度均大于1.5,提示适用性较好。线性关系考察结果显示对照品溶液进样量与以生物碱相应峰面积均具有良好的线性关系。精密度试验测出3 种成分的峰面积RSD 值均小于2%,表明仪器精密度良好。稳定性试验测出3 种成分的峰面积所得RSD 值均小于2%,表明红花供试品溶液在24h 内稳定性良好。重复性试验测出3 种成分的峰面积所得RSD 值均小于2%,表明重复性良好。通过线性关系考察发现,羟基红花黄色素A、槲皮素、山奈酚三者均具有良好的线性关系,见表5。加样回收率试验结果显示,羟基红花黄色素A、槲皮素、山奈酚的平均加样回收率分别为100.6%、99.5%、101.2%,其RSD 分别为0.8%、1.9%、1.2%,见表6。样品测定羟基红花黄色素A、槲皮素、山奈酚的含量稳定见表7。

表5 3 种有效成分线性关系

表6 3 种成分加样回收率

表7 6 批红花药材3 种有效成分含量(mg/g,n=6)
3 讨论
3.1 指纹图谱方法学验证及相似度分析本实验建立了红花药材HPLC 指纹图谱,并考察比较了6 个不同产地红花药材的指纹图谱相似度。本研究色谱条件及样品提取条件优化后经过方法学验证,该HPLC 方法精密度高、重复性好、稳定准确、特征突出、可行性好。
本实验所采用的红花来自我国河南、四川、新疆等地,实验结果显示,指纹图谱共成功匹配10 个共有峰,共有峰基本特征均一致,为红花药材的质量控制提供了相对全面的参考信息,对红花药材质量标准的制定具有一定的借鉴意义[8]。指纹图谱比较后发现,6 批不同产地的红花药材指纹图谱相似度基本一致,经单个对照品对比共确定3 种有效成分,其中羟基红花黄色素A 为红花的标志性成分且含量较高,因此选为指纹图谱的参照峰,研究表明羟基红花黄色素A 具有抗缺血、抗癌、降血糖、改善认知等多重功效[9]。槲皮素与山奈酚结构相似,同属黄酮类化合物,构效关系研究表明这两种化合物具有较好地心血管保护作用和抗癌活性[10],这两种有效成分与标志性成分羟基红花黄色素A 一起更能充分体现红花药材的质量。
3.2 展望红花药材成分复杂,产地较多,不同产地之间地理位置相距较远,因此药材含量不太稳定,难以检测。故本实验仅选用了红花药材中3 种相对稳定、含量较高的指标成分进行质量控制。如果条件允许,未来将进一步研究更具有代表性的不同产地不同批次的红花药材,采用更多的有效成分作为评判指标,使该研究能更加全面客观地反映不同产地红花药材之间的质量差异,为临床合理使用红花药材提供参考。
