射血分数保留的心力衰竭合并心房颤动患者临床特征及再入院危险因素
2023-06-10杨晓月李少杰陈淑霞
王 震, 杨晓月, 李少杰, 王 贤, 陈淑霞, 谷 剑
(1. 河北医科大学 研究生院,河北 石家庄 050011;2. 河北北方学院 研究生院,河北 张家口 075000;3. 河北省人民医院 心血管内三科,河北 石家庄 050057)
慢性心力衰竭(chronic heart failure,CHF)是一组由心脏结构或功能异常引起的临床综合征。心力衰竭(heart failure, HF)合并心房颤动(atrial fibrillation,AF)在临床中十分常见,并与HF病死率的增加密切相关,两者相互影响且具有较多的共同危险因素[1]。弗雷明汉心脏研究指出,在美国HF患者AF的年发生率约为54%,AF患者HF的年发生率约为33%[2]。约有一半的HF是射血分数保留的心力衰竭(ejection fraction preserved heart failure,HFpEF),且HFpEF的发病率有明显增加的趋势[3]。研究发现,随着HF患者年龄的增加和心脏功能的持续恶化,AF的发生率也逐渐增加[4]。目前在全球范围内HFpEF患者的AF发病率为15%~41%[5]。AF在HFpEF患者中比在射血分数减少的HF患者中更为常见[1]。目前关于射血分数减少的HF合并AF的研究较多,关于HFpEF合并AF的研究相对较少。本研究通过探讨HFpEF合并AF患者的临床特征及再入院危险因素,旨在为改善患者预后提供依据。
1 资料与方法
1.1病例选择 本研究为单中心回顾性研究,纳入2018年6月至2020年5月在河北省人民医院心血管内三科住院治疗的HFpEF患者459例。依据住院期间患者是否存在AF分为AF组(n=242)和窦性心律(sinus rhythm,SR)组(n=217)。纳入标准:①年龄≥18岁,病程>6个月;②心功能分级Ⅱ~Ⅳ级;存在HF的症状和体征;③符合《2021年ESC急性和慢性心力衰竭的诊断和治疗指南》中HFpEF的诊断标准[6];④利钠肽水平升高:SR:B型利钠肽(B-type natriuretic peptide,BNP)≥35 ng/L或氨基末端脑钠肽前体(N-terminal pro-brain natriuretic peptide,NT-proBNP)≥125 ng/L;AF:BNP≥105 ng/L或NT-proBNP≥365 ng/L;⑤引起HF的其他心脏结构和功能改变的客观证据;⑥在不确定的情况下,为了证实诊断,可能需要进行负荷试验和测定左心室充盈压是否升高;⑦病历资料完善者。排除标准:①非HFpEF患者;②院内死亡及自动出院的患者;③存在先天性心脏病的患者和妊娠期或哺乳期的妇女;④存在精神或认知障碍和(或)依从性较差者。本研究经医学伦理委员会审批通过,所有患者均知情同意并签署知情同意书。
1.2观察指标 通过河北省人民医院电子病历系统搜集患者临床资料。一般临床资料包括年龄,性别,心率,入院血压,体重指数(body mass index,BMI),纽约心脏病协会(New York Heart Association lassification ,NYHA)分级,吸烟史,2年内住院次数。合并症:是否存在高脂血症、高血压、冠状动脉疾病、心脏瓣膜病、缺血性心肌病、脑血管病、慢性阻塞性肺疾病、2型糖尿病、慢性肾病、高尿酸血症、结缔组织病、躯体化障碍、甲状腺功能疾病、颈动脉粥样硬化。实验室观察指标包括血红蛋白、肾小球滤过率(glomerular filtration rate,GFR)、NT-proBNP。心脏彩色超声检查观察指标包括左室射血分数(left ventricular ejection fraction,LVEF)、左心室收缩末内径(left ventricular end systolic diameter,LVESD)、左心室舒张末内径(left ventricular end diastolic diameter,LVEDD)、肺动脉收缩压(pulmonary artery systolic pressure,PASP)、左房内径(left atrial internal diameter,LA)、右房内径(right atrial internal diameter,RA)、右室内径(right interior diameter,RV)。治疗相关资料包括住院期间是否使用脑啡肽酶抑制剂(enkephalinase inhibitors,ARNI)、重组人脑利钠肽(新活素);是否规律服用药物: β受体阻滞剂、血管紧张素转换酶抑制剂(angiotensin-converting-enzyme inhibitors,ACEI)/ 血管紧张素Ⅱ 1型受体拮抗剂(angiotensin Ⅱ receptor type 1,ARB)、袢利尿剂、钙离子拮抗剂、醛固酮受体拮抗剂、抗血小板药、抗凝药、他汀类、洋地黄类等药物。

2 结 果
2.1两组临床资料比较
2.1.1一般资料 两组性别、舒张压、入院心率、NYHA分级差异无统计学意义(P>0.05)。与SR组相比,AF组年龄较大、吸烟史比例较小、BMI较小、收缩压较低,差异均有统计学意义(P<0.05)。见表1。
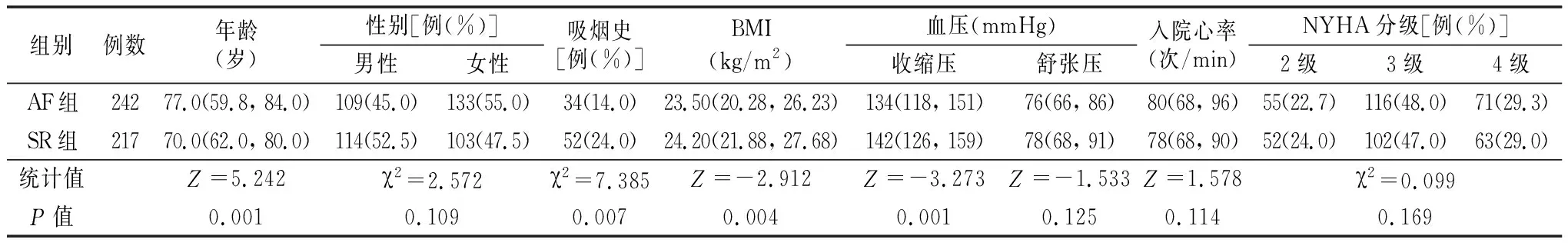
表1 两组一般资料比较
2.1.2合并症 两组合并高血压、冠状动脉疾病、脑血管病、慢性阻塞性肺疾病、2型糖尿病、慢性肾病、高尿酸血症、结缔组织病、甲状腺功能疾病、颈动脉粥样硬化比例差异均无统计学意义(P>0.05)。与SR组相比,AF组合并高脂血症、缺血性心肌病比例较小,合并躯体化障碍、心脏瓣膜病比例较高,差异均有统计学意义(P<0.05)。见表2。
2.1.3实验室资料和心脏彩色超声检查指标 两组LVEF、血红蛋白、GFR差异均无统计学意义(P>0.05)。与SR组相比,AF组LVEDD较小,LVESD、PASP、NT-proBNP、LA、RA、RV较高,差异均有统计学意义(P<0.05)。见表3。
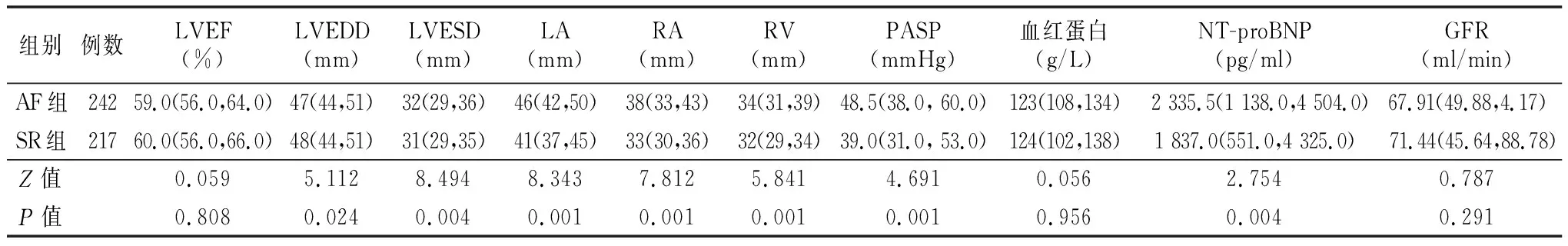
表3 两组实验室资料和心脏彩色超声指标比较[M( Q1,Q3) ]
2.1.4治疗相关资料 两组是否使用新活素、β受体阻滞剂、ACEI/ARB、醛固酮受体拮抗剂、他汀类、利尿剂药物差异均无统计学意义。与SR组相比,AF组使用ARNI、钙离子拮抗剂、抗血小板药比例较小,使用抗凝药、洋地黄类药物比例较高,差异均有统计学意义(P<0.05)。见表4。
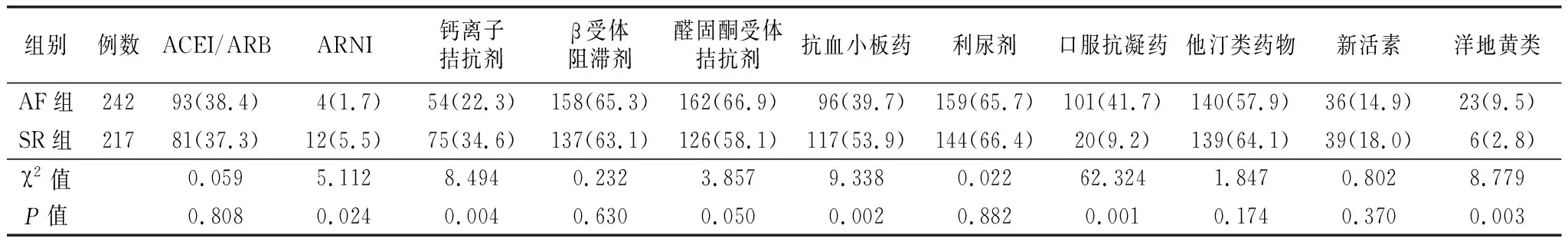
表4 两组治疗相关资料比较[例(%)]
2.2AF组再入院危险因素分析 依据两组2年内住院次数,把AF组患者分为≥2次住院组(n=97)和<2次住院组(n=145)。
2.2.1一般资料 两亚组年龄、性别、吸烟史比例、BMI、舒张压、入院心率、NYHA分级差异均无统计学意义(P>0.05)。与<2次住院组相比,≥2次住院组收缩压较低,差异有统计学意义(P<0.05)。见表5。
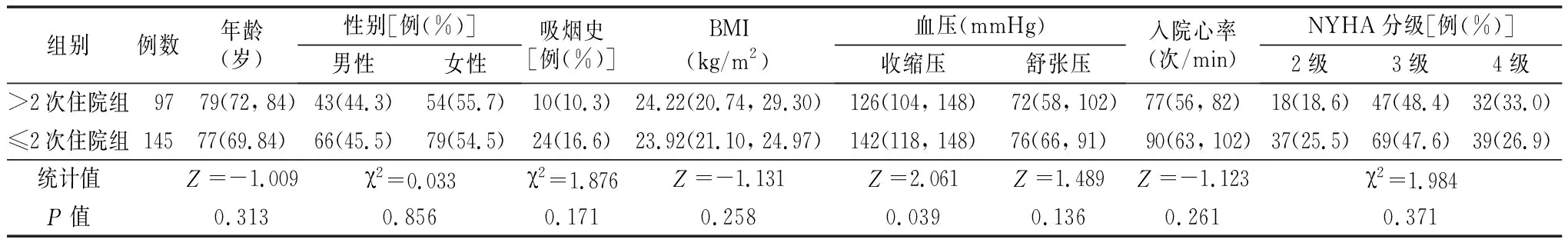
表5 两亚组一般资料比较
2.2.2合并症 两亚组合并高血压、冠脉疾病、脑血管病、缺血性心肌病、慢性阻塞性肺疾病、慢性肾病、结缔组织病、甲状腺功能亢进症、心脏瓣膜病比例差异无统计学意义(P>0.05)。与<2次住院组相比,≥2次住院组合并高脂血症、躯体化障碍、甲状腺功能减退症、2型糖尿病、高尿酸血症比例较大,合并颈动脉粥样硬化比例较大,差异均有统计学意义(P<0.05)。见表6。
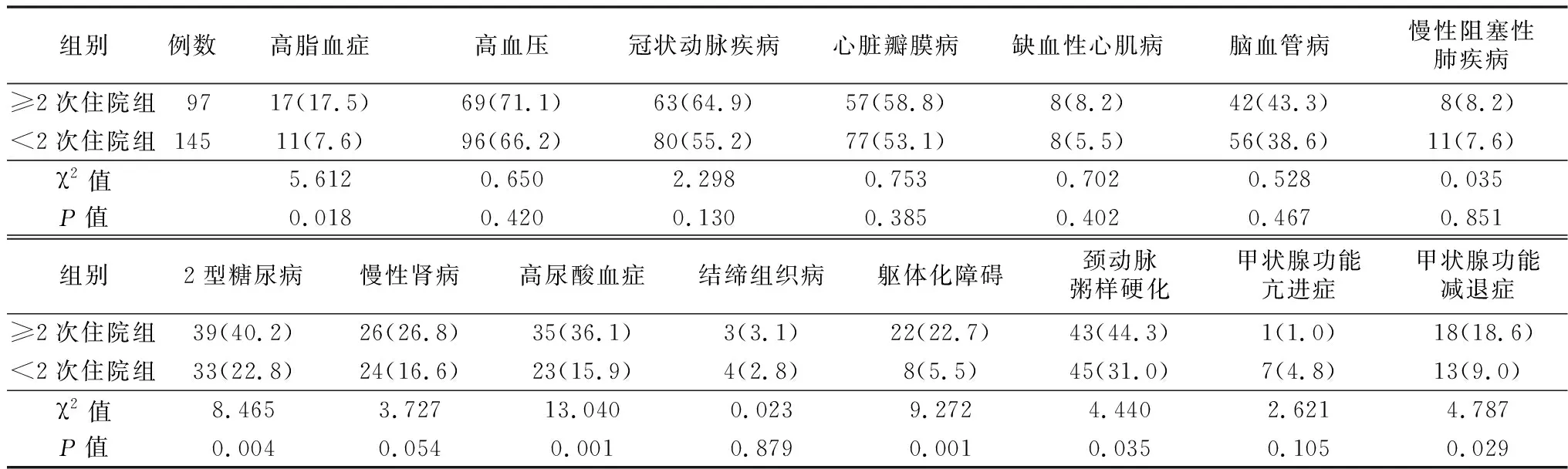
表6 两亚组合并症比较[例(%)]
2.2.3实验室和心脏彩色超声检查 两亚组NT-proBNP、LVEF、LA、RA、RV、GFR、血红蛋白、LVEDD、LVESD、PASP差异均无统计学意义(P>0.05)。见表7。
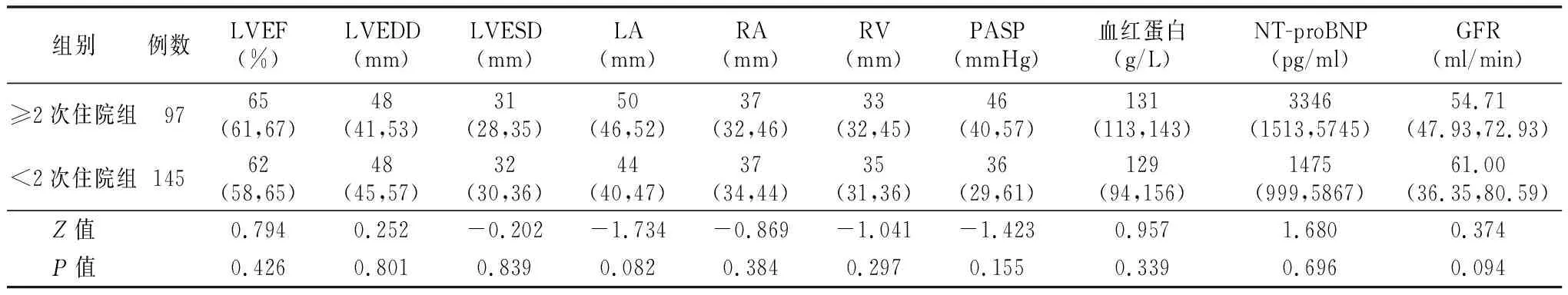
表7 两亚组实验室资料和心脏彩色超声指标比较[M(P25, P75)]
2.2.4治疗相关资料 两亚组是否使用新活素、ARNI、钙离子拮抗剂、ACEI/ARB、袢利尿剂、醛固酮受体拮抗剂、抗血小板药、抗凝药、他汀类、洋地黄类差异均无统计学意义(P>0.05)。与<2次住院组相比,≥2次住院组使用β受体阻滞剂比例较低,差异有统计学意义(P<0.05)。见表8。
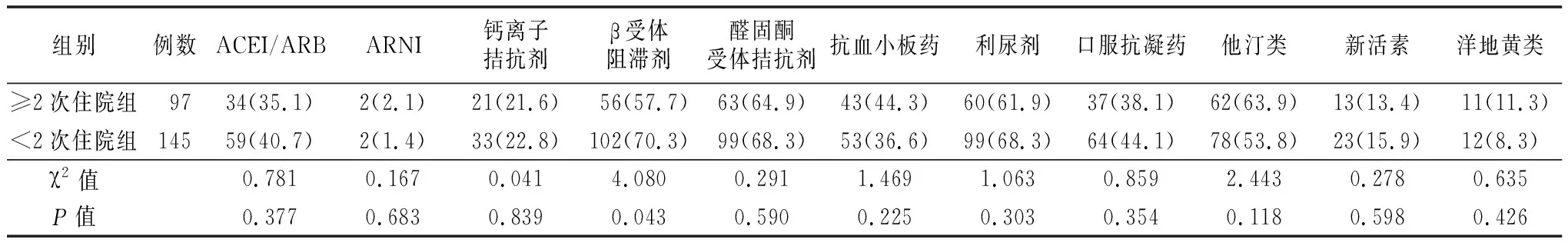
表8 两亚组治疗相关资料比较[例(%)]
2.3Logistic回归分析 将单因素分析中差异有统计学意义的因素进行多因素Logistic回归分析,因变量赋值:住院次数<2次=0,住院次数≥2次=1;自变量赋值:是否合并高脂血症、躯体化障碍、颈动脉粥样硬化、甲状腺功能减退症、2型糖尿病、高尿酸血症,是=1,否=0;使用β受体阻滞剂=1,无=0。结果提示:合并躯体化障碍、2型糖尿病、高尿酸血症是HFpEF合并AF患者再入院的独立危险因素;使用β受体阻滞剂是HFpEF合并AF患者再入院的独立保护因素(均P<0.05)。见表9。
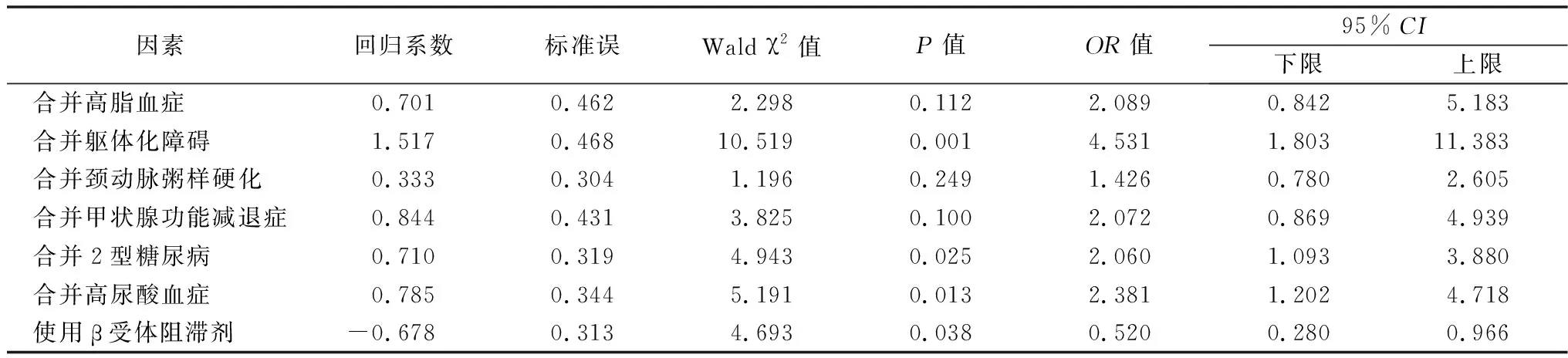
表9 HFpEF合并AF患者再入院的二元多因素Logistic回归分析
3 讨 论
3.1HFpEF合并AF的流行病学和发病机制 HFpEF合并AF有较广泛的流行病学特征。在不同研究中,HFpEF患者AF的患病率有所不同[5]。Eapen等[7]研究显示,美国住院HFpEF患者AF的患病率为48%。PARAGON-HF研究显示,美国HFpEF患者合并AF的患病率为65%[8]。本研究中HFpEF患者AF的患病率为53%,考虑不同研究中HFpEF患者AF患病率的差异可能与人群、地区的差异有关,但总体上AF在HFpEF患者中是常见的[9]。
目前研究表明,HFpEF患者合并AF与进行性左心房重构、充盈压升高和临床风险密切相关,且这些因素可能是HFpEF进展的标志[10]。HFpEF引起AF的最常见的机制是左心房结构纤维化和钠-钙交换通道的表达和功能改变[11]。同时,心房纤维化区域的间隙连接分布异常和细胞间的耦合丧失也会导致电重塑、心房折返性增加和AF的发生[12]。此外,有研究发现野生型转甲状腺素衍生的淀粉样变和心房淀粉样变在HFpEF合并AF的机制中发挥重要作用[13]。有研究证实,AF与HFpEF患者NT-proBNP升高和左心房重构独立相关[14]。本研究发现AF组LA、NT-proBNP高于SR组,与上述研究结果基本一致。
3.2HFpEF合并AF的临床特征 HFpEF合并AF患者和HFpEF不合并AF患者的临床特征不同。与SR组比较,AF组年龄较大、LA、RA、RV、PASP均较高,且在住院期间口服抗凝药、洋地黄类药物比例高。而SR组有吸烟史的占比更高,合并高脂血症、缺血性心肌病的占比更多。与Özlek等[15]研究结果基本一致。但本研究发现HFpEF合并AF患者较SR患者合并心脏瓣膜病、躯体化障碍的占比更高,SR组住院时的BMI更高、住院期间更多的使用ARNI、钙离子拮抗剂类药物。与Özlek等[15]研究相比,本研究中HFpEF合并AF患者心脏瓣膜病占比高于HFpEF合并SR患者。心脏瓣膜病常并发多种心律失常,其中又以AF最常见,其机制可能是主动钙化引起瓣膜关闭不全或狭窄,致使左心室增厚、肥大,进一步扩大左心房,增加其压力,损害心肌超微结构,异常增加心房肌异位起搏点兴奋性和自律性[16]。本研究还发现AF组躯体化障碍的占比高于SR组,推测性别可能是其中原因之一。现有的证据表明,女性更易合并躯体化障碍[17]。本研究中SR组BMI更高,可能与AF组年龄较大、合并基础疾病较多、身体状况较差有关。SR组使用ARNI、钙离子拮抗剂类药物比例更高,与既往研究结果不完全一致,可能与ARNI作为一种新型药物在改善HFpEF合并AF患者的疗效上尚缺乏相关的临床研究和临床医生用药的差异有关。
3.3HFpEF合并AF的再入院危险因素 本研究发现合并2型糖尿病、高尿酸血症、躯体化障碍可能是HFpEF合并AF患者再入院的独立危险因素,规律使用β受体阻滞剂可能是HFpEF合并AF患者再入院的独立保护因素。目前研究认为,高尿酸血症、糖尿病会对HF与AF的预后产生不利的影响[18-19]。氧化应激、炎症和神经重构假说解释了糖尿病在AF中的病理生理,在糖尿病和AF的患者身上都发现了C反应蛋白水平的升高[20]。高尿酸血症在AF人群中占比更高,推测可能与性别、雄激素减少有关,可能的机制为炎症反应,如促炎性细胞因子(肿瘤坏死因子和IL-1)的升高和氧化应激[21]。虽然目前研究缺乏能够直接改善HFpEF预后的证据,但本研究发现规律使用β受体阻滞剂可能是HFpEF合并AF患者再入院的独立保护因素。Veldhuisen等[22]研究表明,β受体阻滞剂可降低HF患者AF的发生率。另外,还有研究证明β受体阻滞剂能够改善HF合并AF患者的预后,可能是由于β受体阻滞剂通过抑制房室结中β1受体的活性,进而降低心室率,改善了心脏重构[23]。这可能是β受体阻滞剂降低HFpEF合并AF患者再入院率的机制之一。
本研究发现患者合并躯体化障碍是HFpEF合并AF患者再入院的独立危险因素。目前关于“心理因素”对HF再入院影响的研究较少,由于目前心内科医师诊断精神心理疾病(如焦虑症、抑郁症)权限有限,本研究中统一使用的是躯体化症状自评量表、患者健康问卷(patient health questionnaire,PHQ-9)筛查量表及CAD7项评估表对患者心理状态进行评估。躯体化障碍以多种多样、反复出现、时常变化的躯体症状为主要特征,是一种常见疾病,其发病率较高,常伴有明显的抑郁和焦虑[24]。研究发现,在我国三甲医院心内科,焦虑障碍、抑郁障碍、躯体化障碍的发病率均较高,且发病率差异无统计学意义[25]。躯体化障碍与抑郁症存在明显的相关性[26]。抑郁症在约20%的HF患者中存在,且与HF患者再入院率和死亡率的增加有关[27]。有研究发现,CHF患者外周促炎因子水平升高,谷氨酸传递失衡,下丘脑-垂体-肾上腺轴激活,促进中枢神经系统多巴胺、去甲肾上腺素和5-羟色胺(5-hydroxytryptamine,5-HT)等神经递质释放、代谢紊乱和炎症反应增加,最终导致患者抑郁[28]。抑郁症患者交感神经激活,分泌和释放更多的儿茶酚胺会增加血小板的活性,激活血小板会激活单核细胞,导致IL-1、IL-6等一系列炎症因子增多。交感神经兴奋的增加也可以通过改善血管壁血流动力学的切应力和抑制血管花生四烯酸的合成来促进凝血和血栓形成,最终共同导致或加重CHF。由此推测5-HT和血小板系统的激活可能是CHF合并抑郁症的中间环节之一[29]。另外交感神经系统功能亢进、副交感神经系统功能降低、心率变异性减低在CHF和抑郁症的发病机制中起到重要作用,但具体机制尚未明确[30]。未来仍需要大样本的研究进一步解释其潜在机制。
合并AF和不合并AF的HFpEF住院患者之间存在显著的临床差异。合并2型糖尿病、高尿酸血症、躯体化障碍可能是HFpEF合并AF患者再入院的独立危险因素,规律使用β受体阻滞剂可能是HFpEF合并AF患者再入院的独立保护因素。此外,“双心医疗”在改善HF患者预后方面具有巨大的潜力,因此需要临床医生建立整合医学观念,充分重视HF患者的心理问题,做到早诊断、早治疗,延长患者寿命,提升生活质量,减少发生心血管不良结局的风险。此外本研究尚存在不足:①本研究为单中心的真实性队列研究,数据量相对较少,仍可能存在偏倚,结果不能推广到更广泛的人群;②本研究为观察性研究,未来仍需要大量的前瞻研究来证实躯体化障碍影响HFpEF合并AF患者预后的病理机制;③本研究回顾分析了HFpEF合并AF患者再入院的影响因素,但并未进行随访调查,部分患者有可能于其他医院就诊,因此造成数据上的误差。
