大型迪庆藏猪不同生长阶段背脂沉积差异基因及其调控通路分析
2023-06-10严达伟王莉兴董新星
王 琳,严达伟,马 黎,张 博,王莉兴,张 浩,董新星
(1.云南农业大学动物科学技术学院,昆明 650201;2.云南农业职业技术学院畜牧兽医学院,昆明 650212;3.中国农业大学动物科学技术学院,北京 100193;4.云南省畜牧总站,昆明 650224)
【研究意义】目前中国猪肉生产中存在的一个主要矛盾是地方猪种生长缓慢、体脂含量高、瘦肉率低,而改良型猪种虽然瘦肉率高、体脂含量低,但肌内脂肪少,肉质差。在不影响猪肉品质的前提下,减少猪脂肪沉积已成为当前畜牧业亟需解决的关键科学问题之一。猪的背膘厚与生长速度和胴体瘦肉率呈负相关,与肌内脂肪含量呈正相关[1-2],研究猪背膘厚的功能基因及其调控机制,对猪瘦肉产量和肉品质的遗传改良具有重要意义。【前人研究进展】Song等[3]发现,瘦肉型猪脂肪沉积较少,可能与脂肪酸氧化能力强和能量代谢快有关。Albuquerque等[4]发现,葡萄牙脂肪型猪较高的脂肪沉积可能与脂肪酸从头合成、胆固醇合成及胰岛素抵抗有关。Zhang等[5]发现,嘉兴黑猪较高的脂肪率可能与PI3K-Akt信号通路和MAPK/p38通路等与脂肪生成相关的通路有关。Yuan等[6]发现,脂肪酸氧化相关基因CPT1A、ENNP1、APOBEC3F、PDK4在长白猪皮下脂肪高表达,长白猪的脂肪分解代谢高于金华猪,pFAM134B基因通过上调PPARγ、FAS、ACC等脂肪合成相关基因表达,下调ATGL、HSL脂肪分解相关基因表达,促进脂肪细胞内甘油三酯的积累。Chen等[7]发现,脂肪代谢相关基因CES1通过参与脂酰和胆固醇代谢而促进甘油三酯生成。Xing等[8]发现,AMPD1基因通过抑制脂肪酸氧化分解相关基因AMPK的活性,减少脂肪酸氧化,促进脂肪积累,CKMT2基因通过促进线粒体呼吸,增加能量消耗,减少脂肪存储。Liu等[9]、Zhao等[10]发现,PPAR信号通路、类固醇激素生物合成、TNF信号通路和甘油酯代谢等通路协同调节猪皮下前脂肪细胞分化,在分化的不同时间点,甘油三酯在脂肪细胞中不断积累。【本研究切入点】不同猪种的不同组织调控脂肪沉积的功能基因及其通路并不完全相同,表现出猪种特异性和时空特异性。迪庆藏猪是中国特有的高原型猪种之一,沉脂能力强、肉质好[11],目前关于藏猪的报道主要集中在血液生理[12]、低氧适应[13]、生长[14]、肉质[15],未见有迪庆藏猪背脂沉积功能基因及其调控机制的报道。【拟解决的关键问题】本研究采用RNA-Seq技术筛选大型迪庆藏猪背部皮下脂肪不同生长阶段的差异表达基因并分析其调控网络,为迪庆藏猪的育种工作提供科学依据。
1 材料与方法
1.1 试验材料
选择胎次相同、日龄和体重相近的纯种大型迪庆藏猪36头随机分3组(均已去势,公母各半),每组12头(表1),在云南省香格里拉市绿源生态种养专业合作社进行育肥试验,分别在体重达40、80和120 kg左右(S1:10~40 kg、S2:40~80 kg、S3:80~120 kg)时屠宰,每组选择接近平均体重的3头去势公猪,采集背部皮下脂肪组织,分别为S1_背脂_1、S1_背脂_2、S1_背脂_3、S2_背脂_1、S2_背脂_2、S2_背脂_3、S3_背脂_1、S3_背脂_2、S3_背脂_3,液氮速冻运回实验室,保存于-80 ℃冰箱,用于提取总RNA。

表1 试验猪只分组情况Table 1 Group of experimental pigs
1.2 试验方法
总RNA提取、mRNA文库构建参照文献[16],用Illumina HiseqTM2000上机测序。用软件Primer Premier 5.0设计qPCR引物(表2),内参基因选用猪GAPDH,qPCR定量验证重要DEGs。
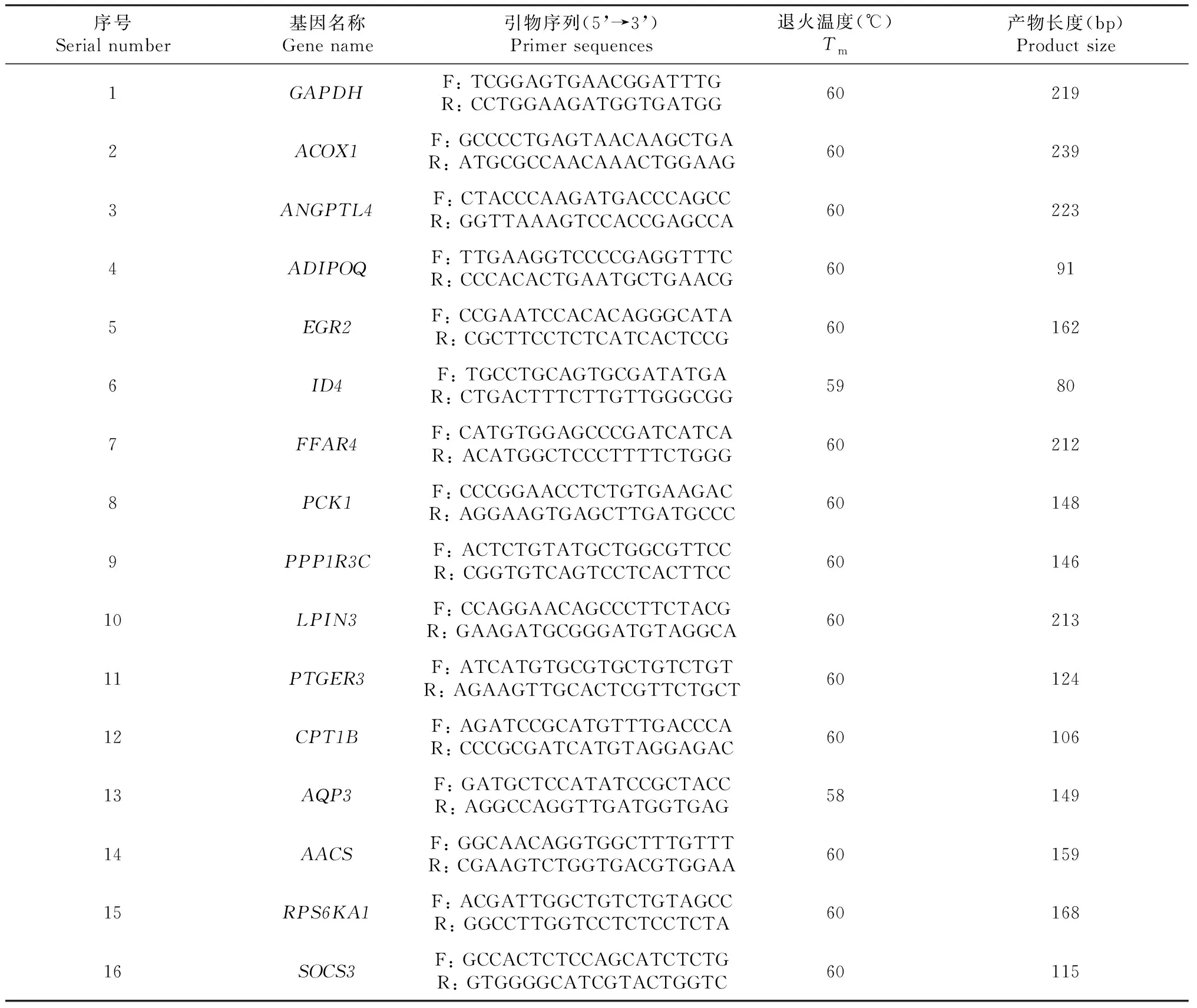
表2 差异表达基因引物Table 2 The primers of differentially expressed genes
1.3 数据处理与分析
1.3.1 测序数据处理 原始数据(Raw data)质控、过滤后(Clean reads)与猪参考基因组(Susscrofa11.1)比对,使用软件StringTie组装、定量比对到基因组各染色体上的reads,得到reads对应的每千个碱基转录每百万映射读取的片段(Fragments per kilobase of exon model per million mapped reads,FPKM)值。
1.3.2 差异基因筛选及功能富集分析 使用软件DEGseq2对归一化的FPKM值进行差异基因分析,参考王志秀[16]方法,以|log2fold change|>1且P<0.05为标准筛选差异表达基因;参考陆秀红等[17]方法,用在线软件DAVID对差异表达基因进行GO和KEGG分析,显著富集基因的阈值定为富集度Count≥2且矫正P<0.05。
1.3.3 差异基因STEM分析 参考Lu等[18]方法,以3个不同生长阶段全部差异基因的表达量数据用短时间序列表达模式分析软件(Short-time series expression miner,STEM)进行表达模式聚类分析,以不同阶段两两比较的组间差异倍数>2倍且P<0.05为数据过滤标准。
1.3.4 差异基因互作网络分析 选择STEM分析中显著富集的模块,参考Chen等[19]方法,利用R语言计算模块中差异基因间的共表达相关性,选择Pearson相关系数大于0.98的转录本,用软件Cytoscape 3.7.1绘制基因共表达网络。
2 结果与分析
2.1 迪庆藏猪背脂转录组测序数据统计
RNA-seq数据(表3)显示,每个样品原始reads数均在46.06 M以上,有效reads比例高于90%,有效 Q30比例均高于94%,3组样品的比对率均高于87%,符合生物信息学分析要求。
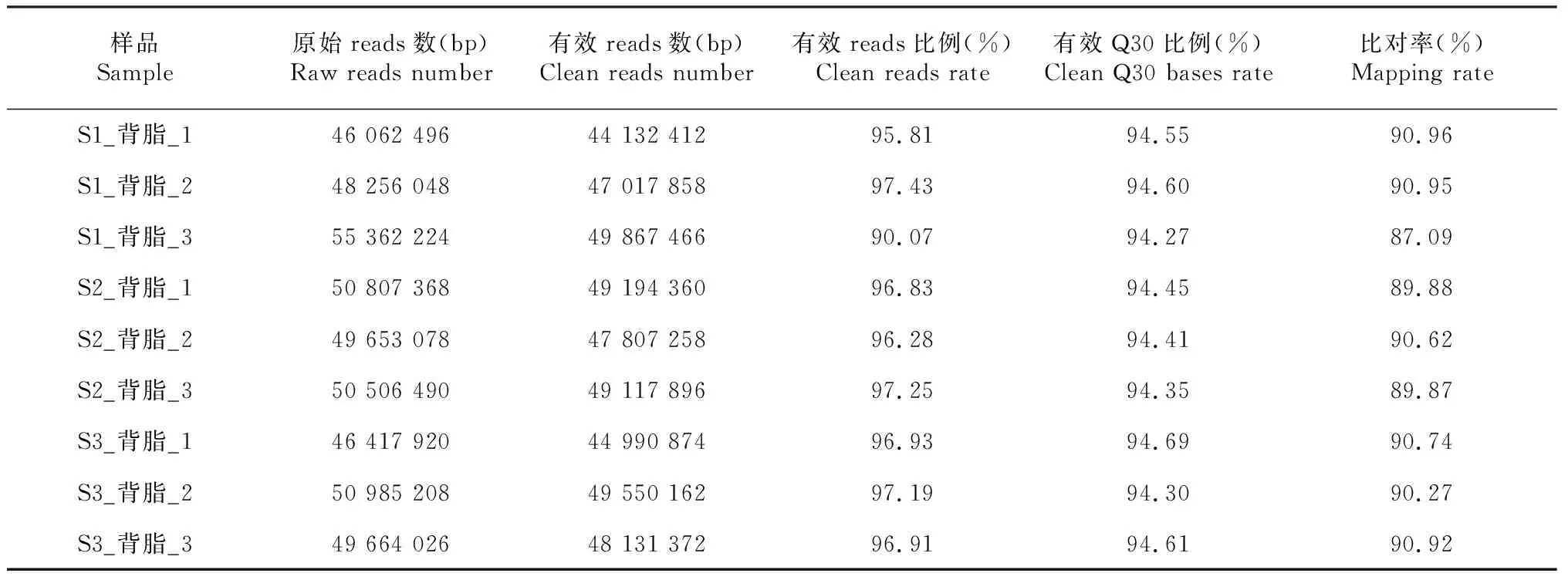
表3 RNA-Seq数据统计Table 3 RNA-Seq data statistics
2.2 qPCR定量验证
对ACOX1、ANGPTL4等15个差异基因进行qPCR验证(图1)。验证结果表明,15个基因在背脂组织中的表达量与转录组测序结果一致。
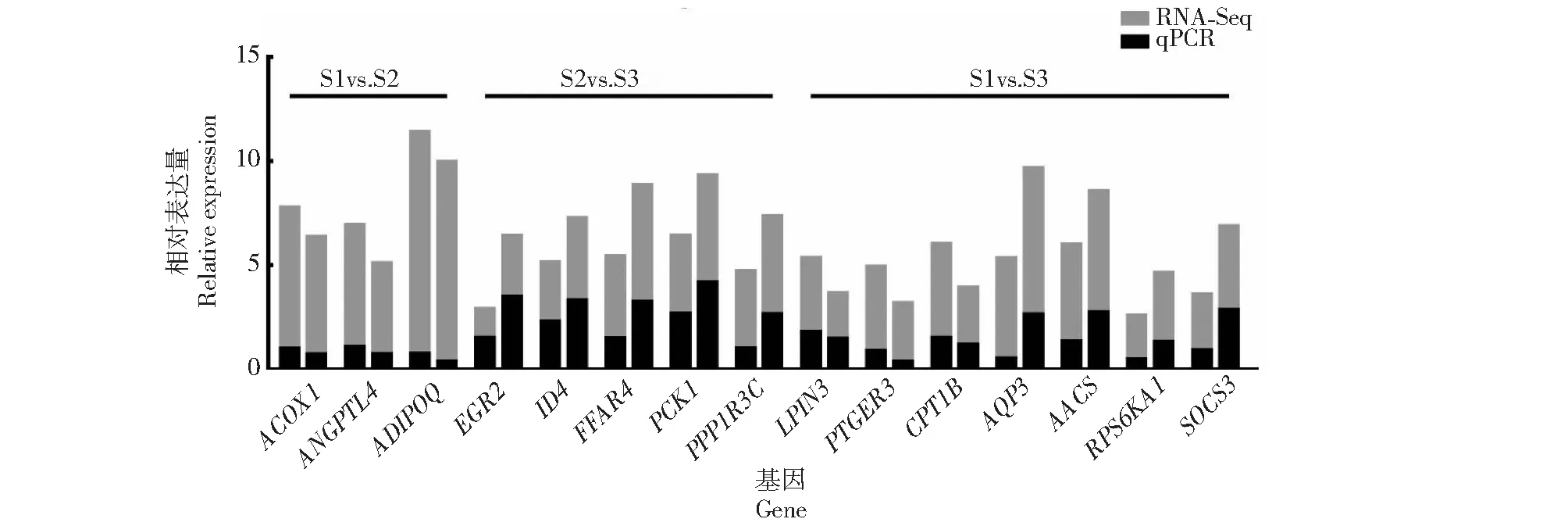
图1 迪庆藏猪背脂差异表达基因qPCR定量验证结果Fig.1 qPCR results of differentially expressed genes in back fat of Diqing Tibetan pigs
2.3 迪庆藏猪背脂差异基因表达水平分析
利用全部DEGs的FPKM值绘制小提琴图,由图2可见,S1、S2和S3组lg(FPKM+1)值的中位数分别为0.81、0.85和0.86。

图2 迪庆藏猪背脂差异基因表达水平的小提琴图Fig.2 Violin diagram of differential gene expression levels of back fat of Diqing Tibetan pigs
2.4 迪庆藏猪背脂mRNA差异表达分析
10~40 kg(S1)、40~80 kg(S2)和80~120 kg(S3)阶段共得到19 706个DEGs(图3),仅在S1阶段表达的基因有835个,仅在S2阶段表达的基因有666个,仅在S3阶段表达的基因有950个。

图3 迪庆藏猪背脂三阶段间基因表达Fig.3 Gene expression between back fat in 3 stages of Diqing Tibetan pigs
2.5 迪庆藏猪不同生长阶段背脂显著差异基因筛选
在S1与S2阶段共筛选到显著差异表达基因845个,其中,263个上调,582个下调(图4-A);在S2与S3阶段共筛选到558个,其中,292个上调,266个下调(图4-B)。

A:S1与S2阶段差异基因火山图;B:S2与S3阶段差异基因火山图。A:Volcanic map of differential genes in S1 and S2; B:Volcanic map of differential genes in S2 and S3.图4 迪庆藏猪背脂差异基因火山图Fig.4 Volcano map of differential genes in back fat of Diqing Tibetan pigs
2.6 迪庆藏猪不同生长阶段背脂显著差异基因功能富集分析
S1与S2阶段:GO分析显示,显著DEGs主要富集在钙离子结合、碳水化合物结合、细胞增殖正调控等(图5-A)。KEGG分析显示,显著DEGs主要富集在PPAR信号通路、PI3K-Akt信号通路、胰岛素抵抗等(图5-B),其中,ACOX1、ANGPTL4和ADIPOQ基因富集于PPAR信号通路并显著下调。

A:S1与S2阶段差异基因GO分析气泡图;B:S1与S2阶段差异基因KEGG分析气泡图;C:S2与S3阶段差异基因GO分析气泡图;D:S2与S3阶段差异基因KEGG分析气泡图。A:GO bubble diagram of differential genes in S1 and S2;B:KEGG bubble diagram of differential genes in S1 and S2;C:GO bubble diagram of differential genes in S2 and S3;D:KEGG bubble diagram of differential genes in S2 and S3.图5 迪庆藏猪背脂差异基因GO和KEGG分析Fig.5 GO and KEGG of differential genes in back fat of Diqing Tibetan pigs
S2与S3阶段:GO分析显示,显著DEGs主要富集在脂肪细胞分化、碳水化合物结合、脂质代谢过程等(图5-C)。KEGG分析显示,显著DEGs主要富集在胰岛素信号通路、PI3K-Akt信号通路、糖酵解/糖异生、PPAR信号通路等(图5-D),其中,EGR2、ID4、FFAR4基因富集于脂肪细胞分化,PCK1、PPP1R3C基因富集于胰岛素信号通路,5个基因均显著上调。
2.7 迪庆藏猪不同生长阶段背脂差异基因短时间序列分析
短时间序列分析(图6)发现共有4个差异显著模块,分别为模块4(P=6.4E-26)、模块0(P=2.0E-9)、模块3(P=7.3E-5)和模块14(P=2.7E-6),其中模块4、模块0和模块3的差异基因总体聚为一类,基因表达量随着大型迪庆藏猪体重的增加逐渐下降;模块14中基因的表达量先上调表达后轻微下调表达;其余模块差异不显著(P>0.05)。
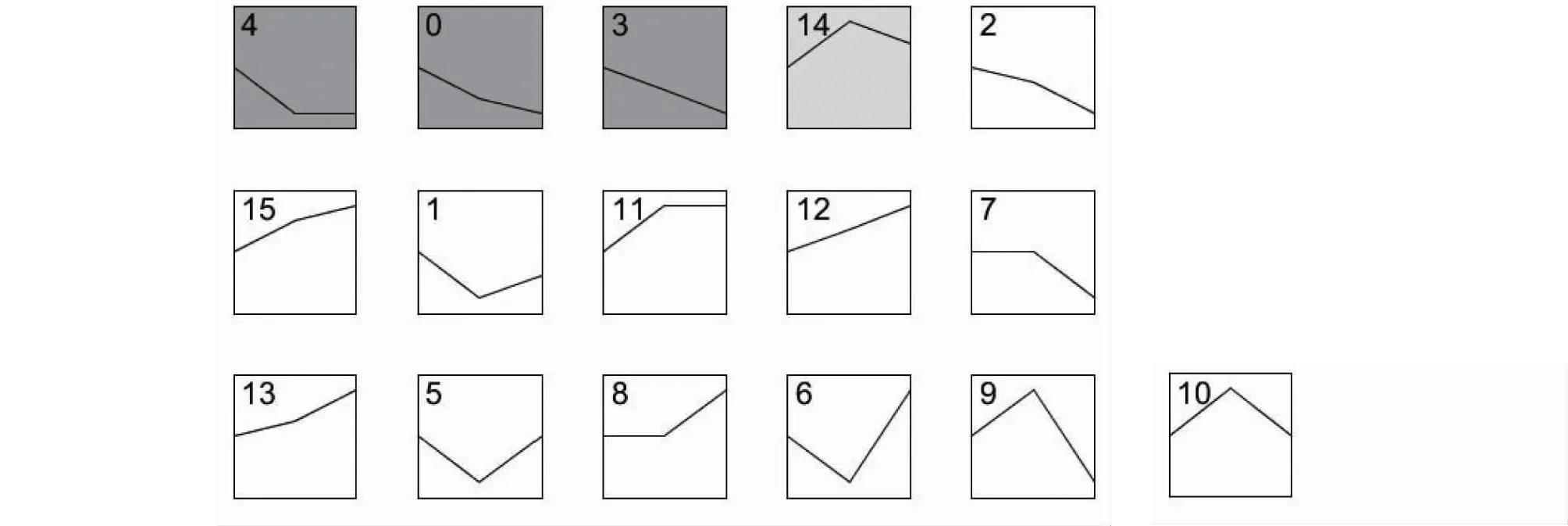
模块以基因数量和模块显著性排序。Clusters are ordered based on number of genes and cluster significance.图6 迪庆藏猪背脂STEM分析Fig.6 STEM analysis in back fat of Diqing Tibetan pigs
2.8 迪庆藏猪背脂差异表达基因互作网络
2.8.1 模块0/3/4差异基因互作网络 将STEM分析中3个阶段均显著下调的差异基因合并,绘制基因互作网络(图7)。CPT1B、LPIN3、PTGER3基因位于网络中心,与ND3、DEGS2、HHIP、CYTB、SMPD3、CALML5基因有互作关系,CPT1B基因调控ND3、DEGS2、HHIP、LPIN3、CYTB、SMPD3、PTGER3、CALML5基因;LPIN3基因调控ND3、DEGS2、HHIP、CYTB、SMPD3、CALML5基因;PTGER3基因调控ND3、DEGS2、HHIP、LPIN3、CYTB、SMPD3、CALML5基因。
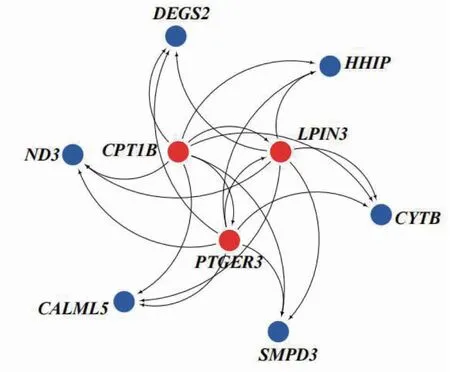
红色节点表示位于网络核心的基因,蓝色节点表示位于网络外周的基因,箭头起始端代表调控关系的上游,箭头末端代表调控关系的下游,即箭头连接两个基因,代表箭头起始端的基因对末端的基因起调控作用,下同。Red nodes represent genes located in the core of the network, and blue nodes represent genes located outside the network. The beginning and end of the arrows represent the upstream and downstream of the regulatory relationship. The arrow connects two genes, where the gene at the beginning regulates the gene at the end. The same as below.图7 迪庆藏猪背脂模块0/3/4差异基因互作网络Fig.7 Interaction network diagram of differential genes at module 0/3/4 in back fat of Diqing Tibetan pigs
2.8.2 模块14差异基因互作网络 将STEM分析中先上调、后轻微下调的基因绘制基因互作网络(图8)。AACS、SOCS3、AQP3、RPS6KA1基因位于网络中心,与STC2、CYP2C42、PCK2、ACP5和SPP1基因有互作关系,AACS基因调控CYP2C42、SOCS3、AQP3、PCK2、RPS6KA1、ACP5、SPP1基因;SOCS3基因调控STC2、SPP1基因;AQP3基因调控STC2、SOCS3、CYP2C42、PCK2、RPS6KA1、SPP1基因;RPS6KA1基因调控STC2、SOCS3、ACP5、SPP1基因。
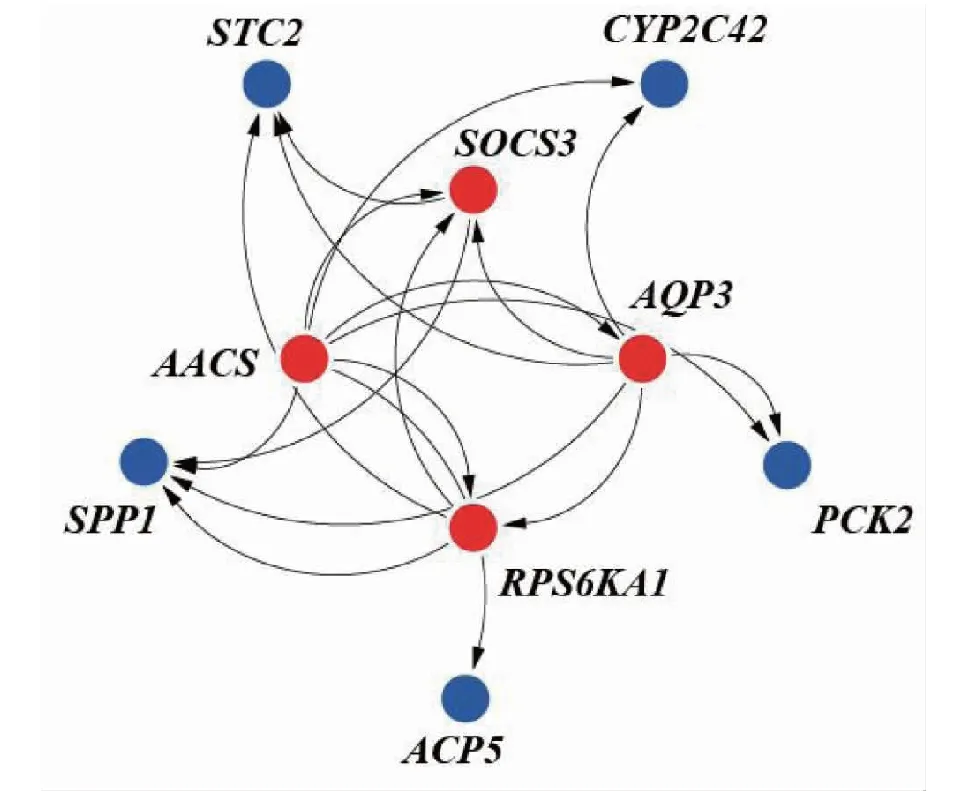
图8 迪庆藏猪背脂模块14差异基因互作网络图Fig.8 Interaction network diagram of differential genes at module 14 in back fat of Diqing Tibetan pigs
3 讨 论
3.1 迪庆藏猪S1与S2阶段背脂沉积差异基因
ACOX1基因编码脂肪酸β氧化的第一限速酶,ACOX1基因表达下调,抑制脂肪酸氧化,体内甘油三酯积累,导致大鼠肥胖[20]。ANGPTL4编码的蛋白可调节血糖稳态、脂质代谢,促进脂肪细胞中的甘油三酯释放到血浆,在缺失ANGPTL4的小鼠血浆中几乎检测不到甘油三酯,过表达ANGPTL4的小鼠血浆甘油三酯含量升高[21],ANGPTL4编码的蛋白可将血浆甘油三酯运送到代谢需求量大的组织,促进甘油三酯分解为脂肪酸,进一步氧化分解,为组织代谢供能[22]。ADIPOQ编码脂联蛋白的C1Q和胶原结构域,它的突变或异常表达都会引起胰岛素抵抗相关的代谢综合征,其仅在脂肪组织中表达,在调节脂代谢和糖代谢中发挥作用[23],ADIPOQ编码的脂联素能在脂肪组织中诱导AMPK苏氨酸残基磷酸化,激活的AMPK促进脂肪酸氧化分解,减少脂肪存储,ADIPOQ是脂肪生成的负调控因子[24]。在本研究中,ACOX1、ANGPTL4和ADIPOQ基因在S1与S2阶段下调,ACOX1基因下调可能抑制脂肪酸氧化、甘油三酯积累,ANGPTL4基因下调可能抑制脂肪细胞中甘油三酯分解,ADIPOQ基因下调可能减少脂肪酸分解、增加脂肪存储,背膘增厚,与S2阶段背膘厚显著高于S1阶段的结果一致。
3.2 迪庆藏猪S2与S3阶段背脂沉积差异基因
EGR2是脂肪形成诱导因子之一,EGR2基因位于C/EBPβ的上游,通过诱导C/EBPβ的表达而促进脂肪细胞分化[25],随EGR2表达量减少,3T3-L1细胞分化能力降低[26]。ID4编码蛋白是DNA结合抑制剂蛋白家族成员,可调节脂肪细胞分化,促进脂肪生成,前脂肪细胞中C/EBPα、PPARγ、FABP4、LPL等脂肪细胞分化标志物表达水平随ID4基因表达降低而降低,ID4基因缺失小鼠,脂肪组织减少、体重降低[27]。FFAR4编码蛋白是G蛋白偶联受体家族成员,作为长链脂肪酸的受体,可调节脂肪生成,FFAR4在ω-3脂肪酸的刺激下,作用于前脂肪细胞的纤毛上,诱导脂肪细胞增殖,产生更多新的脂肪细胞来储存饱和脂肪酸,进而维持脂肪组织的脂质稳态[28],此外,在游离脂肪酸诱导下,FFAR4与脂膜上的G蛋白偶联,抑制细胞内cAMP的积累,cAMP是一种第二信使,可激活脂肪分解、葡萄糖摄取和产热,FFAR4对cAMP抑制,减少脂肪分解和能量消耗,促进脂肪沉积[29]。在本研究中,相比于S2阶段,基因EGR2、ID4、FFAR4在S3阶段上调,可能对脂肪细胞存在诱导分化、促进增殖,降低代谢,维持胞内脂质稳态等作用。
PCK1和PPP1R3C基因在糖代谢和脂代谢中发挥重要作用,PCK1编码促进甘油生成的调节酶,敲除PCK1基因的小鼠,脂肪组织中甘油三酯沉积减少[30],过表达PCK1的转基因小鼠甘油生成增加,游离脂肪酸重新酯化,脂肪细胞大小和脂肪质量增加[31],表明PCK1通过生成甘油三酯的前体—甘油,促进脂肪沉积;PPP1R3C编码碳水化合物结合蛋白,敲除PPP1R3C基因的小鼠,其脂肪组织中脂肪生成的关键基因mTORC1和SREBP1表达水平降低,脂质合成减少[32],表明PPP1R3C基因可促进脂肪合成。在本研究中,与S2阶段相比,PCK1和PPP1R3C基因在S3阶段中显著上调,可能促进甘油三酯合成、脂质生成增加,背膘增厚,符合S3阶段背膘厚显著高于S2阶段的结果。
3.3 迪庆藏猪S1与S2与S3阶段背脂沉积差异基因
PTGER3是G蛋白偶联受体家族成员,能诱导异丙肾上腺素合成而促进脂肪分解,缺失PTGER3基因的小鼠因不能合成异丙肾上腺素,脂肪分解被抑制、脂肪沉积增加;其与正常小鼠相比,有更大的脂肪细胞和更高的体脂含量[33]。CPT1B基因编码长链脂肪酸β氧化的限速酶,脂肪组织CPT1B表达减少会导致脂肪组织中脂肪酸氧化能力降低,未氧化的脂肪酸新酯化为甘油三酯,引起机体肥胖[34]。LPIN3基因编码蛋白是脂蛋白家族成员之一,参与甘油三酯运输,缺失LPIN3基因的脂肪细胞,脂肪生成关键基因PPARγ、FABP4表达降低、脂滴减小,LPIN3的表达水平与脂肪含量呈负相关,肥胖小鼠通过负反馈机制抑制LPIN3基因的表达以维持脂质稳态[35]。本研究中,基因PTGER3、CPT1B和LPIN3在迪庆藏猪3个阶段背脂中均显著下调表达,PTGER3基因下调可能抑制脂肪分解、促进脂肪细胞增大,CPT1B基因下调可能使脂肪酸氧化能力降低、导致甘油三酯增多,LPIN3基因下调可能防止脂滴的过度聚集以维持脂质稳态,最终导致背膘增厚,与S3阶段背膘显著高于S2阶段、S2阶段显著高于S1阶段的结果一致。
AACS编码位于脂滴周围的酮体利用酶,将乙酰乙酸转化为乙酰乙酰辅酶A,为脂肪合成提供乙酰基单位,缺失AACS基因导致脂肪细胞分化标志物PPARγ和CEBP/α表达量降低,脂肪细胞分化受阻[36]。SOCS3编码细胞因子信号传导抑制蛋白,敲除SOCS3基因的肝细胞,与脂肪生成相关的SREBP1c、ACCα和IL-6等蛋白表达显著降低、脂肪生成减少[37]。RPS6KA1基因是丝氨酸/苏氨酸激酶RSK家族成员,RPS6KA1基因可诱导CREB基因磷酸化,激活后的CREB与CEBPB基因启动子结合,促进脂肪生成[38]。AQP3编码水通道蛋白,促进水和甘油的运输,AQP3基因通过促进成脂相关基因PPARγ、aP2等的表达而促进脂肪细胞内甘油三酯沉积[39]。在本研究中,从S1到S2阶段,AACS基因上调,可能促进脂肪细胞分化、细胞数量增多;SOCS3和RPS6KA1基因上调,可能促进脂肪生成;AQP3基因上调,可能导致脂肪细胞内甘油三酯增多、背膘增厚;但从S2阶段到S3阶段,这4个基因均稍下调,可能导致脂肪生成速率降低、脂肪细胞分化减缓,脂肪细胞内甘油三酯速率减慢,背膘增速变慢,与S2阶段平均背膘厚、6~7肋间膘厚比S1阶段分别增加83.26%、75.79%,而S3阶段平均背膘厚、6~7肋间膘厚比S2阶段分别增加38.83%、25.15%,增幅下降的结果一致。
4 结 论
大型迪庆藏猪从40 kg长至80 kg,AACS基因上调促进脂肪细胞分化、细胞数量增多,SOCS3、RPS6KA1基因上调促进脂肪生成,AQP3基因上调促进脂肪细胞内甘油三酯增多;ACOX1基因下调抑制脂肪酸氧化,ADIPOQ基因下调减少脂肪酸分解、增加脂肪存储,PTGER3基因下调抑制脂肪分解,CPT1B基因下调促进甘油三酯合成,ANGPTL4基因下调抑制脂肪细胞中甘油三酯分解,LPIN3基因下调表达调控脂滴的过度聚集以维持脂质稳态,AACS、SOCS3和LPIN3等10个基因协同作用,导致其背膘厚显著增加。从80 kg长至120 kg,EGR2基因上调诱导脂肪细胞分化、促进脂肪细胞增殖,PPP1R3C基因上调促进脂肪合成,ID4基因上调促进脂肪生成,PCK1基因上调促进甘油三酯合成,FFAR4基因上调减少脂肪分解、维持脂质稳态;PTGER3基因下调抑制脂肪分解、脂肪细胞增大,CPT1B基因下调使脂肪酸氧化能力降低、甘油三酯增多,LPIN3基因下调调控脂滴的过度聚集以维持脂质稳态,EGR2、PPP1R3C和LPIN3等8个基因协同作用,导致其背膘厚显著增加。
