3D 胸腔镜与2D 胸腔镜在早期肺癌中的手术疗效对比研究
2023-06-02莫俊贤杨钧铭李畅波
莫俊贤,谢 坚,杨钧铭,李畅波
(广西医科大学第七附属医院胸心外科,广西 梧州 543000)
随着现代医疗技术的发展,微创手术已成为目前外科手术中不可或缺的一种方式,其中电视胸腔镜手术(video assisted thoracoscopic surgery,VATS)因其具有创伤小、恢复快等优点,在胸外科中已得到广泛使用[1-3]。既往胸腔镜多采用二维(two dimensional,2D)的腔镜系统,即通过摄像技术将手术操作过程同步呈现到屏幕中;但2D 的平面图像缺乏深度感知和空间定向,外科医生需要更长的时间来适应2D 系统的使用,手术学习曲线较长[4]。随着三维(three dimensional,3D)腔镜的应用,手术中可以恢复自然的3D 视觉和深度感知,更利于快速、精确地抓取、解剖和缝合组织[5,6]。本研究回顾性分析使用3D-VATS 和同期2D-VATS 治疗的早期肺癌患者的临床资料,以探讨3D-VATS 在早期肺癌手术中的应用效果。
1 资料与方法
1.1 一般资料 收集2018 年1 月-2021 年12 月广西医科大学第七附属医院胸外科行VATS 肺切除手术的早期肺癌患者的临床病理资料进行回顾性分析,本次研究经我院伦理委员会批准,患者知情同意。纳入标准为:①术后病理诊断为非小细胞肺癌;②根据美国癌症联合委员会(American Joint Committee on Cancer,AJCC)第八版TNM 分期中T1~T2期、N0~N1期、M0期;③术前评估美国麻醉医师协会(American Society of Anesthesiologists,ASA)分级为Ⅰ~Ⅱ级;④术前评估可以全胸腔镜下切除者。排除标准:①既往患胸膜腔疾病者,如气胸、脓胸、血胸等;②术前有新辅助化疗、放疗、免疫治疗者;③术前或术后明确合并其它恶性肿瘤者或血液性疾病者;④合并重要器官严重功能损害者。本研究共纳入114 例患者,根据术中所使用的腔镜系统模式将患者分为2DVATS 组(80 例)和3D-VATS 组(34 例)。
1.2 方法
1.2.1 术前准备 所有患者使用双腔气管插管、静脉复合全身麻醉,取90°的健侧卧位,术中采用健侧单肺通气,由具有胸腔镜手术资质的医师进行手术。
1.2.2 切口选择 根据肿瘤所在位置,单孔手术选择腋前线第4/5 肋间约4 cm 作为镜孔及操作孔;双孔手术选择腋前线第4/5 肋间约3 cm 作为操作孔,腋后线第7/8 肋间1.5 cm 作为镜孔;三孔手术在双孔手术基础上,另加肩胛下角线第7/8 肋间1.5 cm 作为副操作孔。
1.2.3 术中操作 3D-VATS 组的患者术中使用奥林巴斯3D 电子腔镜系统(LTF-190-10-3D),手术医师、助手以及器械护士佩戴BKM-30G 圆偏振3D 眼镜。根据肿瘤大小以及位置先进行肺叶楔形切除术、肺段切除或肺叶切除术,再进行胸腔淋巴结切除术,左侧肺癌患者清扫4~12 组淋巴结,右侧肺癌患者清扫2、4、7~12 组淋巴结,术中仔细辨认重要组织、血管,避免损伤。术毕于胸腔低位切口处留置胸管1根。2D-VATS 组患者术中同样使用该电子腔镜系统,但选择2D 图像输出,手术人员不需佩戴3D 眼镜,余下操作同3D-VATS 组。
1.3 观察指标 收集患者的一般临床资料,包括:年龄、身高、体重、肿瘤位置等。术中观察指标包括:手术时间、术中出血量、是否中转开胸、淋巴结清扫个数和总住院时间等。术后观察指标包括:术后总引流量以及肺漏气例数(漏气时间>5 d)、支气管胸膜瘘、肺部感染/肺不张、脓胸/乳糜胸、胸腔出血和心律失常等术后并发症。
1.4 统计学方法 使用SPSS 25.0 及R 语言4.0 软件进行数据分析,计数资料使用[n(%)]表示,采用χ2检验或Fisher 准确检验;计量资料使用()表示,根据变量是否符合正态分布以及方差齐性检验结果,从而进行非参数检验或独立样本t检验。本次研究检验水准α=0.05,P<0.05 认为差异有统计学意义。
2 结果
2.1 两组一般资料比较 两组年龄、身高、体重、ASA分级、操作切口个数、病变部位比较,差异无统计学意义(P>0.05),见表1。
表1 3D-VATS 组与2D-VATS 组一般资料比较[n(%),]
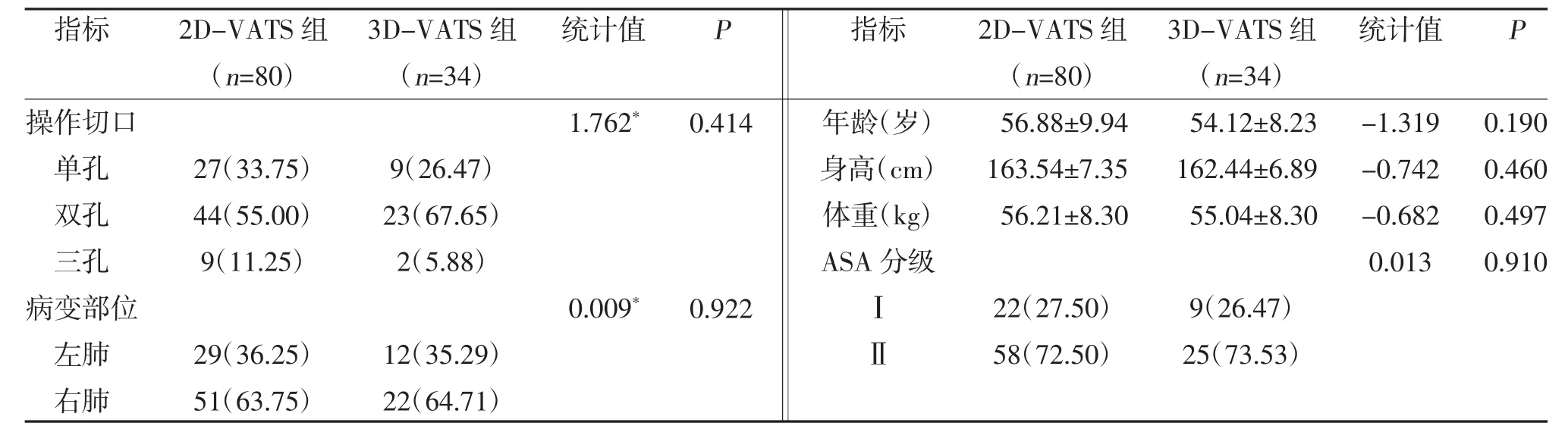
表1 3D-VATS 组与2D-VATS 组一般资料比较[n(%),]
注:*为使用χ2 检验,余为t 检验
2.2 两组术中、术后指标比较 3D-VATS 组患者的手术时间(P=0.000)、术中出血量(P=0.005)、术后胸管总引流量(P=0.009)以及总住院时间(P=0.049)少于2D-VATS 组,见表2。
表2 3D-VATS 组与2D-VATS 组患者的术中、术后指标对比()

表2 3D-VATS 组与2D-VATS 组患者的术中、术后指标对比()
注:#为使用Fisher's 确切概率法,余为t 检验
2.3 两组患者术后并发症比较 3D-VATS 组患者中总体并发症发生率以及术后出现肺漏气时间延长、支气管胸膜瘘、肺部感染/肺不张、乳糜胸/脓胸、胸腔积血以及心律失常等并发症发生率与2D-VATS组比较,差异无统计学意义(P>0.05),见表3。

表3 两组患者术后并发症对比[n(%)]
3 讨论
随着胸腔镜技术的快速发展,胸腔镜手术成像系统已由传统的2D 系统图像发展至3D 系统图像和外科机器人系统[7,8]。2D 图像缺乏深度,可能会导致图像失真、手眼协调能力受损,以及估计大小的能力降低;然而机器人手术需要昂贵的设备,成本较高,现阶段并不利于在我国广泛开展使用[9,10]。相对于2D 胸腔镜,3D 胸腔镜不仅能使手术过程更加具有可视化,而且并不需要增加额外费用。因此3D 胸腔镜系统在我国拥有较好的发展前景[11,12]。
本研究结果表明3D-VATS 组患者的手术时长、术中出血量、术后总引流量以及总住院时间优于2D-VATS 组患者。3D 胸腔镜的图像放大倍数比2D系统高,手术过程中能更清楚地辨别出需切除组织周围的微小血管、神经等,术中操作能更细致,减少副损伤,避免了术中淋巴结细小出血导致的术野血染,以及可以减少术后的淋巴导管渗出,从而减少术后出现乳糜胸、胸腔积液、胸腔积血[13]。3D-VATS 组患者在手术疗效(淋巴结清扫数目)以及术后并发症发生率方面与2D-VATS 组无差异。在进行纵隔淋巴结清扫时,3D 图像能清晰地看到淋巴结的位置及进行深度感知,例如常因顾及避免损伤对侧主支气管,而无法完全清除隆突下淋巴结。3D 图像能实时感知对侧主支气管的位置及深度,使得隆突下淋巴结清扫更为彻底。在分离叶间裂时,3D 图像也有着明显的优势。分离叶间平面时需要根据脏层胸膜的走行紧贴患肺进行分离,3D 图像能清楚地观察到叶间裂的走行,从而避免副损伤,这也是3D 组患者的肺异常漏气比例(8.8%)较2D 组患者(11.3%)少的原因之一。此外,在拟行解剖性肺段切除的手术患者中,术前常规进行CT 三维重建以观察肺段血管、支气管的走行是否存在变异,从而拟定手术方案及手术入路,术中3D 腔镜图像也能与术前的三维重建图像相匹配,在离断段血管和段支气管时可以减少误切除的发生[14]。
3D 胸腔镜相较于2D 胸腔镜的学习曲线更短。既往胸腔镜手术初学者在学习腔镜技术时需要适应从立体视觉转换至平面视觉,因此学习曲线较长,但双目镜的3D 成像技术能够为使用者提供更强烈的深度和位置感,因此能更快捷地熟悉胸腔镜的技术[15]。此外,胸腔内包含有呼吸、消化、心血管系统等多个重要组织、器官,相互之间结构复杂,解剖层次不熟悉容易出现差错导致严重后果。3D 图像能加深年轻医师对于胸腔内立体解剖结构的认识,更快地掌握胸腔内解剖层次,有助于缩短胸腔镜技术的学习曲线。
3D 胸腔镜系统也存在一定的不足。一些使用者在刚接触3D 图像时会出现头晕、恶心、呕吐不适,甚至因此放弃继续使用[16]。出现此种情况的原因是胸腔镜和监视系统的分辨率过低。在高分辨率的3D腔镜系统中,此种症状较为轻微,而且连续进行3~5例3D 胸腔镜手术后能完全克服此种不适感,并会习惯于3D 视觉。镜头不稳导致图像移动过快也是出现头晕不是的另一个原因,3D 胸腔镜的放大倍数比2D 胸腔镜要高,因此3D 术野比2D 术野要小,而且3D 图像是双镜头双目系统的图像重叠构成,镜头晃动或移动过快时导致图像短时失真,这时候需要配合的助手也熟悉3D 胸腔镜系统,增加扶镜的稳定性[17]。
综上所述,3D-VATS 组患者的手术时长、术中出血量、术后总引流量以及总住院时间优于2DVATS 组患者,在手术疗效(淋巴结清扫数目)以及术后并发症发生率方面两者无差异。3D 胸腔镜技术在早期肺癌手术中的应用是安全、有效的,3D 胸腔镜将有助于推动微创胸外科领域的发展。
