基于Q[6]?HAuCl4/AuNPs构建的无标记电化学传感体系对尸胺的检测
2023-05-30范颖王成艳葛庆梅丛航
范颖 王成艳 葛庆梅 丛航
摘 要:利用瓜环基金属有机框架Q[6]·HAuCl4与Au纳米颗粒复合构建了一种电化学传感器GCE-AuNPs-Q[6]·HAuCl4检测尸胺,其中,大环化合物六元瓜环主要用于对尸胺的选择性识别,HAuCl4和Au纳米颗粒极大提高了DPV电化学响应信号。该电化学传感器与电解液中K3[Fe(CN)6]/K4[Fe(CN)6]氧化还原探针的综合应用,开发了一个新颖的无标记定量检测尸胺的电化学分析体系,具有稳定性、选择性和灵敏度高,抗干扰能力强等优势,在0.6~10 μM线性范围内,检出限达到0.03 μM。应用该体系对枸杞酒中尸胺的检测也具有良好的回收率,体现了其实际应用价值。
关键词:瓜环;尸胺;电化学传感器;无标记分析
中图分类号:O657.1
文献标志码:A
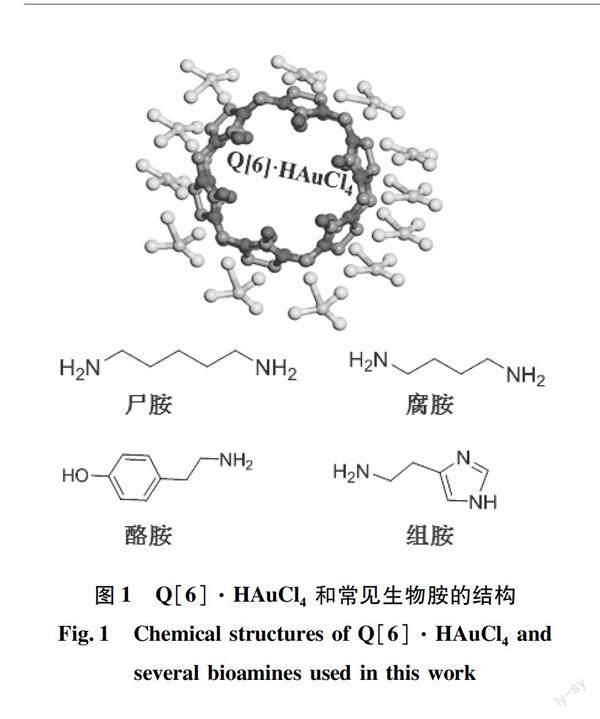
1,5-戊二胺(图1)是一种两端带有氨基基团(—NH2)的天然生物分子,具有多种化学和生物活性的天然多胺,存在于人类、动物、植物、细菌、真菌等微生物中 [1]。1885年,德国医生Ludwig Brieger提出[2],1,5-戊二胺是一种最具特征的死亡气味成分,是氨基酸在分解过程中脱羧产生的恶臭分子,尤其是神经递质或激素,因此,被称为尸胺。其广泛分布于原核生物和真核生物中,是细胞生长过程中发挥重要作用的物质之一。在植物中,尸胺参与调控植物生长发育、细胞信号转导、胁迫响应和昆虫防御等多种过程[3]。在动物体中,尸胺可以释放肾上腺素和去甲肾上腺素,刺激子宫、肠道运动神经,还扮演控制胃酸分泌的角色。尸胺的形成也与动物生长和肿瘤的发生有关[4]。在化学工业方面,尸胺可用来代替六亚甲基二胺生产聚酰胺或聚氨酯[5],可作为喹奥利齐丁生物碱生物合成的前体。尸胺还可以用于评价食品的新鲜或腐败程度,其含量可作为卫生质量的指标。食品中的尸胺被认为对人类健康有潜在的危险,对人体具有强烈的排斥作用,欧洲食品安全局已经确认腐胺(1,4-丁二胺,图1)和尸胺是食品中最常见的生物分子之一[6]。因此,建立快速检测尸胺的方法对食品安全具有重要意义[7]。目前,对于尸胺的鉴别和检测的方法有生物传感器[8]、气相色谱-质谱法[9]、电化学传感器[10]、电泳[11]、高效液相色谱法[12]、比色法[13]等。尸胺缺乏发色团,运用光谱检测需要衍生化,过程复杂,而电化学分析所需化学试剂和设备简单,灵敏度高,是一种快速、准确、低成本的方法。
本文利用六元瓜环(Q[6],图1)作为大环主体,利用其与不同结构胺分子的几何匹配能力不同,实现了对尸胺的超分子识别,并应用于电化学分析;为了提高灵敏度,利用具有良好导电性能的HAuCl4,与Q[6]形成金属有机框架材料(mental-organic-frames, MOFs)Q[6]·HAuCl4,并且应用纳米金(AuNPs)作为信号放大器,制备了对尸胺高灵敏度、高选择性的玻碳电极(GCE)基电化学传感器GCE-AuNPs-Q[6]·HAuCl4(图1)。由于尸胺不具有电化学信号,在电解质溶液中引入了电化学氧化还原可逆的K3[Fe(CN)6]/K4[Fe(CN)6]电对,构建了新型的尸胺无标记电化学分析方法,对该方法的分析性能进行了综合评价。
1 试验
1.1 试验仪器与试剂
巴谢特热重分析(TGA);BAS Epsilion E2-440(USA)电化学工作站;AuNPs溶液购自南京欣福纳米材料科技有限公司;HAuCl4·3H2O购自Ionochem(北京,中国);K3[Fe(CN)6],K4[Fe(CN)6]、KH2PO4,K2HPO4·3H2O、浓盐酸、无水乙醇、1,5-戊二胺、腐胺、组胺、酪胺等购自上海阿拉丁生化科技有限公司;缓冲液为0.1 M磷酸盐缓冲液(PBS, pH=7.4)。所有溶液均用去离子水(DW,18 MΩ·cm-1)配制;Q[6]·HAuCl4根据文献[14]合成。
1.2 溶液的配置
根据缓冲溶液表配制0.1 M PBS(pH=7.4)缓冲溶液。在分析天平上称量11.41 g K2HPO4·3H2O和6.80 g KH2PO4于500 mL的烧杯中,加去离子水溶解,转移到500 mL容量瓶中。再往溶液中滴加微量浓盐酸,通过pH计调节pH=7.4,得到0.1 M PBS(pH=7.4)缓冲溶液,贴好标签备用。
工作溶液的配置。在分析天平上分别称取0.823 g K3[Fe(CN)6]、0.106 g K4[Fe(CN)6]和3.728 g KCl于500 mL的烧杯中,适量的去离子水超声溶解,转移至500 mL的容量瓶中,定容后得到含有0.1 M KCl的5 mM K3[Fe(CN)6]/K4[Fe(CN)6]黄色溶液作为工作溶液。
Q[6]·HAuCl4 复合物溶液的配制。在分析天平上分别称量1、2、3、4、5、6 mg 的Q[6]·HAuCl4 复合物于5 mL试管中,取1 mL去离子水于各试管中,并加入5 μL Nafion溶液,超声2 h后形成分布均匀的1、2、3、4、5、6 mg/mL的Q[6]·HAuCl4悬浊液。
分析物的配制。在分析天平上称量0.044 g 1,5-戊二胺盐酸盐于25 mL烧杯中,加入适量 0.1 M PBS(pH=7.4)缓冲溶液溶解1,5-戊二胺盐酸盐,溶液转移至25 mL容量瓶中,定容后配制成0.01 M 1,5-戊二胺盐酸盐的母液,常温下避光待用。干扰物(腐胺、组胺和酪胺)也配制成母液待用。
1.3 GCE-AuNPs-Q[6]·HAuCl4修饰电极的制备
用少量氧化铝(Al2O3)粉末抛光玻碳电极记为GCE(φ=3 mm),再分别用乙醇和去离子水超声处理60 s,去除电极上吸附的杂质直至电极表面光滑反光,烘干。将5 μL Q[6]溶液滴在电极表面,烘箱中60 ℃干燥,制备Q[6]修饰电极,标记为GCE-Q[6];将5 μL AuNPs溶液(0.1 mg/mL)滴在电极表面,60 ℃干燥,制备标记为GCE-AuNPs的AuNPs修饰电极。5 μL Q[6]·HAuCl4 溶液覆蓋在修饰电极上,标记为GCE-Q[6]·HAuCl4。同样,5 μL AuNPs溶液(0.1 mg/mL)和不同浓度的Q[6]·HAuCl4 逐层修饰电极写成GCE-AuNPs-Q[6]·HAuCl4。
1.4 電化学方法
所有的电化学测量均在5 mM K3[Fe(CN)6]/K4[Fe(CN)6](氧化还原探针)工作溶液中进行,电位范围为初始电位-0.2 V到终止电位+0.6 V,扫描速度为100 mV·s-1。应用DPV测量时,进步电位为5.0 mV,脉冲振幅为40 mV,脉冲宽度为250 ms。尸胺溶于0.1 M PBS(pH=7.4)溶液中,GCE-AuNPs-Q[6]·HAuCl4 电极在不同浓度尸胺孵育20 min,进行电化学测试。
2 结果与讨论
2.1 Q[6]·HAuCl4复合物的表征
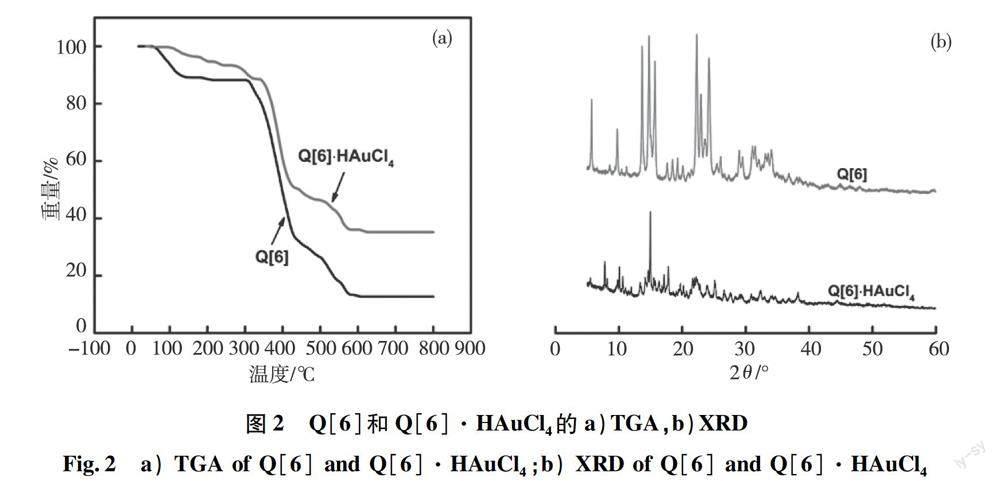
采用多种技术手段对所合成的Q[6]·HAuCl4材料进行了表征。图2(a)是Q[6]和Q[6]·HAuCl4的热重分析图。Q[6]表现为在129.1 ℃以下失掉11.8% 质量的结晶水;在308.3 ℃开始发生热分解,到581.1 ℃失去74.7%的质量。Q[6]·HAuCl4的热分解在342.7 ℃开始,分解温度的升高说明形成了MOFs结构,稳定性提高;到581.5 ℃材料失重52.8%,可计算得到Q[6] 与HAuCl4的作用比接近1∶1。x射线衍射分析发现Q[6]的特征峰很明显,而在Q[6]·HAuCl4复合物不具有游离的Q[6]物相,说明HAuCl4与Q[6]的复合物形成(图2(b))。
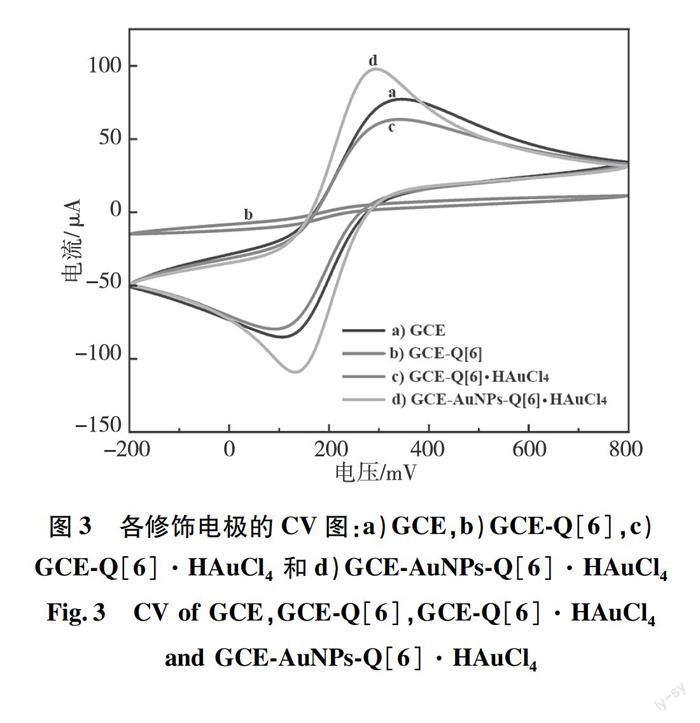
运用电化学方法对制备的各种电极材料(GCE、GCE-Q[6]、GCE-Q[6]·HAuCl4和GCE-AuNPs-Q[6]·HAuCl4)在氧化还原探针K3[Fe(CN)6]/K4[Fe(CN)6]中进行了表征(图3)。循环伏安曲线(CV)表明,各电极材料上的峰电流强度顺序为:GCE-AuNPs-Q[6]·HAuCl4>GCE>GCE-Q[6]·HAuCl4>GCE-Q[6],说明有机大环化合物Q[6]具有较强的绝缘性,而强导电能力的HAuCl4和AuNPs的引入,提高了电极的电化学响应。
为了进一步表征各种材料的电化学性能,对其交流阻抗性能进行了测试(图4)。拟合各材料的Nyquist实验值,得到GCE裸电极的电荷转移电阻Rct=287.9 Ω(曲线(a)),当修饰了Q[6],电极的Rct急剧增加到8 898 Ω(曲线(b)),说明六元瓜环具有很大的电阻;而复合材料Q[6]·HAuCl4修饰的玻碳电极的电荷转移电阻降到了988.5 Ω(曲线(c)),表明HAuCl4提高了材料的导电性能;在复合材料与电极表面之间插入AuNPs,Rct值降低至234.3 Ω(曲线(d)),因此,GCE-AuNPs-Q[6]·HAuCl4电极具有最佳的电化学性能,传感器构建成功。
2.2 尸胺电化学分析性能
应用构建的电化学传感器对尸胺进行了定量检测。将GCE-AuNPs-Q[6]·HAuCl4置于一系列浓度尸胺中孵育20 min,分别测试DPV信号(图5(a)),峰值电流强度与分析物浓度在0.6~10 μM范围呈良好的线性关系,相应的回归方程I(μA)=-1.884 6C (μM)+30.642 (R2=0.987 9),检出限为0.03 μM(图5(b))。
在相同条件下,同一支修饰电极重复测量5次的结果表明,该传感器的信号稳定,重复性好(图6(a))。分别制备6支GCE-AuNPs-Q[6]·HAuCl4修饰电极,置于1.0×10-5 M浓度的尸胺溶液中孵育20 min后,应用DPV考察传感器检测尸胺的电化学响应重现性,经过6次相同的步骤,检测底物在这6支修饰电极上的DPV响应差异不大,峰电流值的计算相对标准偏差仅为3.2%(图6(b)),表明构建传感具有很好的重现性。分别制备6支修饰电极,置于冰箱冷藏24 h,再测试这些电极对尸胺的DPV响应,结果显示DPV的响应电流值波动不大(图6(c)),相对标准偏差仅为7.0%,稳定性好。
尸胺在生物样品中的残留会与多种生物胺共存,成为对尸胺检测的干扰,因此,选择了常见的腐胺、酪胺、组胺作为干扰物质,考察它们对GCE-AuNPs-Q[6]·HAuCl4检测尸胺干扰性。结果如图6(d)所示,在20倍浓度的腐胺、酪胺、组胺存在下,尸胺的DPV响应电流值的变化很小,表明所构建的电化学传感器具有较好的抗干扰能力。
为评价该传感器在实际检测中的实用性和可行性,采用标准添加法对真实枸杞酒样品(在保质期内)进行尸胺分析。具体试验步骤为,取少量枸杞酒经过0.45 μM滤膜过滤后,用0.1 M PBS溶液(pH=7.4)稀释一定倍数,用于电化学分析,尸胺的标示量与测定量之间的电化学信号相差不大,回收率在86.5%~104.3%之间(见表1)。表明修饰的GCE-AuNPs-Q[6]·HAuCl4电极检测结果比较可靠,可用于实际样品中尸胺含量的有效测定。
3 结论
本文制备了新型的金属有机骨架Q[6]·HAuCl4,运用多种谱学技术对其结构和成分进行表征,并与AuNPs复合,构建了玻碳电极基底的GCE-AuNPs-Q[6]·HAuCl4电化学传感器,考察了其电化学性能,并在K3[Fe(CN)6]/K4[Fe(CN)6]氧化还原探针溶液中开发了对尸胺的无标记电化学定量分析方法,结果表明,体系的DPV信号对0.6~10 μM浓度的尸胺具有良好的线性关系,检出限为0.03 μM;该传感器具有稳定性、重复性、重现性和抗干扰性。利用所构建的GCE-AuNPs-Q[6]·HAuCl4传感器在枸杞酒真实样品中检测尸胺获得良好的的回收率,可应用于食品质量评价等领域。
参考文献:
[1]SANZ-VICENTE I, NGEL L M, MARCOS S D, et al. Smartphone-interrogated test supports for the enzymatic determination of putrescine and cadaverine in food[J]. Anal Bioanal Chem, 2020, 412: 4261-4271.
[2] WEI G G, MA W C, ZHANG A L, et al. Enhancing catalytic stability and cadaverine tolerance by whole-cell immobilization and the addition of cell protectant during cadaverine production[J]. Appl Microbiol Biotechnol, 2018, 102: 7837-7847.
[3] JANCEWICZ A L, GIBBS N M, MASSON P H. Cadaverines functional role in plant development and environmental response[J]. Front Plant Sci, 2016, 7: 870-877.
[4] ZARB J, WAITERS D R. The formation of cadaverine, aminopropylcadaverine and N,N bis (3-aminopropyl) cadaverine in mycorrhiral and phytopathogenic fungi[J]. Lett Appl Microbiol, 1994, 19: 277-200.
[5] HUANG Y H, JI X L, MA Z L, et al. Green chemical and biological synthesis of cadaverine: recent development and challenges[J]. RSC Adv, 2021, 11: 23922-23942.
[6] SUDALAIMANI S, SANJEEV K K, ESOKKIYA A, et al. Electrified liquid-liquid interface as an electrochemical tool for the sensing of putrescine and cadaverine[J]. Analyst, 2021, 146: 3208-3215.
[7] RIVAS B D L, CARRASCOSA A V. PCR detection of foodborne bacteria producing the biogenic amines histamine, tyramine, putrescine, and cadaverine[J]. J Food Prot, 2006, 10: 2509-2514.
[8] OH J, YANG H, JEONG G E, et al. Ultrasensitive, Selective, and highly stable bioelectronic nose that detects the liquid and gaseous cadaverine[J]. Anal Chem, 2019, 91: 12181-12190.
[9] ALMEIDA C, FERNANDES J O, CUNHA S C. A novel dispersive liquideliquid microextraction (DLLME) gas chromatographymass spectrometry (GCeMS) method for the determination of eighteen biogenic amines in beer[J]. Food Control, 2012, 25: 380-388.
[10]LEONARDO S, CAMPS M. Electrochemical enzyme sensor arrays for the detection of the biogenic amines histamine, putrescine and cadaverine. using magnetic beads as immobilisation supports[J]. Microchim Acta, 2016, 183: 1881-1890.
[11]KUMAR S, AROCKIARAJ M, ESOKKIYA A, et al. Ion-pair facilitated non-enzymatic electrochemical sensing of cadaverine and putrescin[J]. J Electrochem Soc, 2021, 168: 047505-047514.
[12]KUMUDAVALLY K V, SHOBHA A, VASUNDHARA T, et al. Chromatographic analysis of cadaverine to detect incipient spoilage in mutton[J]. Meat Sci, 2001, 59: 411-415.
[13]LI Y F, LIN Z Z, HONG C Y, et al. Colorimetric detection of putrescine and cadaverine in aquatic products based on the mimic enzyme of (Fe,Co) codoped carbon dots[J]. J Food Meas Charact, 2021, 15: 1747-1753.
[14]WU H, JONES L O, WANG Y, et al. High-efficiency gold recovery using cucurbit[6]uril[J]. ACS Appl Mater Interfaces, 2020, 12: 38768-38777.
(责任编辑:于慧梅)
A Label-Free Electrochemical Sensor Based on
Q[6]·HAuCl4/AuNPs for Cadaverine Detection
FAN Ying, WANG Chengyan, GE Qingmei, CONG Hang*
(Enterprise Technology Center of Guizhou Province, Guizhou University, Guiyang 550025, China)
Abstract:
An electrochemical sensor, GCE-AuNPs-Q[6]·HAuCl4, was constructed to detect cadaverine with cucurbit[n]uril-based metal-organic framework Q[6]·HAuCl4 and Au nanoparticles. Q[6] was used for selective recognition to cadaverine, while HAuCl4 and Au nanoparticles greatly improved the electrochemical signal in DPV. In the presence of K3[Fe(CN)6]/K4[Fe(CN)6] redox probe in the electrolyte, the electrochemical sensor was developed for a novel label-free quantitative detection of cadaverine electrochemical analysis system, which had the advantages of stability, selectivity, high sensitivity and strong anti-interference ability, with a detection limit of 0.03 μM in the linear range of 0.6~10 μM. The application of this system for the detection of cadaverine in wine also afforded good recoveries, exhibiting practical application value.
Key words:
cucurbituril; cadaverine; electrochemical sensor; label-free analysis
收稿日期:2022-08-03
基金項目:贵州省科技计划资助项目(20201Y028);贵州大学人才引进资助项目(201902)
作者简介:范 颖(1979—),女,高级实验师,博士,研究方向:有机化学和超分子化学,E-mail:fy7679@126.com.
通讯作者:丛 航,E-mail:ecnuc@163.com.