培养“科学态度与责任”的化学实验教学
2023-05-30陈艳虹
陈艳虹


摘要:实验是研究化学最主要的方式和手段,在初中化学教学中有着重要的认知价值,对学生核心素养的培养具有重要的作用。初中化学实验教学中,教师可通过强调步骤原理、关注尾气处理、优化实验方案等,帮助学生发展探究欲、树立生态文明的理念、锤炼严谨求实的科学态度。
关键词:初中化学;实验教学;核心素养;科学态度与责任
《义务教育化学课程标准(2022年版)》(以下简称“新课标”)指出“化学课程要培养的核心素养,主要包括化学观念、科学思维、科学探究与实践、科学态度与责任”[1],并进一步指出科学态度与责任的主要表现包括“发展对物质世界的好奇心、想象力和探究欲……具有严谨求实的科学态度……树立生态文明的理念”[2]。初中化学实验教学中,教师可通过强调步骤原理、关注尾气处理、优化实验方案等,帮助学生发展探究欲、树立生态文明的理念、锤炼严谨求实的科学态度。
一、 强调步骤原理,发展探究欲
化学实验中,学生需要仔细观察实验现象,不放过每一个细节。尤其是有一些实验的步骤有明显的先后顺序要求,那么,就可以进行对比实验,通过现象分析,明确并强调实验步骤的原理,帮助学生逐渐发展探究欲,培养科学探究的习惯。
例如,沪教版初中化学九年级下册第8章中的“葡萄糖的检验”实验,步骤为:在试管中加入2mL 10%的氢氧化钠溶液,滴加5%的硫酸铜溶液4—5滴,混合均匀;再向上述试管中加入几滴10%的葡萄糖溶液,并在酒精灯上加热至沸腾。这是利用硫酸铜与氢氧化钠反应制得氢氧化铜,氢氧化铜与葡萄糖在加热条件下反应生成氧化亚铜。本实验的关键是:需要用新制的氢氧化铜;制取氢氧化铜的反应需要在较强的碱性环境下进行;与葡萄糖混合后需要加热。
为了凸显实验步骤的关键之处,教师可增加对比实验,并引导学生根据实验现象的不同理解实验步骤的原理。增加对比实验后的实验过程如下:(1)取适量实验室现有的氢氧化铜固体于试管A中,加入2mL 10%的氢氧化钠溶液,然后加入适量葡萄糖溶液,振荡,加热,观察现象。(2)在试管B中加入6mL 10%的氢氧化钠溶液,滴加5%的硫酸铜溶液12—15滴,混合均匀,观察现象;然后分出约13到试管C中,约13到试管D中;加热试管B,在C、D两试管中分别加入适量葡萄糖溶液,充分振荡后静置试管C,加热试管D,观察现象。(3)在试管E中加入2mL 5%的硫酸铜溶液,滴加10%的氢氧化钠溶液4—5滴,混合均匀,观察现象;加热试管E,观察现象。
学生通过试管A与试管D中的不同现象,可以理解检验葡萄糖需要用新制的氢氧化铜。由此,学生会自然生发的问题是:新制的氢氧化铜与已有的氢氧化铜有什么不同?从试管B与试管E中出现的沉淀颜色的不同,结合试管B加热后蓝色沉淀转变为黑色固体,而试管E加热后没有明显变化,可以推出两种沉淀是不同物质,由此理解检验葡萄糖需要在碱性环境下新制氢氧化铜。自然引发的下一个问题是:不在碱性环境下生成的沉淀是否也能与葡萄糖反应?由试管C不加热的,蓝色沉淀变为深蓝色沉淀,试管D加热后,蓝色沉淀最终转变为砖红色沉淀,可以理解检验葡萄糖的实验需要在加热条件下才能实现。引发的下一个问题是:是否一定需要加热至沸腾?略微加热是否可行?在试管D加热至沸腾的过程中,可以观察到先出现黑色沉淀,然后变为砖红色。学生就会思考:黑色沉淀是什么?是否为氧化铜?后又变为砖红色是氧化铜与葡萄糖反应的结果吗?
初中阶段,并不要求学生掌握葡萄糖的检验方法与原理,所以这部分内容仅在教材的《拓展视野》中出现。补充对比实验的目的并不在于让学生掌握某个知识点,而在于充分利用对实验步骤的分析,加深学生对实验原理的理解;同时,能激发学生的兴趣,引发后续的探究问题,发展学生的探究欲。
二、 关注尾气处理,树立生态文明的理念
化学实验中通常会涉及有害气体,任意排放会环境污染。因此,在相关实验教学中,可有意识地引导学生关注尾气处理,思考如何避免污染环境,促使学生培养保护环境的习惯和意识,树立生态文明的理念。
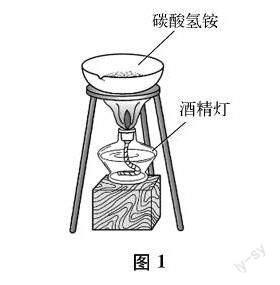
例如,沪教版初中化学九年级上册第1章中的“加热碳酸氢铵”实验,装置如图1所示。
教学中,教师首先按照图1组装实验装置,进行演示实验,请学生观察实验现象;然后提供氨气和二氧化碳的部分信息,并提出三个问题:实验中用到的容器是什么?实验中的产物去哪里了?实验对环境是否有影响?
学生讨论后认为:实验中选择蒸发皿作为反应的容器,蒸发皿是不可能密封的,所以实验中的产物逸散到了空气中;加热碳酸氢铵后的产物中有氨气,根据信息提示,氨气是一种有毒的气体,会污染空气。
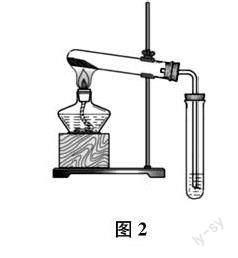
教师顺势引导学生思考:老师想让每一位同学都做一遍这个实验,你们觉得是否妥当?学生由于已经意识到该实验会产生有毒气体污染环境,所以一致认为是不妥当的。顺势,师生一起思考、探究实验装置的改进,最终得到如图2所示的实验装置。
改进后的实验装置有如下优点:选用试管作为反应容器,易密封;另取一支试管盛放澄清石灰水,并把产生的气体通入其中,通过澄清石灰水变浑浊可证明产物中有二氧化碳气体,试管口有小水珠能证明反应生成了水,这些现象充分说明了该反应是有新物质生成的化学变化;氨气是极易溶于水的气体,澄清石灰水能够部分溶解产生的氨气,处理一部分尾气。此外,还可以在盛有澄清石灰水的试管口塞入双孔橡胶塞,接上气球,用以收集尾气,然后集中处理。
三、 优化实验方案,锤炼严谨求实的科学态度
化學实验设计主要考虑以下几个原则:科学性、可行性、安全性、简约性、效果明显。这也是优化实验设计的方向。对此,教师可带领学生通过对实验方案的优化,初步学会批判性思维的方法,锤炼严谨求实的科学态度。
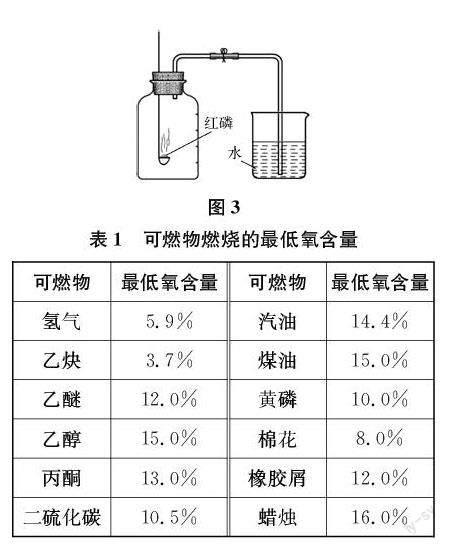
例如,沪教版初中化学九年级上册中的“空气中氧气体积分数的测定”实验,原料是红磷;原理是利用红磷燃烧消耗密闭空间内空气中的氧气,使密闭空间内的压强减小,“压迫”水进入集气瓶中,根据进入集气瓶中水的量推断空气中氧气的体积分数;装置如图3所示。
教学时,教师提供几种可燃物燃烧的最低氧含量数据(如表1所示),请学生讨论分析该实验是否有可以改进的地方。
表1可燃物燃烧的最低氧含量
可燃物最低氧含量可燃物最低氧含量氢气5.9%汽油14.4%乙炔3.7%煤油15.0%乙醚12.0%黄磷10.0%乙醇15.0%棉花8.0%丙酮13.0%橡胶屑12.0%二硫化碳10.5%蜡烛16.0%在教师的指导下,学生交流的成果如下:
(1)该实验的原理是利用红磷燃烧消耗密闭容器内空气中的氧气,那红磷在密闭容器中燃烧能把其中的氧气消耗完吗?
学生虽然没有看到红磷燃烧需要的最低氧含量,但是根据表格数据分析,认为:可燃物燃烧一般都需要达到一定的氧含量,当氧含量低于阈值时,可燃物不会燃烧起来或燃着的物质会熄灭。因此,该实验中尽管红磷过量,但是当红磷熄灭时,并不可能耗尽密闭容器内的所有氧气,所以进入集气瓶中水的量最多只能是消耗掉的氧气在空气中的体积分数,而并非全部氧气在空气中的体积分数。如果其他操作都合理正确的话,那么进入集气瓶的水应小于集气瓶容积的五分之一。因而,要通过消耗氧气来测定空气中氧气的体积分数的话,需要选择能将氧气耗尽的物质和反应。
(2)实验操作时存在不可避免的误差,怎么办?
通过演示实验,学生认为该实验对操作要求比较高,其中之一是“将点燃的红磷迅速伸入集气瓶内,塞紧橡皮塞”。尽管教师在操作时已经很迅速了,学生还是观察到,在将红磷伸入集气瓶时就有白烟从瓶口冒出。白烟是可以看到的,看不到的一些气体是否也“逃”出来了?很难保证没有气体因红磷燃烧放热而被排出集气瓶,那么进入集气瓶内的水就会有所增加。
(3)实验装置是否也会导致误差产生?怎么解决?
学生认为,装置不是一体的,整套装置涉及橡胶塞打孔,一个孔容纳导管插入,另一个孔容纳燃烧匙插入,玻璃导管上要连接橡胶导管,并使用止水夹。这些连接都要求密封性良好,否则会产生较大的实验误差。
在学生分析的基础上,教师提示学生对比拉瓦锡的实验(装置如图4所示)。学生发现,拉瓦锡的实验的原料是汞,原理是汞在加热条件下消耗氧气,使密闭容器内压强减小,液面上升,根据上升的量推断空气中氧气的体积分数,不存在燃烧也就不存在最低需要的氧含量,能将空气中的氧气耗尽。该实验的密封性很容易做到,曲颈甑伸入玻璃钟罩,而玻璃钟罩扣在汞槽中,汞起到液封的作用。
学生基于前面实验的经验,讨论后觉得可以利用“铁的锈蚀”实验(装置如图5所示)进行替换。铁锈蚀会消耗氧气,虽然同样也会存在最低检测含量的问题,但是不燃烧的氧化对氧含量的要求低许多,结果会更接近事实;操作也比较简便,动作快慢都没有影响。
教师追问:同样会有装置密封性问题,能否简单地做到装置密封?能否比较精确地观察到氧气被消耗的量?
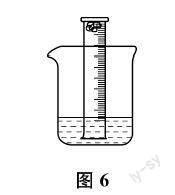
在教师的提示与引导下,学生讨论得到如图6所示的实验装置。可采取的实验步骤如下:取一些细铁丝绕成球,用稀盐酸除去铁锈后,塞到一只10mL量程的量筒底部;然后在量筒内装入少量水,拇指按住量筒口,把量筒倒放在一只盛有水的大烧杯中,读出此时量筒内液面的刻度V1;每天观察现象,一周后再读出量筒内液面的刻度V2;两次液面刻度的差V1-V2(由于量筒倒放,所以水越多刻度越小),即可看作消耗掉的氧气的体积,再除以10-V1,就得到氧气在空气中的体积分数。
本实验对操作的要求较低,学生容易做到,而且能够熟悉量筒的使用。通过每天的观察,学生能体会到有些反应的发生是比较缓慢的。随着每天液面的不斷上升,学生探究的兴趣将持续被缴发。学生还会发现一个实验可以有多种用途,之前学习的实验稍作改进就能用作后续的研究。
参考文献:
[1][2] 中华人民共和国教育部.义务教育化学课程标准(2022年版)[S].北京:北京师范大学出版社,2022:5,7.设计指南
