COPD伴肺动脉高压患者血清HMGB1、TNF-α与病情、肺功能的相关性
2023-05-21王璀瑛陈辉耿芳吴瑞丽吴旭瑞李丽娜
王璀瑛 陈辉 耿芳 吴瑞丽 吴旭瑞 李丽娜
对于慢性阻塞性肺疾病(Chronic Obstructive Pulmonary Disease,COPD)患者而言,肺功能受损是其生活质量下降的主要困扰原因。COPD 患者自身肺部炎性介质增加破坏了肺部组织结构,导致机体出现胸闷气喘、组织水肿及乏力等表现[1]。随着疾病的发展,肺组织进一步被破坏,导致血管异常病变引发肺动脉高压,加重肺血管阻力,导致右心室受压增加,引发右心室肥厚,造成右心衰竭,提高了肺动脉高压患者的致死率[2-4]。为提高COPD 合并肺动脉高压患者的存活率,临床学者对该病病情进展及肺功能各项指标变化进行全面分析,发现血清高迁移率组蛋白B1(High Mobility Group,HMGB1)与肿瘤坏死因子α(Tumor Necrosis Facto,TNF-α)能一定程度上反映COPD 合并肺动脉高压患者肺功能状态[4]。而任旭斌等学者[5]也曾提出过一致观点。因此本文主要探讨血清HMGB1、TNF-α 与COPD 伴肺动脉高压患者病情、肺功能的相关性。报道如下。
1 资料与方法
1.1 一般资料
选取2017 年3 月至2021 年12 月期间郑州市第七人民医院收治的122 例COPD 伴肺动脉高压患者作为治疗组进行研究,另选取115 名健康体检者设对照组。治疗组患者男86 例,女36 例,平均年龄(64.11±7.58)岁;对照组男75 名,女40 名,平均年龄(63.01±7.22)岁。两组性别、年龄等资料比较差异统计学意义(P>0.05),有可比性。
纳入标准:①符合《慢性阻塞性肺疾病治疗新进展》[6]并确诊为COPD;②符合《我国肺动脉高压专家共识阐释》中肺动脉高压的诊断标准[7];③所有COPD 患者均为首次治疗,既往未服用过相关治疗药物;④所有患者肺动脉收缩压均超过40 mmHg;排除标准:①患有先天性心脏病患者;②合并出现其他肺部严重疾病者;③有左心室衰竭患者;④近半年内有大型手术史患者。本研究获得医学伦理委员会同意批准,所有研究对象均签署研究知情同意书。
1.2 方法
收集治疗组患者治疗前、对照组志愿者空腹状态下下的肘静脉血4 mL,3 000 r/min 离心15 min,离心半径10 cm,取血清制成检测样本,放置低温下储存,由一位专业检测人员将所有样本统一进行检测。采用双抗体夹心法联合全自动酶标仪(型号:ELx800,美国博腾仪器有限公司,国械注进20192220616)检查血清样本中TNF-α 因子水平。采用HMGB1 酶联免疫试剂盒(规格:48T,江苏莱尔生物医药科技有限公司,ZDJ1800539)联合酶联免疫吸附法检测HMGB1 因子水平。
肺功能检测:采用肺功能仪(型号:MSA99,北京麦邦光电仪器有限公司,京械注准20182210193)检测治疗组患者治疗前、对照组志愿者第1 秒用力呼吸容积占用力肺活量的百分比(Forced Expiratory Volume in One Second/Forced Vital Capacity,FEV1/FVC%)、用力肺活量(Forced Vital Capacity,FVC)。
肺动脉压测定:由专业检验科医生对治疗组患者治疗前、对照组志愿者进行超声心动图检查,采用超声心动仪(型号:A8200S2P,深圳市安保科技有限公司,粤械注准20172231485)检测受检者的肺动脉收缩压。
1.3 观察指标
对比两组HMGB1、TNF-α 水平、肺功能及肺动脉压。对比不同病情的三亚组治疗前HMGB1、TNF-α 水平:根据治疗组患者病情情况进行分组,分为COPDⅠ组:处于急性期初期,可经门诊治疗,COPDⅡ组:处于急性期且需住院治疗,COPDⅢ组:病情严重需ICU 进行抢救治疗[8]。对比三亚组治疗前肺功能及肺动脉压。分析肺功能相关指标与HMGB1、TNF-α 因子的相关性。
1.4 统计学方法
采用SPSS 27.0 统计学软件分析数据,计量资料采用()的形式表示,组间比较采用t检验,多组间比较采用F检验;采用Spearman相关性分析肺功能相关指标与HMGB1、TNF-α 因子的关系,以P<0.05 为差异具有统计学意义。
2 结果
2.1 两组HMGB1、TNF-α 水平、肺功能及肺动脉压比较
治疗组HMGB1、TNF-α 水平及肺动脉收缩压均高对照组,FVC、FEV1/FVC%均低于对照组,差异有统计学意义(P<0.05)。见表1。
表1 两组HMGB1、TNF-α 水平、肺功能及肺动脉压比较(±s)Table 1 Comparison of HMGB1,TNF-α levels,pulmonary function and pulmonary artery pressure between the two groups(±s)
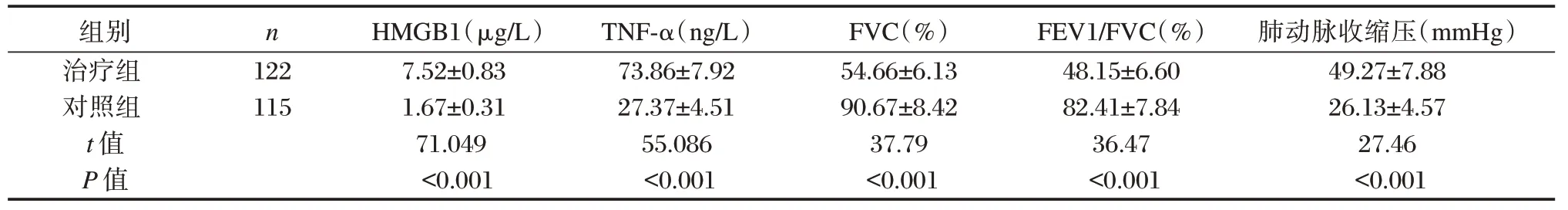
表1 两组HMGB1、TNF-α 水平、肺功能及肺动脉压比较(±s)Table 1 Comparison of HMGB1,TNF-α levels,pulmonary function and pulmonary artery pressure between the two groups(±s)
2.2 不同病情患者治疗前HMGB1、TNF-α水平对比
治疗组患者中,COPDⅠ患者有40 例,COPDⅡ有52 例,COPDⅢ患者有30 例。三亚组患者HMGB1、TNF-α 因子水平:COPDⅢ组>COPDⅡ组>COPDⅠ组,差异有统计学意义(P<0.05)。见表2。
表2 不同病情患者治疗前HMGB1、TNF-α水平对比(±s)Table 2 Comparison of HMGB1 and TNF-α levels in patients with different conditions before treatment(±s)
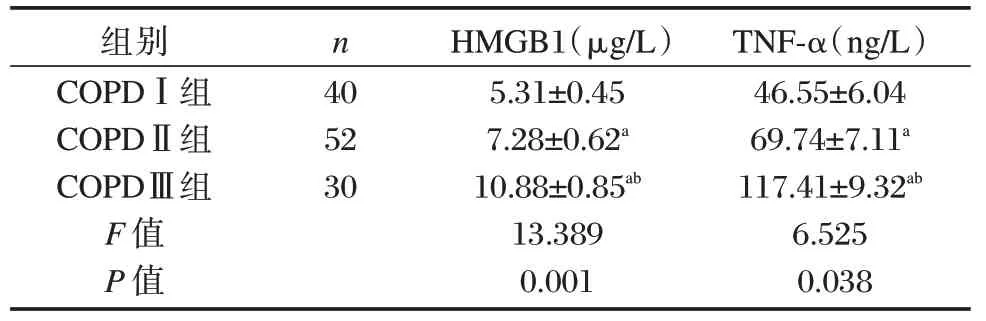
表2 不同病情患者治疗前HMGB1、TNF-α水平对比(±s)Table 2 Comparison of HMGB1 and TNF-α levels in patients with different conditions before treatment(±s)
注:与COPDⅠ组比较,aP<0.05,与COPDⅡ组比较,bP<0.05。
2.3 不同病情患者治疗前的肺功能及肺动脉压对比
三亚组患者FVC、FEV1/FVC:COPD Ⅲ组<COPDⅡ组<COPDⅠ组,肺动脉收缩压:COPDⅢ组>COPDⅡ组>COPDⅠ组,差异有统计学意义(P<0.05)。见表3。
表3 不同病情患者治疗前肺功能及肺动脉压比较(±s)Table 3 Comparison of pulmonary function and pulmonary artery pressure before treatment in patients with different conditions(±s)
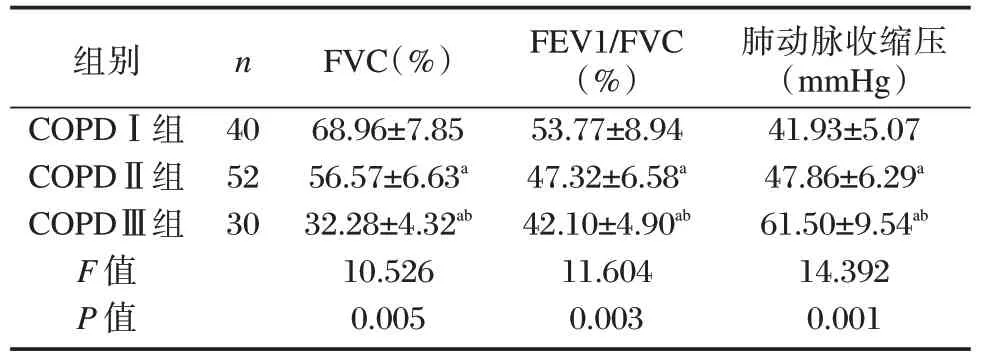
表3 不同病情患者治疗前肺功能及肺动脉压比较(±s)Table 3 Comparison of pulmonary function and pulmonary artery pressure before treatment in patients with different conditions(±s)
注:与COPDⅠ组比较,aP<0.05,与COPDⅡ组比较,bP<0.05。
2.4 肺功能相关指标与HMGB1、TNF-α 因子的相关性
HMGB1、TNF-α 因子水平与FEV1/FVC%、FVC 呈负相关,与肺动脉收缩压呈正相关(P<0.05)。见表4。
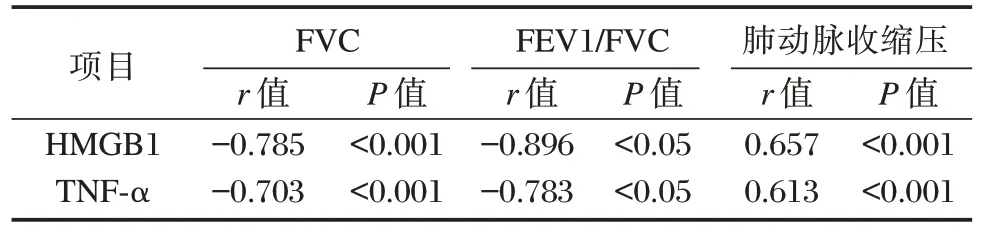
表4 肺功能相关指标与HMGB1、TNF-α 因子的相关性Table 4 Correlation between lung function related indexes and HMGB1 and TNF-α factors
3 讨论
COPD 是一种进行性发展的疾病,会对呼吸道造成不可逆性损伤。COPD 患者肺功能指标的改变可反映患者病情进展,同时也能反映患者肺功能障碍程度,对COPD 的治疗及诊断都有较高价值[8-9]。当肺部严重受损时会引发机体出现肺动脉高压等合并症,进而对右心室造成损伤,加速身体机能下降程度,损害患者生命。
近些年来,临床对如何快速有效地监测COPD伴肺动脉高压患者病情程度展开了大量研究[10]。研究学者常对COPD 患者体内白介素、内皮素等相关因子水平变化进行探究,并证实其相关因子可在临床医生评估患者病情时提供有效帮助[11-12]。HMGB1 是一种炎性介质因子,与白介素等有密切相关性,为此,本文猜测HMGB1、TNF-α等炎性介质因子对COPD 伴肺动脉高压同样具有评估价值。本文结果发现,治疗组HMGB1、TNF-α 水平及肺动脉收缩压均高对照组,其FVC、FEV1/FVC%均低于对照组,与国外Scarlata、Chrtstopher等[13-14]研究基本一致。说明COPD 伴肺动脉高压患者HMGB1、TNF-α 呈高水平表达,进一步分析其原因为,HMGB1 具有较强的免疫刺激性,当机体肺部组织出现病变损伤时,HMGB1 会激活B 细胞进行免疫应答,同时促进炎性因子的表达,从而参与COPD 患者的病变过程[15-16]。TNF-α 是常见的炎症细胞因子,其水平变化反映机体炎症反应情况[17]。而肺部出现炎症反应是呼吸系统疾病患者最主要的致病原因,炎性介质因子通过破坏肺部结构,引发机体氧化应激反应,加速机体损伤。本文进一步对COPD 伴肺动脉高压患者的不同病情进行深入研究结果与鲁立文等[18]在研究中提出的观点相符。说明COPD 伴肺动脉高压患者病情越严重其体内HMGB1、TNF-α 水平越高,而其肺部功能障碍越严重。分析其原因,机体HMGB1、TNF-α 等炎性介质水平上升后促使机体内炎症反应大幅度增加,进一步损害患者肺部组织,加重肺动脉压力,造成机体循环障碍导致病情恶化。结果间接证实HMGB1、TNF-α 与COPD 伴肺动脉高压患者病情发展呈正相关。Vasquez[19]认为HMGB1、TNF-α 两种因子的增长也能反映出COPD 患者肺功能损伤程度。本研究结果表明,HMGB1、TNF-α 因子水平与FEV1/FVC%、FVC 呈负相关,与肺动脉收缩压呈正相关,娄明远等[20]在研究COPD 炎性因子与肺功能关系时提出的观点相符。推测HMGB1、TNF-α 能作为机体肺功能损伤程度的评估指标,对评断患者病情发展、肺动脉压再升高等均有一定指导意义。
综上,COPD 伴肺动脉高压患者血清HMGB1、TNF-α 升高能有效反映其病情进展及机体肺功能情况,可为临床进一步诊断及治疗提高参考资料。
