丹参活性部位丹参二萜醌羟丙基-β-环糊精包合物的制备工艺研究
2023-05-20刘慧芳刘泽莹楼招欢张光霁
苏 行,刘慧芳,刘泽莹,楼招欢,张光霁
丹参活性部位丹参二萜醌羟丙基-β-环糊精包合物的制备工艺研究
苏 行1,刘慧芳2,刘泽莹2,楼招欢2,张光霁1*
1. 浙江中医药大学基础医学院,浙江省中医“瘀毒”证重点实验室,浙江 杭州 310053 2. 浙江中医药大学药学院,浙江 杭州 310053
优化丹参二萜醌(diterpenoid tanshinone,DT)羟丙基-β-环糊精(hydroxypropyl-β-cyclodextrin,HP-β-CD)包合物(inclusion complex,IC)(DT&HP-β-CD@IC)制备工艺。在单因素试验的基础上,选择DT与HP-β-CD的配比、包合温度、包合时间为考察因素,以DT包封率及包合物载药量为综合评价指标,利用Box-Behnken响应面优化DT&HP-β-CD@IC制备工艺,并采用红外光谱法、紫外光谱法、薄层色谱法及扫描电子显微镜法对DT&HP-β-CD@IC进行评价。DT&HP-β-CD@IC最佳制备工艺为HP-β-CD质量浓度0.1 g/mL,药物与载体材料配比1∶3,包合时间2 h,包合温度40 ℃。DT&HP-β-CD@IC的包封率达68.78%,载药量达5.44%。紫外、红外光谱和薄层色谱等结果表明DT&HP-β-CD@IC的形成。DT&HP-β-CD@IC载药量较高,溶解性有一定的提高。
丹参;活性部位;丹参二萜醌;羟丙基-β-环糊精;包合物;Box-Behnken响应面;二氢丹参酮I;隐丹参酮;丹参酮I;丹参酮IIA
丹参为唇形科丹参属植物丹参Bunge的干燥根及根茎,具有活血、化瘀、益气等显著功效,为临床常用活血祛瘀药之一[1]。丹参二萜醌(diterpenoid tanshinone,DT)部位为本课题组前期从丹参中提取获得的二萜醌类成分,在体内外均显示了良好的抗肺癌作用,该作用与DT促进肺癌细胞凋亡、改善肺癌炎症微环境和微循环障碍有关[2-4]。但是DT水溶性极小,生物利用度低下,影响其疗效和成药性,临床使用受到限制。包合物(inclusion compound,IC)是一种分子全部或部分被包藏于另一种分子的空穴结构内形成的络合物[5]。作为一种新型的药物制剂技术,包合物可以提高难溶性药物的溶解度,增加其生物利用度及药物溶出度[6],增加治疗效果;并可以增加药物稳定性、减少药物的不良反应和刺激性以及掩盖药物的不良臭味等[7]。
羟丙基-β-环糊精(hydroxypropyl-β-cyclodextrin,HP-β-CD)属于包合物(CD)衍生物中的水溶性环糊精衍生物,是目前应用最广泛的包合材料,具有外侧亲水、内侧疏水空腔结构,在水中溶解度较大,室温(25 ℃)可高达0.75 g/mL,其水溶液中质量浓度低于0.40 g/mL时,流动性良好,不黏稠[8-9],在增加药物溶解度、提高稳定性和生物利用度方面发挥着重要作用[10-11],本实验采用不饱和水溶液法制备丹参二萜醌羟丙基-β-环糊精包合物(DT&HP-β-CD@IC),对DT药效部位中丹参酮IIA、丹参酮I、隐丹参酮及二氢丹参酮I进行包合,以载药量为主要考察指标,获得包合物的制备工艺,并对其进行验证,以期得到一种可以提高DT溶解度,增加其生物利用度,且制备工艺简便的剂型。
1 仪器与材料
1.1 仪器
Agilent 1200型高效液相色谱仪,美国Agilent有限公司;KQ-500B型超声波清洗器,昆山市超声仪器有限公司;Millipore型超纯水系统,美国Milli- Q Biocel公司;XS105DU型十万分之一天平,瑞士Mettler Toledo公司;DK-S26型电热恒温水浴锅、DGG-9070B型电热恒温鼓风干燥箱,上海森信实验仪器有限公司;SHZ-B型水浴恒温振荡器,上海百典仪器设备有限公司;Thermo Sorvall ST-8R型台式高速冷冻离心机、Nicolet IS50型傅里叶变换红外光谱仪,美国Thermo公司;UV-3600型紫外分光光度计,日本岛津公司;Camag型薄层色谱数码成像系统、Camag Linomat 5型半自动点样仪,瑞士Camag公司。
1.2 药品与试剂
丹参饮片,批号20050101,产地山东,浙江中医药大学饮片有限公司,饮片经浙江中医药大学中药饮片有限公司钱敏副主任中药师鉴定为唇形科丹参属植物丹参Bunge的干燥根和根茎;对照品丹参酮IIA(批号B20257)、丹参酮I(批号B20256)、隐丹参酮(批号B21586)、二氢丹参酮I对照品(批号B20357),质量分数均≥98%,上海源叶生物科技有限公司;分析纯乙酸、甲醇,上海凌峰化学试剂有限公司;分析纯95%乙醇,华东医药股份有限公司;色谱级乙腈、甲醇,德国默克股份有限公司;HP-β-CD,批号S11011,上海源叶生物科技有限公司;溴化钾,批号P116270,上海阿拉丁生化科技股份有限公司;DT样品,实验室自制;硅胶G板,批号20180122,青岛海洋化工有限公司制造。
2 方法与结果
2.1 DT的制备
称取山东产地丹参药材250 g,加入到3000 mL圆底烧瓶中,加2500 mL 95%乙醇,浸泡1.0 h,60 ℃提取2次,每次1 h,合并所得提取液,提取液抽滤,滤液浓缩到一定体积,按照1∶1的比例加入石油醚[12]萃取5次,回收石油醚,称量固形物质量1.725 g,经过石油醚萃取后DT部位的平均得率为0.69%,平均质量分数为20.03%。
2.2 DT&HP-β-CD@IC的制备
选用不饱和水溶液法[13]制备DT&HP-β-CD@ IC。称取1 g HP-β-CD溶于10 mL水中配制成0.1 g/mL的HP-β-CD不饱和水溶液,常温下置于超声仪中充分超声溶解,称取25 mg DT溶于少量甲醇中,缓慢滴加至HP-β-CD不饱和水溶液中,30 ℃下超声1 h,使药物分子被充分包合,然后用石油醚洗涤3次除去未被包合的药物分子,洗涤后的溶液水浴蒸干,即得DT&HP-β-CD@IC粉末。
2.3 DT成分含量测定方法的建立
2.3.1 色谱条件 色谱柱为 XB-C18柱(250 mm×4.6 mm,5 μm);流动相为乙腈-0.2%乙酸水溶液(57∶43);检测波长270 nm;柱温30 ℃;进样量10 μL;体积流量1.0 mL/min;理论塔板数按二氢丹参酮I计算不低于10 000。
2.3.2 对照品溶液的制备 取丹参酮IIA对照品7.41 mg、丹参酮I对照品2.80 mg、隐丹参酮对照品3.63 mg、二氢丹参酮I对照品1.92 mg,分别置于10 mL量瓶中,加甲醇定容。精密移取各对照品溶液5 mL于25 mL量瓶中,加甲醇定容至刻度,制得含丹参酮IIA148.2 μg/mL,丹参酮I 56.0 μg/mL,隐丹参酮72.6 μg/mL,二氢丹参酮I 38.4 μg/mL的混合对照品储备溶液。
2.3.3 DT&HP-β-CD@IC供试品溶液的制备 精密称取DT&HP-β-CD@IC 5 mg,少量甲醇超声溶解,再定溶于1 mL量瓶中,得到DT&HP-β-CD@IC供试品溶液。
2.3.4 HP-β-CD空白对照溶液的制备 精密称取空白HP-β-CD适量,按照“2.3.3”项下方法制备HP-β-CD空白供试品溶液。
2.3.5 分析方法专属性 取DT混合对照品储备溶液、HP-β-CD空白对照溶液、DT&HP-β-CD@IC供试品溶液,按“2.3.1”项下色谱条件进样分析,所得色谱图如图1所示,可知,样品中辅料不会干扰目标成分的测定,表明该分析方法专属性良好。
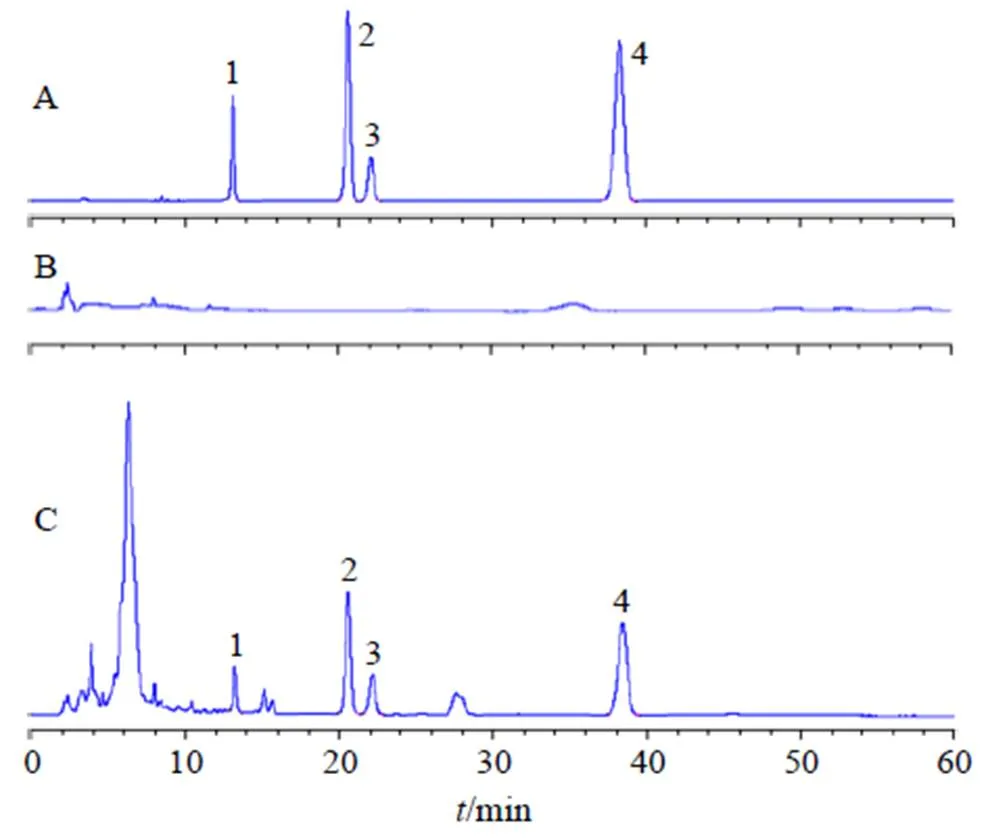
1-二氢丹参酮I 2-隐丹参酮 3-丹参酮I 4-丹参酮IIA
2.3.6 线性关系考察 分别精密量取混合对照品储备溶液0.5、1.0、2.0、3.0、4.0、5.0 mL置5 mL量瓶中,用甲醇定容至刻度,摇匀,得到系列对照品溶液。按“2.3.1”项下色谱条件进样分析,以质量浓度为横坐标(),峰面积为纵坐标(),绘制标准曲线,进行线性回归,得回归方程:丹参酮IIA=55.069+30.373,=0.999 9,线性范围14.82~148.20 µg/mL;丹参酮I=33.372-0.015 1,=0.999 8,线性范围5.60~56.00 µg/mL;隐丹参酮=46.110+2.452 7,=0.999 9,线性范围7.26~72.60 µg/mL;二氢丹参酮I=33.606+3.216 4,=0.999 8,线性范围3.84~38.40 µg/mL。结果表明,4个成分具有良好的线性关系。
2.3.7 精密度试验 取适量“2.3.3”项下DT&HP-β-CD@IC供试品溶液,按“2.3.1”项下色谱条件进样分析,连续进样6次,计算日内精密度,结果丹参酮IIA、丹参酮I、隐丹参酮、二氢丹参酮I峰面积的RSD分别为0.27%、0.40%、0.34%、2.38%,说明仪器精密度良好。
2.3.8 稳定性试验 取适量“2.3.3”项下DT&HP-β-CD@IC供试品溶液,分别于0、2、4、6、8、10、12、24 h进样,依法测定,记录峰面积,计算丹参酮IIA、丹参酮I、隐丹参酮、二氢丹参酮I峰面积的RSD分别为1.30%、1.39%、1.44%、2.66%,表明供试品溶液在室温条件下24 h内稳定。
2.3.9 重复性试验 按“2.3.3”项下方法平行制备DT&HP-β-CD@IC供试品溶液6份,按“2.3.1”项下色谱条件进样分析,测得丹参酮IIA、丹参酮I、隐丹参酮、二氢丹参酮I的质量分数分别为1.71、11.99、0.16、0.55 mg/g,RSD分别为2.48%、2.40%、3.88%、2.28%,表明该方法重复性良好。
2.3.10 加样回收率试验 取已测定DT含量的DT&HP-β-CD@IC粉末6份,分别加入1∶1 DT含量的混合对照品溶液,按“2.3.1”项下色谱条件进样分析,进样量为10 μL,计算加样回收率,结果丹参酮IIA、丹参酮I、隐丹参酮、二氢丹参酮I的平均加样回收率分别为95.6%、95.4%、95.3%、102.7%,RSD分别为3.11%、2.11%、1.37%、3.39%。
2.4 DT&HP-β-CD@IC制备工艺考察
2.4.1 DT&HP-β-CD@IC包封率、载药量的测定 采用超声法[14]测定包合物的包封率和载药量。
包封率=包合物中指标成分的质量/指标成分的实际投入量
载药量=包合物中指标成分的质量/包合物质量
包合物得率=包合物的质量/(HP-β-CD的质量+指标成分的实际投入量)
2.4.2 DT&HP-β-CD@IC制备工艺单因素考察 采用不饱和水溶液法制备DT&HP-β-CD@IC,分别以DT与HP-β-CD的配比、包合时间、包合温度为影响因素,对DT&HP-β-CD@IC包封率和载药量进行考察,包合物包封率与后期制作成本密切相关,载药量能提高DT的溶解度,因此,本实验选择包合物的包封率和载药量2个指标进行综合考量。
(1)DT与HP-β-CD配比考察:控制药物DT与载体材料HP-β-CD的配比分别为1∶25、1∶20、1∶15、1∶10、1∶5、1∶4、1∶3、1∶2、1∶1,称取不同质量DT加适量甲醇溶解,缓慢滴入到10 mL质量浓度为0.1 g/mL的HP-β-CD不饱和水溶液中,30 ℃下超声1 h包合,控制其他因素,按照“2.2”项下制备工艺进行制备,考察包封率、载药量以及包合物得率随DT与HP-β-CD配比变化的情况,结果见表1。结果显示,载药量随着DT与HP-β-CD配比的增加而先增加后降低,包封率和包合物得率与二者配比呈反比,因此,在选择时要综合选择包封率和载药量都较大的情况。
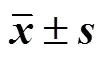
表1 DT与HP-β-CD配比考察结果(, n = 3)
(2)DT与HP-β-CD包合时间考察:控制DT与HP-β-CD的包合时间分别为0.5、1.0、2.0、3.0、4.0 h,称取25 mg DT溶于少量甲醇中,缓慢滴入到10 mL质量浓度为0.1 g/mL的HP-β-CD不饱和水溶液中,30 ℃下超声不同时间包合,控制其他因素,按照“2.2”项下制备工艺进行制备,考察包封率、载药量以及包合物得率随包合时间变化的情况,结果见表2。结果显示,当包含时间在1.0、2.0、3.0 h时载药量最大,考虑到后期的加工成本问题,选择包合物得率最高的2.0 h较为合适。
(3)DT与HP-β-CD包合温度考察:控制DT与HP-β-CD的包合温度分别为30、35、40、45、50 ℃,称取25 mg DT溶于少量甲醇中,缓慢滴入到10 mL质量浓度为0.1 g/mL的HP-β-CD不饱和水溶液中,不同温度下超声1 h包合,控制其他因素,按照“2.2”项下制备工艺进行制备,考察包封率、载药量以及包合物得率随包合温度变化的情况,结果见表3。结果显示,随着包合温度的增加,包封率、载药量以及包合物得率呈现先上升后降低的趋势,当包合温度为35 ℃时包合物的载药量和包封率最大。
2.4.3 Box-Behken响应面法优化DT&HP-β-CD@IC的制备工艺
(1)实验设计与结果:在上述单因素试验的基础上,采用Design-Expert 12.0软件对DT&HP-β-CD@IC进行工艺优化。控制制备工艺中HP-β-CD的质量浓度为0.1 g/mL,采用Box-Behken响应面设计,以包合物的包封率和载药量作为考察指标,对制备工艺中药物DT与载体材料HP-β-CD的配比(1)、包合时间(2)、包合温度(3)进行优化,以期得到DT&HP-β-CD@IC的最佳制备工艺。Box-Behken实验设计与结果见表4。
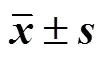
表2 DT与HP-β-CD包合时间考察结果(, n = 3)
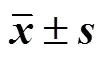
表3 DT与HP-β-CD包合温度考察结果(, n = 3)
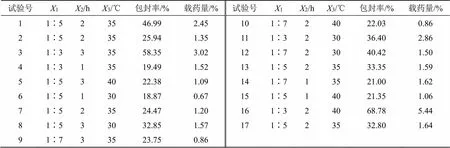
表4 Box-Behnken响应面组合实验设计及结果
(2)响应面模型拟合分析:运用Design-Expert 12.0软件对表4中的数据进行分析,分别对各个考察因素与包封率和载药量之间的关系进行方程拟合,包封率和载药量的方差分析结果见表5。包封率和载药量的拟合方程为包封率=32.71-9.481+7.082+0.753-9.0312-12.6913-3.2423+7.9912-10.0522+1.2132;载药量= 1.65-1.001+0.208 82+0.231 33-0.565 012-0.805 013-0.217 523+0.838 312-0.729 322+0.180 832。

表5 包合物中包封率和载药量的方差分析结果
由表5中的数据可知,包封率和载药量模型的<0.05,具有显著性差异,从而具有统计学意义。模型中考察指标的失拟项>0.05,不具有显著性差异,因而无统计学意义,该模型在预测过程中无失拟项因素存在,拟合性较好,可以对包合物的包封率和载药量进行下一步分析与预测。
由表值可以看出,包封率的影响因素中1、2、13、22项具有显著性差异,载药量的影响因素中1、12项具有显著性差异,说明自变量因素中对包合物包封率和载药量影响较为显著的是HP-β-CD与DT配比以及包合时间这2个因素。
以上结果显示运用该模型可以对实验结果进行一定的分析和预测,用来优化DT&HP-β-CD@IC的制备工艺。
(3)响应面实验结果优化与预测:根据上述实验结果的分析,运用Design-Expert 12.0软件,对包合物包封率和载药量的三维响应曲面图进行绘制。包封率和载药量的三维响应曲面图见图2。
通过分析图2可以得出,HP-β-CD与DT配比、包合温度这2个因素之间的交互作用对DT&HP-β-CD@IC的包封率影响较为显著。通过该软件优化得到的DT&HP-β-CD@IC最佳制备工艺为药物与载体材料的配比为1∶3,反应时间为2.5 h,反应温度为40 ℃,在此条件下得到包封率预测值为68.78%、载药量的预测值4.80%。
(4)工艺验证实验:按最佳制备工艺平行制备3批DT&HP-β-CD@IC,重复测定其包封率和载药量,与模型预测结果进行相应比较,以此来验证模型的可靠性。包封率和载药量的测定结果见表6。结果显示,DT&HP-β-CD@IC的包封率和载药量平均实测值分别为63.49%、5.17%。

图2 DT&HP-β-CD@IC的包封率和载药量响应曲面图
2.5 DT&HP-β-CD@IC的表征
2.5.1 外观 对得到的DT&HP-β-CD@IC粉末进行观察,为黄棕色粉末,结果见图3。
2.5.2 薄层色谱法 取丹参酮IIA对照品溶于甲醇溶液,得到样品1;丹参酮I对照品溶于甲醇溶液,得到样品2;隐丹参酮对照品溶于甲醇溶液,得到样品3;二氢丹参酮I对照品溶于甲醇溶液,得到样品4;HP-β-CD溶于蒸馏水,得样品5;称取DT样品,溶于适量甲醇溶液,得到样品6;称取DT&HP-β-CD@IC溶于适量甲醇溶液,得到样品7。照薄层色谱法(《中国药典》2020年版四部通则0502)试验,吸取上述6种溶液各5 μL,分别点于同一硅胶G薄层板上,以石油醚(60~90 ℃)-醋酸乙酯(5∶1)为展开剂,展开,取出,晾干。由图4可知,DT&HP-β-CD@IC在与DT相应的位置上,显相同颜色的斑点。且DT与丹参酮IIA、丹参酮I、隐丹参酮、二氢丹参酮I在相同位置显相同颜色的斑点,HP-β-CD无展开斑点,表明HP-β-CD不改变药物DT主要成分,包合物形成前后DT的化学成分没有发生变化。

表6 验证实验结果

图3 DT (a) 和DT&HP-β-CD@IC (b) 外观
2.5.3 红外光谱法 取DT、HP-β-CD、DT及HP-β-CD的物理混合物和DT&HP-β-CD@IC各2 mg左右,分别与200 mg左右干燥的KBr粉末在玛瑙研钵中混匀,充分研细至颗粒直径小于2 μm,用不锈钢小勺取适量放入压片模具内,在压片机上压成透明薄片。在4000~400 cm−1进行测定,分辨率为4 cm−1,扫描次数为32次。各物质的特征吸收峰见图5。从图5-A可以看出,3 385.51 cm−1为HP-β-CD的特征峰,该峰为HP-β-CD中-OH的伸缩振动峰,DT的红外吸收图谱见图5-C,1 671.32 cm−1为丹参酮C=O伸缩振动峰,为其特征峰,由图5-A、D可以看出,HP-β-CD和DT&HP-β-CD@IC谱图上的峰形具有较高的相似度,因此,可以推断反应过程中HP-β-CD的基本骨架结构未发生改变,在包合物(图5-D)中,邻苯醌中的羰基C=O在1 670.00 cm−1处的特征吸收峰消失。从图5-C可以看出,DT和HP-β-CD物理混合物的红外图谱为其二者的简单相加,含有DT和HP-β-CD二者的特征峰。通过上述对比分析可证明DT&HP-β-CD@IC形成。

1-丹参酮IIA 2-丹参酮I 3-隐丹参酮 4-二氢丹参酮I 5-HP-β-CD 6-DT 7-DT&HP-β-CD@IC

A-HP-β-CD B-HP-β-CD和DT物理混合物 C-DT D-DT&HP-β-CD@IC
2.5.4 紫外光谱法 称取适量HP-β-CD溶于蒸馏水,得供试品1;DT&HP-β-CD@IC适量溶于蒸馏水,得供试品2;称取适量包合前DT样品,采用无水乙醇溶解,得供试品3;将DT与HP-β-CD物理混合,加无水乙醇超声溶解,得供试品4;称取DT&HP-β-CD@IC适量加无水乙醇超声溶解,得供试品5。各样品溶液在200~500 nm(采样间隔1 nm)进行紫外扫描,供试品1、2以蒸馏水做空白对照,供试品3~5采用无水乙醇做空白对照。各供试品溶液的UV全波长扫描图谱见图6。由图6可知,HP-β-CD与DT&HP-β-CD@IC没有DT特征吸收峰,表明有新物质的形成。包合物所提取的DT、DT和HP-β-CD的物理混合物、包合前的DT三者有着相似的吸收峰,表明DT&HP-β-CD@IC的形成前后DT的主要化学成分没有发生变化。

A-HP-β-CD B-DT与HP-β-CD的物理混合物 C-包合前的DT样品 D-DT&HP-β-CD@IC中提取的DT E-DT&HP-β-CD@IC
2.5.5 扫描电镜法 使用场发射扫描电子显微镜[15]观察DT&HP-β-CD@IC、HP-β-CD、DT以及HP-β-CD和DT物理混合物的表面形态,结果见图7。由图7可知,包合前的DT表面有针状结构,呈不规则的晶体结构,HP-β-CD呈多孔的球状结构,DT&HP-β-CD@IC表面发生变化,不再有DT的针状结构,以及HP-β-CD的球状结构,产生了新的不规则晶体结构,说明DT&HP-β-CD@IC形成。
2.5.6 溶解度测定 分别精密称取4份DT&HP-β-CD@IC粉末和DT样品于15 mL离心管内,加入5 mL pH 1.2盐酸缓冲液、pH 6.8及7.4磷酸盐缓冲液(PBS)、纯水,置于37 ℃水浴中恒温震荡器中(90 r/min),平衡1 d后,用0.45 μm微孔滤膜滤过,取续滤液,HPLC测定含量,结果见表7。DT&HP-β-CD@IC在一定的介质中溶解度有一定的增加,而平衡1 d后,检测到DT在pH 6.8 PBS介质中溶解度为(0.074±0.003)mg/mL,未在其他介质中检测到DT成分。
3 讨论
中药和天然植物药的开发和利用,对于推进中医药现代化和促进人民健康具有重要意义[16]。但部分中药存在成分复杂、水溶性差等问题,给临床前研究,尤其是体外药效学研究带来困扰。包合物通过将客体疏水分子封装在包合材料疏水内部空腔,利用亲水性外表面来增加疏水分子溶解性[17],常采用饱和水溶液法、超声法、研磨法、冷冻干燥法以及喷雾干燥法制备[18-19]。Box-Behnken实验设计可非线性拟合给出各因素之间的交互作用,设计简单、实验次数少、预测值可信度较高,已被广泛用于药学领域中制剂处方工艺的筛选与优化[20-21]。
本实验通过单因素试验筛选出对HP-β-CD-DT包合物制备工艺影响较为显著的几个因素,且得到了包封率和载药量最大时各因素所处的大致范围,以载药量和包封率为主要考察指标,采用Box-Behnken响应面法对其制备工艺进行优化,得到最佳制备工艺为药物与载体材料的配比为1∶3,反应时间为2.5 h,反应温度为40 ℃,在此条件下得到载药量为5.17%、包封率为63.49%,验证实验与预测有所偏差,同时发现在响应面给出的预试16号实验得出的结果更好,因此从实际出发,确认最佳工艺为药物与载体材料的配比为1∶3,反应时间为2 h,反应温度为40 ℃,在此条件下得到载药量为5.44%、包封率为68.78%。最后通过红外光谱法、紫外光谱法以及薄层色谱法对包合物进行表征,验证了包合物形成,这为将DT应用于后续实验和临床提供了支持。
利益冲突 所有作者均声明不存在利益冲突
[1] 钟赣生. 中药学 [M]. 第4版. 北京: 中国中医药出版社, 2016: 277.
[2] 李晓娟, 夏榕蔓, 楼招欢, 等. 丹参二萜醌通过PERK-EIF2α通路诱导肺癌PC9细胞凋亡的机制研究 [J]. 中华中医药杂志, 2017, 32(5): 1897-1902.
[3] 楼招欢, 夏榕蔓, 李晓娟, 等. 丹参二萜醌活化ERS介导的凋亡通路抗肺癌作用机制研究 [J]. 中国中药杂志, 2018, 43(24): 4900-4907.
[4] 张梦阳, 张光霁, 楼招欢. 丹参二萜醌对PC9肺癌移植瘤动物炎症微环境的作用研究 [J]. 浙江中医杂志, 2019, 54(1): 8-9.
[5] 姜兴粲, 李冰, 张继瑜. 环糊精包合物超分子体系的制备与表征研究进展 [J]. 动物医学进展, 2021, 42(3): 96-101.
[6] 张倩, 夏学军. 药物制剂中药物与辅料相互作用的研究进展 [J]. 中国医药工业杂志, 2021, 52(1): 32-41.
[7] 聂晓娟, 李霞, 马红艳. 环糊精聚合物的合成及应用研究 [J]. 精细化工, 2019, 36(12): 2364-2370.
[8] Hsu CM, Yu SC, Tsai FJ,. Characterization ofandbioactivity of a ferulic acid-2-hydroxypropyl-β-cyclodextrin inclusion complex [J]., 2019, 180: 68-74.
[9] 杨云汉, 赵雪秋, 杜瑶, 等. 长春胺与羟丙基-β-环糊精包合物的制备、表征及理论研究[J]. 中草药, 2019, 50(2): 352-363.
[10] 许丹, 刘建英, 刘玉梅. β-环糊精及其衍生物增加客体分子水溶性的研究进展 [J]. 食品工业科技, 2021, 42(16): 404-411.
[11] Sun C, Cao J, Wang Y,. Ultrasound-mediated molecular self-assemble of thymol with 2-hydroxypropyl-β-cyclodextrin for fruit preservation [J]., 2021, 363: 130327.
[12] 张毅, 邓昌平, 时敏, 等. 药用植物丹参中丹参酮IIA的提取分离工艺研究 [J]. 上海师范大学学报: 自然科学版, 2018, 47(6): 754-761.
[13] 吴妮. CS-γ-PGA-丹参酮IIA包合物的制备与评价 [D].西安: 西北大学, 2019.
[14] 李燕华, 王淑慧, 李俊鹏, 等. 漆黄素与β-环糊精衍生物的包合行为及性能研究 [J]. 中草药, 2021, 52(16): 4797-4810.
[15] 李德锋, 樊金玲, 姚培培, 等. 光甘草定/羟丙基-β-环糊精包合物的释放特性、黏液渗透性及细胞摄取[J/OL]. 食品科学: https://kns.cnki.net/kcms/detail/11. 2206.TS.20230413.1954.038.html.
[16] 罗李娜, 陈更新. 关于中药新药开发现代化的几点思考 [J]. 中华中医药杂志, 2017, 32(11): 4798-4800.
[17] 许丹, 刘建英, 刘玉梅. β-环糊精及其衍生物增加客体分子水溶性的研究进展 [J]. 食品工业科技, 2021, 42(16): 404-411.
[18] 刘雪城, 丁平刚, 金皓洁, 等. 反式西红花酸-环糊精包合物的制备、表征、安全性和抗肿瘤评价 [J]. 中草药, 2022, 53(15): 4663-4672.
[19] 朱东方, 陈勇, 黄国清. β-环糊精包埋黑胡椒油树脂工艺研究 [J]. 食品研究与开发, 2022, 43(7): 96-103.
[20] 徐蓓蕾, 韩晓宇, 刘晶晶, 等. 基于Box-Behnken设计-响应面法与质量综合评价优化葛根芩连汤煎煮工艺 [J]. 中草药, 2022, 53(22): 7070-7081.
[21] Amanda, Parra-Campos, Eduardo L,. Natural pigment extraction optimization from coffee exocarp and its use as a natural dye in french meringue [J]., 2019, 285(1): 158.
Preparation technology of diterpenoid tanshinone hydroxypropyl-β-cyclodextrin inclusion complex from active parts of
SU Hang1, LIU Hui-fang2, LIU Ze-ying2, LOU Zhao-huan2, ZHANG Guang-ji1
1. Key Labortary of Blood-Stasis-Toxin Syndrome of Zhejiang Province,School of Basic Medical Sciences, Zhejiang Chinese Medical University, Hangzhou 310053, China 2. School of Pharmaceutical Sciences, Zhejiang Chinese Medical University, Hangzhou 310053, China
To optimize the preparation process of diterpenoid tanshinone (DT) hydroxypropyl-β-cyclodextrin (HP-β-CD) inclusion complex (IC) (DT&HP-β-CD@IC).Based on the single factor test, the ratio of DT and HP-β-CD, the inclusion temperature, and the inclusion time were selected as the investigating factors, the encapsulation efficiency and drug-loading of the inclusion complex were used as the evaluation index. The Box-Behnken response surface was used to optimize the preparation process of the DT&HP-β-CD@IC, and the inclusion complex was evaluated by infrared spectroscopy, ultraviolet spectroscopy, thin layer chromatography and scanning electron microscopy.The optimal preparation process of the inclusion complex was as follows: HP-β-CD concentration was 0.1 g/mL, the ratio of drug to carrier material was 1:3, the inclusion time was 2 h, and the inclusion temperature was 40 ℃. The encapsulation rate of DT&HP-β-CD@IC was 68.78%, and the drug loading was 5.44%. The results of ultraviolet, infrared spectroscopy and thin-layer chromatography indicated the formation of inclusion complex.DT&HP-β-CD@IC has a high encapsulation efficiency and a certain improvement in solubility.
Bunge; active parts; diterpenoid tanshinone; hydroxypropyl-β-cyclodextrin; inclusion complex; Box-Behnken response surface; dihydrotanshinone Ⅰ; cryptotanshinone; tanshinone Ⅰ; tanshinone ⅡA
R283.6
A
0253 - 2670(2023)10 - 3132 - 09
10.7501/j.issn.0253-2670.2023.10.010
2022-12-16
浙江省科技计划项目省级重点研发计划(2019C03072);浙江省中医药科技计划项目(2023ZR081)
苏 行(1996—),男,硕士研究生,专业方向为中医学。
张光霁,男,教授,博士生导师,主要研究方向为中医体质与病因病机学研究和中医药抗肿瘤创新药物研究。E-mail: zgj@zcmu.edu.cn
[责任编辑 郑礼胜]
