经颈静脉肝内门体分流术治疗肝硬化食管胃静脉曲张出血再出血风险
2023-05-13蔡森林吴少杰唐仪周艳峰方主亭
蔡森林, 吴少杰, 唐仪, 周艳峰, 方主亭
食管胃静脉曲张出血(esophagogastric variceal bleeding, EGVB)是肝硬化门静脉高压严重的并发症。静脉曲张出血后,如果不采取预防措施,2 a内再出血的发生率高达60%~70%,病死率达33%[1-2]。经颈静脉肝内门体分流术(transjugular intrahepatic portosystemic shunt, TIPS)具有微创的特点,可迅速止血且有效降低门静脉压力,临床常用于治疗门静脉高压并发症,且已有大量证据[3-4]支持TIPS可显著降低肝硬化EGVB患者死亡和静脉曲张再出血的风险。我国TIPS实践指南[1]推荐,伴有高危因素的EGVB患者在初次药物联合内镜治疗且排除禁忌后,应在早期(72 h内,最佳24 h)行覆膜支架TIPS治疗。TIPS术后仍存在并发肝功能不全、肝性脑病及支架功能障碍的风险,并可能发生静脉曲张再出血[5]。BOUZBIB等[6]提出,当TIPS作为紧急或抢救治疗时,虽可达到迅速止血的效果,但仍伴随较高的静脉曲张再出血的风险和死亡率。在考虑行TIPS时,与肝脏疾病相关的危险因素如凝血功能受损、免疫功能障碍以及严重的分流相关并发症等均需纳入谨慎的风险效益分析。既往研究[7]认为,TIPS手术的相关因素如支架类型、长度和功能及分流道的通畅情况均可影响TIPS术后静脉曲张再出血风险。然而,若能在TIPS术前利用临床指标预测术后静脉曲张再出血的风险,早期识别高危患者并对可干预因素进行早期防治,将有助于严格把握TIPS适应证,改善TIPS预后。目前国内、外文献[8-11]对影响TIPS术后食管胃静脉曲张再出血风险的探讨多集中于手术相关因素。本研究基于TIPS术前指标,探讨影响TIPS术后静脉曲张再出血的危险因素,同时构建预测TIPS术后静脉曲张再出血风险的列线图模型,并评估其预测效能。
1 对象与方法
1.1 对象 回顾性收集2016年3月—2020年12月 共238例在福建省立医院确诊为肝硬化EGVB并行TIPS患者的临床资料。纳入标准:(1)明确诊断失代偿期肝硬化EGVB并行TIPS治疗;(2)TIPS 术中成功植入支架,且造影示支架通畅;门静脉压力差(portal venous pressure gradient, PPG)≤12 mmHg(1 mmHg=133.3 Pa);(3)年龄≥18岁。排除标准:(1)严重的心、肾和肺功能不全;(2)合并恶性肿瘤预期寿命<3个月;(3)资料不完整;(4)失访。根据标准排除51例,纳入研究对象187例。其中,男性84例(44.9%),女性103例(55.1%);年龄(55.3±7.2)岁(34~77岁)。研究流程见图1。本研究经福建省立医院伦理委员会批准(K2022-06-002),患者及其家属均签署知情同意书。

EGVB:食管胃静脉曲张;TIPS:经颈静脉肝内门体分流术。
1.2 方法 收集患者的一般资料,包括年龄、性别、吸烟史、饮酒史、高血压病、糖尿病和肝性脑病病史和失代偿性肝硬化病因。体格检查和实验室指标包括体质量指数(body mass index, BMI)、收缩压(systolic blood pressure, SBP)、舒张压(diastolic blood pressure, DBP)、白细胞计数、中性粒细胞百分比、血小板计数、丙氨酸氨基转移酶(alanine transaminase, ALT)、天门冬氨酸氨基转移酶(aspartate aminotransferase, AST)、血清白蛋白(albumin, ALB)、总胆红素(total bilirubin, TBIL)、肾小球滤过率(estimated glomerular filtration rate, eGFR)、三酰甘油(triacylglycerol,TG)、总胆固醇(total cholesterol, TC)、高密度脂蛋白胆固醇(high-density lipoprotein cholesterol, HDL-C)、低密度脂蛋白胆固醇(low-density lipoprotein cholesterol, LDL-C)和国际标准化比值(international normalized ratio, INR),计算Child-Pugh评分。所有随访患者住院期间未发生静脉曲张再出血。出院1周及1、3、6个月,之后每半年门诊或电话随访。所有纳入对象至少完成1次门诊或随访,内容包括检查患者的一般情况,如血常规、凝血功能、肝肾功能、电解质和腹部超声等,必要时行腹部增强CT和内镜检查。若出现支架狭窄、闭塞及再次出现门静脉高压并发症,如EGVB、腹水等,则进行门静脉造影。随访的结局事件为静脉曲张再出血。
1.3 TIPS手术 门静脉穿刺成功后通过导丝引入导管至门静脉主干,行造影和测压,视情况栓塞反流的侧支血管。后予6 mm × 40 mm球囊扩张穿刺道,结合球囊扩张时的切迹及血管造影结果选择合适的血管内支架,植入8 mm × 80 mm Luminexx裸支架(美国Bard公司)与8 mm × 60 mm Flucency覆膜支架(美国Bard公司)组合,或8 mm × 60 mm、8 mm × 70 mm Viatorr支架(美国Bard公司),远心端覆膜部分应开始于门静脉和肝实质的汇合处,近心端应到达肝静脉下腔静脉入口处。予8 mm × 40 mm球囊后扩张。复查造影显示支架内血流通畅,侧支血管不再显影。测量术后门静脉压力,可见门静脉压力明显下降。术后予门冬氨酸鸟氨酸降血氨,补充支链氨基酸;对于术前曾经发生过肝性脑病的患者,使用乳果糖和利福昔明预防肝性脑病再发;常规使用抗生素预防感染;若分流道内血流充盈,且患者未合并高凝状态,术后不予常规抗凝治疗。

2 结 果
2.1 临床资料 截至2021年12月,中位随访时间40个月(12~68个月)。随访期间食管胃静脉曲张再出血 47 例,死亡 10 例(肝衰竭 5 例,感染性休克 3 例,严重凝血功能障碍 1 例,多器官功能衰竭 1 例)。失代偿性肝硬化病因为乙型病毒性肝炎 108 例,酒精性肝炎 68 例,自身免疫性肝炎 5 例,遗传代谢性肝病 3 例,丙型病毒性肝炎 3 例。食管胃静脉曲张再出血的人群年龄更大、INR水平及Child-Pugh评分更高、合并肝性脑病比例高(P<0.001 或<0.05);血清ALB、血红蛋白、血清钠、LDL-C和eGFR水平更低,栓塞侧支血管比例低(P<0.05,P<0.001)。2 组人群的性别比例、吸烟、饮酒、高血压病病史、糖尿病病史、失代偿性肝硬化病因、TIPS手术时机与植入支架类型、白细胞总数及中性分叶核百分比、血小板计数、BMI、SBP、DBP、ALT、AST、TBIL、TG、TC、HDL-C和血清钾水平等比较,差别均无统计学意义(P>0.05,表1)。
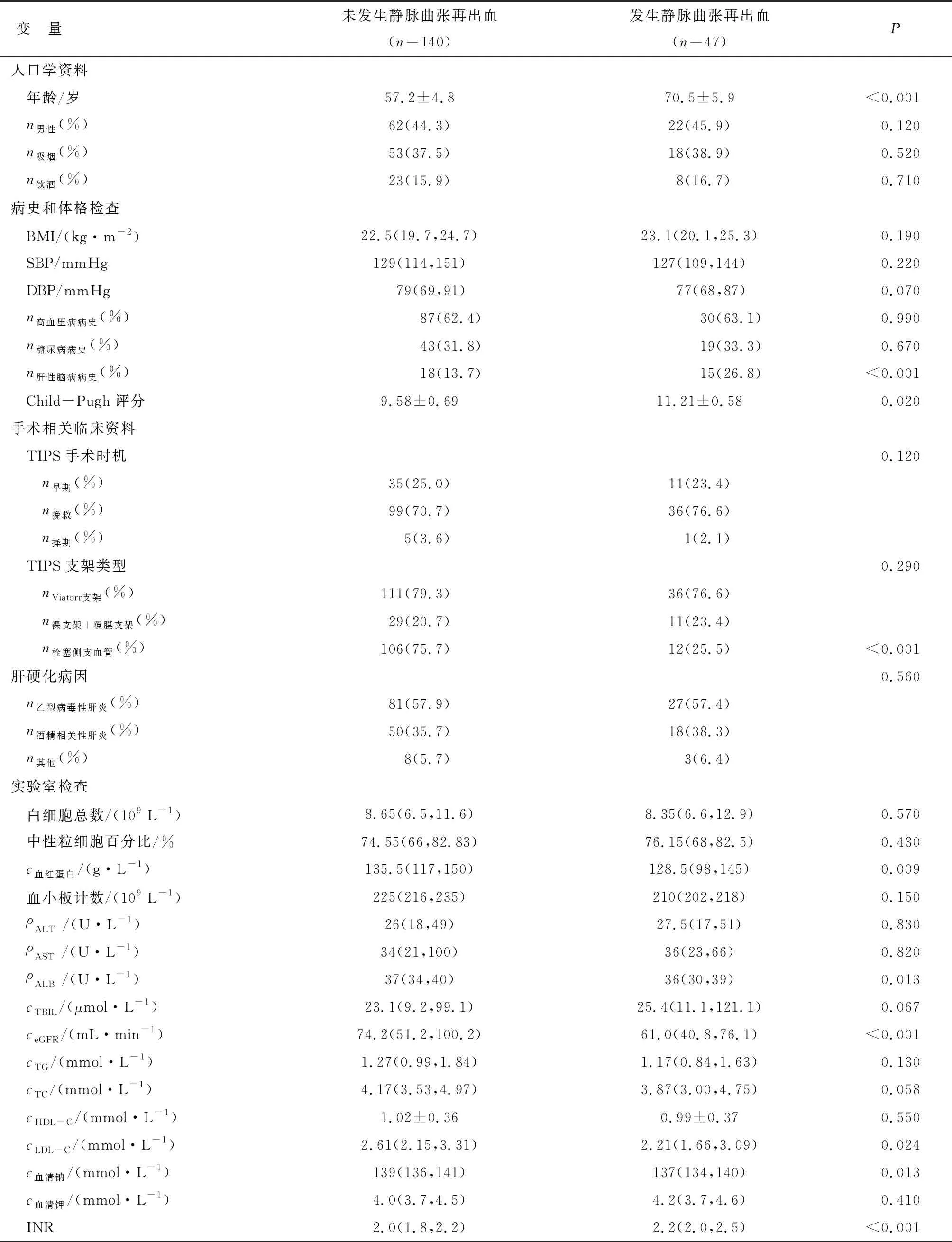
表1 临床资料比较
2.2 TIPS术后静脉曲张再出血预后因素分析 本研究以静脉曲张再出血为结局事件,建立多因素Cox比例风险回归模型,共线性检验和等比例风险假定均通过,逐步后退Cox比例风险回归模型提示,在调整了年龄、性别、吸烟、饮酒、高血压病病史、糖尿病病史、ALT、AST、ALB、TBIL后,INR升高[风险比(hazrd ratio, HR)=1.70]、肝性脑病病史(HR=1.79)是TIPS术后静脉曲张再出血的独立预测因素(P=0.016和0.017)。血清钠每下降1 mmol/L,TIPS术后静脉曲张再出血风险升高6%(P=0.014);eGFR每下降1 mL/min,再出血风险升高1%(P=0.008,表2)。

表2 TIPS术后静脉曲张再出血预后因素分析
2.3 TIPS术后静脉曲张再出血风险预测列线图建立 基于多因素Cox回归分析结果,构建TIPS术后1、3和5 a的静脉曲张再出血风险预测列线图(图2)。绘制ROC曲线,计算ROC曲线下面积为0.724;Hosmer-Lemeshow拟合优度检验计算得出χ2=11.84,P=0.287,提示预测列线图模型的区分度和校准度均理想(图3,图4)。

TIPS:经颈静脉肝内门体分流术。

ROC:受试者工作特征曲线;TIPS:经颈静脉肝内门体分流术。
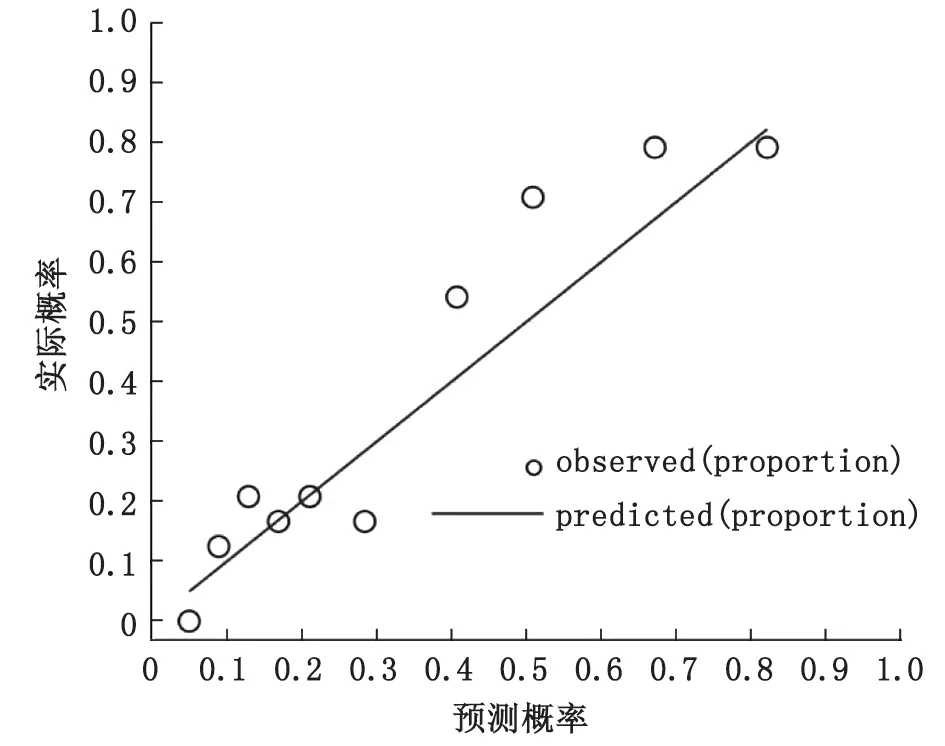
TIPS:经颈静脉肝内门体分流术。
3 讨 论
对于门静脉高压EGVB的高危患者,指南[1]推荐TIPS为一线治疗方案。TIPS能有效降低门静脉压力,并迅速止血;但TIPS术后仍存在较高的食管静脉曲张再出血和死亡风险[6]。本研究依托回顾性人群队列,通过纳入肝硬化EGVB患者分析了TIPS术前可能影响术后静脉曲张再出血的危险因素,并构建再出血风险预测列线图模型。
本研究结果表明:调整了年龄、性别、吸烟、饮酒、高血压病病史、糖尿病病史、肝功能和ALB等因素后,血清钠、INR、肝性脑病病史和eGFR是TIPS术后静脉曲张再出血的独立预测因素。既往文献[12-13]报道,高TBIL、凝血酶原时间延长和低血清ALB是肝硬化食管胃静脉曲张再出血的危险因素,本研究结果与此相符。因此,TIPS术前应严密检测肝功能和凝血功能,若INR明显延长或呈现延长趋势,术前应输注血浆并补充凝血因子,术后减少抗凝药物的使用;TIPS术后存在应激性溃疡、急性胃黏膜病变等非静脉曲张出血的可能,应同时加强胃黏膜保护。BIGGINS等[14]在MELD模型基础上将血清钠水平结合到MELD公式中,提出了MELD-Na评分系统。研究[15]已证实,MELD-Na评分系统可预测肝硬化EGVB患者死亡和再出血的发生风险。RUF等[16]提出,在门静脉高压患者合并难治性腹水和肝肾综合征的级联事件中,低钠血症可能是比血清肌酐升高更早或更敏感的病理生理标志。本研究模型采用eGFR代替肌酐作为预测因素,进一步考虑了年龄和性别对再出血风险的影响。同时,血钠降低、INR延长、肝性脑病病史和低eGFR也说明严重肝病导致多系统功能障碍,提示TIPS术后发生静脉曲张再出血的风险高。新近研究[17]提出的FIPS评分和MOTS评分系统均提示TBIL水平与TIPS预后的相关性。本研究未发现胆红素与TIPS术后再出血风险的关联,可能与纳入人群基线的胆红素水平无明显升高有关。
列线图是一种建立在多因素回归模型的基础上,将多个临床指标整合后绘制而成的可视化图形,可用于预测某一临床事件的发生风险,并直观表达出统计模型分析结果,在量化风险方面更为简洁、有效[18]。目前TIPS预后风险模型多集中于死亡率的预测,有CLIF-C AD评分、MELD评分、MELD-Na评分、Child-Pugh评分、ALBI评分和PALBI评分等[19-20],而TIPS术后静脉曲张再出血风险模型研究较少。有研究[13]显示,ALBI评分、PALBI评分、Child-Pugh评分、MELD评分、门静脉主干直径、胃静脉曲张和门静脉血栓形成是1 a静脉曲张再出血的独立危险因素,基于这些独立危险因素分别建立了ALBI、PALBI、Child-Pugh和MELD列线图,在用列线图和人工神经网络(artificial neural networks, ANNs)进行验证和比较后,得出ALBI评分、PALBI评分、Child-Pugh评分或MELD评分均不是预测 1 a静脉曲张再出血概率的最佳选择。MELD 评分主要针对终末期肝硬化患者,而 Child-Pugh 分级存在 2 个高度主观的变量(腹水分级和脑病分级)。由于ALBI评分和PALBI评分的易用性和客观性,更有可能作为TIPS治疗肝硬化EGVB患者肝功能评估的替代工具,但也需要通过长期随访来验证。本研究基于多因素Cox回归分析结果,在血清钠、INR、肝性脑病病史及eGFR的独立危险因素基础上,构建了TIPS术后静脉曲张再出血风险预测列线图模型,其中也包含了脑病分级主观变量。经过检验,该模型的区分度和校准度较为理想,但也需要进一步的前瞻性试验来验证。TIPS术后静脉曲张再出血风险临床预测模型的建立,有利于在临床实践中采取更有针对性的防治策略,如提高TIPS术前危险因素的筛查意识,关注肝性脑病的发生、肝肾功能的进展、维持电解质平衡并防治低钠血症、定期复查凝血指标等。对于列线图评估TIPS术后再出血发生风险较高的患者,在TIPS术中和术后应严密监测脏器功能和并发症的发生,以获得更好的生活质量和长期生存。
本研究中非出血和再出血组在使用支架类型方面未见明显差异。在TIPS术中支架的选用方面,Viatorr支架较裸支架与覆膜支架组合在解决支架狭窄、闭塞方面有着重要优势,有更高的分流道通畅率[21-22]。目前,对于TIPS术中是否栓塞门静脉侧支血管仍存在争议。本研究结果显示,再出血患者中术中栓塞门静脉侧支血管的比例低于未发生再出血患者,提示TIPS术中联合侧支血管栓塞可能是术后静脉曲张再出血的影响因素。有研究[23]表明,TIPS联合侧支血管栓塞在降低门静脉高压的同时可直接栓塞出血血管,减轻了静脉曲张程度,使分流道狭窄和闭塞的风险下降,从而降低再出血发生率。
本研究可在一定程度上补充提供有关肝硬化EGVB患者TIPS术后再出血风险的证据;同时,通过易于获取的临床指标在TIPS术前计算出TIPS术后1、3和5 a静脉曲张再出血风险,以便及时纠正、控制危险因素,改善TIPS预后。本研究仍存在一定局限性。本研究为回顾性单中心研究,且样本量较小,可能存在选择和回忆偏倚;随访过程中对支架功能、术后脏器功能和门静脉压力变化的评估等仍待完善,以上因素对术后再出血的风险可能存在影响,今后将进一步开展大样本、前瞻性队列研究以获得TIPS预后风险更为可靠的预测模型。
