阿法替尼与吉非替尼治疗EGFR 突变非小细胞癌的效果及生存率比较
2023-05-11罗景方张有华梅浪华邱华平
罗景方,张有华,梅浪华,邱华平
(抚州市第一人民医院,江西 344000)
非小细胞癌(NSCLC)是指起源于支气管黏膜、腺体及肺泡上皮的肺部恶性肿瘤,是肺癌中常见的病理类型之一,有研究表明,近年来NSCLC 发病率及病死率均呈上升趋势[1],成为导致居民死亡的主要因素之一。其诱因复杂[2],环境污染、吸烟、年龄、职业、营养状况等因素均可诱发NSCLC。NSCLC 患者常见EGFR基因突变,表皮生长因子(EGFR)突变是指EGFR 基因序列发生改变而导致基因活性出现异常[3],从而引起疾病发生及进展,其中基因突变常见位点位于EGFR基因酪氨酸激酶区第18-21 外显子,而突变会导致正常细胞生物学特性发生改变,从而引起癌症出现。目前临床以药物治疗、手术治疗、靶向治疗、化疗及免疫治疗等治疗方式为主[4]。而随着人们对肿瘤信号通路认识程度加深,分子靶向治疗成为重要治疗方案,其中EGFR-酪氨酸激酶抑制剂(EGFR-TKI)是常用分子靶向治疗药物。吉非替尼是一种EGFR-TKI[5],属小分子化合物,可通过抑制EGFR-酪氨酸激酶(EGFRTK)来抑制肿瘤生长、转移及血管生成,加速肿瘤细胞凋亡。而阿法替尼是EGFR 与人表皮生长因子受体2(HER2)酪氨酸激酶的强效、不可逆双重抑制剂[6],通过抑制信息传导、阻断与肿瘤细胞生长分裂相关的主要通道来抑制肿瘤生长。然而关于阿法替尼与吉非替尼效果对比相关报道较为少见,基于此,本研究应用阿法替尼与吉非替尼治疗EGFR 突变NSCLC 患者,探讨其效果及生存率差异。
1 资料与方法
1.1 一般资料 选取2018 年1 月—2020 年1 月本院收入EGFR 突变NSCLC 患者68 例,纳入标准:①符合临床中关于EGFR 突变NSCLC 相关诊断标准[7];②预计生存期≥1 年;③患者及家属均知情,且签署知情同意书。排除标准:①存在药物过敏者;②伴有严重心肺疾病;③合并肾脏、肝脏等器官严重功能不全者;④妊娠期女性。按照随机数字表法分为A 组(n=35)与B 组(n=33)。其中A 组男19 例,女16 例;年龄在59~81 岁,平均年龄(72.43±4.72)岁;有吸烟史20 例;平均体质指数(BMI)为(23.58±3.26)kg/m2;病理类型:腺癌25 例,鳞癌7 例,腺鳞癌3 例;TNM 分期:Ⅲb 期9 例,Ⅳ期26 例;EGFR 外显子19 突变19例,21 突变16 例。B 组男18 例,女15 例;年龄在60~80 岁,平均年龄(71.56±4.69)岁;有吸烟史17 例;平均BMI 为(24.12±3.54)kg/m2;病理类型:腺癌22 例,鳞癌9 例,腺鳞癌2 例;TNM 分期:Ⅲb 期12 例,Ⅳ期21 例;EGFR 外显子19 突变15 例,21 突变18 例。两组患者年龄、性别、病理类型等一般资料差异无统计学意义(P>0.05)。具有可比性。本研究经医院伦理委员会批准。
1.2 方法 A 组患者口服阿法替尼,30 mg/次,1 次/d,于餐前至少1 h 或餐后2 h 服用,持续服用。B 组口服吉非替尼,250 mg/次,1 次/d,空腹或与食物同服,持续服用,若患者出现无法耐受的腹泻或皮肤不良反应时,可暂停治疗,暂停治疗最多14 d,恢复后继续服用。
1.3 观察指标 治疗4 周后,根据RECIST 标准,比较两组患者临床疗效;根据患者临床表现,观察、分析两组患者不良反应发生情况,并比较其差异;以PFS为首要终点,以临床疗效、不良反应为次要终点,比较两组患者PFS 差异;治疗前及治疗4 周后测定组织多肽抗原(TPA)、癌胚抗原(CEA)、细胞角质蛋白19 片段抗原21-1(CYFRA21-1)、神经元特异性烯醇化酶(NSE)和CD3+、CD4+、CD8+,比较两组患者治疗前后肿瘤标志物及免疫功能水平变化;通过肺癌患者生存质量测定量表(FACT-L)[8],比较两组患者治疗前后生活质量变化,评分标准:量表共包括生理状况、功能状况、情绪、家庭及社会状况、附加的关注情况共5 个维度、36 条目,单个条目分为0~4 分,量表总分为0~144分,得分越高则代表生活质量越高。
1.4 临床疗效评价标准 完全缓解(CR):所有靶病灶消失,病理结节短直径减少至<10 mm;部分缓解(PR):靶病灶直径之和相比基线水平减少≥30%;疾病进展(PD):所有靶病灶直径之和相对增加≥20%(以靶病灶直径之和最小值为参照);疾病稳定(SD):靶病灶减少程度未达到PR,增加程度未达到PD(以靶病灶直径之和最小值为参照)。有效率=(CR+PR)/总例数×100%[9]。
1.5 统计学方法 应用SPSS 20.0 统计学软件进行数据分析,计量资料以x±s 表示,组间比较行独立样本t 检验,计数资料以百分比(%)表示,行卡方检验,等级资料行秩和检验,生存曲线以GraphPad Prism8制作,通过Kaplan-Meier 曲线描述,组间生存期比较采取Breslow 检验,以P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者临床疗效比较 两组患者临床疗效比较,差异无统计学意义(P>0.05)。见表1。

表1 两组患者临床疗效比较 例(%)
2.2 两组患者不良反应发生情况比较 两组患者不良反应发生率比较,差异无统计学意义(P>0.05)。见表2。

表2 两组患者不良反应发生情况比较 例(%)
2.3 两组患者PFS 比较 A 组患者中位PFS 为10个月,B 组中位PFS 为9 个月,两组比较差异无统计学意义(P>0.05)。见图1。
2.4 两组治疗前后肿瘤标志物水平比较 两组患者治疗前TPA、CEA、NSE 和CYFRA21-1 水平比较,差异无统计学意义(P>0.05);治疗后TPA、CEA、NSE 和CYFRA21-1 水平均低于同组治疗前,且A 组低于B组,差异有统计学意义(P<0.05)。见表3。
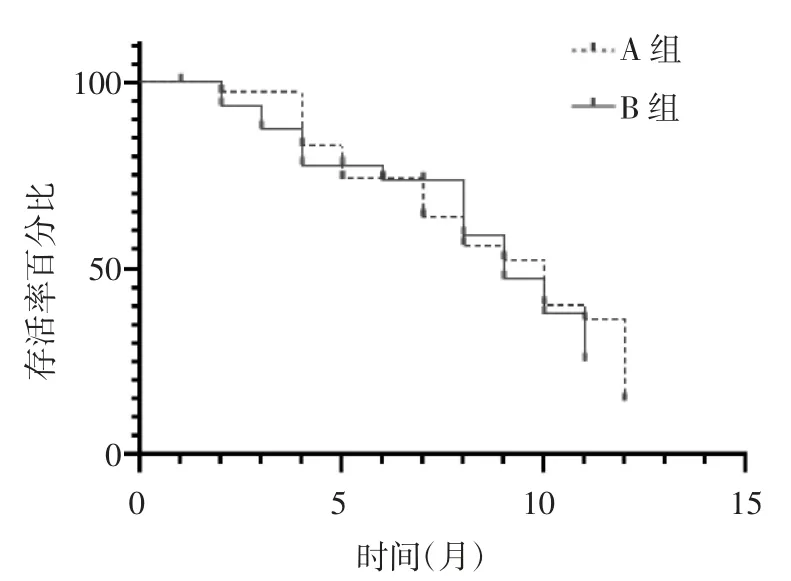
图1 两组患者PFS 比较
2.5 两组治疗前后免疫功能及生活质量比较 两组患者治疗前CD3+、CD4+、CD8+水平及FACT-L 评分比较,差异无统计学意义(P>0.05);治疗后CD3+、CD4+水平及FACT-L 评分均高于同组治疗前,且A 组高于B 组,差异有统计学意义(P<0.05);两组患者CD8+水平均低于同组治疗前,且A 组低于B 组,差异有统计学意义(P<0.05)。见表4。
表3 两组治疗前后肿瘤标志物水平比较(±s)

表3 两组治疗前后肿瘤标志物水平比较(±s)
与治疗前同组比较,P<0.05;与治疗后A 组比较,P<0.05
组别 时间 TPA(U/L) CEA(ng/ml) NSE(μg/L) CYFRA21-1(μg/L)A 组(n=35) 治疗前 169.36±25.84 14.69±2.74 21.47±3.46 16.34±3.87治疗后 138.57±17.38* 9.82±1.38* 18.45±2.93* 12.59±2.12*B 组(n=33) 治疗前 169.67±27.83 14.14±2.98 22.12±3.61 16.93±3.54治疗后 146.42±21.34*△ 10.62±2.05*△ 19.56±2.03*△ 13.86±3.25*△*△
表4 两组患者治疗前后免疫功能及FACT-L 评分比较(±s)

表4 两组患者治疗前后免疫功能及FACT-L 评分比较(±s)
与治疗前同组比较,*P<0.05;与治疗后A 组比较,△P<0.05
组别 时间 CD3+(%) CD4+(%) CD8+(%) FACT-L 评分(分)A 组(n=35) 治疗前 44.83±8.59 29.67±5.42 26.53±3.39 88.37±13.56治疗后 55.92±7.32* 38.19±6.78* 22.27±3.62* 105.68±15.24*B 组(n=33) 治疗前 44.29±8.15 29.21±5.58 27.18±3.82 87.15±12.75治疗后 52.34±7.06*△ 35.03±6.14*△ 23.98±3.13*△ 99.36±14.49*△
3 讨论
EGFR 基因突变属于肿瘤特异性体细胞遗传改变,仅存在于肿瘤组织中[10]。有研究认为,EGFR 基因突变与EGFR-TKI 分子靶向治疗临床敏感性具有较高相关性[11],而NSCLC 不是单一疾病,由于其分子亚型不同,治疗策略也存在一定差异。吉非替尼能够竞争EGFR-TK 催化区域上Mg-ATP 结合位点[12],阻断其信号传递,并且抑制有丝分裂原活化蛋白激酶的活化,从而促进细胞凋亡,抑制肿瘤血管生成;而阿法替尼属EGFR 与人表皮生长因子受体2(HER2)酪氨酸激酶双重抑制剂,可抑制信息传导,阻隔与癌细胞生长分裂有关的主要通道,且由于阿法替尼属ErnB 家族阻断剂[13],以及ErnB 家族信息传导机制可由多个同二聚体与异二聚体引发,阿法替尼可同时抑制多个ErnB 家族成员,能够有效中断下游信息传导,从而抑制肿瘤生长、迁移,促进肿瘤细胞凋亡。而在本研究中,两组患者临床疗效、不良反应及PFS 比较,差异无统计学意义,这说明阿法替尼与吉非替尼在EGFR 突变NSCLC 患者临床疗效、生存期及降低不良反应发生方面无明显差异,这与施霞等[14]研究中阿法替尼组相比吉非替尼组在10 年间可多获得0.29 个质量调整生命年的研究结果不符。考虑其原理,初步推测可能是本研究纳入研究对象例数过少,研究整体尚存在不完善之处,需进一步扩大样本量、完善研究以取得更为确切结果。
TPA 是多肽类物质,在上皮性肿瘤中表达增加,其水平反映肿瘤细胞增殖、分化及肿瘤组织浸润程度,CEA 则反映肿瘤组织复发及转移,CYFRA21-1 是肺泡上皮细胞凋亡的产物,在细胞角蛋白家族中分子量最小[15],在简单上皮细胞及其对应恶性细胞中均有表达,是可靠程度较高的肿瘤标志物;NSE 是神经元与神经内分泌细胞所特有的酸性蛋白酶[16],其水平在神经内分泌系统肿瘤中呈明显高表达状态,是临床中常用的检测指标。在本研究中,两组患者治疗后TPA、CEA、NSE 和CYFRA21-1 水平均低于同组治疗前,且A 组低于B 组,差异有统计学意义,这说明阿法替尼与吉非替尼均可有效抑制肿瘤组织生长,且阿法替尼效果较吉非替尼更为显著,究其原因认为,相较吉非替尼,阿法替尼通过阻断信息传导及肿瘤细胞生长分裂有关的主要通道来抑制肿瘤细胞生长、促进其凋亡,效果更为显著,反映在肿瘤标志物指标中则表现为A 组指标低于B 组。
在肿瘤组织增殖过程中,由于患者机体免疫功能失调,其淋巴细胞表面抗原CD3+和CD4+抗原减少[17],免疫反应诱导及效应下降,机体特异性抗肿瘤效应降低;而CD8+水平则反应性升高[18]。在本研究中,两组患者治疗后CD3+、CD4+水平及FACT-L 评分均高于同组治疗前,且A 组高于B 组,差异有统计学意义;两组患者CD8+水平均低于同组治疗前,且A 组低于B 组,差异有统计学意义,这说明阿法替尼与吉非替尼均可有效改善机体免疫失调,改善生活质量,且阿法替尼相较吉非替尼改善效果更为显著。究其原因认为,阿法替尼对肿瘤组织更为强效的抑制作用,降低肿瘤侵袭,从而调节患者免疫功能。
综上所述,在EGFR 突变NSCLC 患者治疗中,阿法替尼相较吉非替尼,能够更有利于抑制肿瘤细胞增殖、调节免疫功能,改善患者生活质量,具有较高临床价值。
