毛细胞型星形细胞瘤与毛细胞黏液型星形细胞瘤的异同
2023-05-09闫晋生万大海
闫晋生,万大海
毛细胞型星形细胞瘤(pilocytic astrocytoma,PA)最早于20世纪30年代开始被人们认识,“毛细胞(pilocytic)”一词被用来描述有双极突起毛发样结构的肿瘤细胞,其相对良性,世界卫生组织(WHO)分类为Ⅰ级,10年生存率超过90%[1]。1999年一项描述“具有单相性毛状黏液样特征的儿童星形细胞瘤”的研究使人们首次认识到既往PA中一部分具有更明显侵袭性临床进程的肿瘤——毛细胞黏液型星形细胞瘤(pilomyxoid astrocytoma,PMA)[2],WHO(2007)中枢神经系统肿瘤分类认为其为PA的亚型,定为WHOⅡ级,而PA仍为WHOⅠ级[3]。随着临床病理研究的深入,发现了PMA和PA二者成分混合存在的肿瘤,2010年Johnson等[4]提出了“中间型毛细胞黏液样肿瘤(intermedite pilomyxoid tumors,IPMT)或中间型毛细胞黏液样星形细胞瘤(intermediate pilomyxoid astrocytomas,IPA)”的概念。PA与PMA的临床、组织学和生物学联系非常密切,在WHO(2016版)分类中,由于PMA的组织学表型、KIAAI549-BRAF融合基因与PA存在遗传重叠,暂未给出PMA特定分级,PA仍为WHOⅠ级[5]。在2021年第5版WHO中枢神经系统肿瘤分类(WHO CNS5)概述中,PA归类于局灶性星形细胞胶质瘤,突出其更为坚实的生长模式,具体描述有待CNS5后续内容发布后进一步深入解读[6]。
1 组织学与基因表达
PMA与PA的诊断主要依据病理诊断,PA常呈囊性双相组织学特点,含Rosenthal纤维的致密双极细胞区,以及含微囊和嗜酸性颗粒小体/透明滴的疏松多极细胞区(见图1);PMA具有黏液样基质、以血管为中心、形态单一的双极细胞,缺乏Rosenthal纤维、嗜酸性颗粒小体以及致密疏松的双相性细胞组织病理学特征(见图2)。在WHO(2016)中枢神经系统肿瘤分类中,将PMA归类于PA,但PMA与PA两肿瘤实体间存在细微且关键的组织学差异[7]。PA中可能存在黏液成分,但PMA显示更均匀、广泛的黏液样背景;同时相比PA,PMA可见更多的有丝分裂[8]。PA中囊肿在瘤内和瘤周都很常见,有时大的瘤周囊肿可导致肿瘤实体部分局限形成结节[9]。PA是一种低到中等细胞性的肿瘤,有纤维致密区(由富含Rosenthal纤维、长双极毛状纤维和拉长、核淡染的细胞组成)和疏松区(由核淡染、圆形至椭圆形、胞质伸长相对较短、原质星形胶质细胞样的多极细胞组成),致密区双极肿瘤细胞一般具有强烈的神经胶质纤维酸性蛋白(GFAP)免疫反应,而疏松区原质星形胶质细胞样多极肿瘤细胞则较少[1,10]。PMA呈单相性,肿瘤细胞对GFAP具有典型的强阳性和弥漫性阳性,但缺乏诊断特异性[9]。

图1 毛细胞型星形细胞瘤[可见含Rosenthal纤维的致密双极细胞区及含微囊和嗜酸性颗粒小体/透明滴的疏松多极细胞区(SP×200)。基因检测提示,存在KIAA1549-BRAF。图片来自山西医科大学第一医院神经外科住院病人资料]
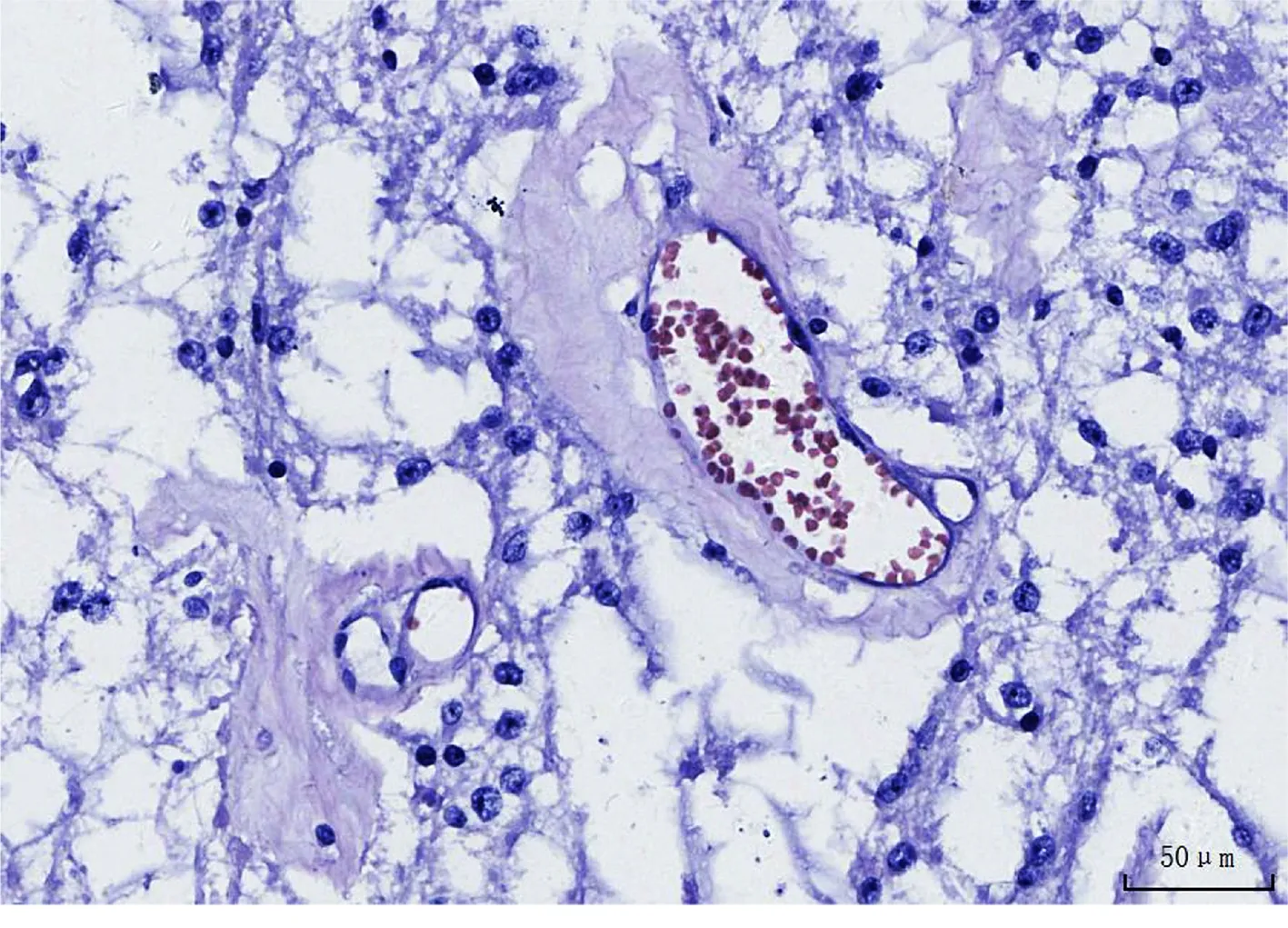
图2 毛细胞黏液型星形细胞瘤[可见黏液样基质,肿瘤细胞血管周围排列的典型特征(SP×200)。图片来自山西医科大学第一医院神经外科住院病人资料]
两种肿瘤最常改变的信号传导通路是丝裂原活化蛋白激酶(MAPK)通路,其次是成纤维细胞生长因子受体(FGFR)通路;最常改变的基因是BRAF、NF1、FGF R1和PT PN11[11-12]。目前,研究已经表明,许多肿瘤中存在解剖位点特异性的基因表达差异,PA在不同解剖位置MAPK通路改变的频率不同[11-13]。Lambert等[14]研究PA幕下和幕上部位的基因表达,发现不同解剖位置的PA存在基因甲基化的差异表达,这表明不同位置的PA可能来自特定区域的起源细胞,且阐述了一些发育调节因子在肿瘤发生过程中存在潜在干扰。Kleinschmidt-Demasters等[10]在解剖位置限制下研究幕上PMA与PA基因差异表达,发现PMA中有丝分裂相关基因和细胞外基质基因过表达,而PA中质膜和胶原相关基因存在弱的过表达;同时该研究中PMA和PA有丝分裂相关基因的富集与MIB-1指数升高和侵袭性生物学行为具有相关性[15]。有丝分裂相关基因在PMA中的过表达被认为可能是这些肿瘤不良临床过程的原因,研究还发现,所有PMA病例中毛状星形胶质细胞均具有细短、发育迟缓的轴突纤维,而不是粗长的轴突纤维,并认为可能是PMA与PA的诊断特点之一[10]。在Jeon等[16]的研究中,PA和PMA中都可见染色体复制数的改变,PA中染色体复制数增加的频率更高,而PMA中存在染色体丢失。有研究报道,部分复发的PMA存在“成熟”化转变为PA的倾向[10]。也有研究报道,一例鞍上视交叉区PA,全切后迅速再生,并在随后的复发中“分化”为PMA[17],这进一步说明了PMA与PA间复杂且密切的关系。
2 临床与影像
PA多见于后颅窝,小脑是最常见的起源部位,其次是下丘脑/视交叉区,整个视路神经轴(视神经、视交叉、下丘脑、脑干、丘脑、基底节和大脑半球)都可能受累,发病部位不同,症状不尽相同[18](见图3)。PMA可以发生在中枢神经系统的任何地方,最常见的部位是下丘脑/视交叉区,在脊髓和小脑中少见(见图4)。PMA通常出现在生命的早期阶段,由于这一点,这组肿瘤曾经被认为是PA的“幼稚形式”[2,19],PA的平均诊断年龄为58个月,而PMA为18个月[20]。PMA发生于下丘脑/视交叉区病人的发病年龄较小,主要临床表现为头痛、呕吐、视力、意识水平改变及内分泌症状等[13];PMA发生于后颅窝表现为步态异常、辨距不良、眼球震颤等[8]。

图3 幕上深部中脑、丘脑、基底节区毛细胞型星形细胞瘤CT、MR表现(图片来自山西医科大学第一医院神经外科住院病人资料)

图4 幕下小脑蚓部毛细胞黏液型星形细胞瘤CT、MR表现(图片来自山西医科大学第一医院神经外科住院病人资料)
PA的囊性成分T1上为低信号,T2上为高信号,囊肿壁通常会增强明显,可以看到钙化,周围水肿很少;PMA囊性成分较少,缺乏大的肿瘤囊肿,因此,PMA往往比PA更均质[21]。与PA相比,PMA的类囊体基质使T2信号强度增高、表观扩散系数(apparent diffusion coefficient,ADC)值增高,但上述特点均缺乏特异性[22]。PMA和PA常规MRI十分相似,在T1序列上均为低信号,在T2、FLAIR上均为高信号[21-22]。30%~60%的后颅窝PA病例为囊肿结节型,MRI表现为一个大的囊肿,结节与部分囊壁明显强化;PA也可能会出现肿块型,主要是实体成分,几乎没有囊性成分,但较少见;PMA看起来与PA非常相似,但PMA通常是实性的,囊性少见,其往往有更突出的增强成分。同时,PMA有更高的软脑膜播散可能[21,23-24]。在一项关于动态磁敏感对比灌注成像(DSC)和弥散加权成像(DWI,包括rCBV、K2、ADC)鉴别PA和PMA的研究中,共入组49例病人(幕上:8例PA,6例PMA;幕下:30例PA,5例PMA),结果表明幕上结果均无明显统计学意义;幕下仅rCBV存在统计学意义,受试者工作特征曲线下面积(AUC)=0.867,具有诊断价值,与PA相比,PMA的rCBV更高,特别是在幕下,但样本量较小,有待进一步研究验证[22]。
3 治疗与预后
早期回顾性研究表明,PMA组和PA组的平均发病年龄分别为18个月(2~84个月)和58个月(4~189个月),差异有统计学意义(P<0.01),PMA组和PA组的平均无进展生存期(progress free survival,PFS)分别为26个月和147个月(P<0.001),两组平均总生存期(overall survival,OS)分别为63个月和213个月(P<0.001)[19]。与典型PA相比,PMA病人的PFS和OS时间明显缩短。对于视路胶质瘤,早期放疗为标准治疗,但考虑到儿童脑辐射影响,目前化疗作为一线治疗方案,新研制的靶向药物作为二线甚至首选治疗[25-27]。早期儿童建议化疗,减少放疗;同其他低级别胶质瘤一致,建议术后辅助放疗限制在3~5岁以上病人[8]。对于所有新诊断的儿童低级别星形细胞瘤建议手术尽可能最大范围安全切除,避免造成严重的神经功能缺损[28]。然而,PMA更具有侵袭性的生物学行为可能会影响肿瘤全切除(gross-total resection,GTR),有研究表明,在幕下区域如小脑,90.9%的小脑PA可以实现GTR,而PMA与IPA全切率仅为13.6%[28]。
对于视路PA/PMA,手术治疗效果明显,但可能会带来严重并发症,目前的治疗模式倾向2岁以下视路PA/PMA推荐化疗[29]。3~5岁以上符合手术指征的病人建议手术最大范围安全切除[28],对以下3种情况建议手术基础上进一步放化疗:①首次全切后肿瘤复发;②部分切除后出现神经功能障碍;③部分切除后在长期随访过程中出现影像上的增长,即使没有神经功能症状[8]。同时,对于确诊PMA建议行全脊髓MRI明确有无播散。
在同一解剖位置,PMA比PA更具有侵袭性及更短的PFS和OS[19]。有研究分析83名儿童视路PA/PMA手术治疗后临床预后,结果显示,手术治疗的总体5年和10年PFS率分别为55%和46%,5年和10年的总体OS率分别为87%和78%;相较于PA,PMA的5年OS更短,差异有统计学意义,但仅入组12例PMA或混合型PA/PMA,样本量较小[29]。小脑PMA和IPA统称为“毛黏样谱系星形细胞瘤(PMSAs)”[4]。一项关于小脑PMSAs的研究表明[28],小脑PMA和IPA谱系均表现出较高的脑干侵袭、内部坏死空洞形成、肿瘤复发和软膜播散(leptomeningeal dissemination,LD)发生率(P<0.001),入组66例病人,年龄(7.0±1.5)岁,术中观察脑干粘连/侵袭,在44例PA中观察到4个,10例IPA中有9个可观察到,所有12例PMA均可观察到;术中发现20例PMSA病例存在内部坏死性空洞的形成,9例PA病人存在单纯囊肿形成;术后采用基于儿童肿瘤组(the children′s oncology group,COG)研究的埃及儿童癌症医院(CCHE)低级别胶质瘤(LGG)标准治疗方案中方案A(长春新碱/卡铂)联合化疗,其中10例PMSA(45.5%)与4例PA(9.1%)肿瘤复发(P<0.001);PMSA平均复发间隔为(9.0±1.5)个月,PA为(42±2)个月;PA的复发是实性部位原位复发,而PMSA的复发是囊性复发并贴附于脑干上;同时,PMA肿瘤复发的发生率高于IPA(66.7%和20.0%);PMSA总切除率为13.6%,PA为90.9%(P<0.001);PA的5年总生存率为100%,PMSA为87.5%。
4 中间型毛细胞黏液样肿瘤的形成
2010年Johnson等[4]提出中间型毛细胞黏液样肿瘤(intermedite pilomyxoid tumors,IPMT)或中间型毛细胞黏液样星形细胞瘤(intermediate pilomyxoid astrocytomas,IPA),IPMT的组织学定义是肿瘤中存在一些典型的PMA特征(如小的单形性双极细胞、局灶性黏液样物质、不固定的血管中心生长),且合并一些典型PA的特征(如微囊性改变、 细胞更厚、突起更长、致密的纤维组织和Rosenthal纤维)。
PMA通常位于下丘脑/视交叉区,IPA与PMA类似并同属于毛细胞黏液样肿瘤谱系(PMSAs),均表现出较PA更强的生物学侵袭性[28]。PMA发生于小脑中较少见,小脑IPA比PMA更罕见,除El Beltagy教授等[28]研究入组10例小脑IPA[年龄(7.0±1.5)岁]之外,仅见少数个例报道[4,30-31]。El Beltagy教授等[28]的研究中小脑PMSA的复发率为66.7%,GTR率为8.3%,LD为75%,5年总生存率为87.5%;而在小脑IPA中复发率为20%,GTR率为20%,LD为40%,小脑IPA的预后较小脑PMA更佳。
研究显示,部分复发的PMA,存在“成熟”化转变为PA的倾向[10]。中间肿瘤的存在,以及一些PMA和中间肿瘤随着时间的推移成熟为PA样肿瘤[4],都为PMA和PA之间的生物学关系提供了强有力的支持。El Beltagy等[28]提出,这些肿瘤可能代表一个临床谱系,其良性末端是PA,侵袭性末端为PMA,IPA次于PMA。
综上所述,目前证据表明PMA是PA的变异体,二者在临床、组织学、基因表达等方面有着非常密切的关系,且PMA有更具攻击性的生物学行为。目前,WHO分类还未给出PMA的明确分级,也没有给临床医生留下任何明确的建议。IPA可能是PMA与PA转化过程中的中间类型,需要对IPA进行更多的观察和研究,明确肿瘤形成的生物学机制,进一步整合和分层诊断,从而制定更恰当的治疗方案,改善病人的生存预后。
