化痰逐瘀散结汤联合放化疗治疗晚期非小细胞肺癌的疗效及对免疫功能的影响
2023-05-06张莹陈名涛陈军梅
张莹,陈名涛,陈军梅
目前,肺癌发病率及病死率均居恶性肿瘤的首位。非小细胞肺癌(NSCLC)是肺癌较常见的病理类型,因肺癌早期症状具有隐匿性,导致近70%的NSCLC患者在确诊时病情已发展至中晚期。同步放化疗是临床治疗晚期NSCLC的标准方案之一[1],但不同化疗药物的作用机制、治疗效果及不良反应不尽相同。放化疗相关不良反应是影响肺癌患者生活质量及近期疗效的主要因素。研究表明,中药不良反应少,且有助于提高恶性肿瘤患者的生活质量、延长生存期[2-3]。现观察化痰逐瘀散结汤联合放化疗对晚期NSCLC患者免疫功能的影响,报道如下。
1 资料与方法
1.1 临床资料 选取2019年4月—2022年4月华润武钢总医院收治的100例晚期NSCLC患者作为研究对象,按照随机数字表法分为观察组50例和对照组50例。观察组:男24例,女26例;年龄(57.63±7.15)岁;病理类型:鳞癌28例,腺癌22例;TNM分期:Ⅲa期15例,Ⅲb期12例,Ⅳ期23例。对照组:男27例,女23例;年龄(56.98±7.32)岁;病理类型:鳞癌30例,腺癌20例;TNM分期:Ⅲa期14例,Ⅲb期14例,Ⅳ期22例。2组临床资料比较,差异无统计学意义(P>0.05),具有可比性。本研究内容及流程均符合世界卫生组织《赫尔辛基宣言》中关于人体临床试验伦理学的相关要求。
1.2 病例选择标准 纳入标准:(1)符合《2018年V3版NCCN非小细胞肺癌指南》中的相关诊断标准[4],且为首次确诊;(2)TNM分期为Ⅲ~Ⅳ期;(3)有明确的可评估的肿瘤病灶;(4)卡氏(KPS)评分>60分,预估生存期>6个月;(5)无心、肝、肾等重要脏器功能障碍,可耐受治疗;(6)患者对本研究知情同意。排除标准:(1)既往有肺癌病史者;(2)复发者;(3)近1个月内接受过其他抗癌药物或影响机体免疫功能的药物者;(4)妊娠期或哺乳期妇女;(5)合并其他严重的肺部疾病者,如感染性疾病、活动性结核等;(6)合并精神疾病、血栓/栓塞性疾病、造血系统疾病及出血倾向等疾病者;(7)对本研究药物过敏者。剔除标准:(1)依从性差,未按本研究方案完成治疗者;(2)中途自行退出治疗者;(3)中途脱落者。
1.3 治疗方法
1.3.1 对照组:患者接受同步放化疗综合治疗[5-6]。GP化疗方案:化疗第1、8天,予以注射用盐酸吉西他滨(湖北一半天制药有限公司生产,国药准字H20093568,批号:20190107,2020506,20211103,规格:0.2 g)1 g/m2静脉滴注;第1、2、3天,予以注射用顺铂[费森尤斯卡比(武汉)医药有限公司生产,国药准字H20044945,批号:20190203,2020611,20210905,规格:10 mg/支]30 mg/m2静脉滴注,并予以止吐、保肝、护胃等药物进行对症治疗。以28 d为1个疗程,连续治疗2个疗程。放疗方案:化疗1 d后开始进行第1次的三维适形放射治疗,放疗总剂量为60 Gy,2 Gy/次,5次/周。
1.3.2 观察组:患者在对照组基础上加用化痰逐瘀散结汤治疗,组成包括蜈蚣、红花、牛膝、甘草各10 g,当归、白芍、党参、夏枯草、牡蛎各15 g,黄芪20 g,加水煎至250 ml,于化疗3 d后开始服药,1剂/d,分早、晚两次温服。以4周为1个疗程,连续治疗2个疗程。
1.4 观察指标与方法 (1)免疫功能指标:采用流式细胞仪检测2组治疗前及治疗2个疗程后T淋巴细胞亚群,主要包括CD3+、CD4+、CD8+,计算CD4+/CD8+。(2)不良反应。
1.5 近期疗效判定标准[7]治疗2个疗程后复查胸部CT,根据WHO《实体瘤疗效评价标准》判定临床疗效,完全缓解(CR):病灶基本消失,未发现新病灶;部分缓解(PR):病灶总面积缩小,单个病灶面积缩小≥50%,且未发现新病灶;稳定(SD):病灶总面积缩小,单个病灶面积缩小<50%,或任一病灶面积增大但<25%,且无新发病灶;恶化(PD):病灶总面积或单个病灶面积增大>25%,或出现新病灶。客观缓解率(RR)=(CR例数+PR例数)/总例数×100%。

2 结 果
2.1 近期疗效比较 观察组RR为74.0%,高于对照组的46.0%(χ2=8.167,P=0.004),见表1。
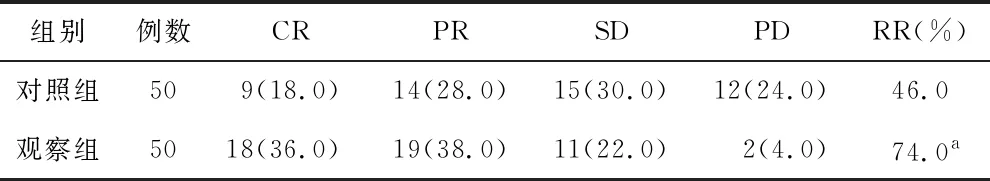
表1 对照组与观察组近期疗效比较 [例(%)]
2.2 T淋巴细胞亚群比较 治疗前,2组CD3+、CD4+、CD8+、CD4+/CD8+及治疗2个疗程后CD3+、CD8+比较,差异无统计学意义(P>0.05)。治疗2个疗程后,对照组CD4+、CD8+、CD4+/CD8+较治疗前降低,观察组CD4+、CD4+/CD8+较治疗前升高,而观察组CD4+、CD4+/CD8+高于对照组(P<0.05),见表2。

表2 对照组与观察组治疗前后T淋巴细胞亚群比较
2.3 不良反应发生率比较 治疗期间,观察组不良反应总发生率为8.0%(4/50),低于对照组的24.0%(12/50)(χ2=4.762,P=0.029),见表3。
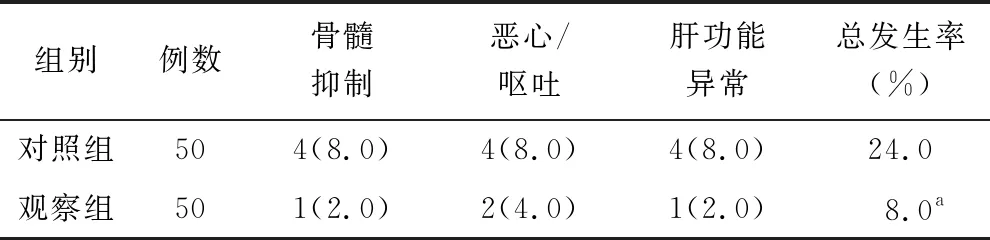
表3 对照组与观察组不良反应发生率比较 [例(%)]
3 讨 论
多数NSCLC患者在确诊时病情多为晚期,预后差,复发率高。晚期NSCLC患者的5年生存率不超过15%。目前临床对晚期NSCLC的治疗主要采用放化疗、生物分子免疫治疗等综合治疗方案[8-10]。针对NSCLC患者的放化疗治疗在抗肿瘤的同时也会对机体正常组织、免疫系统造成损伤。化疗及放疗相关不良反应可导致NSCLC患者机体受损,影响疗效。目前晚期NSCLC的治疗原则以降低不良反应、提高近期疗效及在一定程度上提高患者的生存质量为主。中医研究认为,对放化疗的NSCLC患者应用中医药汤剂有助于改善肺功能、稳定病情[11-12]。
中医学认为,晚期NSCLC以“正气亏虚、癌毒四散”为病机,因患者正气亏虚、脏腑虚弱,导致邪毒内生或外侵,机体内瘀、毒、痰、热凝聚成肿块。肺癌属“因虚致实、因虚致病”。肺癌患者普遍表现为痰凝、气滞、血瘀、毒聚等中医证候,晚期患者的正气虚损更甚。同步放化疗是临床治疗晚期NSCLC患者的常用治疗方案,但其对发挥抗肿瘤作用的同时存在较大的治疗/药物相关不良反应,部分患者可能由于骨髓抑制、免疫功能下降等不良反应而终止治疗。中医学认为,晚期NSCLC患者治疗应以“扶正”为主、兼顾“祛邪”为辅的原则。
放化疗相关不良反应主要包括骨髓抑制、消化道反应(恶心/呕吐)和肝功能异常。本研究结果显示,观察组不良反应总发生率(8.0%)低于对照组(24.0%),表明联合化痰逐瘀散结汤可降低放化疗相关不良反应,具有较高的安全性。晚期NSCLC患者的病情发展与免疫功能关系密切。相关研究表明,晚期NSCLC患者多存在免疫功能下降[13],直接影响其生存质量。机体通过细胞免疫应答发挥抗肿瘤作用。T淋巴细胞介导的特异性免疫反应能促使机体发挥抗肿瘤作用,T淋巴细胞异常表达,如Th1细胞下降、Th2细胞升高,Th1/Th2下降,则提示机体免疫功能下降。因此,T淋巴细胞亚群CD3+、CD4+、CD8+是评估肿瘤患者免疫功能的重要指标。本研究中观察组RR及CD4+、CD4+/CD8+高于对照组,表明化痰逐瘀散结汤联合放化疗治疗晚期NSCLC的近期疗效更佳,可提高机体免疫功能。笔者分析认为,观察组患者在放化疗基础上联合应用中药方剂化痰逐瘀散结汤,该方中的蜈蚣、牡蛎可软坚散结;黄芪、党参可扶正;当归、红花可化瘀;甘草可祛痰、调和药效;夏枯草可理气;甘草可调和药效,诸药组分共同作用可起到扶正、软坚、散结的作用[14-15]。故该中药方可增加机体免疫力,将其用于放化疗的晚期NSCLC患者有助于促进病灶消失,减轻病情,提高疗效。
综上所述,化痰逐瘀散结汤联合放化疗治疗晚期NSCLC的近期疗效确切,可提高机体免疫力,减少不良反应,安全性较高。
利益冲突:所有作者声明无利益冲突。
