MnOx-CeO2催化剂中元素价态对低温SCR还原NOx性能的影响
2023-03-16李松达郑红梅郭成成赵志浩杨杭生
郑 拓,王 飞,2,李松达,郑红梅,2,3,张 彦,张 玉,郭成成,张 凯,邵 博,赵志浩,王 勇,2,杨杭生
(1.浙江大学硅及先进半导体材料全国重点实验室,材料科学与工程学院, 浙江 杭州 310027; 2.浙江大学电子显微镜中心,硅及先进半导体材料全国重点实验室,材料科学与工程学院, 浙江 杭州 310027; 3.浙江巨化技术中心有限公司, 浙江 衢州 324004; 4.浙江衢化氟化学有限公司, 浙江 衢州 324004; 5.浙江巨化环保科技有限公司, 浙江 衢州 324004)
1 前 言
随着国民经济的快速发展和人民消费水平的不断提升,环境污染的问题也越来越严重并日益威胁到人类的健康。其中大气污染是环境问题中尤为突出的一个。在硫氧化物的排放得到有效控制后,氮氧化物(NOx)成为了最主要的大气污染物[1]。目前成熟的NOx排放控制技术包括低氮燃烧技术、选择性非催化还原技术、以及选择性催化还原技术(SCR)[2]。其中SCR因其合理的运行成本和理想的脱硝效率,已经在我国的燃煤电厂得到普及,保障了燃煤电厂NOx的达标排放。
SCR技术是在催化剂表面利用NH3作为还原剂与NO反应生成无害的N2和水,其核心技术是催化剂制备技术[2]。在燃煤电厂使用的SCR催化剂的主要成分是V2O5(WO3)/TiO2,适合的工作温度是320~400 ℃,工作温度低于320 ℃会导致催化剂活性下降和SO2中毒,而当工作温度超过400 ℃时,会引起NH3的深度氧化,降低脱硝效率[3],针对许多非电锅炉的尾气脱硝而言,理想的工作温度一般是100~300 ℃的低温范围,并不适合采用V2O5(WO3)/TiO2催化剂,因而低温活性SCR脱硝催化剂成为研究热点,其中锰基催化剂由于其具备多种化学价态而显示出极强的低温SCR活性,CeO2因其优异的储释氧能力以及Ce3+和Ce4+之间的快速转换而成为最佳的低温脱硝催化剂载体。所以MnOx-CeO2复合催化剂显示优异的低温活性而备受关注[4]。
研究显示,制备方法上的差异会使催化剂具有不同的催化活性,并且锰铈之间的相互作用也会随制备方法的不同发生变化。姚小江等[5]测试了不同制备方法对MnO2-CeO2催化剂低温下的NH3-SCR脱硝性能的影响,发现不同方法制备的锰铈催化剂的低温脱硝性能有如下顺序:水热法>溶胶-凝胶法>共沉淀法>浸渍法。并认为该排序与催化剂表面Ce3+、Mn4+含量、氧空位、吸附氧物种浓度及酸位数量的顺序一致。
姜冬宇[6]制备了一系列的MnOx-CeO2催化剂,通过对其进行催化反应活性测试,焙烧温度500 ℃,锰元素摩尔占比为32%时,纳米球催化剂表现出最好的脱硝性能。结合表征结果,认为该条件下的催化剂拥有较大的比表面积,以及丰富的表面活性氧是高催化活性的关键。但是,该体系催化剂中Mn和Ce元素的多种变价并相互作用,近来的研究结果显示,Mn-Ce之间可能的电荷转移是协同作用的本质[7-10]。因此系统研究Mn和Ce元素的化合价对脱硝性能的影响,对揭示其协同机制的具有重要价值。
金属有机骨架结构(MOFs)及其衍生物具有多变的结构,高比表面积等特点[11],是催化剂制备过程中结构调控的一种有效选择,也为调控MnOx-CeO2催化剂的结构与性能提供了一条新的途径[12]。基于此,本研究以Ce-MOFs材料为前驱体,优化制备出了一系列价态与浓度可调的MnOx-CeO2低温SCR催化剂,然后结合一系列表征手段合理解释了不同催化剂脱硝性能差异的可能原因。
2 实 验
2.1 催化剂的制备
以Ce-MOFs结构为牺牲模板制备MnOx-CeO2催化剂,CeO2-MOFs前驱体的具体合成过程为:配置浓度为0.5 mol/L的Ce(NO3)3溶液,浓度为12.5 mol/L的1,3,5-间三苯甲酸溶液,溶剂为体积分数为50%的乙醇-水溶液,溶质为1,3,5-间三苯甲酸。将Ce(NO3)3溶液和1,3,5-间三苯甲酸溶液混合,搅拌10 min后将得到的悬浊液进行3次离心和洗涤,将获得的沉淀物在40 ℃烘干12 h后研磨,得到粉末状的CeO2-MOFs前驱体。
合成CeO2载体的过程为:将CeO2-MOFs前驱体在300~900 ℃下煅烧,煅烧条件:5 ℃/min的升温速度升温至指定煅烧温度后保温120 min,然后自然降温,得到需要的CeO2粉末载体。
用研磨法负载MnOx制备MnOx-CeO2催化剂,具体过程为:将得到的CeO2粉末载体用少量乙醇润湿,加入CeO2质量分数10%的四水乙酸锰进行混合研磨,将研磨均匀的粉末在马弗炉中300~700 ℃保温360 min,自然降温后得到所需的MnOx-CeO2催化剂。
为了便于讨论,把催化剂的设计分为二段式,首先固定了Mn的负载温度为300 ℃,同时将CeO2的热处理温度分别设定为300,500,700及900 ℃,定义为催化剂M3Cx。在找出最优性能所对应的CeO2热处理温度(700 ℃)后,固定此载体热处理温度,将Mn负载温度分别设定为300,500和700 ℃,定义为催化剂MyC7。其中,M代表MnOx,C代表CeO2,x是CeO2制备过程中的热处理温度,而y是负载MnOx时的催化剂的热处理温度,单位是100 ℃。
2.2 SCR脱硝活性测试
将制备得到的MyCx催化剂在SCR微型反应器中进行脱硝性能测试。具体测试条件为:先将煅烧得到的催化剂粉末进行压片,而后过筛选取40~60 目之间的催化剂粉末0.5 g装进石英管中。测试过程中气体配置为:NH3和NO的浓度分别为612和347 mg/m3,同时混入体积分数5%的O2,以N2作为载气,将气体总流量保持在600 sccm。将混气通过装有催化剂的石英管,并使石英管在300 ℃保温40 min,之后以2 ℃/min的速度降低微型反应器的温度直至100 ℃,期间每间隔25 ℃保温记录石英管出入口处NO、NO2、O2、N2O的含量。
氮氧化物转化率的计算公式为:
(1)
式中:NOx(入口)和NOx(出口)分别表示石英管入口处和出口处测定的NOx浓度,NOx浓度为NO和NO2浓度的总和。
N2选择性的计算公式为:
(2)
式中:N2O表示出口处N2O的浓度。
2.3 催化剂的结构表征
使用X射线衍射仪(Rigaku Smartlab)测量催化剂的XRD图谱。使用场发射扫描电子显微镜(Hitachi SU70,SEM)和透射电子显微镜(日本JEOL JEM-F200,TEM)观察催化剂的微观形貌。采用美国Micromeritics ASAP 2460进行比表面积、平均孔径、和孔容的测试。采用美国Thermo Scientific K-Alpha XPS光电子能谱仪分析催化剂的XPS图谱,该仪器的XPS光源为Cu Kα,其能量为1 486.6 eV,并用位于284.8 eV的C 1s进行峰位校正。采用日本Microtrac BELCat II测试催化剂的NH3和NO的吸脱附情况,具体条件为:称取100 mg样品置于反应管中,以10 ℃/min从室温程序升温至300 ℃干燥预处理,He 气流(30~50 mL/min)吹扫1 h,冷却至50 ℃,通入10% NH3(NO)/He混合气(30~50 mL/min)1 h至饱和,切换He气流 (30~50 mL/min)吹扫1 h 除去表面弱的物理吸附NH3(NO),最后在He气氛下以10 ℃/min 的升温速率升至500~800 ℃脱附,用TCD测量脱附气体的浓度。
3 结果与讨论
3.1 催化剂的SCR脱硝活性
利用Ce-MOFs前驱体制备的纯CeO2载体的脱硝性能,如图1(a)所示,在100~300 ℃的温度范围内,四种煅烧温度下获得的CeO2催化剂的低温脱硝活性顺序依次为:500 ℃>300 ℃>700 ℃>900 ℃,并且NO转化率都低于30%,说明以Ce-MOFs为前驱体通过煅烧制备的纯CeO2并不是非常好的低温SCR脱硝催化剂。
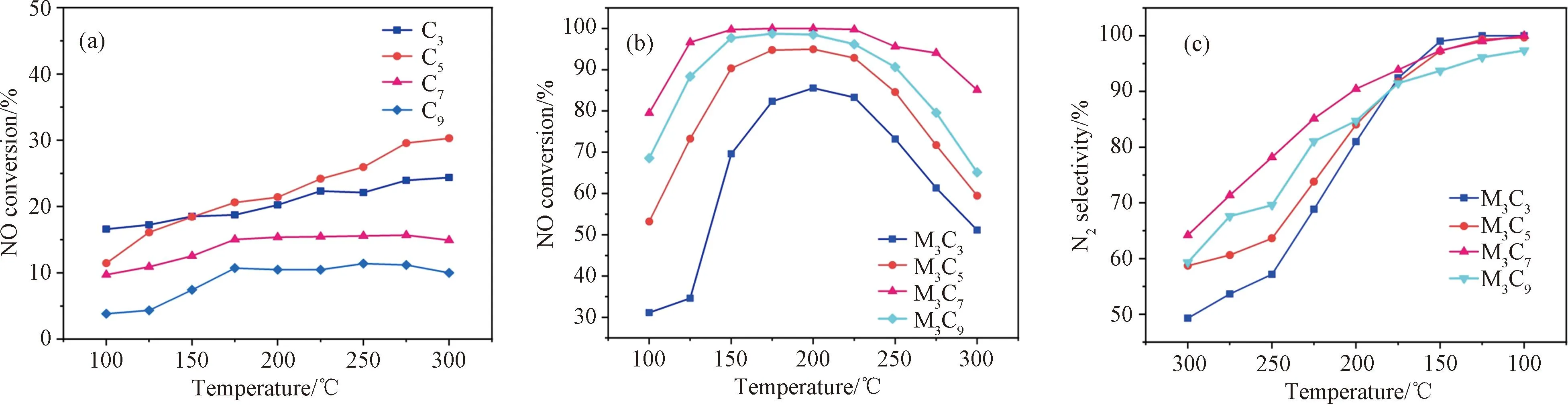
图1 MCx催化剂脱硝效率的温度依存性,(a) 纯CeO2;(b) M3Cx催化剂;(c) M3Cx的N2选择性
以CeO2为载体制备的M3Cx催化剂的NO转化率如图1(b)所示。在100~300 ℃的温度范围内,催化剂脱硝性能得到了全面的提升,脱硝活性顺序如下:M3C7>M3C9>M3C5>M3C3,简言之,脱硝性能随载体CeO2热处理温度而升高,700 ℃达到最佳,继续升高温度性能开始下降。尤其在催化剂M3C7上,在100 ℃时已经达到80%的脱硝效率,在150~250 ℃的温度范围内,脱硝效率接近100%。其中催化剂MC3的性能略差,推测可能是300 ℃的低温下热处理,MOFs结构没有完全坍塌分解。
M3Cx催化剂的N2选择性如图1(c)所示,MnOx的强氧化性易使NH3深度氧化,在脱硝过程中产生N2O副产物[12],可以看到在100~300 ℃的温度范围内,催化剂的N2选择性随反应温度的升高逐渐降低,当温度在150~175 ℃时,N2的选择性基本能达到90%以上,尤其是催化剂M3C7,在200 ℃时的N2的选择性还能保持90%,而在该温度窗口MC7催化剂的催化脱硝性能已可以接近100%。
使用不同温度负载Mn所制备的MyC7的NH3-SCR脱硝性能如图2(a)所示,发现随负载温度的升高,对应的SCR脱硝性能会有一定程度的下降,M3C7能在150~200 ℃达到接近100%的NO转化率,M5C7在150~220 ℃的温度窗口内最高转化率下降到90%,M7C7则下降到80%左右,比M3C7下降了大约20%。催化剂的N2选择性如图2(b)所示,可以看到与图1(c)类似,三组催化剂的N2选择性都随着反应温度升高的而下降,并且在200 ℃以下可以达到90%。
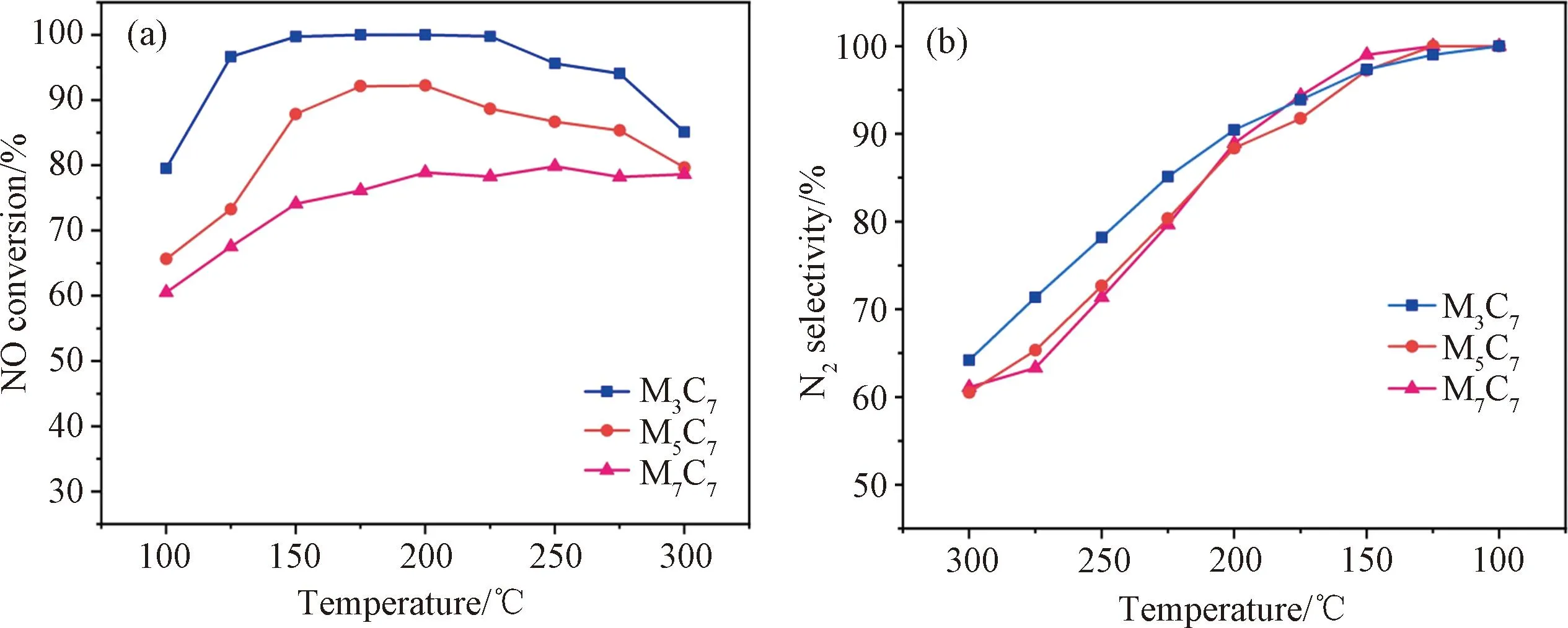
图2 MyC7催化剂的脱硝效率的的温度依存性,(a) NO转化率;(b) N2选择性
综上所述,700 ℃热处理CeO2载体,然后300 ℃热处理负载锰的催化剂制备的MnOx-CeO2催化剂的低温SCR脱硝性能优异,同时,在反应温度不高于200 ℃时,可以保持90%的N2选择性。
3.2 催化剂的结构与形貌分析
催化剂M3Cx和MyC7的XRD图谱如图3所示。图3(a)为M3Cx的XRD图谱与CeO2(PDF#78-0694)标准卡片对比,可以看出,所有的衍射峰都可以归属于CeO2,并未发现与MnOx相关的任何衍射峰,这说明锰氧化物在CeO2上的负载后的分散性较好,或者因为热处理温度偏低,MnOx以无定形的方式负载在CeO2上[13]。利用谢乐公式计算图3(a)中四种M3Cx的CeO2晶粒尺寸显示,分别为M3C3:7.08 nm,M3C5:10.52 nm,M3C7:22.59 nm和M3C9:40.62 nm。随着CeO2载体的热处理温度的升高,CeO2的衍射峰变得尖锐,半高宽变窄,晶粒变大,一定程度上降低了催化剂的比表面积,这也与文献报道一致[14]。
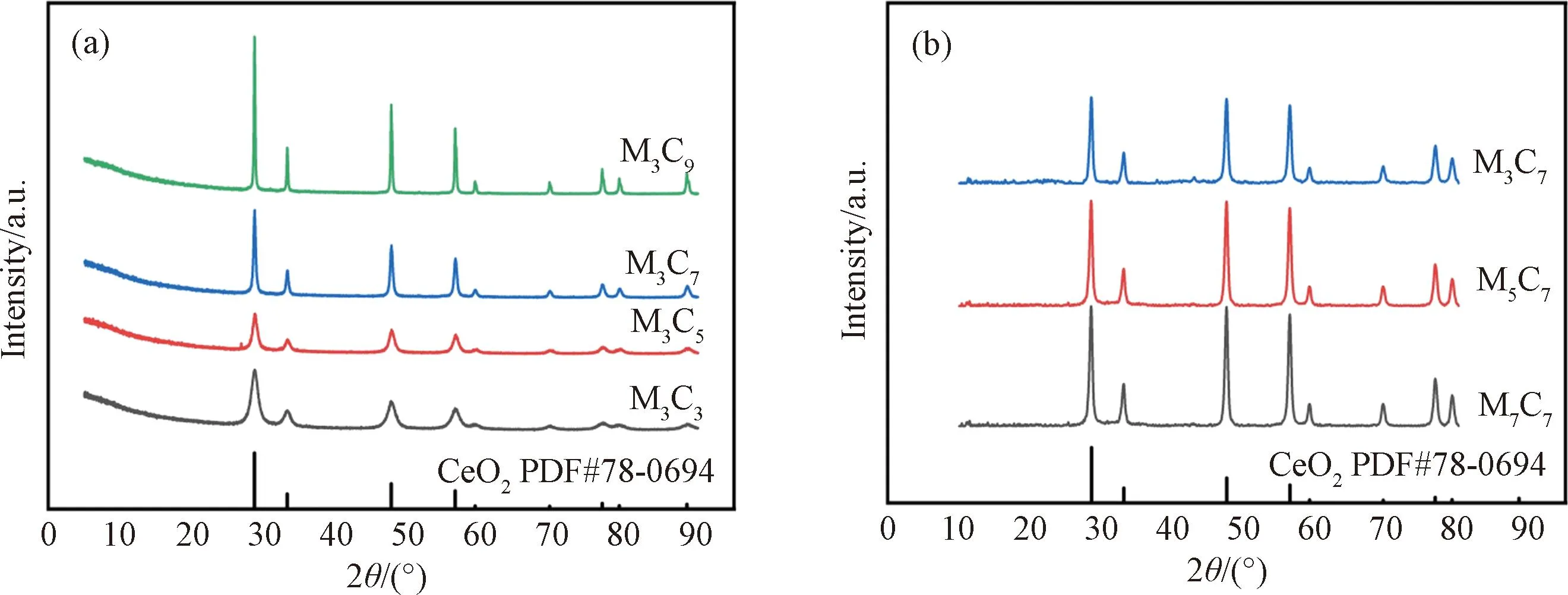
图3 催化剂的XRD图谱 (a) M3Cx (b) MyC7
不同温度负载MnOx的MyC7催化剂的XRD衍射图谱如图3(b)所示,所有的衍射峰都可以归属于CeO2,这个温度范围的热处理没有改变锰氧化物在CeO2上的负载,说明MnOx高度分散[13]。随着热处理温度的升高,MyC7催化剂中CeO2的衍射峰变化不明显,通过谢乐公式进行计算,M3C7、M5C7以及M7C7催化剂的平均晶粒尺寸分别为 22.59,25.79和29.40 nm。说明负载温度的提升基本不改变催化剂载体的晶粒尺寸。这是因为在CeO2载体制备的过程中,对Ce-MOFs的热处理温度已经达到700 ℃,而在不同MxC7催化剂制备过程中锰的负载温度均不超过700 ℃,所以负载MnOx时不改变CeO2载体的烧结状态。
CeO2载体、M3Cx和MyC7的BET比表面积、平均孔径和平均孔容如表1~3所示。与CeO2载体的比表面积相比(表1)可以发现,负载锰氧化物之后,催化剂的比表面积有小幅度的增大,但是300 ℃煅烧的CeO2在负载Mn之后比表面积出现巨大的增大,从27.40 m2·g-1增加到98.20 m2·g-1,进一步说明300 ℃下2 h的煅烧并不能使CeO2-MOFs的MOFs结构完全坍塌[15],这与图1(b)的性能结果相对应。图4是催化剂M3Cx的扫描电镜图,可以看出,M3C3样品的棒状结构保持最好,用500 ℃煅烧得到的CeO2样品的仍有比较清晰的棒状结构,而700 ℃和900 ℃煅烧得到的CeO2的棒状结构被显著破坏,并出现明显的烧结和晶体长大的现象,验证了其比表面积的差异。同时结合催化剂的脱硝性能进行比较,发现在不负载Mn时,CeO2的催化性能与比表面积大小呈现正相关[15],说明对于纯CeO2而言,由于其本身催化性能较差,比表面积是影响其脱硝性能的主要原因之一。如表2所示,M3Cx催化剂的脱硝性能并没有随比表面积的增大而增加,说明催化性能提升不是由比表面积的变化引起的。随着负载Mn时的热处理温度升高,MyC7催化剂的比表面积呈现下降趋势。如表3所示,与CeO2载体的平均比表面积6.71 m2/g相比,M3C7的平均比表面积为21.10 m2/g,M5C7为15.31 m2/g,而M7C7为9.31 m2/g。可知提高Mn负载时的热处理温度,会使催化剂上的MnOx一定程度烧结团聚。M7C7的比表面积比M3C7的比表面积下降了50%,进一步说明比表面积大小不是本研究制备的催化剂的性能决定性因素。
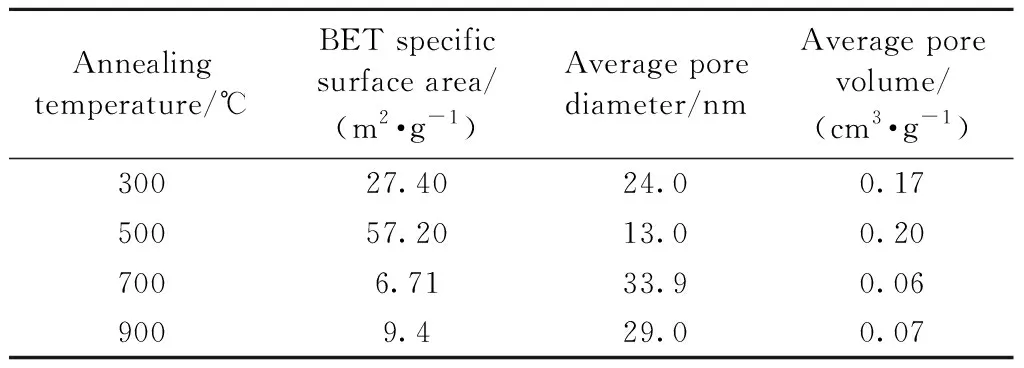
表1 催化剂载体CeO2的BET比表面积、平均孔径和平均孔容
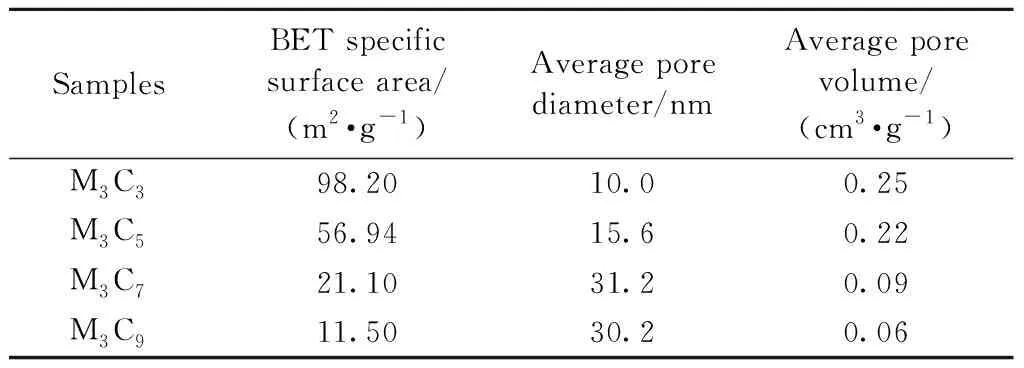
表2 催化剂M3Cx的BET比表面积、平均孔径和平均孔容
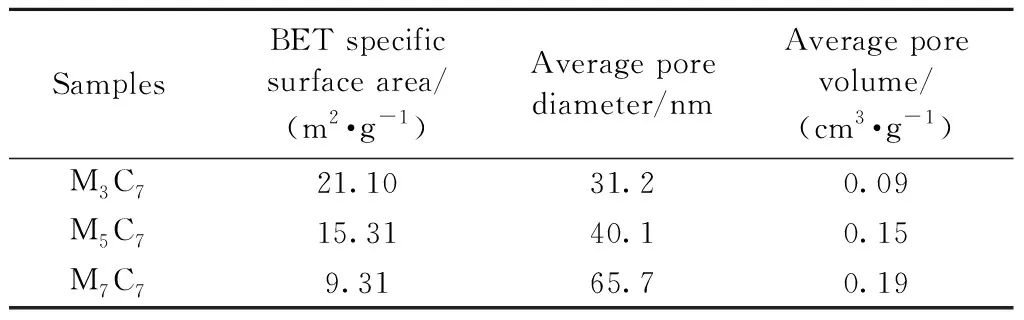
表3 催化剂MyC7的BET比表面积、平均孔径和平均孔容

图4 催化剂的SEM图修和EDX线扫分析 (a) M3C3的SEM图像; (b) M3C5的SEM图像; (c) M3C7的SEM图像; (d) M3C9的SEM图像; (e),(f) M3C7的EDS线扫能谱
进一步使用TEM电镜观察M3C7催化剂,如图5所示,测量催化剂的晶面间距,发现观测到的晶面主要是CeO2(111)晶面,同时还能发现少量的(220)以及(200)晶面,没有看到MnOx相关的晶格条纹,进一步说明MnOx的高度分散,符合图3的XRD测试结果。

图5 不同分辨率下M3C7催化剂的TEM图像
3.3 XPS结果分析
在锰铈体系催化剂中,催化剂表面的元素组成以及价态影响催化剂对反应物分子的吸附和活化,进而对其催化性能产生重要的影响。图6是催化剂的XPS图谱,其中图6(a)是M3CxCe 3d的XPS图谱,根据文献报道[16-20],Ce 元素电子结合能位于882.3,900.8,888.5,907.4,898.2和916.6 eV的峰归属于表面Ce4+,884.4和903.0 eV的峰归属于表面Ce3+。在M3Cx催化剂中,四价铈离子作为强氧化剂,可以把体系中的Mn2+离子氧化成Mn3+,同时将氧空位固定在表面[7]。原始CeO2载体中的Ce4+离子浓度越高,氧化Mn2+离子的能力就越强,就会在CeO2载体的表面生成氧空位,活化O2,从而提升催化剂的脱硝性能。而当原始CeO2中含有高浓度的Ce3+时,CeO2中的氧空位只能稳定存在于CeO2的亚表面,会降低CeO2的氧化能力,不利于Ce4+氧化Mn2+,CeO2表面的氧空位浓度就会下降,不利于活化O2分子,从而降低M3Cx催化剂的低温活性[7]。
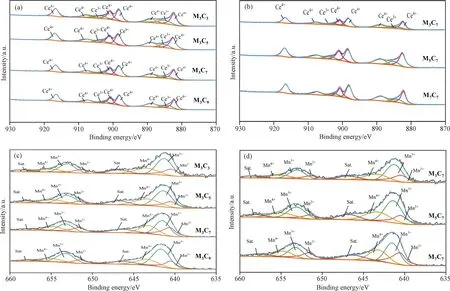
图6 催化剂的XPS图谱: (a) M3Cx Ce 3d; (b) M3Cx Mn 2p; (c) MyC7 Ce 3d; (d) MyC7 Mn 2p
图6(c)是M3Cx催化剂的Mn 2p的XPS谱图,根据文献报道[18-24],电子结合能位于640.48和651.38 eV 分别对应Mn2+的2p 3/2 和2p 1/2,电子结合能位于641.29和653.04 eV分别对应Mn3+的2p 3/2和2p 1/2,电子结合能位于643.34和655.04 eV分别对应Mn4+的2p 3/2和2p 1/2,电子结合能位于646.77和658.57 eV的是卫星峰。催化剂M3Cx中的Ce4+离子浓度和Mn2+、Mn3+离子浓度如表4所示,可以看到四组催化剂中催化活性最好的M3C7催化剂拥有最高的Ce4+、Mn2+与Mn3+浓度,和最低的Mn4+离子浓度。
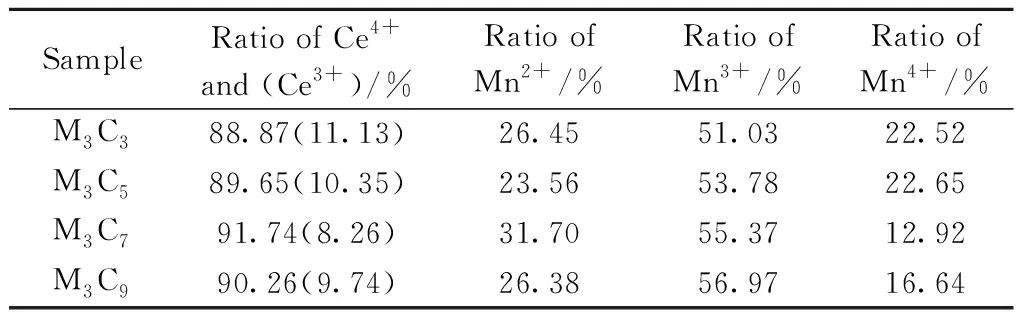
表4 催化剂M3Cx中的Mn、Ce元素价态分布
图6(b)是催化剂MyC7的Ce 3d的XPS图谱,图6(d)是MyC7催化剂的Mn 2p的XPS谱图,其Ce4+比例以及Mn元素各价态的比例如表5所示。Mn负载时的从300~700 ℃热处理,基本不改变样品中的Ce4+(大约90%)和Mn3+离子的浓度(大约55%),但是伴随温度的提升,Mn4+的占比逐渐增加,从M3C7的13.7%增加到了M7C7的20.2%,而Mn2+离子浓度从31.2%降低到24%。即催化活性随着Ce4+离子、Mn2+离子和Mn3+离子的提高而提高,随着Mn4+离子的提高而降低。
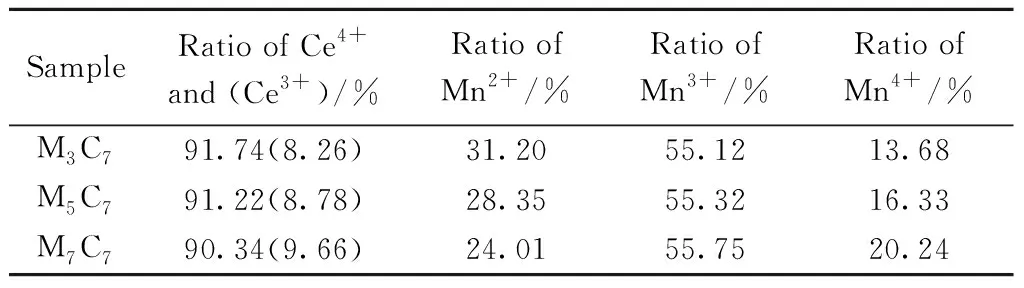
表5 催化剂MyC7中的Mn、Ce元素价态分布
3.4 NH3-TPD分析
图7是催化剂的NH3-TPD曲线,从图7(a)可以看到M3Cx催化剂有三个明显的NH3脱附峰,分别位于100、150和300 ℃附近,对应于催化剂表面弱酸性位、中强酸性位和强酸性位。随着原始CeO2载体的热处理温度的提高,相应的催化剂的NH3脱附峰面积增大且向高温移动,说明增加了酸性位点的密度和酸强度,有利于NH3的吸附活化。图7(b)是MyC7催化剂的NH3-TPD曲线,可以看到负载MnOx时的热处理温度同样有利于增加催化剂的表面酸性位点密度和强度。从NH3的完全脱附温度可知,在反应条件下NH3应该是仍然吸附在催化剂上的。对比图7和图1与图2,说明酸性位点密度和强度也不是决定脱硝性能的关键因素。
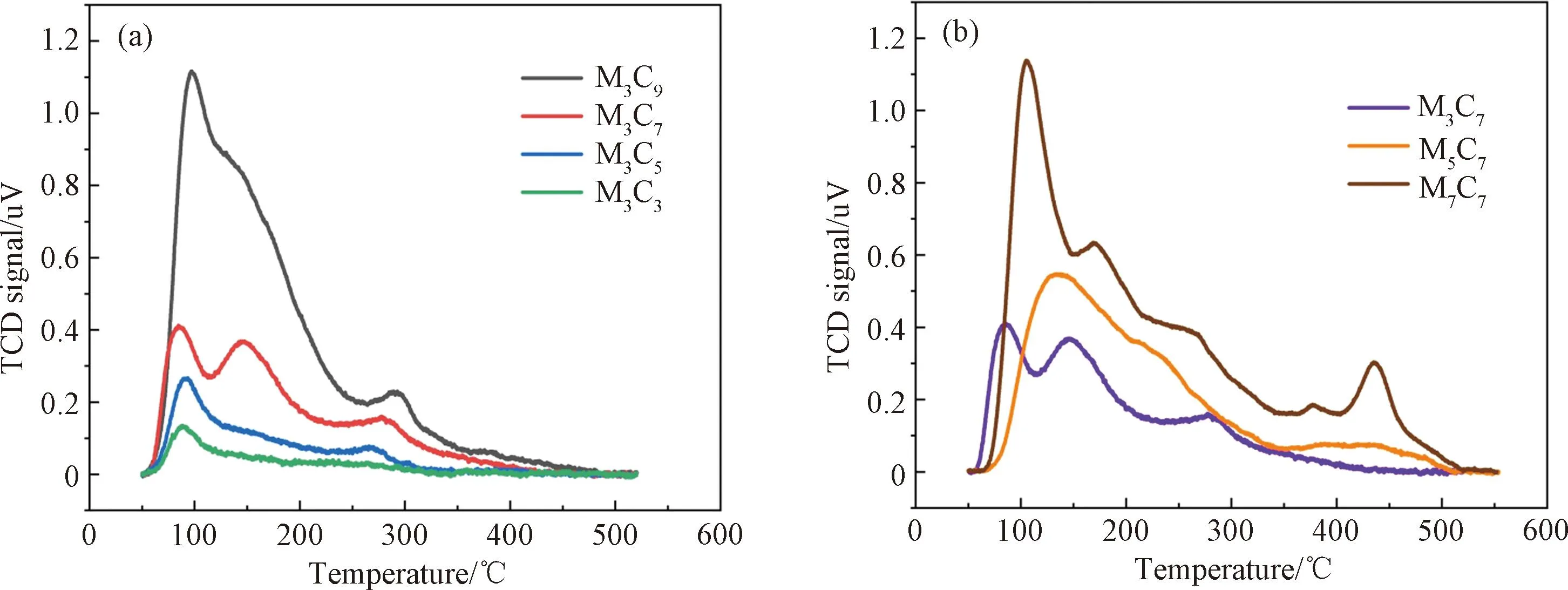
图7 催化剂的 NH3-TPD图谱:(a)M3Cx;(b)MyC7
3.5 NO-TPD分析
图8(a)是催化剂M3Cx的NO-TPD曲线,NO有两个的脱附峰,分别位于100~300 ℃和300~600 ℃。尤其是第二个脱附峰高于300 ℃,说明在整个100~300 ℃的实验温度范围内,催化剂上仍然有NO的吸附,且伴随着CeO2的制备温度的提高,NO的吸附量增加,吸附强度也有所增强。其吸附性能受温度的影响趋势与图7(a)的NH3-TPD一致。MyC7催化剂的NO-TPD结果如图8(b)所示,三个样品有非常类似的NO脱附行为,同时在300 ℃以上还存在一个较强的脱附峰。图7和图8说明在整个催化剂性能测试过程中NO和NH3都吸附在催化剂上。

图8 催化剂的 NO-TPD图谱: (a) M3Cx;(b) MyC7
3.6 催化剂上SCR反应路径分析
在SCR反应过程NH3与NO的反应涉及到气体的扩散、吸附、活化、反应等过程,其中存在两种可能的反应路径,分别为L-H路径和E-R路径。在E-R路径中,NH3气体分子首先吸附在催化剂表面酸性位点上,NH3由气体变为吸附态的NH3/NH4+物种,接着这些物种在高价态的氧化还原位点反应生成活性NH2/NH3+物种,这些活性氨物种随即与气态NO反应生成活性中间产物NH2-NO/NH3+-NO,最后的反应产物为N2和H2O。而在L-H路径中,不但NH3吸附活化形成NH3/NH4+物种,NO也被吸附在表面后被氧化成活性硝酸盐或亚硝酸盐,这些活性产物与NH3/NH4+反应形成NH4-NO2/NH4-NO3,最后反应产物为N2和H2O。该路径中的氧化还原循环与E-R路径一致,高价态氧化还原位点的再生意味着整个循环的完成[25]。

需要强调的是,催化剂的活性随Mn4+离子的浓度增加而下降,说明Mn4+离子应该不是催化剂的活性位点。在MyC7催化剂中,随着负载温度的升高,Mn4+离子浓度升高的同时,比表面积也明显下降,说明MnOx存在烧结长大的可能,Mn4+离子被固定在MnOx团簇的内部,不参与脱硝反应,应该是导致催化活性降低的原因。而催化活性随Mn2+离子浓度的增加而增加,可能的原因是Mn2+参与了CeO2表面氧空位的形成,有利于活化O2,从而有利于低温脱硝,另一个可能的原因是Mn2+参与了快速SCR反应。
3.7 催化剂的稳定性分析
在实际使用中,催化剂的稳定性是重要的评价标准之一,所以选取MC7催化剂,保持实验的混气测试条件在175 ℃保温测试50 h的脱硝性能。结果如图9所示,在50 h内的NOx转化率接近100%,且保持不变,没有性能下降的趋势,证明该催化剂具有良好的稳定性。
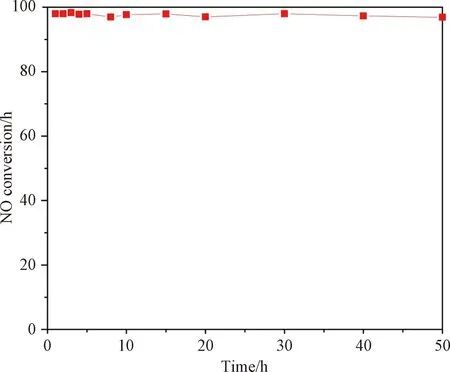
图9 M3C7催化剂在175 ℃下的稳定性测试
4 结 论
本研究以Ce-MOFs结构为前驱体,通过不同温度煅烧得到CeO2载体后,负载MnOx制备得到一系列的MnOx-CeO2催化剂,其中性能最好的MnOx-CeO2催化剂是由700 ℃热处理CeO2温度,300 ℃负载MnOx制备得到的,在100~300 ℃温度范围内的脱硝效率超过90%,且在175~200 ℃范围内的NOx转化率近乎100%。实验结果显示,在MnOx-CeO2催化剂上SCR脱硝反应主要遵循L-H路径,整个催化过程可以分为两个循环,分别是Mn的氧化还原循环和Ce的氧化还原循环。催化剂表面的高浓度Ce4+离子、Mn2+和Mn3+浓度,促进了催化剂表面的两个氧化还原循环过程,从而促进了催化剂的低温SCR脱硝活性。该实验结果对进一步开发优异的低温SCR脱硝催化剂,以及揭示低温SCR脱硝机理具很好的参考价值。
