4种狂犬病病毒ELISA抗体检测试剂盒的评价
2023-03-14刘婷芳蔡冬冬李盛琼杨天俊黄雅琳袁东波阳爱国
高 露,刘婷芳,蔡冬冬,李盛琼,尹 杰,杨天俊,张 亮,黄雅琳,袁东波,阳爱国,侯 巍
(1.四川省动物疫病预防控制中心,四川成都 610041;2.军事医学研究院军事兽医研究所,吉林长春 130122;3.富顺县农业农村局,四川富顺 643200)
狂犬病(rabies)是由狂犬病病毒(rabies virus,RV)感染引起的人兽共患烈性传染病,临床表现为特异性恐风、恐水以及咽肌痉挛、进行性瘫痪等,病死率高达100%,给公众生命健康带来严重威胁。我国报告的狂犬病发病数仅次于印度,居世界第二位[1]。分析我国狂犬病患者发现,经犬咬伤感染的达90%以上[2]。狂犬病目前尚无有效治疗手段,疫苗免疫是预防该病的唯一途径[3],因此对犬进行疫苗免疫能有效筑牢狂犬病防控的第一道防线。
世界动物卫生组织(WOAH)和世界卫生组织(WHO)推荐,当血清中RV中和抗体效价大于0.50 IU/mL时,疫苗免疫才视为成功,能够产生免疫保护效力。目前,WOAH和WHO均推荐的狂犬病血清学检测方法只有两种,分别是荧光抗体病毒中和试验(fluorescent antibody virus neutralization test,FAVN)和快速荧光灶抑制试验(rapid fluorescent focus inhibition test,RFFIT)。这两种方法均能检测血清样品中的RV中和抗体效价,可有效评估疫苗免疫效力,但均需高度可控的环境用于细胞培养和病毒复制,且需耗时48 h[4]。因此,需要更快速、常规的技术替代这些试验。酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA)目前在很多感染性疾病的血清学诊断中应用较广泛,其操作简便,也不需要生物安全高级别实验室[5]。此外,ELISA对野外收集的因溶血有细胞毒性,对血清中和试验结果有影响的样品同样有效[6]。根据WOAH《陆生动物诊断试验与疫苗手册》,ELISA 是评估免疫效果的最佳方法之一。目前国内常用商品化ELISA试剂盒检测犬RV疫苗免疫后抗体,国外也有经WOAH评估后推荐的ELISA试剂盒,用于犬猫免疫后血清学检测。为了解国产ELISA抗体检测试剂盒的性能,本研究选择了4种国产试剂盒,分别检测463例犬血清样本,以血清学检测方法金标准FAVN为对照,分析比较这几种试剂盒的诊断敏感性、诊断特异性、符合率等,以期为犬RV疫苗免疫效力评价时选用更好的试剂盒提供参考。
1 材料和方法
1.1 材料
1.1.1 血清 犬血清共计463份,来自军事医学研究院军事兽医研究所。样品已通过FAVN检测RV中和抗体效价,根据不同抗体效价范围分为5组(表1)。从5组血清中,每组随机选择2份,共10份血清,用于重复性试验。
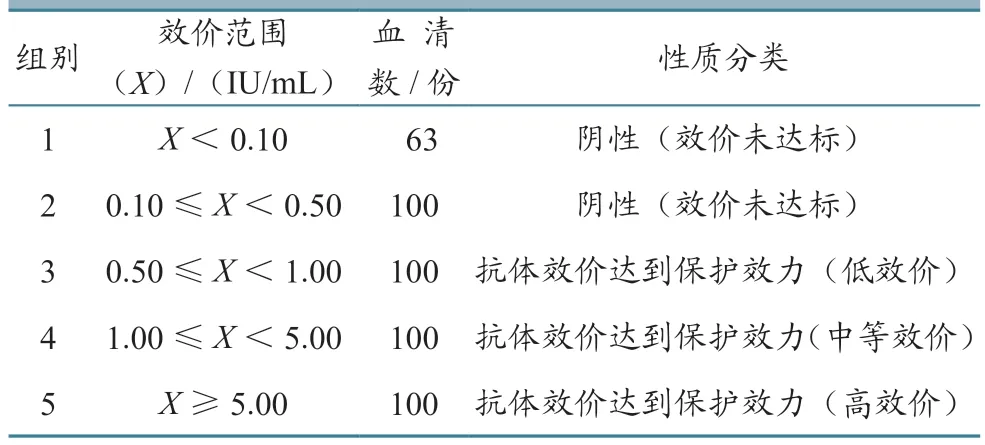
表1 不同中和抗体效价范围的血清分组
1.1.2 ELISA抗体检测试剂盒 从四川省多地动物疫病预防控制机构常用的RV ELISA抗体检测试剂盒中,选择4种国产品牌试剂盒进行评估,分别编号为A试剂盒(批号202110003A)、B试剂盒(批号RV20211008E)、C试剂盒(批号20210708)和D试剂盒(批号20210817)。
1.1.3 主要仪器设备 酶标仪:日本BIO-RAD公司产品,型号iMarkTM;电热恒温鼓风干燥箱:上海齐欣科学仪器有限公司产品,型号DGX-9243B;移液器:德国Brand公司产品,型号Transferpette-S。
1.2 方法
1.2.1 ELISA抗体检测 用4种ELISA抗体检测试剂盒检测463份样品(阴性163份、阳性300份),严格按照试剂盒说明书进行试验以及结果判定。
1.2.2 性能指标测定 利用四格表法(表2)统计比较不同品牌试剂盒和FAVN的检测结果,用SPSS等软件进行数据分析,通过Kappa检验和配对卡方检验(McNemar检验),评估ELISA与FAVN检测的一致性和差异性,并计算ELISA试剂盒的诊断敏感性、诊断特异性和符合率。Kappa检验评定标准:Kappa系数<0,一致性程度极差;0~0.20,微弱;0.21~0.40,弱;0.41~0.60,中度;0.61~0.80,显著(或高度一致);0.81~1.00,极佳。McNemar检验评定标准:P<0.05为差异显著,P>0.05差异不显著。诊断敏感性、诊断特异性和符合率分别按公式计算。
1.2.3 重复性测定 对用于重复性试验的10份血清,分别用4种ELISA抗体检测试剂盒检测。每种试剂盒批内重复性试验选择1个板检测,批间重复性试验选择3个板检测。每份血清每个板重复3孔。计算每种试剂盒的批内变异系数和批间变异系数,评估试剂盒的重复性。
1.2.4 试剂盒参数比较 对4种试剂盒的使用范围、样品稀释倍数、孵育与显色时间、判定标准等参数进行比较,考察试剂盒的可操作性。
2 结果与分析
2.1 一致性检验与差异性分析
使用4种ELISA试剂盒检测463份血清,与FAVN比较结果见表3。
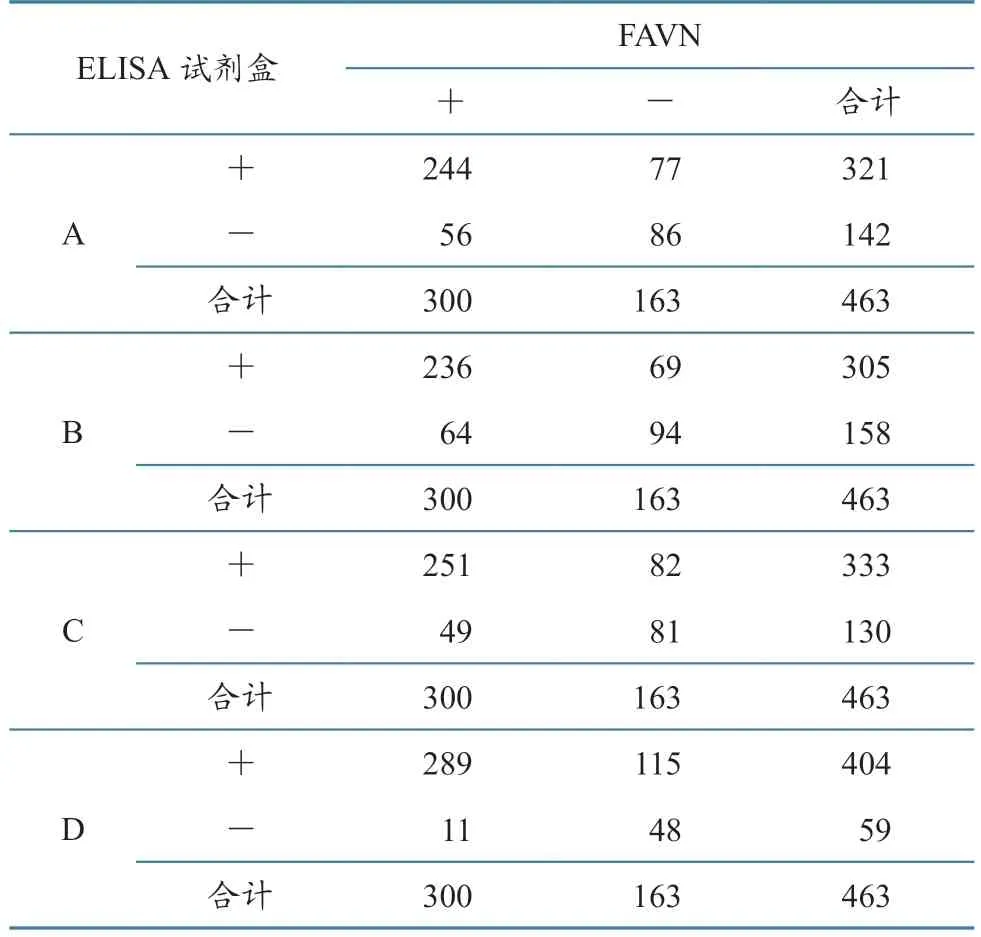
表3 4种ELISA试剂盒与FAVN检测结果四格表统计 单位:份
4种ELISA试剂盒的一致性检验与差异性分析结果(表4)显示:4种试剂盒Kappa系数处于0.21~0.40范围内。根据Kappa检验评定标准,判定4种试剂盒与FAVN一致性程度均为弱。McNemar检验A和B试剂盒的P值大于0.05,与FAVN结果的差异不显著;C和D试剂盒P值小于0.05,差异显著。可见A、B试剂盒与FAVN的差异性小于C、D试剂盒。

表4 4种ELISA试剂盒的一致性检验与差异性分析结果
2.2 检测性能指标
计算得到的4种试剂盒诊断敏感性、诊断特异性和符合率数据见表5。在诊断敏感性方面,D试剂盒更好,为96.3%,其他3种试剂盒差异较小,诊断敏感性排序为D>C>A>B。诊断特异性方面,各试剂盒诊断特异性普遍不高,为29.5%~57.7%,其中B试剂盒最高,各试剂盒诊断特异性排序为B>A>C>D。4种试剂盒符合率相当,为71.3%~72.8%,符合率排序为D>C>A/B。
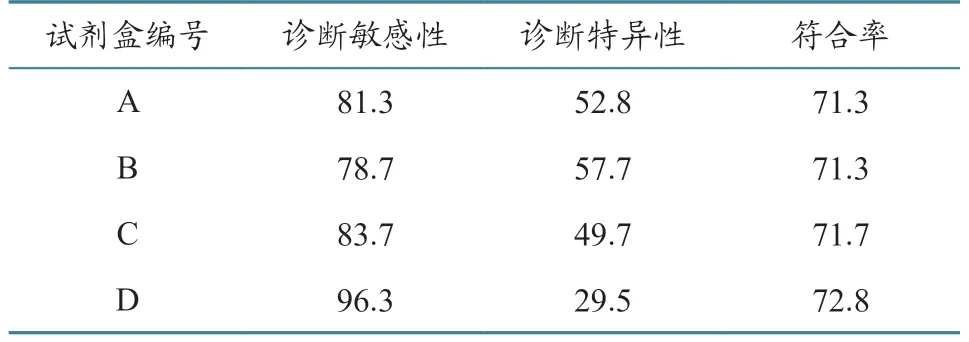
表5 4种ELISA试剂盒检测结果比较 单位:%
2.3 重复性试验
从表6可知:批内变异系数均值,A试剂盒最小,B试剂盒均值大于5%,10个样品批内变异系数均值排序为A<C<D<B;批间变异系数均值,C试剂盒最小,A、B、D试剂盒均大于10%,其中B试剂盒大于20%,说明这些试剂盒批间稳定性普遍较差,批间变异系数均值排序为C<A<D<B。因变异系数越小,重复性越好,可见A、C试剂盒的重复性好于D试剂盒,而B试剂盒效果最不理想。
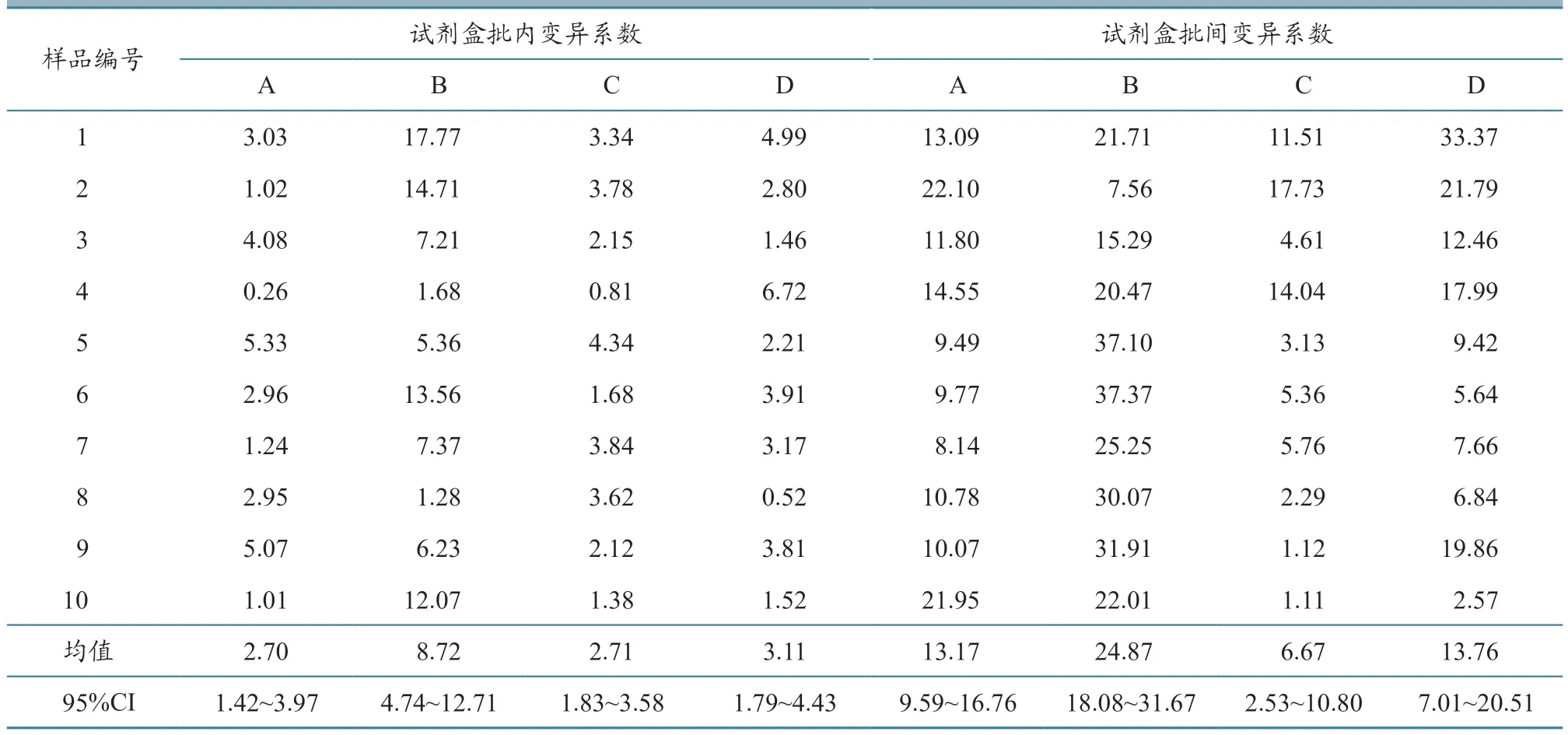
表6 试剂盒批内和批间变异系数 单位:%
2.4 不同中和抗体效价范围血清符合率
从每组中和抗体效价范围血清检测的符合率(表7)可知:第2组(0.10≤X<0.50)符合率最低,第3组(0.50≤X<1.00)稍高,这两组FAVN效价均处于0.50 IU/mL这一临界值附近;其他组中,除第1组(X<0.10)D试剂盒出现低符合率(29%)外,符合率普遍较高。

表7 4种试剂盒检测不同中和抗体效价范围血清的符合率 单位:%
2.5 试剂盒参数比较
将4种国产试剂盒的使用范围、样品稀释倍数、孵育与显色时间等参数进行比较。结果(表8)显示:4种试剂盒均为间接法,其中C试剂盒样品稀释度低,需要量多,可有助于提高灵敏度;D试剂盒虽然孵育时间较长,但其可定性或定量检测,判定标准分为阳性、弱阳、阴性3个等级,结果判定方式较精确。

表8 试剂盒参数比较结果
3 讨论
四川省是我国狂犬病高发省份之一,做好狂犬病的预防尤为重要。为犬注射疫苗是预防狂犬病的有效策略,因为疫苗产生的抗体能有力抵抗RV。免疫后抗体监测有助于评估疫苗免疫效力,也可用于分析抗体消长规律,为制定疫苗免疫程序提供辅助。商品化ELISA试剂盒操作简便、快速,适用于在基层开展抗体监测。目前国内有报道[7-9]将狂犬病ELISA试剂盒与FAVN检测方法进行比对,发现两者符合率较高,但是比对样品数量偏少。本试验扩大了样品数量,用463份已知RV抗体效价的犬血清科学评估了4种国产狂犬病ELISA试剂盒性能参数,为试验提供了有力的数据支持。
通过试验结果可知,试剂盒诊断敏感性为78.7%~96.3%,诊断特异性较低,为29.5%~57.7%。罗静霞等[10]将间接ELISA法与RFFIT比较检测人群RV免疫抗体,发现两者阳性符合率为85.30%,阴性符合率为52.94%,与本试验敏感性和特异性的结果接近。诊断敏感性越高的试剂盒,易出现假阳性,诊断特异性趋于更低,如试验中的D试剂盒诊断敏感性最高,诊断特异性最低,但总体符合率4种试剂盒差别不大,为71.3%~72.8%。国外有研究[5]发现ELISA试剂盒测试多血清样本与FAVN的符合率为86.2%,提示国产试剂盒检测技术仍有提升空间。本试验中的D试剂盒虽然敏感性更高,但检测低中和抗体效价血清(<0.10 IU/mL)符合率低,特异性差,容易将阴性样品判定为阳性,不利于免疫后抗体监测;B试剂盒敏感性和稳定性均不理想;C试剂盒敏感性次于D试剂盒,但特异性较好,且重复性表现更好,因此认为C试剂盒更能满足免疫后抗体检测需求;A试剂盒敏感性较好,特异性、重复性和差异性也表现不错,因此也可作为临床选用的候选试剂盒。
相比金标准检测方法FAVN,国产狂犬病 ELISA抗体检测试剂盒符合率不够高,特异性低,假阳性高。一些制约因素可能影响了狂犬病ELISA试剂盒检测的准确性,如包被抗原质量、非中和抗体结合物干扰等。FAVN方法采用固定病毒稀释待检血清的办法,将固定浓度的病毒和不同稀释度的待检血清中和,经细胞培养、荧光染色等步骤后判定结果,检测的是血清中和抗体,而间接ELISA检测的是与包被抗原结合的“结合抗体”,有些“结合抗体”不一定是中和抗体[11],这可能会增加ELISA结果的假阳性率。其次是方法的转换问题,有研究[12-13]建议将FAVN标准从0.50 IU/mL这一临界值调低至0.24 IU/mL,即试剂盒在表6中第2组测出的部分阳性可认为是FAVN阳性,因此金标准临界值一定范围的摆动,可造成在临界值附近ELISA与FAVN符合率不高的问题。此外,由于RV基因组序列比较保守,各国流行毒株的G蛋白差异不大,国内外间接ELISA试剂盒多采用RV G蛋白包被酶标板,但国内部分产品使用片段未知的重组RV重组抗原,造成包被抗原质量各异,可能影响检测效果。
狂犬病是目前病死率最高的人兽共患病,按照全国畜间人兽共患病防治规划,严格实施犬只免疫和开展监测流调是狂犬病的重点预防措施。因此,ELISA作为检测基层大样本量的快速简便方法,对狂犬病的清除具有重要意义。本次试验发现,国产狂犬病ELISA试剂盒诊断敏感性、诊断特异性、批间稳定性等性能均需进一步提高,但也有综合性能较好的试剂盒,建议在基层犬只狂犬病免疫后抗体水平检测中,可通过与FAVN方法比对,选用与其符合率较高的试剂盒,从而可以准确掌握辖区内的犬狂犬病免疫状况,保障实现区域间犬只免疫抗体合格率达到75%以上的目标。
4 结论
本研究以RV血清中和抗体检测金标准FAVN方法测得的抗体效价为标准,评估了4种国产狂犬病ELISA试剂盒的诊断敏感性、诊断特异性等性能参数,发现不同的国产试剂盒诊断性能存在一定差异,整体来看诊断特异性普遍较低,各项检测性能还需进一步提升,实际应用时应与FAVN方法进行比对,筛选性能最佳的试剂盒用于犬只狂犬病免疫后抗体水平监测与评估。
