枳术便秘通丸成型工艺及质量控制研究
2023-03-02何英蒙米晓琴蒲清荣赵春妮赵福兰
何英蒙,赖 慧,米晓琴,蒲清荣,赵春妮,梁 刚,赵福兰△
(西南医科大学附属中医医院 1.药剂科,2.制剂室,3.肿瘤科,四川 泸州 646000)
便秘是导致肛肠疾病、胃肠神经功能紊乱、心脑血管疾病、直肠癌等发生的重要原因[1],更是恶性肿瘤患者在化学药物治疗(简称化疗)过程中常出现的副反应之一[2]。晚期癌症患者的便秘率为40%~60%[3-4]。常见的便秘治疗药物虽能有效缓解短期症状,但长期使用可能会导致其他不良反应,如腹泻和代谢紊乱[5-6]。枳术便秘通丸是以古方枳术丸结合临床加减而成,主要由大黄、麸炒枳实、麸炒白术等6味中药材组方,具有健脾化湿、行气通便功效。该方自2016年用于临床,不仅能有效缓解化疗过程中出现的便秘症状,同时还可减轻腹胀腹痛、恶心呕吐等伴随症状,改善癌症患者的生活质量[7]。本研究中初步探讨了其成型工艺和质控标准,为后续规模化生产和质量控制提供依据。现报道如下。
1 仪器与试药
仪器:ZEJ-Z型全自动中型制丸机(甘肃恒悦制药设备有限公司);LC-20AT型高效液相色谱仪(日本Shimadzu公司);101-2AB型电热鼓风干燥箱(杭州江锐仪器设备有限公司);JA-Series电子天平(常州市幸运电子设备有限公司);JPCQ1020型超声波提取器(武汉嘉鹏电子有限公司);DOODLOOK-1000型薄层色谱成像系统(上海科哲生化科技有限公司)。
试药:大黄、麸炒枳实、麸炒白术、木香、茯苓、砂仁饮片(成都吉安康药业有限公司,批号分别为200101,200501,200401,200401,200401,00501)。大黄素对照品(批号为110756-201913,含量为89.7%)、大黄酚对照品(批号为110796-201922,含量为99.4%)、辛弗林对照品(批号为110727-202110,含量为99.5%),均购自中国食品药品检定研究院;淀粉(批号为200907)、羧甲基纤维素钠(CMC-Na,批号为201108)、羟丙纤维素(HPC,批号为201011),均购自淄博丰汇生物科技有限公司;糊精(汉中秦发糊精责任有限公司,批号为200606);硅胶G薄层板(青岛海洋化工厂);甲醇为色谱纯;其余试剂均为分析纯;水为纯化水。
2 方法与结果
2.1 成型工艺
2.1.1 制法
按处方量称取大黄60 g,麸炒枳实、麸炒白术、木香、茯苓各150 g,砂仁80 g,粉碎,过筛,混合均匀,得混合药粉;黏合剂用热水溶解后与混合药粉搅拌均匀;采用塑制法制丸、干燥,即得。流程见图1。
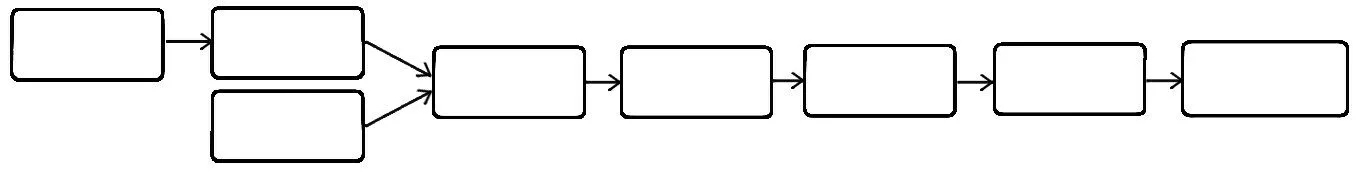
图1 成型工艺流程图Fig.1 Flow chart of forming process
2.1.2 黏合剂选择
按处方量称取混合药粉5份,每份740 g;分别取水740 g及淀粉、糊精、CMC-Na、HPC各178 g,用593 mL热水溶解后作为黏合剂,充分拌匀后转入制丸机,观察中药条的性状及成丸情况,烘干,参照2020年版《中国药典(四部)》溶散时限测定法测定溶散时限。
以纯化水、CMC-Na和HPC为黏合剂时,药条成丸性较差;以淀粉或糊精为黏合剂时,药条韧性良好,均可成丸。但以淀粉为黏合剂,所制得的丸剂呈棕黄色,表面粗糙且溶散时限较长;以糊精为黏合剂所制得的丸剂呈棕黄褐色,表面较光滑,溶散时限较短,故选择糊精。各黏合剂成丸情况及溶散时限详见表1。

表1 不同黏合剂下的成丸情况和丸剂溶散时限Tab.1 Pellet formation and dissolution time limit under different adhesives
2.1.3 成型工艺优化
以糊精浆体积分数[因素A,糊精浆体积分数(%)=糊精量/纯水量×100%]、药粉与水质量比(因素B)、干燥时间(因素C)为考察因素,以丸剂溶散时限和含水量(参照2020年版《中国药典(四部)》水分测定法测定)的综合评分(以综合加权评分法[8-10]计算)为评价指标,采用L9(34)正交试验优化。综合评分=溶散时限最小值/溶散时限×0.5+含水量最小值/含水量×0.5,综合评分越高表明丸剂质量越好。因素与水平见表2。
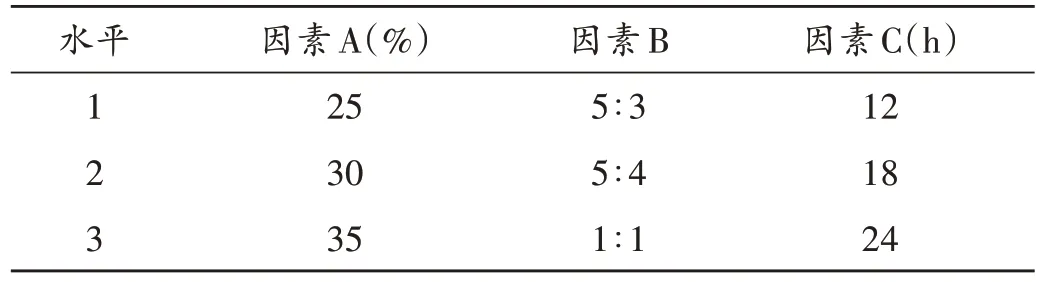
表2 因素与水平Tab.2 Factors and their levels
正交试验设计与结果见表3。枳术便秘通丸成型工艺的3个主要因素影响大小顺序依次为A>B>C。由方差分析结果(表4)可知,3个因素均对成型工艺有显著影响,最佳成型工艺为A2B1C3,即以30%糊精浆为黏合剂,药粉∶纯水为5∶3(m/m),干燥24 h所得产品最佳。

表3 L9(34)正交试验设计与结果Tab.3 Design and results of the L9(34)orthogonal test

表4 方差分析结果Tab.4 Results of the ANOVA
2.1.4 验证试验
根据上述试验结果,进行枳术便秘通丸成型工艺的验证试验。取灭菌后的药粉混合,粉碎成细粉;糊精用0.6倍药粉量的热水溶解制成30%糊精浆,与药粉混匀,使药粉充分润湿转入制丸机,制丸,将湿丸粒转入抛光机,50℃烘干24 h,选丸,即得。
2.2 质量标准
2.2.1 定性鉴别
麸炒枳实:取样品5 g,研细,加甲醇20 mL,超声(功率100 W,频率20 kHz;下同)处理20 min,滤过,取续滤液,蒸干,残渣加甲醇0.5 mL使溶解,即得供试品溶液。取辛弗林对照品适量,精密称定,加甲醇制成每1 mL含0.5 mg的对照品溶液。按枳术便秘通丸处方和工艺制备缺麸炒枳实的阴性样品5 g,同供试品溶液制备方法制成阴性对照品溶液。按2020年版《中国药典(四部)》薄层色谱(TLC)法试验,吸取上述溶液各2μL,分别点于同一硅胶G薄层板上,以正丁醇-冰醋酸-水(4∶1∶5,V/V/V)的上层溶液为展开剂,展开,取出,晾干,喷以0.5%茚三酮乙醇溶液,105℃加热至斑点显色清晰。供试品溶液色谱中,在与对照品溶液色谱相应位置上显相同颜色斑点,阴性对照无干扰。详见图2。
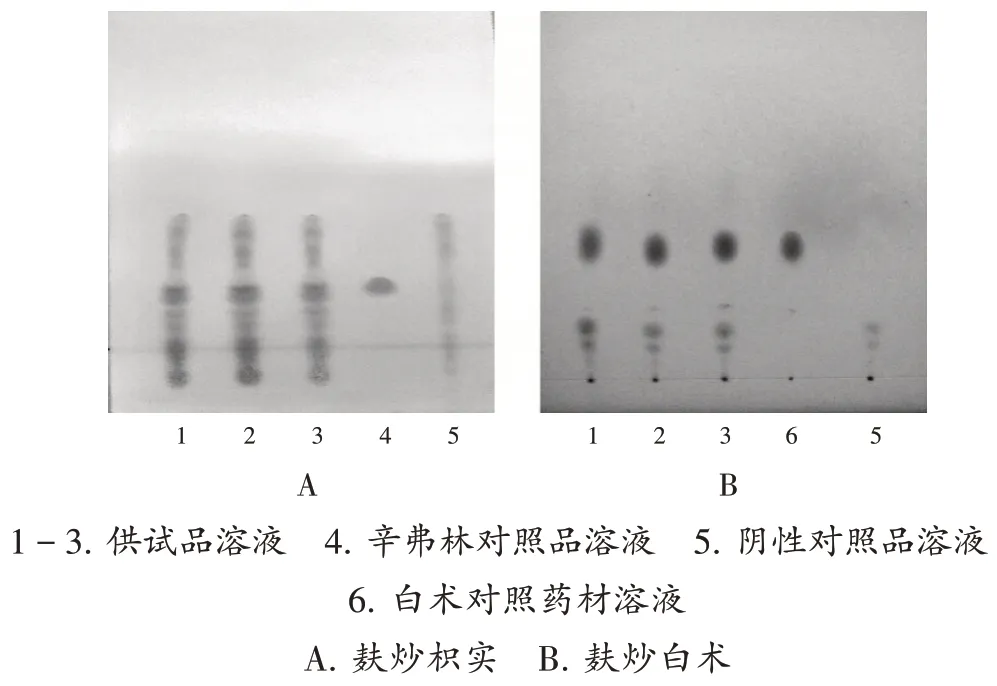
图2 薄层色谱图1-3.Test solution 4 Synephrine reference solution 5 Negative reference solution 6.Reference medicinal materials solution of Atractylodis Macrocephalae Rhizoma A.Bran-fried Aurantii Fructus B.Bran-fried Atractylodis Macrocephalae RhizomaFig.2 TLC chromatograms
麸炒白术:取样品5 g,研细,加正己烷10 mL,超声处理15 min,滤过,取滤液,即得供试品溶液。取白术对照药材0.5 g,精密称定,加正己烷2 mL,同供试品溶液制备方法制成对照药材溶液。按枳术便秘通丸处方和工艺制备缺麸炒白术的阴性样品5 g,同供试品溶液制备方法制成阴性对照品溶液。按2020年版《中国药典(四部)》TLC法试验,吸取上述溶液各10μL,分别点于同一硅胶G薄层板上,以石油醚(60~90℃)-乙酸乙酯(50∶1,V/V)为展开剂,展开,取出,晾干,喷以5%香草醛硫酸溶液,105℃加热至斑点清晰。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色斑点,阴性对照无干扰。详见图2。
2.2.2 含量测定[11-14]
色谱条件:色谱柱为Kromasil C18柱(250mm×4.6mm,5μm);流动相为甲醇-0.1%磷酸溶液(85∶15,V/V);流速为1.0 mL/min;检测波长为254 nm;柱温为40℃;进样量为10μL。
溶液制备:分别取大黄素、大黄酚对照品4.25,4.32 mg,精密称定,置50 mL容量瓶中,加甲醇溶解并定容,摇匀,得混合对照品溶液。取样品粉末0.5 g,精密称定,置具塞圆底烧瓶中,精密加入甲醇25 mL,称定质量,加热回流1 h,放冷,再次称定质量,用甲醇补足减失的质量,摇匀,滤过,取续滤液;精密量取10 mL,置圆底烧瓶中,挥去溶剂,加8%盐酸溶液10 mL,超声处理2 min;再加三氯甲烷10 mL,加热回流1 h,放冷,置分液漏斗中,用少量三氯甲烷洗涤容器并倒入分液漏斗中,分取三氯甲烷层,酸液再用三氯甲烷提取3次,每次10 mL,合并三氯甲烷液;加压回收溶剂至干,残渣加甲醇溶解,转移至10 mL容量瓶中,加甲醇定容,摇匀,经0.22μm微孔滤膜滤过,取续滤液,即得供试品溶液。按枳术便秘通丸处方和工艺制备缺大黄的阴性样品,按供试品溶液制备方法制成阴性对照品溶液。
适用性试验与专属性试验:取上述混合对照品溶液、供试品溶液、阴性对照品溶液各适量,按拟订色谱条件进样测定,记录色谱图。结果,理论板数按大黄素和大黄酚峰计应不低于3 000;分离度均大于1.5,基线分离良好;阴性对照品溶液在与混合对照品溶液色谱相同保留时间处无干扰峰,表明专属性良好。详见图3。

图3 高效液相色谱图1.Emodin 2.Chrysophanol A.Mixed reference solution B.Test solution C.Negative reference solutionFig.3 HPLC chromatograms
线性关系考察:分别精密量取混合对照品溶液,制成系列混合对照品溶液。精密量取10μL,按拟订色谱条件进样测定,记录峰面积。以待测成分质量浓度(X,μg/mL)为横坐标、峰面积(Y)为纵坐标进行线性回归,得大黄素和大黄酚回归方程分别为Y1=35 017X1-9 008.6(r=0.999 9)、Y2=54 345X2-3 280.9(r=0.999 9)。结果表明,大黄素和大黄酚质量浓度分别在0.848~34.01μg/mL和0.864~34.56μg/mL范围内与峰面积线性关系良好。
精密度试验:取混合对照品溶液适量,按拟订色谱条件连续进样测定6次,记录峰面积。结果,大黄素和大黄酚峰面积的RSD分别为0.12%和0.07%(n=6),表明仪器精密度良好。
稳定性试验:取供试品溶液适量,分别于室温下放置0,2,4,6,8,12,24 h时按拟订色谱条件进样测定,记录峰面积。结果,大黄素和大黄酚峰面积的RSD分别为0.34%和0.42%(n=7),表明供试品溶液在室温放置24 h内基本稳定。
重复性试验:精密称取样品适量,各6份,按拟订方法制备供试品溶液,再按拟订色谱条件进样测定,记录峰面积并计算含量。结果,大黄素和大黄酚含量的RSD分别为1.70%和1.03%(n=6),表明方法重复性良好。
加样回收试验:取已知含量样品适量,共9份,分别加入低、中、高质量浓度的混合对照品溶液,按拟订方法制备供试品溶液,再按拟订色谱条件进样测定,记录峰面积并计算加样回收率,结果见表5。

表5 加样回收试验结果(n=9)Tab.5 Results of the recovery test(n=9)
样品含量测定:取样品各适量,分别按拟订方法制备供试品溶液,再按拟订色谱条件进样测定,平行3次,记录峰面积并计算样品含量,结果见表6。

表6 样品含量测定结果(mg/g,n=3)Tab.6 Results of the content determination of emodin and chrysophanol in the samples(mg/g,n=3)
按2020年版《中国药典(四部)》中药品质量标准与指导原则9101“分析方法验证指导原则”相关要求,以大黄素和大黄酚总量下浮20%计算,将本品的大黄素和大黄酚总含量定为不得少于0.466 mg/g。
3 讨论
枳术便秘通丸处方作为经验方已在临床使用多年,治疗脾虚气滞所致的便秘效果显著。与市场中其他同类制剂相比,枳术便秘通丸对化疗或阿片类药物等引起的脾虚气滞型便秘疗效尤其显著,能同时起到健脾、化湿和行气的作用。本课题组在原有组方的基础上进行制剂工艺研究,优化丸剂成型工艺,便于患者服用、携带和保存。
制剂工艺过程中,考虑到砂仁含有挥发性成分,在灭菌时选择乙醇密闭灭菌法;其他药味采用电热灭菌法,且灭菌后均符合微生物限度要求。本试验中通过正交试验优化确定的枳术便秘通丸自动化生产最佳成型工艺,相比于传统手工泛丸,具有操作简便、生产高效、质量与药物疗效稳定等优点。
在生产工艺的基础上建立了麸炒枳实、麸炒白术专属性强且简便的TLC法,对比了3种不同展开系统,结果均显示斑点清晰,分离效果良好,且阴性对照无干扰,可作为质量标准项下的鉴别方法。对枳术便秘通丸中大黄的有效成分进行定量控制,药典中对大黄饮片的含量测定包括了大黄素、芦荟大黄素、大黄酚、大黄酸和大黄素甲醚5种成分,但在实际检测时发现,芦荟大黄素和大黄酸的出峰时间接近,且由于制剂中含有其他药材及辅料,可能对芦荟大黄素和大黄酸的测定造成干扰,影响准确度。因此,参考文献[14]等中的含量测定方法,最终以大黄素和大黄酚为指标,对枳术便秘通丸中大黄质量进行控制。
综上所述,枳术便秘通丸成型工艺合理,所建标准可用于制剂的质量控制。
