酸响应性槲皮素聚合物前药的制备与表征*
2023-02-17周蓉蓉王致雅
张 韫,周蓉蓉,王致雅,李 婷
(西安医学院 药学院,陕西 西安 710021)
1975年Helmut Ringsdorf教授提出了聚合物前药(Polymeric Prodrugs)[1],即通过可刺激响应性化学键将药物分子进行分散、键合或吸附制成纳米材料。通过引入可逆性化学键,在pH值、温度、还原性物质等因素的刺激下,聚合物前药可对肿瘤组织或细胞内微环境或外界刺激产生响应[2]。相较于传统的小分子药物,其具有如下优势[1]:降低药物毒副作用,改善药物溶解性,增加生物利用度,延长体内循环时间,通过肿瘤的高通透性和滞留(Enhanced Permeability and Retention,EPR)效应实现被动靶向等。目前,聚合物前药的功能化设计与合成已成为药剂学、高分子化学等领域研究的热点课题。
槲皮素(Quercetin)是一种天然黄酮类化合物,具有抗炎、抗菌、抗氧化等多种药理活性[3],对多种恶性肿瘤具有明显抑制作用[4]。但由于槲皮素含有酚羟基而具有弱酸性[5],难溶于水,光热稳定性和生物利用度欠佳。槲皮素半衰期短,肠道首过效应(First Pass Effect)显著,以原药入血液循环的比例小于5%[6],临床应用受到极大限制。研究表明,槲皮素纳米制剂对改善槲皮素水溶性、提高生物利用度等起到积极的作用。孙丽等[7]利用阴离子乳液制备以聚氰基丙烯酸正丁酯为载体的槲皮素纳米粒子,杨小云等[8]以三嵌段两亲共聚物为载体制备的槲皮素纳米胶束,均可延长药物体内作用时效,增加溶解度,提升药物疗效。
点击反应作为药物递送和生物医用材料合成中最有效的合成方法之一,具有简单、高效、快速、产物易分离等优势。Ni Peihong等[9]制备了一种酸响应聚合物前药,该物质是一种炔基封端小分子,通过点击反应将其键合到聚乙二醇侧链,并与阿霉素反应形成含pH敏感基团的聚合物前药。在酸性条件下发生pH响应性化学键断裂,实现药物在肿瘤细胞的高效递送。
本实验设计合成具有双官能团的丁烷-1,4二丙炔酸二酯,并将其与槲皮素直接发生聚合反应,制备具有主链结构的聚合物前药纳米递送系统。通过引入pH刺激响应性化学键实现对药物的控制释放,并采用紫外光谱和荧光光谱、粒径分布和透射电镜对纳米材料进行结构及形貌表征,获得聚合物前药的可控性制备工艺。本实验的研究对提升常规药物疗效,促进纳米递药系统的深入研究和应用提供了新思路。
1 实验部分
1.1 仪器与试剂
UV-2600型紫外-可见分光光度计(日本岛津仪器有限公司);F-4500型荧光分光光度计(日本日立株式会社);JEM-F200型透射电子显微镜(日本电子株式会社);ZS90型纳米粒度电位仪(英国马尔文仪器有限公司);400 Plus型核磁共振波谱仪(德国布鲁克公司),VION IMSQTOF型高分辨质谱仪(美国沃特世科技有限公司);BSA224-CW型电子天平(德国赛多利斯有限公司);SB-5200DT/200W型超声波清洗器(宁波新芝生物科技股份有限公司)。
槲皮素(95%)、1,4-丁二醇(98%)、丙炔酸(95%)、氘代氯仿(99.8%)、对甲苯磺酸(98%),上海阿拉丁试剂有限公司;乙腈、乙醇、NaHCO3、三氯甲烷、乙酸乙酯,均为分析纯,天津科密欧化学试剂有限公司;无水MgSO4、NaCl、NH4HCO3等,均为分析纯,上海萨恩化学技术有限公司;实验用水为超纯水(18.2MΩ·cm)。
1.2 聚合物前药的制备
1.2.1 丁烷-1,4-二丙炔酸二酯的合成与表征 精密称取1,4-丁二醇4.3g和丙炔酸13.5g,对甲苯磺酸(TsOH)18.2g溶于100mL三氯甲烷(CHCl3)中,于圆底烧瓶中加热回流约18h。冷却后用饱和NaHCO3溶液、水、饱和NaCl溶液分别洗涤3次,并用无水MgSO4干燥。旋转蒸发除去溶剂,粗产物用正己烷/乙酸乙酯重结晶,得到淡黄色的晶状固体产物[10]。合成的反应式见图1。取适量产物于核磁管中,用氘代氯仿(CDCl3)溶解,采用核磁共振波谱仪测定该物质中氢原子的化学位移。采用高分辨质谱仪(ESIMS)精确测定其分子量。
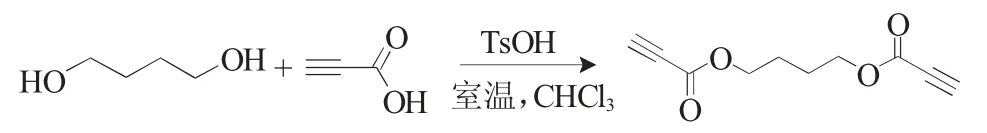
图1 丁烷-1,4-二丙炔酸二酯的合成反应式Fig.1 Resynthesis of butane-1,4-diyl dipropiolate diester
1.2.2 丁烷-1,4-二丙炔酸二酯-槲皮素聚合物前药的制备 精密称取2.8mg丁烷-1,4-二丙炔酸二酯溶于0.2mL无水乙醇,2.9mg槲皮素溶于0.4mL无水乙醇,15.0mg NaHCO3溶于4.0mL超纯水。取20mL 30%乙醇溶液(v/v)于100mL锥形瓶中,缓慢滴加丁烷-1,4-二丙炔酸二酯溶液,超声约3min后滴加槲皮素溶液,反应约30min(超声功率为200W,水浴温度为40~45℃),静置约72h至反应体系浑浊后离心,弃上清液,所得产物用无水乙醇和超纯水分别洗涤,最后将所制材料均匀分散在超纯水中,即得产物聚合物前药(BQ)的纳米混悬剂,避光保存。
1.3 聚合物前药的结构表征
1.3.1 紫外光谱表征 使用紫外-可见分光光度计对样品的紫外吸收进行定性测试分析。聚合物前药(BQ)的纳米混悬剂超声分散均匀,于200~700nm进行紫外光谱扫描。
1.3.2 荧光光谱 采用荧光分光光度计,激发和发射狭缝宽分别为10nm和20nm,扫速速率1200nm·min-1,扫描聚合物前药(BQ)的纳米混悬剂在450~700nm的荧光光谱,记录荧光强度(F)的变化。
1.4 聚合物前药的形貌表征
1.4.1 粒径分布 取BQ的纳米混悬剂少许加超纯水稀释至适宜浓度,超声使其分散均匀,采用激光粒度仪,在25°C条件下以水为分散介质测定粒径分布和多分散系数(PDI)。
1.4.2 透射电镜 取BQ的纳米混悬剂少许,超声将样品分散均匀后滴于200目普通碳支持膜,待自然干燥后在透射电镜下观察形貌。
2 结果与讨论
2.1 丁烷-1,4-二丙炔酸二酯的表征
核磁共振氢谱表征1H NMR(CDCl3;δ(ppm)):1.81(m,4H),2.92(s,2H),4.25(m,4H)。4.25ppm为靠近氧的4个氢的信号峰,2.92ppm为两个炔基氢的信号峰,1.81ppm为中间4个氢的信号峰。
高分辨质谱表征 丁烷-1,4-二丙炔酸二酯的相对分子质量理论值为194.18600,高分辨质谱(ESI-MS)的(M+H)模式检测m/z为195.06456,证明该化合物为丁烷-1,4-二丙炔酸二酯。
2.2 聚合物前药的结构表征
2.2.1 紫外光谱表征 聚合物前药(BQ)和槲皮素(QUE)的紫外-可见吸收光谱,见图2。
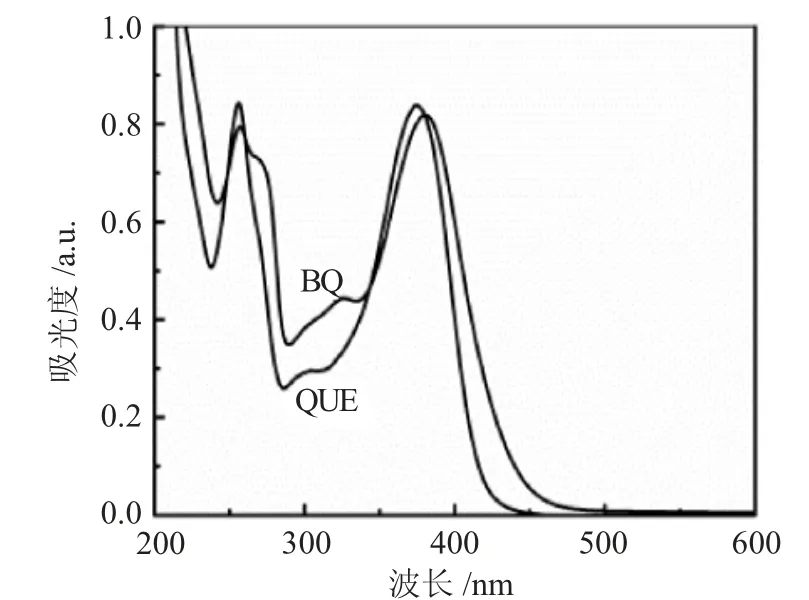
图2 聚合物前药的紫外吸收光谱图Fig.2 Ultraviolet spectra of the polymeric prodrug
由图2可见,槲皮素的最大吸收峰出现在260nm和381nm左右,由于丁烷-1,4-二丙炔酸二酯自身没有紫外吸收,与槲皮素键合生成BQ后槲皮素的特征吸收峰蓝移约10nm。故推断丁烷-1,4-二丙炔酸二酯与槲皮素发生了聚合反应。
2.2.2 荧光光谱表征(图3)
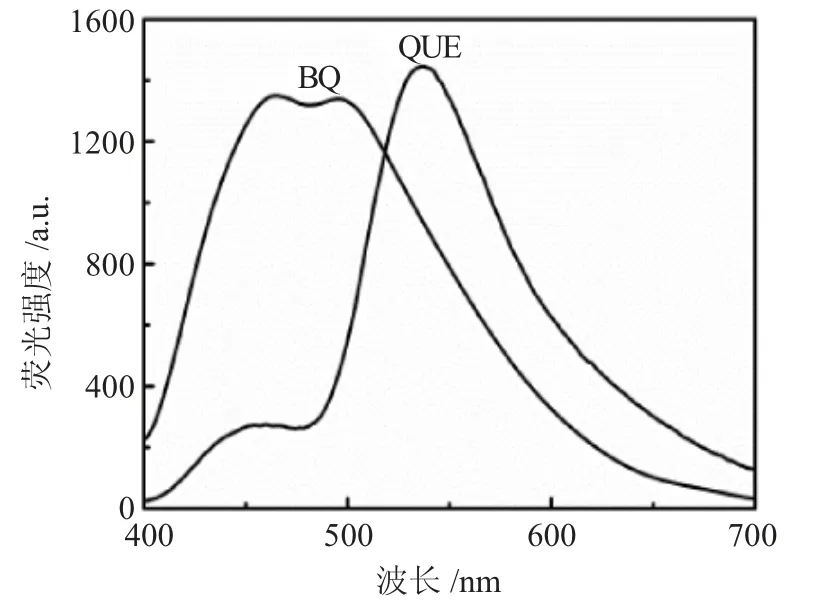
图3 聚合物前药的荧光光谱图Fig.3 Fluorescence spectra of the polymeric prodrug
由图3可见,槲皮素(QUE)的荧光最大发射波长为536nm,聚合物前药(BQ)荧光最大发射波长为496nm,较槲皮素蓝移约40nm且峰顶平缓,峰形也有所变化。这可能是因为槲皮素与丙炔酸酯结合后结构发生了改变,酚羟基变少导致特征峰移动。故推断丁烷-1,4-二丙炔酸二酯已与槲皮素发生了聚合反应。
2.3 聚合物前药的形貌表征
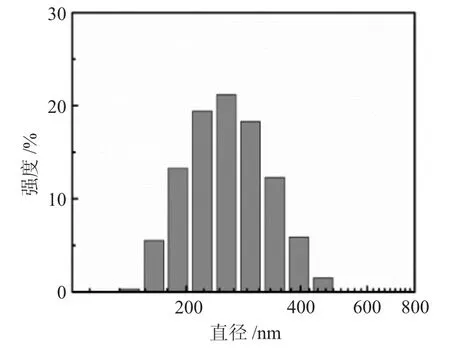
图4 聚合物前药的粒径分布图Fig.4 Particle size distribution of the polymeric prodrug
2.3.1 粒径分布(图4)由图4可知,在动态光散射下由激光粒度仪测得聚合物前药BQ的平均水合直径为274.7nm;多分散指数PDI为0.242,当PDI<0.3时,说明纳米粒子分散度较好。
2.3.2 透射电镜表征(图5)

图5 聚合物前药纳米粒子的透射电镜图Fig.5 TEM image of the polymeric prodrug
由图5可见,BQ是粒径为100~200nm的球形纳米粒子,轮廓清晰,分散均匀,这与纳米粒子较低的多分散系数具有相关性,聚合物前药粒径大小符合EPR效应要求,具备进入实体肿瘤细胞的条件。
3 结论
本实验基于点击反应,将合成的双官能团丁烷-1,4-二丙炔酸二酯与槲皮素分子共聚,生成具有主链结构的新型纳米递送药系统;引入肿瘤微环境pH响应性化学键,可实现药物的智能化控制释放。采用紫外和荧光光谱进行结构表征,激光粒度仪和透射电镜进行形貌表征,得到聚合物前药的可控性制备工艺。结果表明,基于点击反应获得的聚合物前药纳米粒子符合EPR效应,可增加纳米粒子在肿瘤部位的被动靶向聚集,以期获得良好的抗肿瘤效果。本实验为进一步深入研究化学键、官能团对前药理化性质影响及聚合物前药中刺激响应性化学键的设计提供了实验基础。
