甘肃河西地区肉羊肌肉和肝肾组织中抗菌药物残留的检测
2023-02-16魏衍全苟惠天李天昊委慧玲齐玉梅田常青史文静祁国军薛惠文
宋 晨,格 代,魏衍全,苟惠天,李天昊,委慧玲,齐玉梅,田常青,史文静,祁国军,薛惠文*,张 勇*
(1.甘肃农业大学动物医学院,甘肃兰州 730070;2.甘南藏族自治州农业农村局/甘南州农产品质量安全检测检验中心,甘肃合作 747000)
兽药被广泛用于食品动物养殖中[1],因其不当使用或滥用造成动物性食品中兽药残留[2],尤其是抗微生物药物的残留较为突出。据我国农业农村部2020年度动物及动物产品兽药残留监控结果显示,猪肉、鸡蛋等34批不合格样品中94.12%检出抗微生物药物[3]。当人体摄入抗微生物药物残留超标的动物性食品,具有潜在风险,会导致过敏反应或其他毒副作用,并出现了细菌耐药性和菌群失调等问题,严重影响公众健康,而且对生态环境会产生不良影响,已引起全世界的广泛关注[4]。因此,开展动物性食品抗微生物药物检测具有重要意义,但目前尚未见到甘肃省河西地区羊肉产品中抗微生物药物残留情况的报道。
肉类食品中抗微生物药物残留的检测方法有快速检测试纸条、酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA)、高效液相色谱法(high performance liquid chromatography,HPLC)、气相色谱-质谱法(gas chromatography-mass spectrometry,GC-MS)、液相色谱串联质谱法(liquid chromatograph tandem mass spectrometer,LC-MS/MS)[4-9]等。快速检测试纸条兼具检测线低、耗时短、操作简便等优点,有利于跨地区或在不同环境中开展检测工作,但存在无法准确定量的问题,适合快速筛选。LC-MS/MS具有检测灵敏度高、分离能力强的特点,在实际工作中作为定量检测使用[10-14]。
本研究从甘肃河西地区采集肉羊主要可食组织样品,采用兽药残留快速检测试纸条对试样进行初步筛查,再用LC-MS/MS对筛查阳性样品中抗微生物药物残留进行定量测定,以明确当地羊肉食品中抗微生物药物残留的类别和种类,以期为制定抗微生物药物监控措施提供数据支撑,为建立羊肉中抗微生物药物残留的快速筛选和精准识别技术奠定基础。
1 材料与方法
1.1 材料
1.1.1 样品 2020年8月下旬从甘肃省酒泉、张掖、武威、金昌4个市各选取1家羊屠宰企业,根据屠宰场规模及当日屠宰量从屠宰线上随机采集羊的肌肉(39份)、肝脏(51份)、肾脏(39份)3种可食组织,每份不少于20 g,组织匀浆后装于清洁自封袋中,置-80 ℃保存。
1.1.2 试剂和药物标准品 甲酸、甲醇、乙腈为国产色谱纯,柠檬酸、磷酸二氢钠、乙二胺四乙酸二钠等试剂均为国产分析纯;恩诺沙星、环丙沙星、氧氟沙星、替米考星品、泰乐菌素、庆大霉素标准品(纯度≥98%),上海Macklin生化科技有限公司产品;兽药残留检测试纸条,北京勤邦生物技术有限公司产品。
1.1.3 仪器 液相色谱-质谱联用仪(Agilent 1290-6460 LC/MS)、色谱柱:Eclipse Plus C18(粒径1.8 μm规格2.1 mm×50 mm)、固相萃取小柱(SPE),美国Agilent公司产品;高通量组织研磨仪(SCIENTZ-48),宁波新芝生物科技股份有限公司产品;高速冷冻离心机(3-18 ks),德国Sigma公司产品;冷冻台式真空离心浓缩仪(CVS-3110),东京理化械株式会社产品。
1.2 方法
1.2.1 兽药残留检测试纸条初筛 将匀浆好的肌肉、肝、肾共129份样品,每份取2.5 g分别加入样本提取液,涡旋混匀后离心,取上清液,用兽药残留检测试纸条进行喹诺酮类(11种)、磺胺类(7种)、四环素类(4种)、大环内酯类(2种)、氨基糖苷类(2种)、β-内酰胺类(1种)、氟苯尼考(1种)等7大类28种抗微生物药物的快速检测(表1)和初步筛查,确定阳性样品及残留药物类别,再结合当地肉羊养殖防疫常用药物以确定抗微生物药物种类。操作方法参考兽药残留检测试纸条说明书。
1.2.2 LC-MS/MS测定
1.2.2.1 样品前处理 将兽药残留检测试纸条初筛检出抗微生物药物阳性的肌肉、肝、肾样品进行提取及净化,处理方法按照“食品安全国家标准”规定的恩诺沙星、氧氟沙星、环丙沙星、泰乐菌素、替米考星、庆大霉素检测方法进行[16-18]。
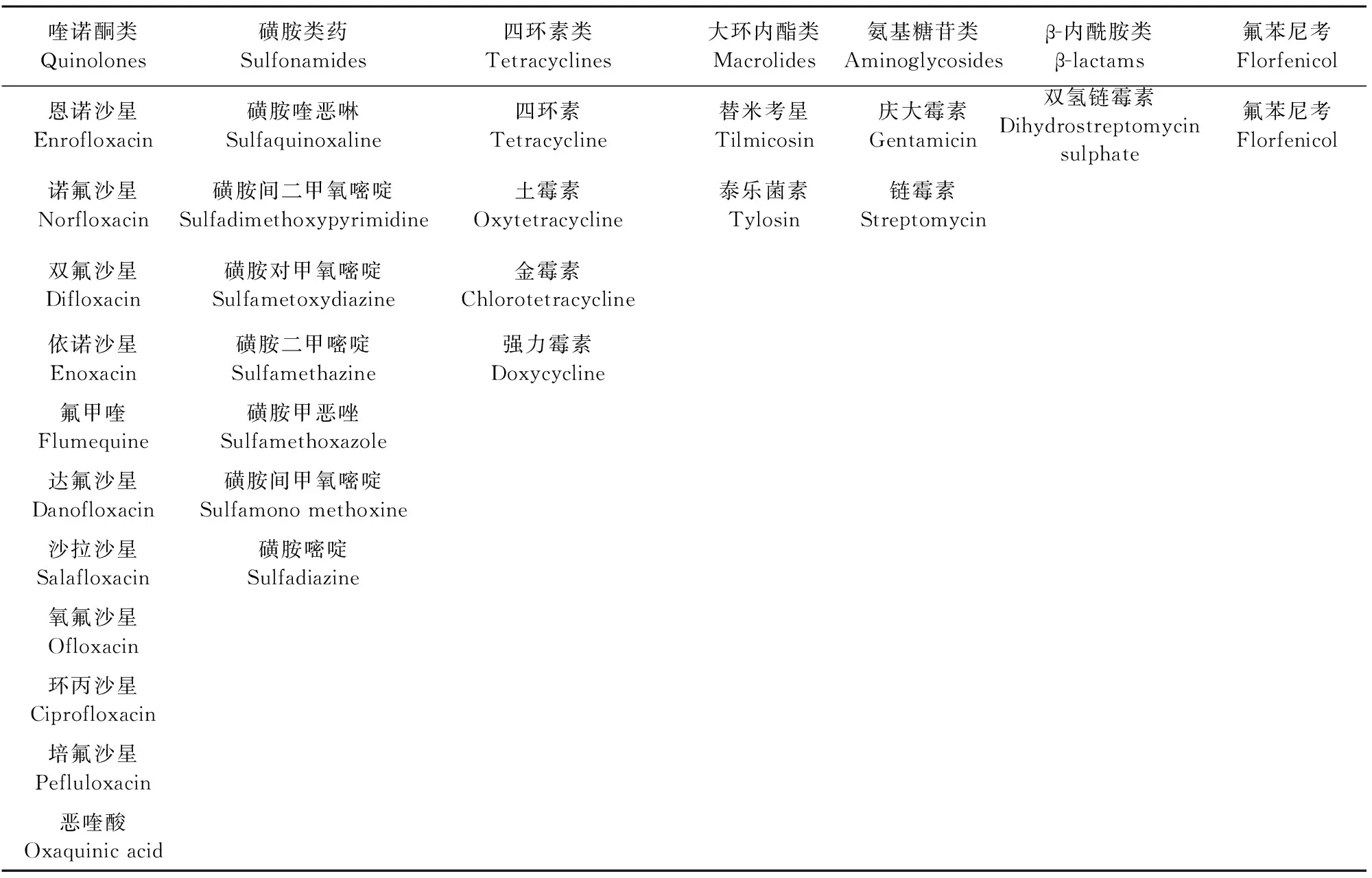
表1 初筛药物类别与药物名称
1.2.2.2 测定条件
(1)液相色谱条件
(a)色谱柱:Agilent Eclipse Plus C18,1.8 μm,2.1 mm×50 mm或相当者;(b)进样量:1 μL;(c)流速:0.3 mL/min;(d)柱温:35 ℃;(e)流动相:A:0.1 mmol/L甲酸水溶液;B:甲醇。梯度洗脱条件见表2。
(2)质谱条件
(a)离子源:电喷雾离子源;(b)扫描方式:正离子扫描(ESI+);(c)检测方式:多反应监测(MRM);(d)离子源温度:350 ℃;(e)母离子、子离子、碎裂电压和碰撞气能量:见表3。
1.2.3 样品测定 通过“1.2.2.1”前处理提取及净化的样品经0.22 μm滤膜过滤后,按照食品安全国家标准规定的液相色谱-质谱/质谱法(LC-MS/MS)对试样中残留的抗微生物药物进行测定。

表2 梯度洗脱条件

表3 母离子、子离子、碎裂电压和碰撞气能量
1.2.4 统计学分析 使用Excel对数据进行整理并采用无重复双因素方差分析,对肌肉、肝、肾3种可食组织中检出的抗微生物药物的结果进行分析,比较不同种类药物检出率之间差异是否显著;对4个市之间检出的不同种类抗微生物药物进行方差分析,比较检出药物种类之间的差异性。
2 结果
2.1 兽药残留检测试纸条初筛结果
2.1.1 抗微生物药物类别筛查结果 采用兽药快速检测试纸条对129份样品进行7大类28种抗微生物药物残留初步筛查,结果表明,57份样品呈阳性,检出率44.19%(57/129),39份肌肉、51份肝、39份肾的抗微生物药物阳性样品数分别为6、47、4份,检出率分别为15.38%(6/39)、92.16%(47/51)、10.26%(4/39),肝脏检出率高于肌肉和肾脏(表4)。
确定了氨基糖苷类(庆大霉素)、喹诺酮类(恩诺沙星、环丙沙星、氧氟沙星)以及大环内酯类(泰乐菌素、替米考星)3类药物,其中氧氟沙星为不得用于食品动物的药物;未检出磺胺类、四环素类、β-内酰胺类、氟苯尼考4类药物。
2.1.2 初筛数据统计学分析 对3种可食组织中检出的抗微生物药物初筛数据进行无重复双因素方差分析,结果显示,肌肉、肝、肾中3种抗微生物药物检出率之间差异显著(P<0.05),但大环内酯类、氨基糖苷类、喹诺酮类3类不同类别抗微生物药物检出率之间差异不显著(P>0.05)。
2.2 LC-MS/MS测定结果
2.2.1 抗微生物药物种类检出结果 采用LC-MS/MS对初筛阳性的57份样品中6种抗微生物药物测定结果显示,6种药物均有检出,并检出了不得用于食品动物的氧氟沙星,与初筛的药物种类和类别一致。恩诺沙星、环丙沙星、氧氟沙星、庆大霉素、替米考星、泰乐菌素检出的样品份数分别为3、31、20、29、50、6份,其中替米考星检出率最高(38.76%),恩诺沙星最低(2.33%);6种抗微生物药物残留范围分别为:(0.275 8~0.362 0)、(0.716 9~12.194 2)、(0.250 5~0.517 4)、(131.235 8~135.496 0)、(0.720 1~39.194 9)、(0.258 2~2.069 4)μg/kg(表5)。
恩诺沙星、环丙沙星、替米考星及泰乐菌素残留量均未超过我国食品安全国家标准[19],样品合格率达100%;2份肌肉样品中庆大霉素残留量超标,合格率为98.45%;20份组织样品中检出了禁用药物氧氟沙星,样品合格率为86.05%,6种抗微生物药物检出数量及超标数量对比见图1。

表4 3种可食组织中抗微生物药物初筛统计结果

表5 LC-MS/MS测定样品中抗微生物药物残留结果
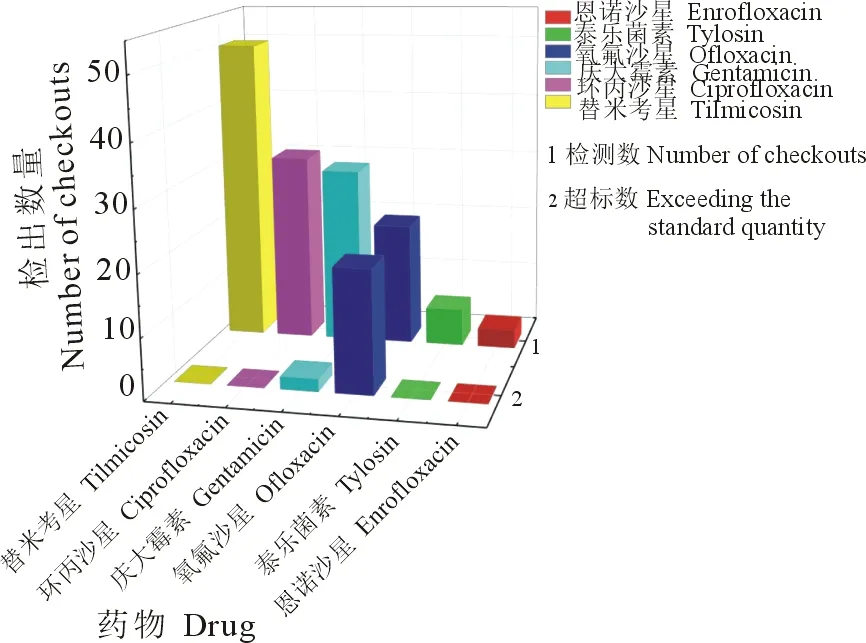
A.6种抗微生物药物检出数量;B.6种抗微生物药物超标数量
2.2.2 抗微生物药物的LC-MS/MS检出结果 采用LC-MS/MS对初筛抗微生物药物呈阳性的6份肌肉、47份肝、4份肾进行6种抗微生物药物检测,结果显示,肌肉中检出氧氟沙星(1/6)、庆大霉素(2/6)和替米考星(3/6)3种药物,替米考星检出率最高(50%),未检出其他3种药物;肝中检出了恩诺沙星(2/47)、环丙沙星(30/47)、氧氟沙星(17/47)、庆大霉素(26/47)、替米考星(46/47)、泰乐菌素(6/47)6种药物,以替米考星检出率最高(97.87%);肾中检出了恩诺沙星(1/4)、环丙沙星(1/4)、氧氟沙星(2/4)、庆大霉素(1/4)、替米考星(1/4)5种药物(表6)。
2.2.3 河西4市肉羊产品抗微生物药物检出结果对比 通过对酒泉、张掖、武威、金昌4市肉羊3种可食组织中的大环内酯类、氨基糖苷类和喹诺酮类检测结果进行对比可见(图2),酒泉、张掖、金昌3市肉羊产品以庆大霉素检出率最高(27.27%、33.33%、16.67%),武威市肉羊产品则以泰乐菌素和替米考星检出最为明显(33.33%)。

表6 3种可食组织中6种抗微生物药物检出情况

图2 河西4市肉羊样品抗微生物药物残留检出率
对河西4市羊肉样品中恩诺沙星、环丙沙星、氧氟沙星、庆大霉素、替米考星及泰乐菌素检出的残留数据进行方差分析,结果显示,从3种可食组织中检出的抗微生物药物残留量,4市之间差异不显著(P>0.05),且6种抗微生物药物之间差异不显著(P>0.05)。
2.3 两种检测方法结果对比分析
2.3.1 3种组织两种检测方法的吻合率 在肌肉、肝、肾3种组织中,兽药残留快速检测试纸条筛查结果与LC-MS/MS检测结果对比显示,肌肉和肝中检出的组织样品完全吻合,但在2份肾组织中通过LC-MS/MS未检出抗微生物药物残留(表7)。
2.3.2 4个市两种方法检出阳性样品吻合率 对4个市肉羊3种可食样品通过兽药残留试纸条检测与LC-MS/MS检测结果的吻合率对比可见,酒泉、张掖、武威、金昌样品经两种检测方法吻合率分别达100%、81.48%、93.75%、90.91%(表8),说明兽药残留快速检测试条初步筛查结果可靠。

表7 3种组织中两种检测方法结果对比

表8 4市两种检测方法结果对比
3 讨论
本研究应用兽药残留快速检测试纸条(胶体金标检测试纸条)对甘肃省河西4个市肉羊3种可食组织(肌肉、肝、肾)进行7大类28种抗微生物药物残留进行非靶向初筛,129份样品共检出57份阳性样品,包含3大类抗微生物药物的6种药物,分别为氨基糖苷类的庆大霉素,氟喹诺酮类的恩诺沙星、环丙沙星、氧氟沙星,以及大环内酯类的泰乐菌素和替米考星;这与曹忠君[20]在猪肉中检出氟喹诺酮类药物残留的报道也相符合,但检出的具体药物不同,说明在食品动物养殖过程中,喹诺酮类药物存在滥用或使用不规范等现象[21]。恩诺沙星、环丙沙星、氧氟沙星、庆大霉素、替米考星及泰乐菌素6种抗微生物药物之间差异不显著(P>0.05),说明不同种类药物在临床不存在特定用药情况。并且在129份样品未检出磺胺类、四环素类、β-内酰胺类、氟苯尼考4大类药物,28种抗微生物药物未检出22种,包括喹诺酮类(8种)、磺胺类(7种)、四环素类(4种)、氨基糖苷类(1种)、β-内酰胺类(1种)、氟苯尼考(1种)。
本研究采用LC-MS/MC对抗微生物药物初筛呈阳性的肌肉、肝、肾3种组织中6种药物进行定量检测,结果表明初筛57份阳性组织样品含上述6种抗微生物药物中的一种或多种,其中恩诺沙星、环丙沙星、替米考星及泰乐菌素残留量均未超标,但2份肌肉中庆大霉素残留量超标。《中华人民共和国农业部公告第2292号》[22]明确规定,自2016年12月31日起在食品动物中停止使用氧氟沙星,但本研究在22份样品中检出了该药物,说明肉羊养殖中仍有非法使用氧氟沙星的现象,这对肉羊养殖业和人体健康存在潜在风险。
本研究采用的快速检测初筛和LC-MS/MC证实,肝中抗微生物药物检出率高于肌肉和肾,这与肝脏为药物主要代谢器官有关[23]。但方差分析结果显示,肌肉、肝、肾中不同类别抗微生物药物检出率之间差异不显著(P>0.05),这可能与药物的吸收及代谢过程在体内受诸多因素影响有关。此外,根据药物种类以及给药方式、给药途径的不同,其吸收速率、程度也会有所差异,这也是造成抗微生物药物在不同组织中残留量不同、分布不均的原因[24]。
抗微生物药物初筛检测结果显示肾中有4份阳性样品,但通过LC-MS/MS只检出2份阳性样品,表明除胶体金标试纸条存在假阳性的因素外,还可能与基质效应有关。对于动物性食品而言,样品前处理技术在药物痕量测定中起到决定作用[25],对于提取溶剂、除水剂、净化过程中填料的选择就显得尤为关键。由于动物组织含有大量蛋白质和脂肪等物质,即使通过净化也不能完全达到理想效果,从而影响化合物在离子源中的离子化,使化合物的响应出现增强或抑制,出现基质效应[26]。而消除基质效应的方法也比较多,如充分净化样品、用基质匹配标准曲线[27]、用同位素做内标校正[28]、加入分析保护剂[29]等。近些年兴起的一种快捷经济高效基质分散固相萃取技术(quick,easy,cheap,effective,rugged,and safe,QuEChERS)相对于传统的液液萃取、固相萃取而言,净化操作流程更加便捷、填料选择更加灵活[25,30-31],是未来高效提取目标化合物的理想手段。
通过对河西地区4个市肉羊3种可食组织中抗微生物药物残留检测结果进行对比,酒泉、张掖、金昌3个市的试样中以氨基糖苷类的庆大霉素检出率最高,武威市的试样则以大环内酯类的泰乐菌素和替米考星检出率最高,但4个市之间差异不显著(P>0.05)。在临床上,使用庆大霉素对于控制和治疗由沙门氏菌、金黄色葡萄球菌、铜绿假单胞菌、大肠埃希氏菌、巴氏杆菌等细菌引起的局部或全身感染具有良好效果,如泌尿生殖道、呼吸道、胃肠道等部位感染以及乳腺炎、骨关节炎及软组织感染等[32]。钱坤等[33]在内服和皮下注射两种给药途径对替米考星药代动力学进行研究,结果表示其吸收均极为迅速,达峰快,血液中药物半衰期长,药物组织穿透力强,体内分布容积大,在组织中药物浓度高,维持时间长,这些特殊的药动学特性尤其适合于家畜肺炎治疗。8月下旬,河西地区气候干燥高热,规模化养羊场如通风不畅、缺水则易引起羊呼吸道疾病和继发性感染等,而庆大霉素和替米考星适用于上述病症,羊在屠宰前若不能严格执行停药期,则极易引起羊可食组织中抗微生物药物残留。此外,抗微生物药物残留也与各地实行不同的防疫政策以及防治羊常见病所用药物基本一致[34]。对此,笔者建议畜牧兽医主管部门加强抗微生物药物使用监管、残留检测,临床兽医和养羊企业合理规范使用抗微生物药物,严格遵守停药期,禁止使用国家规定的禁用药物;屠宰企业应提高抗微生物药物残留检测频率,防止不合格产品流入市场。
对3类可食组织样品,采用LC-MS/MS测定抗微生物药物残留结果与兽药快速试纸卡初筛结果筛选出的药物种类一致,但在检出的样品数量上结果不全相同。本研究验证结果表明,快速检测试纸条检测效果较好,检测速度快、耗时短、使用更方便,可以用于抗微生物药物的快速和非靶向的调查、检测;羊可食组织存在基质背景干扰严重、定性困难、抗微生物药物在样品组份残留含量较低等情况,本试验采用LC-MS/MS[16-18],可发挥其灵敏度高、精准度高、检测限低的特点,作为精准识别羊肉产品中抗微生物药物残留的有力技术支撑。肉品中抗微生物药物检测方法较多,本研究采用胶体金技术和LC-MS/MS有机结合,应用于实际检验检测工作中,可为肉羊可食组织中抗微生物药物的快速检测及精准识别、开展肉品抗微生物药物残留的监测奠定基础,为加强羊肉产品安全检测和管理提供科学数据,以保障肉羊产品质量安全。
