七清止泻颗粒的制备及质量控制
2023-02-16侯佳琪辛怡霖李青云潘康锁李引乾
张 欣,侯佳琪,辛怡霖,李青云,唐 熙,潘康锁,李引乾*
(1.西北农林科技大学动物医学院,陕西杨凌 712100;2.陕西省农业检验检测中心,陕西西安 710016)
七清止泻颗粒是在传统中医经验方基础上,结合中医理论、文献调研和长期临床实践等,对原散剂处方优化改造而成。全方由黄芩、白头翁、苦参、石榴皮、黄芪、藿香、山楂7味药组成,具有清热除湿、益肠止痢之功效,其中黄芩清热解毒,对多种均有杀抑制作用,为君药[1];白头翁和苦参在中兽药性味与归经上和黄芩一致,具有清热燥湿,凉血解毒,可增强黄芩的抗菌活性和抑菌效果,为臣药[2-3];石榴皮和黄芪性温,提高鸡的机体免疫能力,减少苦寒类药物对幼禽的刺激,为佐药[4-5];藿香芳香化湿、山楂清香微甜,能刺激胃液分泌帮助消化,调和药性,促进生长,为使药[6-7]。7味中药相互配合,相辅相成,增加抑菌效果,兼顾清热除湿,扶正祛邪,补中益气的效果。
传统中药散剂一般成分复杂,含量均匀度差,在鸡育雏过程中,因给药方式单一,不适用现代规模化养殖的需求,中药颗粒剂具有改善适口性、用药方便、可饮水给药、便于储藏及提高生物利用度等优点[8-9],基于质量源于设计(quality by design,QbD)理念[10],本研究对原散剂进行改造,优化提取工艺及其颗粒剂成型工艺,制定质量标准,为七清止泻颗粒的质量控制试验依据。
1 材料与方法
1.1 材料
1.1.1 药品及试剂 黄芩、白头翁、苦参、石榴皮、黄芪、藿香、山楂,购自杨陵华仁堂大药房;黄芩苷对照品,批号201021,中检计量生物有限公司产品,供含量测定用;高效硅胶G薄层板,青岛海洋化工有限公司产品;糊精,批号T14A10Z95117,上海源叶生物科技有限公司产品;蔗糖,批号201229,西陇科学股份有限公司产品;水为高纯水,其余试剂均为分析纯。
1.1.2 主要仪器 A60多功能分体煎药煲,潮州市湖安区康雅顺电器有限公司产品;RE52-98旋转蒸发仪,上海亚荣生化仪器厂产品;UV-1200型,紫外分光光度仪,上海美谱达仪器有限公司产品。
1.2 方法
1.2.1 七清止泻颗粒干浸膏的制备
1.2.1.1 工艺方法 将药材按处方称重,黄芩15 g、白头翁10 g、苦参10 g、石榴皮10 g、黄芪15 g、藿香10 g、山楂10 g,采用传统水煎法,利用正交试验设计,研究出药物复方的最佳提取条件,其制法如下:按照处方称取药品,粉碎成小块,加适量的水进行煎煮数次,煎煮完成后合并煎液,对煎液进行过滤,经旋转蒸发后的浓缩药液进行减压干燥制成干浸膏,浸膏研磨成粉,快速称重,备用[11]。
1.2.1.2 正交试验优化提取工艺 利用正交试验对提取工艺进行优化探索。本试验根据前期文献查阅[12],选择加水倍数(A)、提取次数(B)和提取时间(C)作为考察因素,以干浸膏得率为评价指标,各因素取3个水平,正交试验因素水平设计见表1。

表1 七清止泻颗粒的提取正交因素水平
1.2.1.3 验证试验 按照药方称取药材,按上述筛选的工艺进行重复试验,计算干膏得率,观察该工艺可行性。
1.2.2 七清止泻颗粒的制粒工艺
1.2.2.1 辅料种类的筛选 参考多种中药颗粒剂的制粒方法,考虑经济性,选用加入适量的蔗糖和糊精作为辅料,以增加药品颗粒的稳定性和颗粒口感,混匀,选用适量乙醇作为润湿剂,制成颗粒,干燥,制成80 g,即得。
1.2.2.2 辅料用量的筛选 按照《中华人民共和国兽药典》2020版二部附录0106颗粒剂的要求,以及参考其他收录颗粒剂的制法[3],由1.2.1方法得干浸膏粉,加入含不同配比糊精和蔗糖的辅料,混匀,对混合药粉进行制成颗粒,干燥,制成80 g,观察其形状,对产物颗粒的成型性、休止角、溶化性和吸湿性进行评分,4个指标各占比25%,对其结果进行综合评价。
1.2.2.3 润湿剂浓度的筛选 将1.2.1方法得干浸膏粉,按照上述筛选的最佳辅料比例混匀,分别加入浓度为500、750、950 mL/L的乙醇作为润湿剂进行制粒,以成型率为评价指标,优选最佳乙醇浓度。
1.2.3 七清止泻颗粒试制的质量控制 按照1.2.1和1.2.2的最佳提取和制粒工艺试制,制备210405、210406、210407、210408共4个批次进行质量控制。
1.2.3.1 质量检查 按照《中华人民共和国兽药典》2020版二部附录0106颗粒剂要求分别对4个批次七清止泻颗粒进行性状、粒度、水分和溶化性等考察[3]。
1.2.3.2 黄芩的薄层色谱鉴别 对七清止泻颗粒君药黄芩主要有效成分黄芩苷进行薄层色谱鉴别,取本品210405、210406、210407、210408共4个批次各15 g,分别各加甲醇50 mL,超声处理20 min,滤过,滤液蒸干,残渣,分别各加甲醇2 mL使溶解,滤过,滤液作为供试品溶液。另取黄芩苷对照品,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。按照《中华人民共和国兽药典》2020版二部附录0502薄层色谱法进行试验[3]。吸取上述5种溶液各5 μL,分别点于同一硅胶G薄层板上,黄芩苷对照品溶液点2次,以乙酸乙酯-丁酮-甲醇-水(10∶3∶1∶2)为展开剂,置展开缸内预饱和30 min,展开,取出,晾干,喷以10 mg/mL的氯化铁乙醇溶液。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
1.2.3.3 黄芩苷的含量测定
(1)对照品溶液的配制:准确称取黄芩苷标准品10 mg,于适量甲醇中溶解,经超声处理30 min,使黄芩苷完全溶解,再加入甲醇至刻度,摇匀,定容于50 mL棕色容量瓶中,即得对照品溶液(浓度200 μg/mL)。
(2)供试品溶液的制备:准确称取本品0.5 g,适量甲醇中溶解,经超声处理30 min,使其完全溶解置50 mL量瓶中定容,再精密量取1 mL,置50 mL棕色容量瓶中,加甲醇至刻度摇匀,即得供试品溶液(浓度200 μg/mL)。
(3)测定波长的选择:黄芩苷最大吸收波长的选择用可见紫外分光光度法分度计对黄芩苷标准液进行全波段扫描,以其最大吸收波长作为黄芩苷的吸收波长。取0.5 mL黄芩苷对照品溶液,再加入甲醇于10 mL容量瓶定容,得到10 μg/mL黄芩苷溶液,在230 nm~350 nm范围内将对照品与供试品溶液进行全波长扫描。
(4)黄芩苷标准曲线的制作和精密度试验:分别取0.1、0.2、0.3、0.4、0.5 mL黄芩苷对照品溶液,分别加入甲醇于10 mL容量瓶定容,得到2、4、6、8、10 μg/mL的黄芩苷溶液,以甲醇为空白试剂,用紫外-可见分光光度计在其最大吸收波长处测定吸光度值OD,重复3次,取平均值,以黄芩苷标准品的浓度C为横坐标,测出的吸光度值OD为纵坐标绘制标准曲线。
(5)重复性试验:按照供试品溶液的制备方法,分别准确称取批号为210405颗粒6份,在最大吸收波长处测定吸光度,依次进样分析,计算吸光度的RSD。
(6)加样回收试验:分别准确称取批号为210405颗粒0.25 g,6份,分别精确加入10 mg黄芩苷对照品溶液,按供试品溶液的制备方法,在最大吸收波长处测定吸光度,依次进样分析,计算吸光度回收率和RSD。
(7)样品中黄芩苷含量测定:按供试品溶液的制备方法,分别准确称取本品批号为210405、210406、210407、210408各0.5 g,制得供试品溶液,在最大吸收波长处测定吸光度,由回归方程式计算出对应浓度,计算样品中黄芩苷含量。
2 结果
2.1 七清止泻颗粒干浸膏的制备结果
2.1.1 提取正交试验结果 选用L9(34)正交表对七清止泻颗粒的制粒工艺进行考察,以干膏得率作为评价指标,七清止泻颗粒的提取正交试验结果见表2。

表2 七清止泻颗粒的提取正交试验结果
方差分析结果表明,以干膏得率为考察指标,由表中极差大小显示,各影响因素影响次序依次为C(提取次数)>B(提取时间)>A(加水量)。分析极差最佳的提取工艺为A2B3C2,但提取次数过多会损失药效,另从节约能源的角度,确定最终提取工艺为加10倍量水、提取2次、每次1.5 h。
2.1.2 提取工艺验证试验结果 称取处方药品,按照1.2.1筛选的最佳工艺重复提取试验2次,称量产物干膏质量,计算干膏率。
按照正交试验最佳提取工艺重复5次,RSD为2.74%(表3),表明该提取工艺稳定可行,重复性良好,为下一步制粒配方提供了依据。
2.2 七清止泻颗粒的制粒工艺结果
2.2.1 辅料用量的筛选结果 将提取的干膏粉和含不同配比糊精和蔗糖的辅料混合制粒,综合评价产物(表4)。直观分析表明,当加入糊精和蔗糖质量比为7∶3的辅料,混合制成的颗粒容易制粒,稳定性良好,不易吸湿,易于溶化,且流动性好,有助于制成颗粒后分装和贮存。
2.2.2 润湿剂浓度的筛选 对不同浓度的乙醇作为润湿剂制粒的成型率进行试验,由试验可得,颗粒剂的成型率随乙醇浓度的增加而增加;当乙醇浓度为950 mL/L时,成型率最高,故确定950 mL/L的乙醇作为润湿剂。
2.3 七清止泻颗粒试制的质量控制结果
2.3.1 试制颗粒的质量检查 试验可得,4个批次均为棕色至棕褐色、干燥、大小形态均匀、色泽一致的颗粒剂,无吸潮、软化、结块等现象,粒度、水分、溶化性均符合《中华人民共和国兽药典》相关规定。
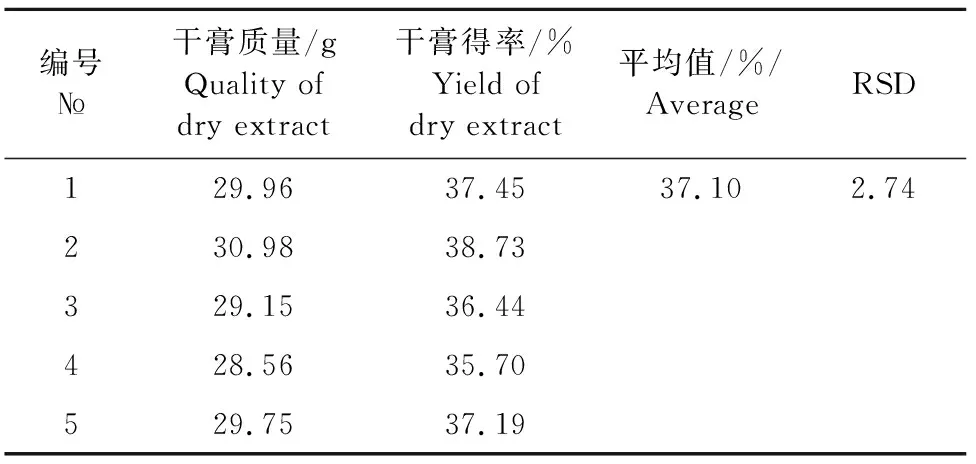
表3 提取工艺验证试验结果

表4 七清止泻颗粒辅料用量试验表
2.3.2 黄芩苷的薄层色谱鉴别 由结果可以看出,4个批次颗粒色谱中,在与黄芩苷对照品色谱相应的位置上,供试品色谱显示相同颜色的斑点(图1)。
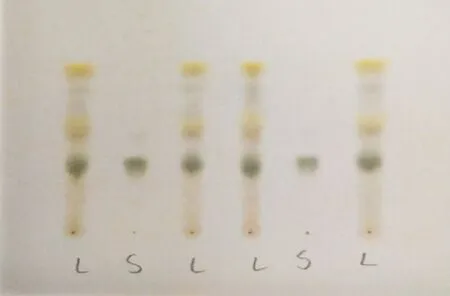
L表示4个批次颗粒,依次为210405、210406、210407、210408 4个批次,S表示黄芩苷标准品对照品
2.3.3 黄芩苷的含量测定
(1)测定波长的选择:经试验,黄芩苷在278 nm 处有最大吸收,故选择278 nm波长为测定波长。
(2)标准曲线绘制和精密度试验:按1.2.3.3试验测定吸光度,各浓度吸光度(OD)的RSD≤0.72%,表明仪器精密度良好。进行回归分析得回归方y=0.073x-0.025 5,R2=0.997,表明黄芩苷在2 μg/mL~10 μg/mL浓度范围内线性关系良好(图2)。
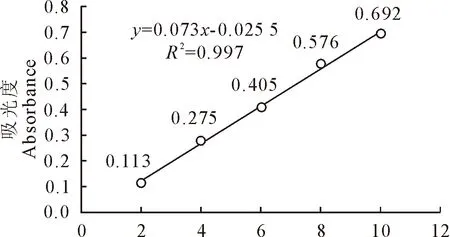
图2 黄芩苷吸收度线性关系图
(3)重复性试验:重复6次试验,以吸光度(OD)代入回归方程,计算可得批号为210405的七清止泻颗粒中黄芩苷平均含量为4.00%,RSD值为1.25%,表明本方法的重复性良好。
(4)加样回收试验:按照1.2.3.3试验方法下操作,精密称取批号为210405的七清止泻颗粒0.25 g,共6份,精确加入黄芩苷对照品,按照样品测定项下方法操作,结果见表5。试验结果可得,样品中的平均加样回收率为98.18%,RSD值为1.66%,表明本方法的加样回收率良好。
(5)含量测定结果:按照1.2.3.3试验方法下操作,对4个批次七清止泻颗粒进行含量测定,依照标准曲线法计算样品中黄芩苷含量,结果见表6。结果表明,4个批次样品中,其样品中黄芩苷的最低含量为4.003%。

表5 加样回收率试验结果

表6 4个批次七清止泻颗粒含量测定结果
3 讨论
在提取工艺中,采用传统水煎中药提取方法,用正交试验探究最佳提取工艺,3个因素增加都会提高干浸膏得率,但相对增加幅度较小,且提取次数过多会损失药效,考虑时间和低碳理念,最终确定提取工艺为加10倍量水、煎煮2次、每次1.5 h,合并煎液,对煎液进行过滤,经过旋转蒸发和减压真空干燥制成干浸膏,研磨成粉,备用。
在制粒工艺中,中药浸膏通常具有较强的吸湿性,实验室直接制粒有一定难度且稳定性差,为降低其吸湿性,增加溶化率和流动性,便于制粒和储存,需要探索合适的辅料[13]。前期试验表明,七清止泻颗粒中药浸膏软材黏度较大,无法直接制粒,直接加入辅料混合困难,制粒损耗也比较多,质地较硬,颗粒不均匀,不符合颗粒剂的有关要求,后采用将浸膏干燥成药粉和辅料混合,用适量的乙醇作为润湿剂,喷淋混合药粉,均匀搅拌,再制粒。对产物进行综合评价,当加入糊精和蔗糖质量比为7∶3的辅料,混合制成80 g颗粒剂,制备颗粒效果最佳,工艺稳定可靠,均符合《中华人民共和国兽药典》对中药颗粒剂的要求。
由于实验室条件的局限性,传统湿法手工制粒耗能过大,以及相对生产周期和暴露时间过长,增加染菌的机会,下一步中试试验要明确进行商业规模化的生产条件验证,进一步优化生产工艺和工艺参数。
在质量控制中,黄芩为处方中君药,黄芩苷为黄芩主要活性成分之一,具有广谱抗菌、抗病毒、抗真菌及抗支原体作用[14]。中药有效含量复杂,加上本药由七味药组成,已知化学物质几十种,因此选用药物原料的时候应严格控制质量,再根据中药的检验标准特性,结合中药质量标志物的概念[15],为了更有效控制七清止泻颗粒的质量,选择君药的有效成分黄芩苷进行定性和定量监控[16]。结果表明,4个批次样品中,其样品中黄芩苷的最低含量比为4.00%,根据《中华人民共和国兽药典》2020版二部规定,黄芩干燥品含黄芩苷不少于8%,结合处方,以每克样品中各成分含量的85%作为七清止泻颗粒含量测定的限度,因此将本品黄芩苷不少于3.40%作为后续中试试验标准。
本研究对原散剂进行处方和剂型优化改造,制备成七清止泻颗粒剂,研究考察了七清止泻颗粒的最佳提取工艺,加入辅料种类的比例用量以及润湿剂等进行了优化筛选,得到相应的最佳制备工艺,并对该工艺进行了重复验证,建立了有关定性和定量的测定方法。该方法制得的七清止泻颗粒成型性良好,稳定不易吸湿,流动性好,溶解性佳,制备工艺稳定可靠,建立的含量测定方法准确度高、专属性强、重现性好,能够作为七清止泻颗粒的质量控制标准,为后续药理学研究和中试试验奠定了基础。
