藏红花总苷片的制备及质量标准的初步研究*
2023-02-13王光雨
陈 雁,王光雨
(扬州市职业大学医学院,江苏 扬州 225200)
藏红花总苷是一类以藏红花素1为主的二萜类化合物[1],具有广泛而良好的药理活性,对中枢神经系统和心血管系统疾病均具有良好的疗效,同时,还具有抗肿瘤、抗氧化、抗炎、保肝利胆、抗糖尿病等作用[2]。许多传统名贵方药中均含有藏红花苷类成分,如市场出售的西红花总苷片。其具有活血化瘀、通脉、止痛等功效,是胸痹心痛、心血瘀阻患者的治病良药。但由于以名贵稀缺药材——藏红花为原料药材,藏红花产量极低,价格非常昂贵,堪比黄金,因此,开采利用的成本极高。有研究表明,栀子药材中也含有该类成分[3],故本研究依据选用藏红花的平价替代药材——栀子进行了深度研究,不仅节约了成本,还为栀子的开发利用提供了依据。作者前期已开展了栀子药材中藏红花总苷成分的提取纯化工艺研究[4]。现将从便于携带、药物显效迅速、提高药物生物利用度等角度制成片剂,从辅料选择、用量确定、湿法制粒、压片、包衣等角度确定片剂制备工艺并进行质量研究,旨在为该类制剂的应用提供参考依据。
1 材料与方法
1.1材料
1.1.1仪器 UV-1200紫外可见分光光度计购自美国安捷伦公司,高效液相色谱仪购自美国安捷伦公司,AY120电子天平购自日本岛津公司,ZP-9旋转式压片机购自上海天阖机械设备有限公司,GHL-10湿法混合制粒机购自长沙市岳麓区中南制药机械厂,ZBJ-01智能崩解仪购自上海精胜科学仪器有限公司。
1.1.2实验材料 藏红花总苷为自制(批号分别为211203、211209、211214),淀粉、糊精、硬脂酸镁均购自河北省廊坊市淀粉厂,微晶纤维素购自上海昌为医药辅料技术有限公司,羧甲基淀粉钠(CMS-Na)购自苏州依俐法化工有限公司,滑石粉购自青岛盛达源滑石粉开发有限公司,对照品为藏红花素1及藏红花酸标准品,均购自中国药品生物制品检定所(纯度均在98%以上),市售西红花总苷片购自瑞阳制药有限公司(国药准字:Z20163079)。
1.2方法
1.2.1剂型选择 在开发藏红花总苷片方面遵循国际通行的能口服不注射的原则,藏红花苷类化合物在水中溶解性较好,可选择口服制剂。拟开发为片剂是由于藏红花总苷具有一定苦味,制成片剂包衣对药物有一定程度上的遮蔽、保护与稳定作用,实现了良药不苦口、便于患者吞服等优势;且片剂质量稳定,剂量准确,携带、运输及贮藏均较为方便,成本相对低廉[5]。
1.2.2辅料筛选 藏红花总苷原料为中药浸膏,具有吸湿性,长期放置会出现硬结现象,这就要求选择合适的辅料改善主药的吸湿性质,使主药干燥,从而保证制剂质量稳定[6]。
1.2.2.1润湿剂选择 由于藏红花总苷中含有大量易溶于水的成分——藏红花素1,在制备颗粒的过程中选用含水乙醇作为润湿剂要充分考虑含水量,含水量不宜过高,以防药粉粘结成块,难以制粒。选择60%、75%、90%乙醇做平行试验,观察制粒情况。
1.2.2.2稀释剂选择 选择市场常用的稀释剂进行试验。淀粉价廉易得,性质稳定,是制备片剂最常用的稀释剂;乳糖流动性和可压性较好,性质也稳定,但成本较一般稀释剂偏高;甘露醇易溶于水,无引湿性,不适用;糊精可与淀粉相配伍,微溶于水,不溶于乙醇,兼有黏合作用;微晶纤维素近年来被广泛用作片剂的辅料,除作为稀释剂外,还兼有润滑、崩解和黏合作用[7]。故选用淀粉、糊精和微晶纤维素作为混合稀释剂进行制粒,并对颗粒的流动性进行考察,以休止角作为判定依据,使用休止角测定仪测定,考察颗粒的流动性[8]。休止角小于40°,摩擦力较小,可满足生产中的流动性需求;≥40°时摩擦力大,则流动性较差。
1.2.2.3崩解剂选择 分别以CMS-Na和干淀粉为崩解剂开展预试验,以崩解时间和制剂性状作为依据进行考察。
1.2.2.4润滑剂选择 硬脂酸镁、滑石粉为常用润滑剂,考虑滑石粉用量较大,选择硬脂酸镁开展预试验,并比较所制片剂外观。
1.2.3正交设计 选取4个因素(乙醇用量、混合稀释剂用量、硬脂酸镁用量、CMS-Na用量),每个因素取3个水平设计正交试验表开展平行试验。并以软材黏性、颗粒外观、片剂成型、硬度、脆碎度作为评价指标,确定最终综合评分(软材黏性×10%+颗粒外观×10%+片剂成型×30%+硬度×40%+脆碎度×10%)[9]。
1.2.4质量检查 依据药典标准开展片剂常规数据检查。
1.2.4.1重量差异 参照《中国药典》2020版四部片剂重量差异项规定的方法进行检查[10]。分别取不同批次藏红花总苷片20片,精密称定总重量和每片重量,计算平均片重及重量差异限度。
1.2.4.2崩解时限 取藏红花总苷片6片,按崩解时限检查法(《中国药典》2020版四部0921项)检查,分别置于连接吊篮的玻璃管中,加挡板,启动崩解仪,记录崩解时间。
1.2.4.3鉴别 取藏红花总苷片5片研细后精密称取,加50%甲醇超声溶解,滤纸常压过滤,制得供试品溶液备用;另取藏红花素1及藏红花酸对照品各2 mg至10 mL容量瓶中,加甲醇溶解稀释分别制得对照品溶液;同时,制备空白溶剂作为参照,进行薄层色谱法(《中国药典》2020版四部0502项)试验[10-11]。
1.2.5含量测定方法学考察 依据药典标准开展实验,具体方法如下。
1.2.5.1色谱条件 吸收波长:440 nm;色谱柱:ZORBAX SB-C18柱;流动相:甲醇-0.05%醋酸水55∶45;流速:0.8 mL/min;柱温:30 ℃[12]。
1.2.5.2对照品溶液的制备 精密称取藏红花素1对照品2.5 mg和藏红花酸对照品2.0 mg分别置于10 mL容量瓶中,加50%甲醇水溶液溶解稀释至刻度,即得浓度为0.25 mg/mL的藏红花素及0.2 mg/mL的藏红花酸对照品储备液。
1.2.5.3供试品溶液的制备 取藏红花总苷若干片研细,精密称定0.3 g,置于100 mL具塞锥形瓶中,加50%甲醇水溶液超声溶解、补足重量、过滤、摇匀,得到3 mg/mL的供试品溶液。
1.2.5.4专属性试验 分别取藏红花素1、藏红花酸对照品溶液、供试品溶液各10 μL注入高效液相色谱仪,比较高效液相色谱图。
1.2.5.5线性关系考察 精密吸取藏红花素对照品储备液0.1、0.2、0.4、0.8、1.0 mL,藏红花酸对照品储备液0.1、0.2、0.4、0.8、1.0 mL,分别置于1 mL容量瓶中,加入50%甲醇水定容至刻度即得。以峰面积为纵坐标、对照品浓度为横坐标绘制标准曲线。
1.2.5.6精密度试验 分别精密量取藏红花素1对照品溶液和藏红花酸对照品2 mL各置于6只10 mL的容量瓶中,50%甲醇水溶液溶解稀释至刻度,摇匀。将溶液分别进样,记录峰面积,考察精密度。
1.2.5.7重复性试验 取供试品按“1.2.5.3”项方法平行制备6份,分别注入高效液相色谱仪,记录峰面积,计算相对标准偏差(RSD)。
1.2.5.8稳定性试验 精密吸取供试品溶液10 μL,分别于0、4、8、12、16、24 h注入高效液相色谱仪,测定峰面积,考察稳定性。
1.2.5.9回收率实验 精密称取已知含量藏红花总苷片6份,按高、中、低3个水平精密加入各对照品适量,计算藏红花素1和藏红花酸回收率。
1.2.5.10含量测定 分别取市售西红花总苷片和自制藏红花总苷片各5片,精密称定,研细,按“1.2.5.3”项方法制成西红花总苷片待测液和藏红花总苷片待测液,分别注入高效液相色谱仪进行检测,计算平均每片西红花总苷片中藏红花素1和藏红花酸含量。
2 结 果
2.1辅料筛选结果
2.1.1润湿剂 选用75%乙醇作为润湿剂制粒情况较好。见表1。

表1 润湿剂选择结果
2.1.2稀释剂 用淀粉∶糊精∶微晶纤维素1∶1∶2比例混合时制得的颗粒流动性较好。见表2。

表2 稀释剂选择结果
2.1.3崩解剂 干淀粉用量大,并且可压性和流动性较差;而CMS-Na用量适宜,具有良好的润湿性和崩解作用,故选用CMS-Na作为崩解剂,以100粒用量0.2 g为宜。见表3。

表3 崩解剂选择结果
2.1.4润滑剂 用硬脂酸镁作为润滑剂,100粒用量0.1 g更符合要求。见表4。

表4 润滑剂选择结果
2.2正交设计结果 正交设计因素水平见表5。根据药典要求片剂载药量对应的日服生药不得超过20 g,结合前期实验结果,20 g栀子药材中约提取藏红花总苷0.24 g,参考市场西红花总苷片每次服用4片,每天3次,设计片重为0.04 g,载药量为50%。称取藏红花总苷2.0 g,采用湿法挤出制粒的压片工艺,按正交设计量加入辅料,反复过筛混合均匀、制软材、制粒、55°干燥2.5 h、压片。综合评分实验结果见表6。4个因素对片剂处方的影响顺序依次为B>D>C>A,确定片剂成型的优选处方为A2B1C2D3。

表5 L9(34)正交设计因素水平
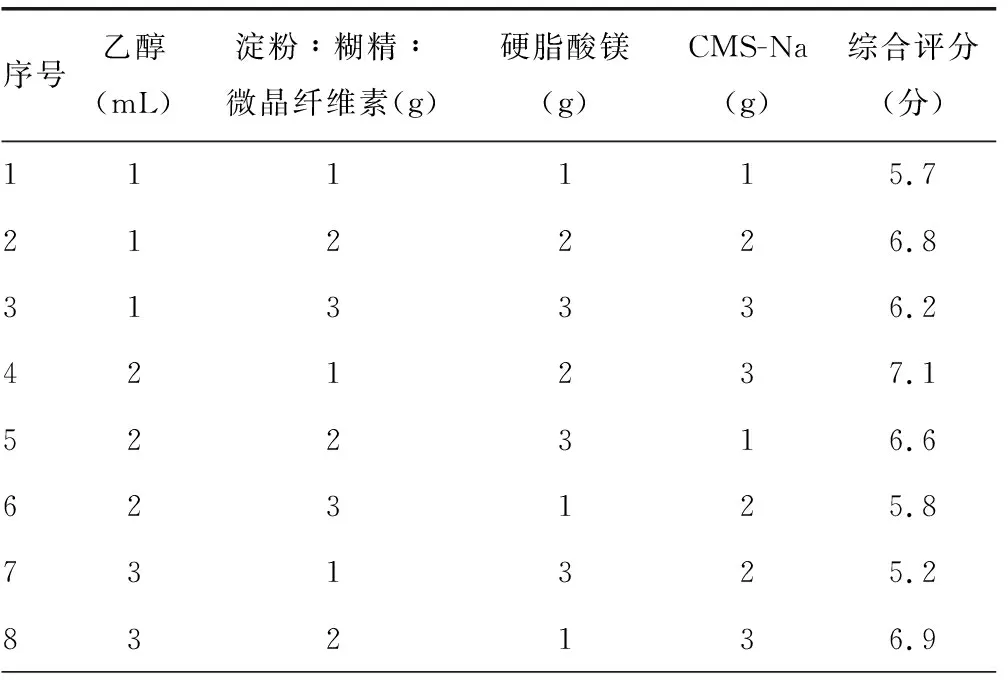
表6 L9(34)正交设计安排及实验结果

续表6 L9(34)正交设计安排及实验结果
2.3质量检查结果 本品为薄膜衣片,外表光滑,除去薄膜衣后显橙黄色至棕红色,气微香,味辛辣。
2.3.1重量差异结果 符合药典规定标准,结果见表7。

表7 片剂重量差异检查
2.3.2崩解时限结果 符合药典规定标准,结果见表8。

表8 崩解时限测定
2.3.3鉴别结果 供试品色谱中在与对照品溶液色谱相应的位置上显相同的黄色斑点;再喷以浓硫酸-香草醛溶液,斑点显色清晰。
2.4方法学考察结果 在藏红花素1及藏红花酸保留时间附近无其他成分峰干扰,证明该方法的专属性较强。色谱图见图1。

A:藏红花素1对照品;B:藏红花酸对照品;C:供试品。1.藏红花素1;2.藏红花酸。
2.4.1线性关系考察 藏红花素1线性回归方程:Y=122.24X-0.012 3,r=0.999 9;线性范围:0.25~2.50 μg;藏红花酸线性回归方程:Y=115.53X-0.306 6,r=0.999 7;线性范围:0.2~2.0 μg。见图2。

图2 线性关系考察
2.4.2精密度RSD分别为1.01%和0.98%,表明仪器精密度和方法精密性均良好。
2.4.3重复性RSD分别为1.51%和1.18%,表明方法的重复性良好。
2.4.4稳定性RSD分别为1.45%和1.26%,表明样品在24 h内稳定性良好。
2.4.5回收率 藏红花素1和藏红花酸的回收率测定结果见表9。
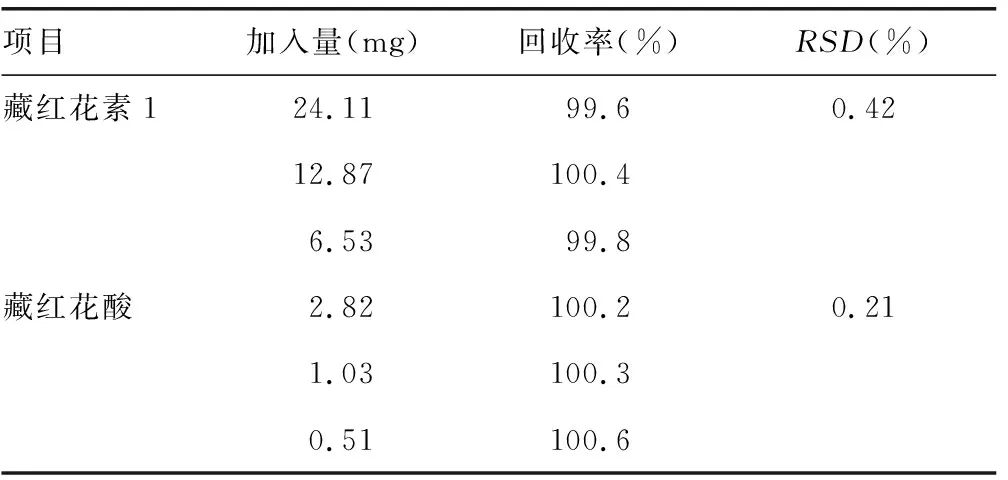
表9 回收率测定结果(n=6)
2.4.6含量测定结果 每片西红花总苷片中含藏红花素1和藏红花酸的量分别为12.011、1.321 mg,每片自制的藏红花总苷片中含藏红花素1和藏红花酸的量分别为12.512、1.208 mg。
3 讨 论
藏红花总苷是药材藏红花和栀子中共有的一类化合物,目前,市场上该类成分相关制剂多以藏红花为原料药材,价格高昂。本研究首次选用我国资源丰富的栀子作为原料药材可节约成本,制成藏红花总苷片可作为市场西红花总苷片的补充和参考。提取纯化工艺中通过重结晶的方法,解决了单纯大孔树脂分离纯度不高的缺陷。采用单因素考察、正交设计等方法对提取方案中的溶剂、温度及提取次数,吸附试验中吸附树脂的选择、温度对吸附剂性能的影响、洗脱流速等进行了充分的考察和研究,从而筛选出最佳提取纯化工艺,提高了实验效率;制备工艺研究中充分考虑药粉吸湿性、片剂成型、崩解、脆碎度及制粒和压片时的环境湿度,通过单因素考察和正交设计比较不同辅料种类和用量最终确定制备工艺条件;并结合药典对片剂的基本要求确保药品质量。在方法学考察实验过程中建立了藏红花素1和藏红花酸2种成分同时测定的方法,并尝试了多种流动性系统,如甲醇-水、乙腈-水,发现55∶45甲醇-0.05%醋酸水可获得较好峰形且样品的分离度较好。对所制制剂开展质量标准的相关研究进行了系统的方法学验证,为后续研究奠定了基础。同时,2010、2015、2020版《中国药典》均以栀子苷作为指标成分对栀子及制剂进行定量分析,对栀子中另一重要成分——藏红花苷类化合物尚未建立相关质量标准,在对栀子药材进行客观评价及栀子制剂质量控制时缺乏说服力,本研究结果为将藏红花素1或藏红花酸作为对照品一同纳入药典标准对栀子及其制剂进行质量控制提供了数据参考。
综上所述,栀子是我国一种常见的果实类药材,其成分的开发、利用已有悠久历史,随着现代医学药学和分子生物学等领域的飞速发展,栀子中藏红花总苷的药理作用已得到充分肯定,特别是其抗癌活性和抗癌机制的研究使该类物质很有可能成为未来理想的抗癌药物之一;其强力的降血脂和活血化瘀功效也使藏红花苷类单体化合物有望成为治疗心脑血管疾病的主流药物[13]。本研究以栀子作为原料药材,提取分离出藏红花总苷类成分并纯化,选择适当辅料确定片剂的最终制备工艺,并初步开展了该制剂科学、合理的质量研究,为藏红花总苷片的发展及药典中其质量标准的正式建立提供了一些新的思路和参考。
