中标与原研盐酸莫西沙星片治疗门诊社区获得性肺炎的有效性、安全性与经济性比较 Δ
2023-02-09庞婕吴晓雯李春华金泰宇游维丽连云港市第一人民医院药学部江苏连云港22202南京医科大学康达学院第一附属医院药学部江苏连云港22202连云港市第一人民医院呼吸与危重症医学科江苏连云港22202连云港市第二人民医院药学部江苏连云港22202
庞婕 ,吴晓雯 李春华 ,金泰宇 ,游维丽 (.连云港市第一人民医院药学部,江苏 连云港 22202;2.南京医科大学康达学院第一附属医院药学部,江苏 连云港 22202;.连云港市第一人民医院呼吸与危重症医学科,江苏 连云港 22202;.连云港市第二人民医院药学部,江苏 连云港 22202)
社区获得性肺炎(community-acquried pneumonia,CAP)是世界范围内较常见的呼吸系统感染性疾病之一。近年来,CAP在全球的发病率和病死率节节攀升,医药资源消耗巨大,成为世界各国共同关注的公共卫生问题之一[1-2]。为有效防治和规范管理,各国相继出台了CAP临床诊疗指南,推荐门诊CAP患者单独口服β-内酰胺类药物或联合大环内酯类药物,或者单独使用呼吸喹诺酮类药物治疗[3-4]。鉴于我国非典型病原体对大环内酯类药物的耐药率较高[3,5]、门诊患者对联合用药方案的依从性较差[6],我国医院门诊大多以相关指南为依据[3],选择以莫西沙星为代表的呼吸喹诺酮类口服药物单药治疗CAP。
为减轻患者药费负担、提高药品可及性,我国从2018年底开始在全国范围内推进药品集中带量采购(以下简称“集采”)政策,以实现临床药品的“降价提质”[7]。本课题组前期问卷调查发现,随着药品集采政策在各个地区的深入推广,抗菌药物的价格大幅度降低,但患者和医生对中标抗菌药物有效性和安全性的疑虑也随之产生:药品价格降低,其临床疗效能否得到保证?针对上述问题,迫切需要开展中标抗菌药物品种临床应用综合评价,为临床提供更加全面、真实和可靠的用药数据,以打消患者和医生的疑虑。为此,本研究从有效性、安全性及经济性方面评估了中标与原研盐酸莫西沙星片治疗门诊CAP的差异。
1 资料与方法
1.1 数据来源
本研究采用回顾性队列研究设计,筛选并纳入2021年1-12月在江苏省连云港市第一人民医院呼吸与危重症医学科(以下简称“我科”)门诊就诊的CAP患者,通过医院信息管理系统、医师-药师联合门诊以及电话访视等方式获取患者的基本资料和用药信息,用于药物有效性与安全性评价。通过医院信息管理系统提取盐酸莫西沙星片实施集采前后1年即2019年4月-2020年3月和2020年4月-2021年3月使用量的相关数据,用于药物经济性评价。
本研究方案经医院医学伦理委员会审核通过(批件号LW-20220423001-01)。患者纳入标准包括:(1)年龄≥18周岁;(2)生命体征平稳;(3)临床诊断为CAP(国际疾病分类第10版编码J15.901);(4)用药疗程≥3 d;(5)病历资料完整。排除标准包括:(1)接受家庭氧疗或来自养老院等机构的患者;(2)合并有肺外感染性疾病、恶性肿瘤或其他终末期疾病者;(3)妊娠或哺乳期妇女;(4)免疫功能低下者;(5)病历资料缺失者。对于多次就诊患者,本研究只纳入首次门诊病历资料进行统计分析。
入选患者均采用口服盐酸莫西沙星片单药抗感染治疗方案,用法用量均为每次0.4 g,每天1次。根据入选患者门诊处方中盐酸莫西沙星片的生产厂家分为原研药组(德国某制药公司,规格0.4 g/片,包装规格3片/盒,价格69.31元/盒)和中标药组[四川某制药公司,规格0.4 g/片(按C21H24FN3O4计),包装规格6片/盒,价格16.24元/盒]。
1.2 观察指标
1.2.1 有效性指标
(1)治疗效果:经盐酸莫西沙星片治疗后达到临床稳定视为治疗有效,需符合下列所有5项标准——①体温≤37.8 ℃;②心率≤100次/min;③呼吸频率≤24次/min;④收缩压≥90 mmHg(1 mmHg=0.133 kPa,下同);⑤血氧饱和度≥90%(或者动脉血氧分压≥60 mmHg,吸空气条件下)[3]。治疗失败标准为符合下列2项标准中的任一项——①临床症状无改善,需要更换抗菌药物;②临床症状一度改善又恶化,病情进展[3]。临床治疗有效率(%)=治疗有效例数/总例数×100%。
(2)缓解时间:患者临床表现,即症状(咳嗽、咳痰、发热、胸痛)和体征(肺部干/湿性啰音)达到缓解所需要的时间。将体温正常时间≥48 h、临床表现异常项目≤1项定义为“缓解”[3]。
(3)用药疗程:患者使用盐酸莫西沙星片连续治疗的总时间。
(4)再次就诊率:患者接受盐酸莫西沙星片治疗结束后1~3 d内再次因肺部感染就诊的发生率。再次就诊率(%)=再次就诊例数/就诊总例数×100%。
1.2.2 安全性指标 按照盐酸莫西沙星片说明书中记录的药品不良反应(adverse drug reaction,ADR)确定安全性指标,包括变态反应、神经系统反应、消化系统反应、Q-T间期延长、肌腱损伤、血糖异常等。
1.2.3 经济性指标
(1)使用数量:药品使用数量可标化为用药频度(defined daily doses,DDDs),该参数可反映药品在临床使用的频率,其值越大,表明该药在临床使用的频率越高[8]。DDDs=某时段某药品消耗总剂量/该药品限定日剂量(defined daily dose,DDD)。DDD主要根据药品说明书以及WHO推荐的2020版《药品的解剖学-治疗学-化学分类索引/限定日剂量》(Anatomical Therapeutic Chemical/Defined Daily Dose,ATC/DDD)[9]确定。
(2)销售金额:某时段内某药品的销售金额,单位以“元”计。
(3)日均费用:日均费用(defined daily dose cost,DDDc)指某药品平均单日消耗金额,该参数可反映该药的使用成本和可负担性,其值越大表示使用该药的患者经济负担越重,其值越小则表示该药的经济效应越大[10]。DDDc=某时段某药品销售金额/该药品DDDs值,单位以“元/d”计。
(4)价格比:中标药与原研药的价格比=中标药DDDc/原研药 DDDc。
(5)中标药替代率:该参数是衡量中标药替代政策实施效果的重要指标[10]。中标药替代率=中标药DDDs/该药(原研药+中标药)总DDDs×100%。
1.3 统计学方法
采用SPSS 25. 0软件对有效性和安全性数据进行统计分析;使用Excel 2019软件记录经济性数据。符合正态分布的计量资料以±s表示,采用t检验;偏态分布的计量资料以M(P25,P75)表示,采用秩和检验;分类数据采用例数或率表示,采用Pearson卡方检验或Fisher精确概率检验。采用多因素修正Poisson回归模型分析门诊CAP患者临床治疗失败的影响因素。检验水准α=0.05。
2 结果
2.1 2组患者一般资料
2021年1-12月,在我科门诊就诊的CAP患者共计5 578例,依据纳入与排除标准共得到符合要求的患者2 179例(筛选流程见图1),其中原研药组1 058例、中标药组1 121例。原研药组中合并慢性阻塞性肺疾病(24.39% vs. 14.63%,P<0.001)、有发热症状(27.50%vs. 23.19%,P=0.021)的患者比例显著高于中标药组,而2组患者的性别、年龄等其余人口学特征和临床特征基本一致,组间比较差异均无统计学意义(P>0.05),详见表1。
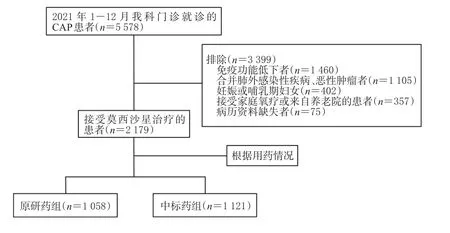
图1 研究对象的筛选流程
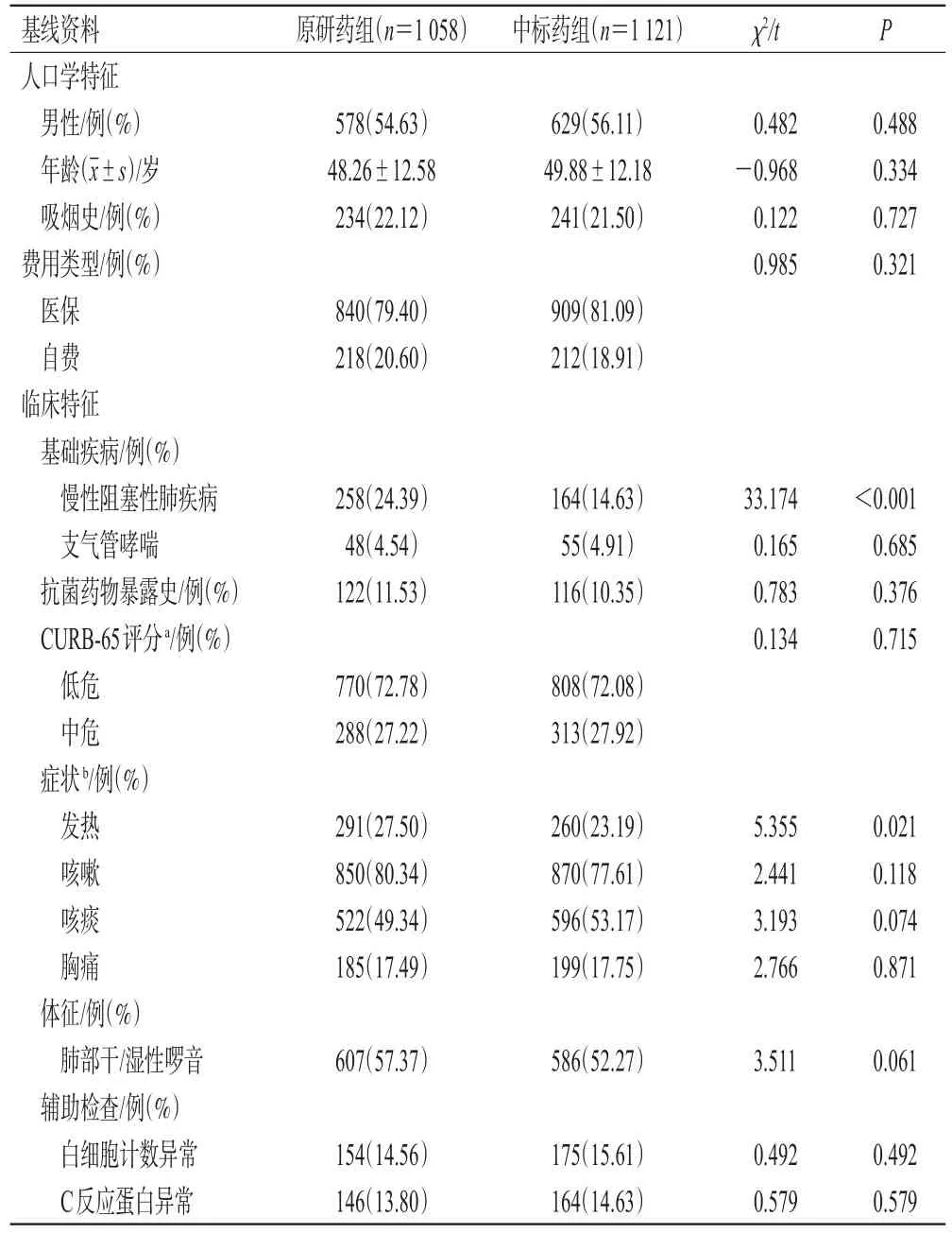
表1 2组患者人口学及临床特征基线资料比较
2.2 有效性比较结果
2 179例CAP患者均在我科门诊完成诊疗,共有1 838例患者临床治疗有效,其中原研药组906例、中标药组932例。原研药组患者的缓解时间显著短于中标药组(P<0.05),而2组患者的临床治疗有效率、用药疗程、再次就诊率比较差异均无统计学意义(P>0.05),详见表2。
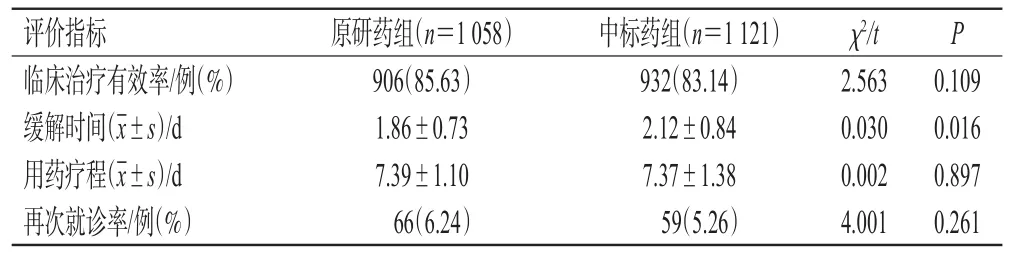
表2 2组患者的有效性指标比较
以临床治疗结局为因变量(0=失败,1=成功),药品来源、性别、年龄、吸烟、基础疾病、抗菌药物暴露、CURB-65评分、临床表现异常项目和辅助检查异常项目为自变量建立多因素修正Poisson回归模型。结果显示,与原研药相比,使用中标药不会增加CAP患者临床治疗失败风险[相对危险度(RR)=1.132,95%置信区间(CI)(0.883,1.542),P=0.327];相较于无抗菌药物暴露史患者,有抗菌药物暴露史患者的临床治疗失败风险将增加1.376倍(P=0.001);相较于临床表现异常项目<1项的患者,临床表现异常项目≥2项患者的临床治疗失败风险将增加0.386倍(P=0.010);相较于辅助检查异常项目<1项的患者,辅助检查异常项目≥2项患者的临床治疗失败风险将增加1.052倍(P=0.015);其余因素皆对患者临床治疗失败风险没有显著影响(P>0.05),详见表3。
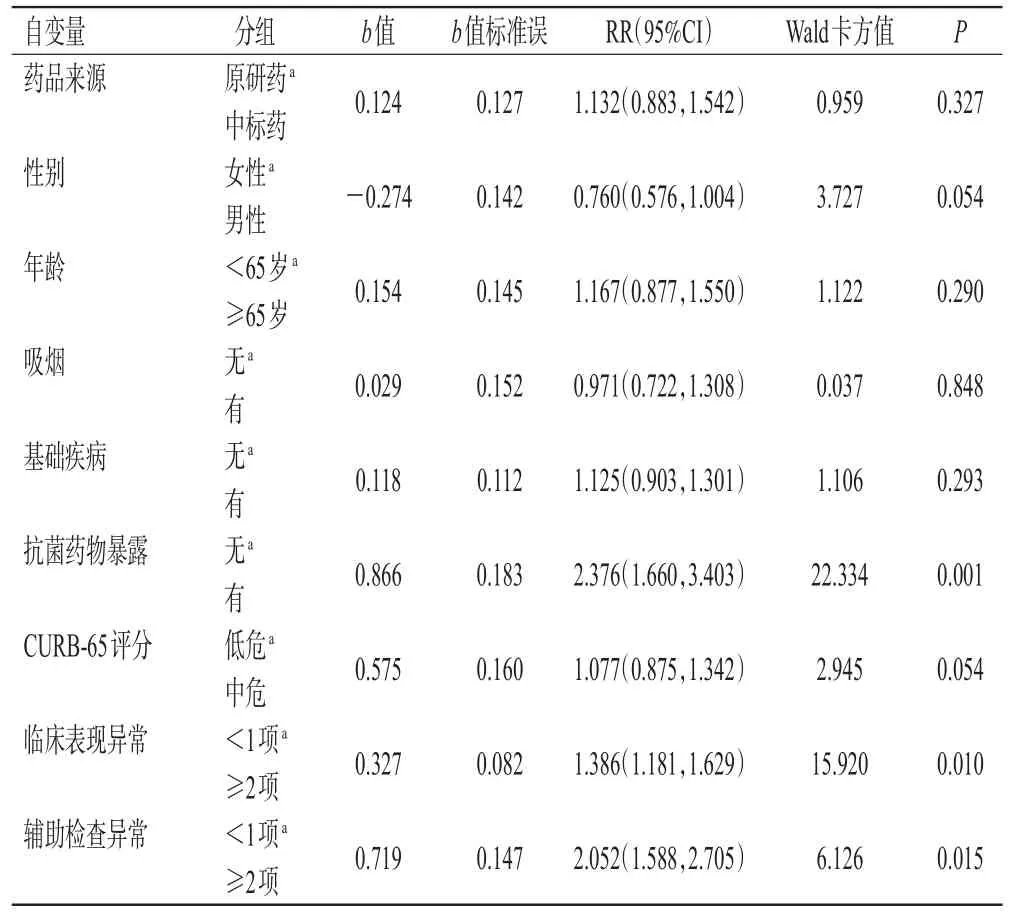
表3 临床治疗失败影响因素的Poisson回归模型分析结果
2.3 安全性比较结果
在治疗过程中,原研药组有25例患者发生ADR,中标药组有76例患者发生ADR,均以消化系统反应为主。原研药组患者总ADR(25例vs. 76例,P<0.001)、变态反应(3例vs. 18例,P=0.002)、消化系统反应(11例vs.30例,P=0.009)、血糖异常(5例vs. 17例,P=0.015)的发生率均显著低于中标药组,详见表4。
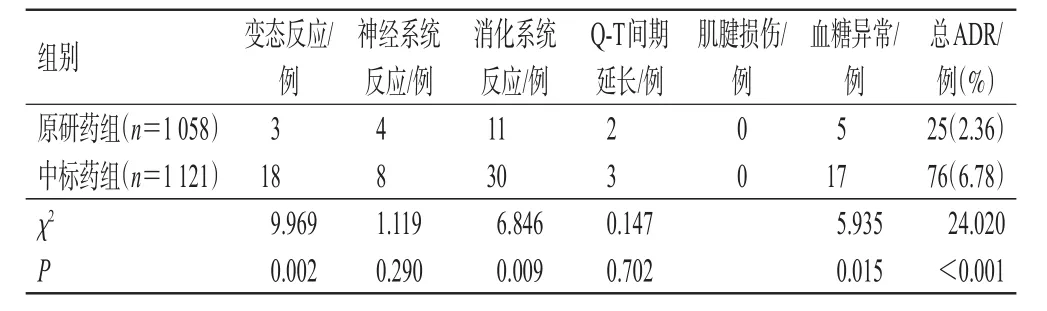
表4 2组患者ADR发生情况比较
2.4 经济性比较结果
实施集采后1年期间盐酸莫西沙星片的使用数量较实施集采前1年增加3 297.60 g,增幅35.98%;销售金额下降250 545.28元,降幅47.35%;DDDs增加8 244,增幅35.98%;中标药DDDc下降20.29元/d,降幅88.22%;中标药与原研药的价格比降至0.117,中标药替代率升至69.44%,详见表5。
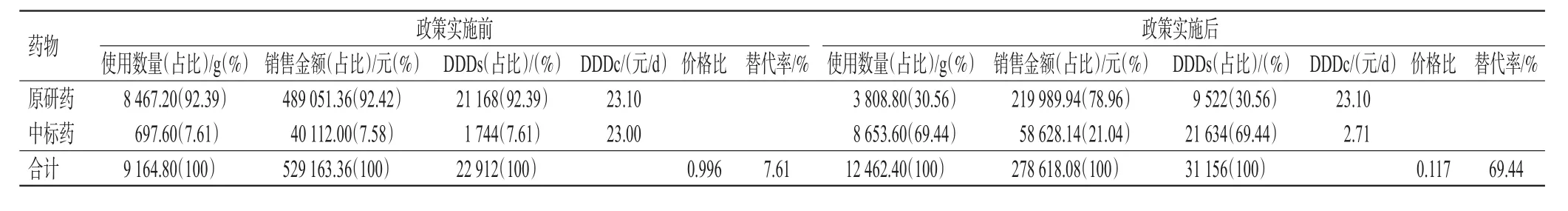
表5 2组药物的经济性指标比较
3 讨论
莫西沙星属于第四代喹诺酮类药物,其抗菌活性、用药安全性、药动学行为均较左氧氟沙星等同类药物更有优势[11]。莫西沙星的抗菌谱能够覆盖肺炎链球菌、流感嗜血杆菌、卡他莫拉菌、肺炎克雷伯菌以及非典型病原体等门诊CAP患者常见致病菌,口服生物利用度较高,ADR发生率相对较低,患者耐受性好、用药依从性佳。大规模的临床试验已经证实了莫西沙星治疗CAP的临床优势及用药安全性,其单药治疗合并急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)的重症CAP患者的效果与其联用β-内酰胺类药物的效果相当[12-15],是治疗CAP的经典药物。
有研究显示,在我国健康受试者空腹和餐后状态下,盐酸莫西沙星片国产制剂与原研制剂具有生物等效性且安全性良好[16]。一项纳入了85例住院CAP患者的研究对比了原研与仿制莫西沙星注射液的临床疗效和ADR发生情况,结果显示,2组患者的临床有效率接近(P=0.809),但仿制药组患者的变态反应和血糖异常的发生率均显著高于原研药组(P<0.05)[17]。本研究纳入的是门诊CAP患者,但取得了与之相似的研究结果:中标组患者的临床治疗有效率、用药疗程和再次就诊率与原研药组基本一致,但在缓解时间和用药安全性方面有明显差异,这可能与纳入患者的基础情况、国产制剂工艺的稳定性等因素有关。
集采中标药品为通过我国一致性评价的仿制药,拥有与原研药相当的药物疗效[16]。多因素修正Poisson回归模型进一步证实,门诊CAP患者使用中标盐酸莫西沙星片并没有增加临床治疗失败的风险,这一结果有利于提高医生和患者对集采药品的信任程度。本研究还发现,有抗生素暴露史、临床表现异常项或辅助检查异常项目≥2项均会增加门诊CAP患者临床治疗失败的风险。这是因为前期抗生素暴露增加了患者罹患多重耐药菌感染的风险[1,3],而多项临床表现和辅助检查异常提示患者病情在短期内难以改善或存在进行性加重的可能[18],导致临床治疗难度系数增大、治疗失败的风险提高。
原研盐酸莫西沙星片的价格较高,导致部分患者因经济原因而放弃治疗。张亮等[17]对住院CAP患者应用原研与仿制莫西沙星注射液治疗进行了成本-效果分析,结果显示,2组患者的治疗总成本比较差异有统计学意义(P<0.001),仿制药的成本-效果比低于原研药。本研究结果显示,集采后盐酸莫西沙星片的价格大幅度降低,中标药的DDDc低于原研药,中标药对原研药的价格比降至0.117,替代率升至69.44%,进一步凸显了仿制药的经济优势。但国内制药企业仍需不断提升仿制药的质量水平,以免弱化仿制药的价格优势[19]。
本研究样本量较大且评价指标较多,研究结果的可信度较高。但本研究依然存在一些不足之处:由于患者记忆偏差,临床疗效评价指标结果可能有所偏倚;研究的开展局限于某一家三级甲等综合医院,其结果尚需多中心研究予以进一步证实;此外,还需进一步探讨集采抗菌药物对医疗机构细菌耐药性的影响等。
综上所述,与原研药相比,中标盐酸莫西沙星片治疗门诊CAP的临床疗效可靠,且具有明显的价格优势,但不良反应发生率较高,尚需不断提高我国仿制药质量水平。
