FAAS法测定海带中微量元素的不确定度评定
2023-02-08刘兰英吕新李莹罗土炎上官亮李玥仁
刘兰英,吕新,李莹,罗土炎,上官亮,李玥仁*
1. 福建省农业科学院农业质量标准与检测技术研究所(福州 350003);
2. 福建省农产品质量安全重点实验室(福州 350003)
海带中含有丰富的膳食纤维、多糖、多酚等功能性物质,具有降血糖、降血脂、抗氧化、抗病毒及提高免疫力等多种药理活性[1-2]*,是一种经济价值很高的海藻养殖品种。同时海带还含有极丰富的微量元素,微量元素在维持生命及人体正常新陈代谢中发挥重要作用,其含量与海带的营养价值密切相关[3-4]*。因此,开展海带中微量元素的检测分析对于评估其营养价值具有重要意义。测量不确定度是表征合理地赋予被测量值分散性的非负参数[5]*,将测量不确定度引入海带微量元素的检测过程中,对于测量结果可信程度的评价很有必要。
现有方法主要是利用火焰原子吸收光谱法(FAAS)、电感耦合等离子体质谱法(ICP-MS)和电感耦合等离子体发射光谱法(ICP-OES)测定食品中微量元素的含量。其中,关于FAAS法测定食品中微量元素的不确定度评定主要集中在饮用水[6-7]*、粮食[8-9]*、酒类[10-11]*、奶粉[12-13]*等方面。如:赵立群等[9]*对小麦粉中锌的不确定度评定结果表明,测量不确定度主要来源于方法回收率,其次是校准曲线拟合和测量重复性;彭珍华等[10]*对葡萄酒中铁的不确定度评定结果表明,测量不确定度主要来源于标准工作溶液配制和校准曲线拟合;钟加成等[13]*对婴儿配方乳粉中锌的不确定度评定结果表明,测量不确定度主要来源于样品溶液中锌浓度的测定和测量重复性。然而在众多研究中,关于海带中微量元素测量不确定度的报道还比较欠缺。
试验以GB 5009.90—2016《食品安全国家标准 食品中铁的测定》和GB 5009.14—2017《食品安全国家标准 食品中锌的测定》为检测依据,采用FAAS法对海带中铁、锌2个微量元素进行测定,参照JJF1059.1—2012《测量不确定度评定与表示》和CNAS GL006:2019《化学分析中不确定度的评估指南》的要求和规定,对测量不确定度进行相应分析,以期为海带中微量元素含量检测的质量控制提供理论依据。
1 材料与方法
1.1 主要材料与试剂
海带样品(取自福州市连江县某海带养殖区)。
硝酸(优级纯,上海阿拉丁生化科技股份有限公司);铁、锌标准储备液(1 000 μg/mL:国家有色金属及电子材料分析测试中心)。
1.2 主要仪器与设备
AA-6880原子吸收光谱仪(日本岛津公司);G-400智能控温电加热器、TOPEX微波消解仪(上海屹尧仪器科技发展有限公司);AL204电子天平(梅特勒公司)。
1.3 样品前处理
将海带样品烘干、粉碎混合均匀后,称取0.3 g左右(精确至0.000 1 g)于微波消解内罐中。加入5.0 mL硝酸溶液,置于微波消解仪中进行消解,消解升温程序:120 ℃保持5 min,160 ℃保持10 min,190℃保持20 min。消解结束后冷却至室温,取出消解内罐,置于配套电加热器中赶酸至1.0 mL左右,冷却后将消解液转移至25 mL容量瓶中,定容至刻度,混匀备用。同时做试剂空白试验。
1.4 标准溶液配制
准确吸取适量铁、锌标准储备液(1 000 μg/mL),用1%硝酸溶液稀释配成质量浓度均为10 μg/mL的标准中间液;吸取适量此标准中间液,配成铁的质量浓度分别为0.0,0.05,0.1,0.2,0.4和0.6 μg/mL以及锌的质量浓度分别为0.0,0.1,0.2,0.4,0.8和1.0 μg/mL的标准系列工作液。
1.5 样品测定
仪器预热至稳定后,将铁、锌标准系列工作液按质量浓度由低到高的顺序分别注入火焰原子化器,测定其吸光度,得到标准曲线,再分别测定空白样液和样品溶液的吸光度,通过校准曲线得到消解液中铁、锌的质量浓度。
1.6 数学模型
海带样品中待测元素的数学模型见式(1)。

式中:X为试样中待测元素含量,mg/kg;ρ为试样溶液中待测元素的质量浓度减去空白溶液中待测元素的质量浓度,μg/mL;V为试样消化液定容体积,mL;f为试样稀释倍数;m为试样质量,g。
2 结果与分析
2.1 测量结果
对海带样品进行12次测定,测定结果如表1所示。

表1 海带样品中铁、锌的测定结果
2.2 测量不确定度来源识别
根据检测过程和数学模型,采用基本因果图分析测量不确定度的来源(图1)。海带中铁、锌的测量不确定度分量主要来源有样品质量(m)、样品消解液定容体积(V)、样品溶液质量浓度(ρ)、消化液稀释因子(f)、样品测量重复性(Rep)和方法回收率(Rec)。其中,测量重复性(Rep)包括样品测定过程中称量、定容等操作的重复性,为总试验的一个合成重复性分量。

图1 海带中铁、锌测量不确定度评定因果关系图
2.3 测量不确定度分量的量化
2.3.1 样品质量(m)引入的不确定度
样品称量过程产生的不确定度主要由天平校准和重复性2个分量组成,由于引入已确定的合成重复性,因此没有必要考虑称量的重复性。
试验样品称量所使用的天平为特种准确度等级,从校准证书上获得,测量范围在0~50 g时,天平的最大允许误差为±0.5 mg,该不确定度分量需计算2次(皮重1次、毛重1次)。假设服从均匀分布,取包含因子3,则样品称量过程产生的标准不确定度试验海带平均质量为m=0.304 5 g,即304.5 mg,则样品质量引入的相对标准不确定度urel(m)=0.408 2/304.5=0.001 34。
2.3.2 样品消解液定容体积(V)引入的不确定度
样品消解液定容过程产生的不确定度主要由容量瓶校准、温度效应和体积重复性3个分量组成,同样这里不考虑体积重复性。
2.3.2.1 容量瓶校准所产生的不确定度
试验海带样品消解后使用25 mL容量瓶定容,所用容量瓶经计量校准均为合格,依据JJG196—2006《常用玻璃量器》标准规定,25 mL容量瓶(A级)的容量允差为±0.03 mL。按照CNAS GL006:2019推荐,玻璃器皿假定为三角分布,取包含因子6,得到由容量瓶校准所产生的标准不确定度u1(V25)=
2.3.2.2 温度效应所产生的不确定度
试验使用的容量瓶校准温度为22.7 ℃,样品消解液定容时环境温度为25 ℃,液体的体积膨胀系数为2.1×10-4*℃-1*,则温度波动(2.3 ℃)产生的液体体积变化区间为±(25 mL×2.3 ℃×2.1×10-4*℃-1*)=±0.012 08 mL。假设服从均匀分布,得到由温度效应所产生的标准不确定度
将上述2个分量合成,得到样品消解液定容体积引入的标准不确定度u(V25)=u12*(V25)+u22*(V25)=其相对标准不确定度
2.3.3 样品溶液质量浓度(ρ)引入的不确定度
样品溶液质量浓度测定过程产生的不确定度主要由标准工作溶液配制、校准曲线拟合、检测仪器校准3个分量组成。
2.3.3.1 标准工作溶液配制所产生的不确定度urel(ρ1)
由标准物质证书查得,铁、锌标准贮备液的相对扩展不确定度均为0.7%(包含因子k=2),换算成相对标准不确定度urel(ρstock)=0.7%/2=0.003 5。标准溶液配制过程中,铁、锌元素使用到1 mL,5 mL移液器和50 mL容量瓶,分别进行不确定度分析。
依据JJG196—2006规定,50 mL容量瓶(A级)的容量允差为±0.05 mL,同2.3.2的计算,得出由50 mL容量瓶定容所产生的相对标准不确定度urel(V50)=0.000 494。从校准证书上获得,标称容量1 mL的移液器,在移取0.1,0.5和1.0 mL体积时的容量允差分别为±2.0%,±1.0%和±1.0%,因未给出移取0.25 mL体积的容量允差,故移取0.25 mL体积的容量允差取最大值±2.0%。标称容量5 mL的移液器,在移取0.5,2.5和5.0 mL体积时的容量允差分别为±1.0%,±0.5%和±0.6%,因未给出移取2.0,3.0和4.0 mL体积的容量允差,故移取2.0,3.0和4.0 mL体积的容量允差取最大值±1.0%。假设服从均匀分布,则各移液体积对应的相对标准不确定度为:
铁元素标准溶液配制过程中使用50 mL容量瓶6次,1 mL移液器分别移取0.25 mL体积1次、0.5 mL体积2次、1.0 mL体积1次,5 mL移液器分别移取2.0 mL、3.0 mL体积各1次,故铁元素标准溶液配制中所产生的相对标准不确定度为uFe,rel2*(ρ1)=urel2*(ρstock)+6×urel2*(V50)+urel2*(0.25)+2×urel2*(0.5)+urel2*(1.0)+urel2*(2.0)+urel2*(3.0)=0.017 712*。锌元素标准溶液配制过程中使用50 mL容量瓶6次,1 mL移液器分别移取0.5 mL体积2次、1.0 mL体积1次,5 mL移液器分别移取2.0、4.0、5.0 mL体积各1次,故锌元素标准溶液配制中所产生的相对标准不确定度为uZn,rel2*(ρ1)=urel2*(ρstock)+6×urel2*(V50)+2×urel2*(0.5)+urel2*(1.0)+urel2*(2.0)+urel2*(4.0)+urel2*(5.0)=0.013 862*。
2.3.3.2 校准曲线拟合所产生的不确定度urel(ρ2)
采用FAAS法测定海带中的铁、锌含量,分别对配制的6个标准系列工作液进行3次测定,得到相应吸光度,结果如表2所示。
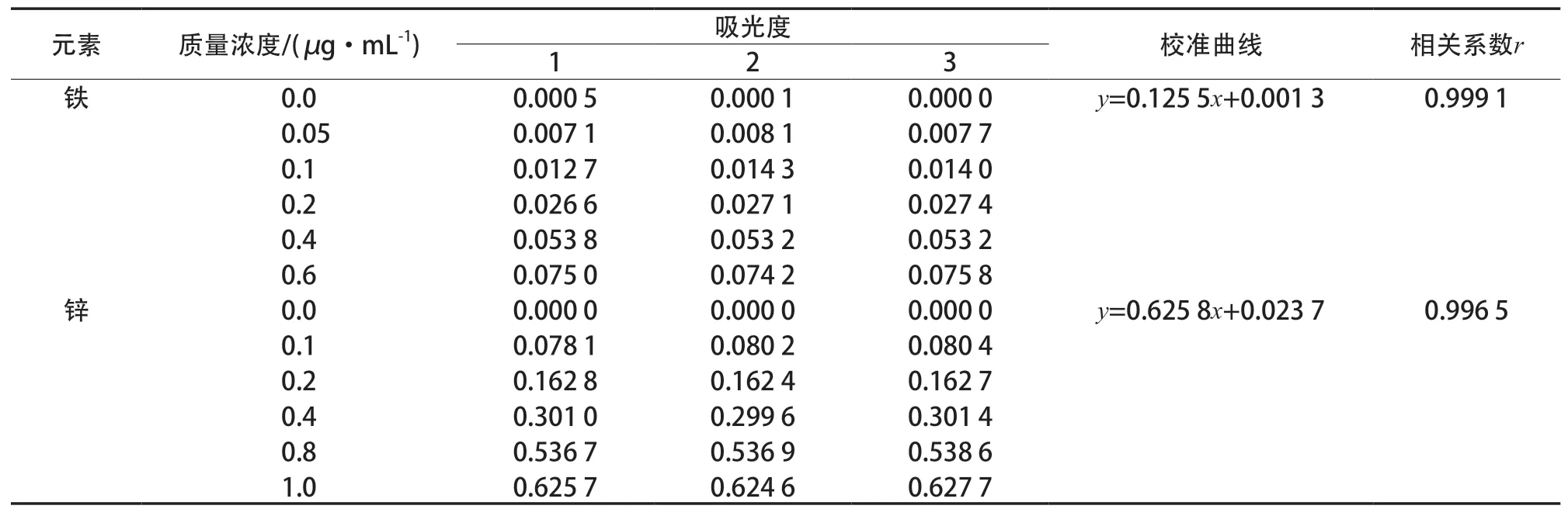
表2 标准系列工作溶液测定结果
对海带样品消解液进行12次测量后,由吸光度求得样品中铁、锌的平均质量浓度:ρFe=0.307 μg/mL;ρZn=0.194 μg/mL(表1),则此过程带来的标准不确定度为:

式中:SR为曲线的标准偏差;Yj为第i个校准溶液的第j次吸光度;Xi为拟合曲线第i个校准溶液的质量浓度,μg/mL;B1为曲线斜率;B0为曲线截距;n为测量校准溶液的次数,n=18;P为测量样品溶液的次数,P=12;为拟合曲线各校准点浓度的平均值(n次)。mL;锌元素SR=0.02046,?=0.417 μg/mL。
计算得到:铁元素SR=0.00131,=0.225 μg/
将各值代入u(ρ2)的计算中,得出由校准曲线拟合所产生的标准不确定度,分别为uFe(ρ2)=0.004 23 μg/mL,uZn(ρ2)=0.014 64 μg/mL。其相对标准不确定度为uFe,rel(ρ2)=0.013 78,uZn,rel(ρ2)=0.075 46。
2.3.3.3 仪器校准所产生的不确定度urel(ρ3)
根据火焰原子吸收光谱仪检定证书,其扩展不确定度为0.004 μg/mL(包含因子k=2),换算成标准不确定度urel(ρ3)=0.004/2=0.002 μg/mL,其相对标准不确定度分别为uFe,rel(ρ3)=0.006 51,uZn,rel(ρ3)=0.010 31。
合并3个分量,则样品溶液质量浓度测定过程引入的相对标准不确定度为urel(ρ)=计算得到uFe,rel(ρ)=0.023 36,uZn,rel(ρ3)=0.077 41。
2.3.4 方法回收率(Rec)引入的不确定度
对海带中铁、锌进行6次加标回收试验,加标量分别为75 μg和4.5 μg,6次回收试验的加标回收率结果见表3。根据贝塞尔公式,回收率试验的标准偏差为计算得到sFe(Rec)=3.00%、sZn(Rec)=5.39%。则方法回收率引入的标准不确定度为计算得到uFe(Rec)=1.23%,uZn(Rec)=2.20%,其相对标准不确定度为uFe,rel(Rec)=0.011 39,uZn,rel(Rec)=0.020 19。
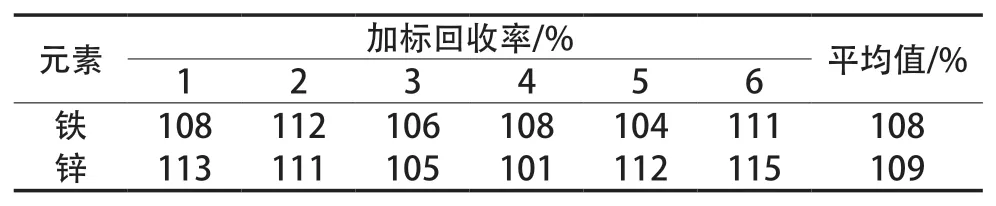
表3 海带样品加标回收测定结果
2.3.5 测量重复性(Rep)引入的不确定度
在相同条件下,对同一海带样品进行12次独立的重复测定(表1),同2.3.4的计算,得出重复性试验的标准偏差分别为sFe(Rep)=8.623 5 mg/kg,sZn(Rep)=0.409 0 mg/kg。则样品重复性测量引入的标准不确定度为uFe(Rep)=2.489 4 mg/kg,uZn(Rep)=0.118 1 mg/kg,其相对标准不确定度为uFe,rel(Rep)=0.009 88,uZn,rel(Rep)=0.007 43。
2.3.6 消化液稀释因子(f)引入的不确定度
试验海带测定过程中,因样品消化液中铁含量超出校准曲线的线性范围,故对消化液进行10倍稀释,用1 mL移液器移取1 mL测试液到10 mL容量瓶中,定容至刻度,则稀释因子带来的不确定度主要由稀释过程中容量瓶定容和使用移液器引起的不确定度分量组成。其中,移液器移取体积所产生的不确定度同2.3.3的计算,可知urel(1.0)=0.005 77。依据JJG196—2006规定,10 mL容量瓶(A级)的容量允差为±0.02 mL,同2.3.2的计算,得出由10 mL容量瓶定容所产生的相对标准不确定度urel(V10)=0.000 862,故铁元素由消化液稀释因子引入的相对标准不确定度uFe,rel2*(f)=urel2*(V10)+urel2*(1.0)=0.005 832*。
2.4 合成标准不确定度
综合各不确定度分量,试验海带中铁、锌含量测定的相对合成标准不确定度为计算得到铁元素ucrel(X)=0.028 47,锌元素ucrel(X)= 0.080 42。
海带经重复测定12次后,样品中各元素的平均含量分别为XFe=252 mg/kg,XZn=15.9 mg/kg(表1),其合成标准不确定度uc(X)=ucrel(X)×X,计算得到铁元素uc(X)=7.174 4 mg/kg,锌元素uc(X)=1.278 7 mg/kg。
2.5 扩展不确定度
依据CNAS GL006:2019推荐,取95%的置信水平,包含因子k=2,则扩展不确定度U=kuc(X),计算得到铁元素U=14 mg/kg,锌元素U=2.6 mg/kg。
2.6 各不确定度分量的相对贡献
从各分量的相对标准不确定度可知,影响海带中铁、锌含量检测结果不确定度的最大因素是样品溶液质量浓度,其次为方法回收率、测量重复性。相关研究在食用植物油微量元素的不确定度评定中也得到相似结果[14]*。与彭珍华等[10]*的研究结果相似,试验在样品溶液质量浓度测定过程中,又以标准溶液配制和校准曲线拟合产生的不确定度分量较大。
通过对比移液器在移取标准溶液时引入的不确定度发现,移液器在移取低体积溶液时,其产生的不确定相对更大些,这与所用移液器的体积误差有关,因此在配制标准工作溶液时,要特别加强各种规格移液器的计量检定,尽量移取较大体积的溶液,以减少此过程引入的不确定度。对于校准曲线的质量控制,可通过选择适当浓度梯度的工作曲线,尽可能使待测元素浓度靠近曲线的中间位置,从而减少由此引入的不确定度。此外,通过使用精密度更高的器具配制标准溶液、增加工作曲线各浓度点的测量次数也可在一定程度上降低不确定度的引入[15]*。为降低方法回收率带来的不确定度,在测量过程中须充分了解样品的特性,优化样品的前处理方法,消解液转移定容时少量多次清洗消解罐,尽可能彻底消解样品并减少待测元素的损失。测量重复性带来的不确定度主要受样品前处理和测量仪器的影响[16]*,在实际工作中可通过增加样品重复测定次数、定期对仪器进行维护保养和期间核查,提升仪器性能稳定性等进行控制。
3 结论
采用FAAS法测定海带中铁、锌的含量,并从样品质量、样品消解液定容体积、样品溶液质量浓度、方法回收率、测量重复性、消化液稀释因子等影响因素对测量结果的不确定度进行评定。结果表明:海带样品中铁含量252 mg/kg时,其扩展不确定度为14 mg/kg(k=2);锌含量15.9 mg/kg时,其扩展不确定度为2.6 mg/kg(k=2)。在各不确定度分量中,由样品溶液质量浓度引入的不确定度对测量结果影响最大,其次是方法回收率和测量重复性,而样品消解液定容体积引入的不确定度影响最小。在样品溶液质量浓度测定过程中,又以标准溶液配制和校准曲线拟合带来的不确定度贡献较大。因此,在海带微量元素检测过程中,要加强标准溶液配制的规范性和校准曲线的质量控制。
