儿童心脏移植的治疗进展与展望
2023-02-03朱家德吴敏
朱家德 吴敏
儿童心脏移植是合并难以通过常规手术或药物治疗的顽固性心力衰竭患者的标准治疗方式,儿童心脏移植受者为18岁以下儿童。目前,全球儿童心脏移植的开展愈发广泛[1-3],但国内的开展经验仍较为缺乏。儿童心脏移植的适应证选择、治疗策略以及治疗结果等方面,仍缺乏充足的循证医学证据。本文拟从儿童心脏移植的发展历史、治疗策略进展及预后方面进行综述。
1 儿童心脏移植的发展历史
第1例儿童心脏移植发生于1967年12月6日[1],人类首例成人心脏移植术后第3日,Kantrowitz医师在纽约布鲁克林为1例患有Ebstein畸形、难治性心力衰竭、曾因严重紫绀而进行主-肺动脉分流术的18 d新生儿进行了手术。受者于移植术后5 h因心力衰竭和难治性酸中毒死亡。该病例因术后过早死亡而被人们诟病为不成功的儿童心脏移植。然而该例手术的开展却也证明了儿童心脏移植技术上的可行性,从而为未来儿童心脏移植的开展创立了先河。Kirk等[1]对国际心肺移植学会(International Society for Heart and Lung Transplantation,ISHLT)数据库的最早期数据进行回顾性分析后发现,第1例真正意义上成功的儿童心脏移植可以追溯到1968年,该例患儿顺利度过围手术期,并在术后存活超过1年。
1984年10月26日,Bailey等[4]将1颗狒狒的心脏移植到1例患有左心发育不良综合征的新生婴儿身上,该婴儿移植术后存活了20 d,这唤起了人们对儿童异种心脏移植的强烈兴趣。然而,第1例新生儿的异种移植在此后10年中尚未进行第2次尝试,却掀开了心脏移植作为儿童终末期心力衰竭治疗手段的序幕。近10年来,儿童心脏移植的开展越来越广泛。据ISHLT注册报道,近10年全球儿童心脏移植数量已超过每年500例[5]。然而,国内儿童心脏移植开展仍较为缓慢,广东省心血管病研究所是国内开展儿童心脏移植例数最多的心脏移植中心之一,2018年1月至2022年6月共完成儿童心脏移植41例。
2 儿童心脏移植的手术适应证与时机
目前对于儿童心脏移植的手术适应证选择尚未形成共识[6]。儿童心脏移植目前不推荐作为任何儿童心脏畸形的首选治疗方式。一些特定的复杂先天性心脏病(先心病)患儿,如单心室矫治后合并心力衰竭[7],严重冠状动脉异常、瓣膜返流或心室功能不全者,可考虑移植或经姑息治疗过渡后移植。
美国心脏协会(American Heart Association,AHA)基于专家共识意见对心肌病或既往接受矫正的先心病患儿的心脏移植指征进行了初步总结:(1)心功能差、心输出量低,需要持续静脉使用正性肌力药物或机械循环支持;(2)使用洋地黄类、利尿药、血管紧张素转化酶抑制剂和β受体阻滞剂处理,但心室功能仍在进行性恶化;(3)恶性心律失常或心律失常引起的心脏骤停,对药物治疗、导管消融或植入式自动除颤器无反应;(4)与反应性肺动脉高压相关的限制性心肌病;(5)进行性左心源性肺动脉高压,可能妨碍以后的心脏移植;(6)常规药物治疗无效型心力衰竭所致的生长受限;(7)心力衰竭伴生活质量严重受累;(8)Fontan术后心功能持续恶化[7-8]。根据AHA青年心血管疾病委员会建议,合并以下情况的儿童患者禁止心脏移植:(1)心脏疾病与其他系统不可逆受损有关,考虑单纯心脏移植可能无效,可考虑多器官联合移植;(2)心力衰竭合并不可逆性肺动脉高压;(3)肺动脉、静脉发育严重不良患者。
部分儿童可能无法评估心功能和活动耐量水平,导致心脏移植手术指征难以确定。美国器官资源共享网络(United Network for Organ Sharing,UNOS)/器官获取与移植网络(Organ Procurement and Transplantation Network,OPTN)委员会于2014年6月制定了儿童心脏分配优先级标准,移植指征明确患儿的手术时机选择见表1[9],满足1A级分配等级的儿童患者需尽快进行移植治疗。值得注意的是,先心病患儿的移植时机相对提前,在血流动力学受损时就可能需接受移植治疗;而扩张性心肌病患儿,鉴于其等待供心期间较好的生存率结果[10],移植时机可稍靠后。

表1 儿童心脏分配优先级标准[9]Table 1 Priority criteria for heart allocation in children
3 儿童心脏移植的治疗策略
《中国儿童心脏移植操作规范》[11]及Barnes等[12]已详细描述了儿童心脏移植的手术操作过程。ABO血型不相容(ABO incompatible,ABOi)移植、应用儿童心室辅助装置(ventricular assist device,VAD)及体质量不匹配移植是儿童心脏移植领域近年来主要治疗进展,能减少等候时间、扩大供心匹配范围,从而减少因儿童供心缺乏带来的诸多问题。
3.1 ABO血型不相容心脏移植
人类在婴儿早期缺乏针对血型A、B抗原产生的天然抗体,这为ABOi移植的开展提供了可能。儿童心脏移植研究数据库显示,近年来ABOi心脏移植数量不断增加,2010年1月至2018年6月纳入研究队列的ABO血型信息完整的4 529例患儿中,ABOi心脏移植比例高达27.7%。而同时间段年龄<2岁的幼儿心脏移植受者中,该比例更是高达57.48%(1 172/2 039)[2]。
ABOi心脏移植策略可以有效缩短儿童受者等待时间与降低死亡风险[13]。其术后1年与5年生存率与血型相容型移植受者接近[2],术后1年排斥反应发生率与ABO血型相容组差异亦无统计学意义[13]。
鉴于ABOi心脏移植策略能显著缩短供心等待时间,且术后生存率及排斥反应发生率与血型相容型受者相当,其可用于可能需长时间等待供心或急需供心而短期内难以获得血型相容供心的患儿。2020年4月,笔者所在中心完成了中国历史上首例ABOi心脏移植,将1颗B型血供者心脏移植到了O型血患儿身上。次年11月,再次将1颗B型血供者心脏移植到了A型血患儿身上,至此已独家完成全国第1和第2例ABOi心脏移植。两例患儿平均年龄7个月(5个月6日,9个月18日),术后均恢复良好顺利出院。
3.2 心室辅助装置在儿童心脏移植中的应用
1990年第1例儿童VAD的成功植入,使1例患有终末期心力衰竭的儿童患者得以顺利接受心脏移植。这一里程碑事件使VAD作为移植前过渡支持(bridge to transplant,BTT)应用于儿童心脏移植成为可能。然而,目前应用的儿童VAD种类十分有限,主要包括体外植入的EXCOR(德国)系统及体内植入式的HeartWare HVAD系统(美国)、Infant Jarvik 2015系统(美国)。EXCOR为世界首例植入的儿童VAD(1990年),也是目前使用范围最广的儿童VAD[14-15]。HeartWare HVAD系统为一款磁水混动离心直流泵,主要应用于大体质量儿童的BTT治疗[16-17]。Infant Jarvik 2015系统的临床应用经验较缺乏,PumpKIN研究的开展及未来结果的披露,有望使其填补小体质量儿童VAD的市场空白[18]。笔者对上述3种VAD的主要特点总结如下(表2)。
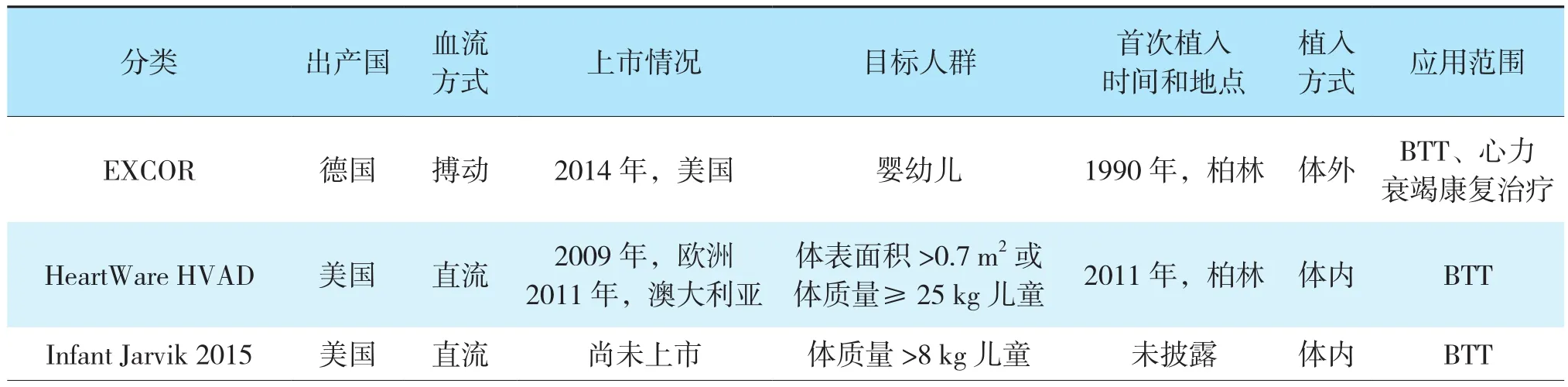
表2 3种VAD的主要特点比较Table 2 Comparison of main characteristics among three types of VAD
值得注意的是,与心肌病及心肌炎患儿相比,先心病患儿术前接受VAD比例更低,尽管先心病患儿相比于心肌病、心肌炎患儿预后更差[19]。先心病复杂的解剖结构和特殊的血流动力学过程可能是导致VAD植入率偏低的原因之一。
儿童辅助泵一般需根据体质量选择泵体大小,理想的循环流量为120~150 mL/kg(小体质量)和100 mL/kg(大体质量),以保证儿童生长所需心输出量[20-21]。目前儿童VAD植入指征尚无定论,一般作为BTT手段应用于临床[22-25]。对于体质量<2.5 kg、有严重神经系统并发症和抗凝禁忌证的极度早产儿,以及有一系列先天性疾病和染色体异常且预后不良的极度早产儿,不适宜接受VAD支持。未来随着2012年9月开始建立的儿童机械循环辅助支持(Pediatric Mechanically Assisted Circulatory Support,PediMACS)数据库结果披露,有望为儿童VAD植入的选择提供充分的循证医学证据。
大量临床证据表明,VAD作为BTT手段可延长供心等待时间、改善生存预后[22-26]。一项来自德国柏林的随访长达20年的研究结果提示,接受EXCOR过渡进行移植后的累积生存率分别为93.6%(30 d)、84.6%(1年 )、79.1%(5年 )、63.8%(10年 )和52.1%(20年)[14]。Edelson等[22]的研究进一步分析发现,与单纯心脏移植的同年龄或同紧急程度患者相比,使用VAD过渡进行移植的受者术后生存率差异无统计学意义。同时,相比于体外膜肺氧合作为BTT手段,VAD作为BTT手段的预后明显更佳[22]。
3.3 体质量不匹配儿童心脏移植
一般而言,供受者体质量匹配的参考范围为供受者体质量比为0.8~1.2。对于供受者体质量比>1.2或<0.8的情况,可视为供受者体质量不匹配。由于儿童生长过程中体质量变化大,供受者体质量不匹配的现象十分常见。目前,儿童患者大供心(供受者体质量比>1.2)的使用比例要高于小供心(供受者体质量比<0.8),超过50%儿童患者接受较大体质量供者提供的供心进行移植[27]。鉴于儿童心脏移植体质量不匹配现象十分常见,不断有研究探讨其对于儿童心脏移植预后的影响。2019年ISHLT儿童心脏移植报告对儿童供受者体质量比与术后生存率结果进行了专项研究[28]。14 000例儿童心脏移植患儿被纳入国际胸部器官移植注册数据库,多因素分析结果提示,小供心的使用可能会增加术后1年的死亡风险,此外,对于1~5岁接受移植的低龄受者而言,供受者体质量比>1.3的供心相对于供受者体质量比<0.7的供心会带来明显的生存获益。Patel等[27]对UNOS数据库中15 284例心脏移植受者进行研究时发现,对于术前合并肺高压的患者,小供心的使用可能会降低患者的生存预后。
总的来说,合并肺动脉高压及1~5岁的低龄患儿,需尽量避免使用小供心。而大供心则可作为小儿心脏移植的常规治疗策略之一。为方便大供心植入,可选择完全或部分打开受者纵膈胸膜以增加心腔体积。笔者所在中心2021年曾将1例60 kg供者的供心移植到8 kg的儿童受者身上,供受者体质量比高达7.5,该患儿术后恢复良好。
综上,ABOi型、体质量不匹配型心脏移植与VAD-BTT治疗策略,可以有效缓解儿童供心缺乏问题、改善儿童心力衰竭患者预后,是儿童心脏移植领域有力的补充治疗策略。
4 儿童心脏移植的预后
随着时代进步,儿童心脏移植的生存预后结果也逐年提高。Kirk等[1]对最早期儿童心脏移植历史进行回顾时发现,1967年至1982年儿童心脏移植受者的术后中位生存期仅为0.6年,术后存活超过1年的受者,其中位条件生存期也仅为4.6年。相比之下,根据2013年ISHLT儿童心脏移植报告结果[29],1982年至1989年接受手术的患儿中位生存期为9.5年,而接下来的10年该结果进一步提高至13.9年(2000年后的儿童中位生存期结果,由于随访尚未完全结束而无法统计)。1岁以内婴儿的术后生存结果提高最为显著,1982年至1989年中位生存期为10.8年,而到了1990年至1999年,该结果升高至18.3年。
与成人心脏移植类似,影响儿童心脏移植术后生存的危险因素包括术前体外膜肺氧合的使用、术前机械通气和肾功能不全[29]。此外,供心缺血时间、人类白细胞抗原阳性、免疫系统功能低下亦为术后早期死亡的危险因素[29]。
值得注意的是,先心病患儿心脏移植术后预后最差。Burstein等[19]对UNOS数据库和儿童健康信息系统(Pediatric Health Information System,PHIS)数据库中26个美国医疗中心的儿童心脏移植数据进行合并与分析时发现,无论先心病的复杂程度如何,其心脏移植术后的围手术期病死率、重症监护室入住时间、术后住院时间及住院期间花费,均明显高于心肌病或心肌炎的儿童受者[19]。先心病的具体类型也同样会影响术后结果。接受一期Fontan手术的患儿,移植术后病死率是其他先心病患儿的8倍[30]。此外,诊断为单心室的患儿其术后病死率是其他先心病患儿的12倍[19]。
5 结语与展望
儿童心脏移植能显著改善顽固性心力衰竭患儿的生存预后,近年来在国际上已得到迅速发展,然而,其开展仍面临着供心缺乏、适应证难以把握等问题。针对儿童供心缺乏问题,ABOi心脏移植及VAD的使用可能成为有效的解决策略,有望在未来逐渐应用。同时,儿童心脏移植适应证的选择较为复杂,仍需依赖于未来大样本量研究的开展。
