COPD合并VAP患者的微生物学特征及CPIS SOFA评分的预测价值
2023-02-01李世亮马冬梅相晓波
李世亮, 马冬梅, 相晓波
(北京中医药大学第三附属医院检验科, 北京 100029)
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)是一种具有持续气流受限特征的可以预防和治疗的慢性气道疾病,与有害气体、有害颗粒的异常炎症反应有关,致残率、病死率均较高,全球40岁以上发病率已高达9%~10%,已成为与高血压、糖尿病等量齐观的重大慢性病,患者主要表现为咳嗽、咳痰、气短、呼吸困难[1]。COPD患者往往需要进行呼吸机辅助通气,改善患者呼吸困难症状,但长期呼吸机通气也容易导致患者出现呼吸机相关肺炎(ventilator-associated pneumonia,VAP),影响其预后[2]。VAP是呼吸机通气过程中常见而严重的并发症之一,也是医院获得性肺炎最常见、最重要类型,具有地方性和流行病特点。有研究[3]报道,国外VAP 致死率约20%~70%,国内为51.6%,病死率极高。因此,需了解COPD合并VAP的危险因素及病原体,适当为患者制定合适的预防策略,但目前有关COPD合并VAP微生物学特征的报道较少。由于COPD合并VAP的患病率、病死率均较高,因而备受关注,如何改善该病的预后,降低患者病死率成为难题。近年来,临床肺部感染评分(clinical pulmonary infection score,CPIS)、序贯器官衰竭评分(sequential organ failure score,SOFA)评分得到多数学者的广泛关注,认为与COPD合并VAP的发展关系密切[4]。因此,本研究旨在探讨COPD合并VAP患者的微生物学特征及CPIS、SOFA评分的预测价值。现报道如下。
1 资料与方法
1.1一般资料:选取我院2019年11月至2021年11月收治的136例COPD患者,按照患者是否合并VAP将其分为研究组60例,男性35例,女性25例,年龄55~75(63.43±4.28)岁;参照组76例,男性33例,女性27例,年龄54~75(63.37±4.25)岁;另选同期50例健康体检者为对照组,男性25例,女性25例,年龄55~75(63.39±4.32)岁。本研究经医学伦理委员会批准。纳入标准:①参照《慢性阻塞性肺疾病的诊断》[5]中COPD及《呼吸机相关性肺炎诊断,预防和治疗指南(2013)》[6]中VAP的诊断标准;②呼吸机通气>48h;③患者知晓并同意本研究。排除标准:①存在支气管、社区获得性肺炎及免疫缺陷者;②住院48h后转院、存在认证、意识障碍者;③存在恶性肿瘤、信息资料不完整者。
1.2方法:记录患者基线特征,将诊断为VAP的患者进行气管内抽吸获取标本,通过革兰染色涂片镜检,对标本进行细菌培养,标本合格为白细胞≥10×109L-1,严格根据《全国临床检验操作规程》[7]进行细菌培养,药敏结果根据美国国家临床实验室标准委员会对药敏实验的相关规定判定。CPIS评分[8]:包括体温、白细胞计数、气管分泌物、氧合情况、X线胸片、肺部浸润影的进展情况、气管吸取物培养。12h平均体温36℃~38℃为0分,38℃~39℃为1分,>39℃、<36℃为2分;白细胞计数(4~11)×109L-1为0分,(11~17)×109L-1为1分,<4×109L-1、>17×109L-1为2分;24h吸出气管分泌物性状数量,无痰、少许为0分,中量~大量,非脓性为1分,中量~大量,脓性为2分;氧合情况,气体交换指数>33kPa为0分,<33kPa为2分;X线胸片无浸润影为0分,斑片状为1分,融合片状为2分;齐观吸取物培养无致病菌生长为0分,有致病菌生长为1分,两次培养到同一种细菌、革兰染色与培养一致为2分;总分12分,评分越高,病死危险性越高、病情越重,评分越低,病情缓解。SOFA评分,包括呼吸、血液、肝脏、循环、神经、肾脏等系统,呼吸系统:动脉血氧分压与吸入气氧浓度比值>400mmHg为0分,≤400mmHg为1分,≤300mmHg为2分,≤200mmHg为3分,≤100mmHg为4分;血液系统:血小板>150×109L-1为0分,≤150×109L-1为1分,≤100×109L-1为2分,≤50×109L-1为3分,≤20×109L-1为4分;肝脏系统:平均动脉压≥70mmHg为0分,<70mmHg为1分,多巴胺≤5μg·kg-1·min-1为2分,多巴胺>5μg/ (kg·min),肾上腺素≤0.1μg·kg-1·min-1、去甲肾上腺素≤0.1μg·kg-1·min-1为3分,多巴胺>5μg·kg-1·min-1,肾上腺素>0.1μg·kg-1·min-1、去甲肾上腺素>0.1μg·kg-1·min-1为4分;神经系统:格拉斯哥昏迷评分15分为0分,13~14分为1分,10~12分为2分,6~9分为3分,<6分为4分;肾脏系统:肌酐<106μmoL/L为0分,≤176μmoL/L为1分,≤308μmoL/L为2分,≤442μmoL/L、尿量≤500mL/d为3分,肌酐>442μmoL/L、尿量≤200mL/d为4分,总分16分,评分越高,预后越差。
1.3观察指标
1.3.1比较3组基线特征及CPIS、SOFA评分,患者基线资料包括性别、年龄、体质量、COPD病程、吸烟史、高血压、糖尿病、高血脂、肺结核、慢性肾病、因COPD多次住院、呼吸衰竭、3个月内使用过抗生素等。
1.3.2分析COPD合并VAP的Logistic回归分析,将基线特征中存在差异的因素及CPIS、SOFA评分纳入Logistic回归分析。
1.3.3与VAP相关病原体肺炎克雷伯菌、铜绿假单胞菌、鲍曼不动杆菌对常用抗生素的耐药性分析
1.3.4比较不同预后患者CPIS、SOFA评分,根据入组后1个月内死亡者记为预后不良组,存活者记为预后良好组。
1.3.5COPD合并VAP预后不良的Logistic回归分析。
1.3.6CPIS、SOFA及联合评分对COPD合并VAP预后的预测价值分析并绘制ROC曲线。
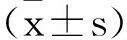
2 结 果
2.13组基线特征及CPIS、SOFA评分比较:研究组有糖尿病、肺结核、因COPD多次住院、3个月内使用过抗生素占比、CPIS、SOFA评分高于参照组,差异具有统计学意义CPIS、SOFA评分高于参照组(P<0.05), 见表1。

表1 3组基线特征及CPIS SOFA评分比较
2.2COPD合并VAP的Logistic回归分析:有糖尿病、肺结核,因COPD多次住院、3个月内使用过抗生素、CPIS、SOFA评分升高是COPD合并VAP的危险因素(P<0.05),见表2。

表2 COPD合并VAP的Logistic回归分析
2.3VAP相关病原体肺炎克雷伯菌、铜绿假单胞菌、鲍曼不动杆菌对常用抗生素的耐药性分析与VAP相关病原体耐药性分析:在60例COPD合并VAP患者中,微生物肺炎克雷伯菌感染16例,共24株病原菌、铜绿假单胞菌感染22例,共50株病原菌、鲍曼不动杆菌感染22例,共38例病原菌,肺炎克雷伯菌、铜绿假单胞菌、鲍曼不动杆菌3种微生物病原菌对亚胺培南、亚胺培南的耐药率低于<10%,耐药率低。 见表3。

表3 VAP相关病原体肺炎克雷伯菌铜绿假单胞菌鲍曼不动杆菌对常用抗生素的耐药性分析与VAP相关病原体耐药性分析
2.4不同预后患者CPIS、SOFA评分比较:在60例COPD合并VAP中,预后良好38例,预后不良22例。预后不良组CPIS、SOFA评分显著高于预后良好组(P<0.05),见表4。

表4 不同预后患者CPIS SOFA评分比较(分,
2.5COPD合并VAP预后不良的Logistic回归分析:CPIS、SOFA评分是COPD合并VAP预后不良的危险因素(P<0.05),见表5。

表5 COPD合并VAP预后不良的Logistic回归分析
2.6CPIS、SOFA及联合评分对COPD合并VAP预后的预测价值分析:CPIS联合SOFA评分预测COPD合并VAP预后的AUC高于CPIS、SOFA评分AUC(P<0.05),见表6、图1。

表6 CPIS SOFA及联合评分对COPD合并VAP预后的预测价值分析

图1 CPIS、SOFA评分预测COPD合并VAP预后的ROC曲线
3 讨 论
COPD通常由于吸烟、生物燃料等吸入导致肺功能损伤的属破坏性肺部疾病,可削弱患者呼吸功能,目前尚未研制出可以阻碍其进展和发病率的药物,患者需呼吸机氧疗,能缓解患者呼吸困难症状同时也但容易引起VAP。针对VAP临床虽提出了预防指南,但仍有大量患者患病增加病死率[8]。因此,分析COPD患者合并VAP的危险因素可能有利于患者危险分层和预后。
本研究结果发现,有糖尿病、肺结核,因COPD多次住院、3个月内使用过抗生素、CPIS、SOFA评分升高是COPD合并VAP的危险因素,糖尿病常引起患者免疫力下降、肺功能受损,对抗菌药物治疗反应较差,相比正常血糖患者,糖尿病患者获得肺部感染的机率较高,有文献[9]表示,糖尿病患者发生VAP的风险是正常血糖患者的1.2倍。;杨海龙等[10]研究表示,糖尿病是增加VAP患者死亡的重要因素,影响VAP患者病情转归。肺结核属慢性呼吸道传染病,可破坏患者免疫力、呼吸道黏膜结构,病情迁延不愈容易引起肺组织损害发生肺部感染。李燕平等[11]研究表示,肺结核患者发生VAP出现呼吸衰竭风险高于未发生肺结核患者。COPD是一个种反复发作、迁延不愈的疾病,因此COPD患者可短时间内多次住院治疗,而反复机械通气可增加VAP发生风险。静脉抗生素是治疗VAP的基石,但临床上需避免无效治疗,不恰当的抗生素应用可提高病死率,广谱抗生素的应用可诱导耐药,因此,故在进行VAP抗生素用药应用时,需询问患者3个月内有无使用过抗生素使用史,避免患者产生耐药性。Tsakiridou等[12]研究表示,COPD患者存在糖尿病、先前使用过抗生素是VAP的危险因素,与本研究结果一致。CPIS评分是一项将临床、影像学、微生物学综合来评估患者感染严重程度,预测和、调整患者抗生素使用,减少不必要的抗生素暴露的方法,SOFA评分则测定主要器官功能损害程度对患者进行预后判断的评分系统,在危重患者中应用较广,两者评分升高提示患者预后不良,病情严重,因此,对于COPD患者CPIS、SOFA评分给予关注,评分升高及时采取治疗措施,降低VAP发生。本研究中,60例COPD合并VAP患者微生物肺炎克雷伯菌16例、铜绿假单胞菌22例、鲍曼不动杆菌22例,3种微生物病原菌对亚胺培南、亚胺培南的耐药率低于10%,耐药率低,但对多种抗生素药物出现耐药性,COPD合并VAP患者年龄偏大,基础疾病较多,免疫力低下,病原菌对抗生素敏感性随大量使用广谱抗生素而降低,患者在治疗中上期使用抗生素治疗,易发生菌群紊乱,产生耐药性。吕培瑾等[13]研究表示,VAP抗菌治疗应覆盖具有多重耐药性的革兰阴性杆菌,鲍曼不动杆菌最常见,铜绿假单胞菌检出率较低,而本研究中铜绿假单胞菌、鲍曼不动杆菌检出相同,可能与医院用药习惯、患者病情、医务人员水平存在差异有关。在COPD合并VAP患者的治疗中,应按照药敏结果选择合理抗生素治疗。
COPD合并VAP致死率较高,本研究在60例COPD合并VAP中发现,预后不良22例,预后不良组CPIS、SOFA评分显著高于预后良好组,是COPD合并VAP预后不良的危险因素,CPIS、SOFA评分越高,患者病情越严重,预后越差,但两者单独预测COPD合并VAP预后的AUC、特异度低于联合预测,提示CPIS、SOFA评分联合预测可作为COPD合并VAP预后预测指标。谢柏梅等[14]研究发现,COPD合并VAP患者预后死亡组CPIS评分高于存活组患者,以6分为截断值,AUC为0.715,发现该评分在VAP患者预后中存在一定价值,但联合其他指标预测可确保特异度、敏感度,协助预后评估。张春玲等[15]研究表示,SOFA评分在重症肺炎预后不良患者中评分高于预后良好组,与本研究相符,预测预后AUC为0.774,联合其他指标有助于判断患者预后,降低患者病死率。郑娜敏等[16]研究认为,SOFA评分预测VAP患者预后AUC为0.649,结果较本研究低,原因可能与本研究样本量较小、合并COPD,在研究对象上存在差异,导致结果不一致;CPIS、SOFA评分联合评估COPD合并VAP患者预后不良的价值优于单项评估预测。但由于本研究样本量较小,对COPD合并VAP患者未进行实验室检查分析,CPIS、SOFA评分影响患者预后的机制未进行详细分析,观察时间较短,结论难免存在偏倚,需临床多方面、多数据的进一步研究。
综上所述,CPIS、SOFA评分是COPD合并VAP和预后不良的危险因素,联合预测对患者预后具有一定价值,肺炎克雷伯菌、铜绿假单胞菌、鲍曼不动杆菌是COPD合并VAP常见病原体,应根据药敏结果选择治疗药物,CPIS、SOFA评分操作简单,联合预测COPD合并VAP预后具有一定价值,值得推广。
