一款国产疫苗宣布免疫原性优于mRNA疫苗
2023-01-25彭丹妮
彭丹妮
中国多地正经历或已度过新冠感染的高峰。2022年12月22日,公共卫生与流行病学专家、中国疾控中心流行病学前首席科学家曾光在一场会议中强调,“(接种新冠疫苗)第四针一定要变换疫苗。”
随着新冠病毒感染回归“乙类乙管”,不管是从12月26日国务院联防联控机制发布的《重点人群、重点机构、重点场所新型冠状病毒感染“乙类乙管”防控指引》,还是从既往其他乙类传染病的管理经验来看,具有更好保护力、更加可及性的疫苗,势必将成为疫情防控的冲要之地。
国内多数人是通过接种灭活疫苗完成基础免疫的,随着新冠病毒的不断变异,亟待接种更有效的加强针。越来越多的国产新冠疫苗正在加速其上市的步伐,这些公司推出的疫苗涵盖了多种技术路线——从重组蛋白疫苗、腺病毒载体疫苗到mRNA疫苗等,为后续的加强免疫提供了更多的选择。截至目前,国内已有13款新冠疫苗产品获批上市,14款处于临床三期,其中多款产品为近期获批紧急使用的品种。
其中不乏可以为目前的新冠疫情免疫水平带来突破性改善的解决方案。比如创新型疫苗公司瑞科生物的新佐剂重组蛋白新冠疫苗ReCOV,其最新出炉的数据就显示,在以灭活疫苗为基础免疫的人群中,针对BA.2、BA.5、BF.7等变异株,序贯ReCOV作为加强针诱导的中和抗体滴度,显著优于序贯辉瑞mRNA疫苗作为加强针所诱导的中和抗体滴度。
越来越多公卫专家指出,新冠病毒很可能与人类社会长期共存。届时,正如全球疫苗免疫联盟(GAVI)所指出的,新一代的新冠疫苗和加强针可能会像流感疫苗一样,需要针对流行毒株定期注射。随着更多新冠疫苗推向市场,一位疫苗科学家告诉《中国新闻周刊》,接下来就是“长江后浪推前浪”了。
2022年12月14日,瑞科生物发布了ReCOV与辉瑞mRNA疫苗头对头的数据。这是一项在菲律宾开展的II期序贯加强临床试验,共入组受试者600例,所有受试者均完成2剂灭活疫苗基础免疫。按照随机分组方案,分别采用ReCOV疫苗和辉瑞mRNA疫苗进行加强接种对照,以比较两种疫苗作为加强剂的免疫原性和安全性。
序贯接种,又称异源接种,即采用和基础免疫及第一针加强免疫不同类型的疫苗接种。已经有许多文献指出,异源接种在临床试验结果上效果更好。
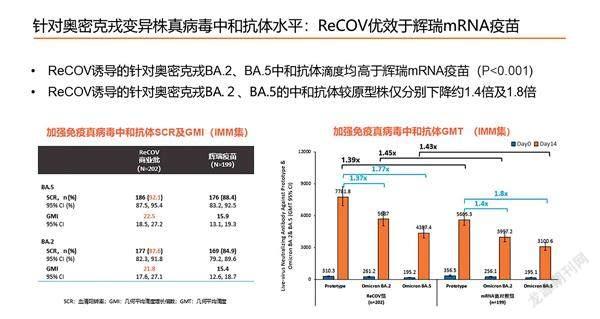
研究结果显示,在针对原型株、奥密克戎变异株BA.2、BA.5和BF.7的试验中,ReCOV疫苗诱导的中和抗体水平均优于mRNA疫苗。以BA.5的数据来看,接种14天时,ReCOV组、辉瑞mRNA疫苗组中和抗体的阳转率分别为92.1%及88.4%,中和抗体几何平均滴度GMT分别为4387.4及3100.6,ReCOV组均高于辉瑞mRNA疫苗组,且安全性良好。
中和抗体是指在病原体感染过程中,可以阻止病原体与宿主细胞表面受体相互结合、保护人不被感染的抗体,因此中和抗体滴度是评价新冠疫苗保护效力的关键指标。除了看中和抗体的绝对数,上海市公共卫生临床中心新发与再现传染病研究所所长徐建青曾告诉《中国新闻周刊》,还要看GMT的相对指标,他认为,一款有效的新冠疫苗,注射疫苗前后对比,中和抗体滴度至少提升4倍以上。在这方面,ReCOV组诱导的中和抗体较接种加强针前升高22.5倍,而mRNA疫苗的这一指标是15.9倍。
一位疫苗科学家在接受《中国新闻周刊》采访时表示,现在国内新批准和研发的几款重组蛋白疫苗,都使用了新型佐剂,在免疫原性方面比國内第一批疫苗更出色,甚至优于mRNA疫苗;更值得注意的是,这些疫苗的安全性比mRNA疫苗更好,因此对疫情防控很有意义。

瑞科新冠疫苗ReCOV产业化生产基地。
除此以外,mRNA疫苗的储存、运输条件极为苛刻,以辉瑞和BioNTech研发的mRNA疫苗为例,从装瓶到为患者接种前一刻,都必须在-70℃的低温条件下保存,大规模接种将极大增加物流等方面的成本,严重影响可及性。ReCOV则可在室温储存运输,无疑将更利于在全社会范围内大规模使用,而不会造成额外的经济负担。
2011年,在中国疾控中心工作了10年的研究员刘勇从该机构离职,并于次年创立了瑞科生物。之所以辞职“下海”,一个很重要的原因是,在与美国同行频繁的交流中,他看到,美国的疫苗行业非常强大,不光有顶尖的研发能力,而且一款疫苗从实验室走向产业界的路径也非常顺畅。反观国内疫苗工业领域仍有很大提升空间。
ReCOV疫苗的最新研究数据出来时,刘勇告诉《中国新闻周刊》,他感到结果还是有点超出预期,“在设计阶段,我们就觉得这款产品是有长期竞争力的,但是直到临床试验数据,尤其是头对头的对比数据出来之后,就能够很客观地下一个结论了。”
2020年初,当新冠疫情刚刚暴发时,尽管全球已经有很多疫苗厂商和研究机构开启了疫苗研发的竞赛,刘勇的团队并未立刻参与。
过去有一些病毒,只是在人类当中造成局部的传播然后就很快消失了,就像SARS病毒。不过,2020年5月份,当新冠在全球蔓延、呈现大流行趋势的时候,刘勇判断:作为一种RNA病毒,新冠与人类长期共存将成为必然,它将会进化、变异,在与免疫系统的斗争中寻找生存空间。
这种情况下,该公司的新冠疫苗立项时,刘勇希望,比起研发的速度,这款疫苗更重要的目标是比质量,“在全球疫苗竞争的背景下,我们希望研发的是一款长期使用的、具有国际竞争力的疫苗。”
疫苗设计上,团队初步筛选了至少28种初始方案。这些方案截取了新冠病毒的不同片段、不同抗原靶点进行组合实验,并在不同的动物模型中开展试验,最后“优中选优”,定下来的抗原蛋白是一种NTD-RBD-foldon三聚体的设计。该蛋白由CHO细胞高效表达,可以形成与新冠病毒S蛋白高度相似的结构,且由于具有双组分的序列考虑,纳入了更多进化方向上更为保守的抗原片段,因此针对包括BA.5在内的新冠病毒不同变异株,均有激发较高免疫保护的潜力。
刘勇介绍,这一经优化的抗原结构有很多优势,不仅在免疫原性上是所有备选方案中最强的,而且产量也是最高的。因为它基本没有多余的、免疫功能不大的病毒蛋白片段,这一结构也意味着蛋白比较稳定、容易生产。
要充分发挥和放大一款疫苗的免疫原性,佐剂的加持也非常重要。佐剂是在疫苗中帮助提高免疫应答水平的一类物质,可以在很大程度上决定产品的性能。刘勇介绍,佐剂被比作疫苗的“芯片”。目前,全球大多数疫苗企业都不具备新型佐剂的自主研发能力。从葛兰素史克(GSK)等极少数国外公司购买佐剂,是多数疫苗厂商唯一的解决方案。然而,这不仅意味着高价、断供等风险,更重要的是,无法采用新型佐剂开发更多强效的疫苗。
这方面,瑞科生物恰恰可以发挥其多年积累的优势。从刘勇进入疫苗领域以来,他一直在关注佐剂问题;瑞科生物成立以后,公司也有7年时间集中投入到佐剂的研发当中,如今,瑞科生物在佐剂领域已跻身全球领先。刘勇介绍,瑞科生物目前的新型佐剂平台具备“系统性”和“持续创新”两大显著特点。
系统性是指世界范围内,现有5种新型佐剂已应用于人用疫苗并获得FDA批准,瑞科生物均已开发出对标的佐剂品种。“这种系统性的新型佐剂研发,让我们再开发新型疫苗时有更多选择,是我们疫苗研发的工具箱和武器库。”刘勇表示。“持续创新”是指在已获批的新型佐剂基础上,公司还有10多款新一代佐剂,有望实现疫苗免疫原性与安全性方面的进一步提升。
基于强大的佐剂工具箱,瑞科生物在恒河猴模型中对比了多种新型佐剂和传统的铝佐剂,并筛选了佐剂BFA03,用于ReCOV新冠疫苗。BFA03对标GSK的AS03佐剂,后者已用于针对甲型大流感流行的疫苗。BFA03佐剂已经有了在上亿人中使用的安全性记录,其在产生中和抗体速度、滴度方面都有不错的表现。
在ReCOV疫苗的研发中,瑞科几乎是最大地发挥了它的几大技术平台能力。刘勇指出,瑞科生物综合运用新型佐剂、蛋白工程平台等技术平台,而且几个平台间的协同做得比较好。“即便是放到现在来看,这款两年多以前设计出来的疫苗,依然很有竞争力。”
中国疾控中心病毒病所所长许文波近来指出,2022年12月1日以来的奥密克戎基因组测序提示,目前全国检出9个奥密克戎亚型毒株正在流行,其中,BA.5.2和BF.7是占全国流行的绝对优势,占约80%。
尽管ReCOV的抗原是基于原始毒株,但是,其靶点设计、新型佐剂的应用,却保证了它对于当下流行的突变株也有很好的免疫原性。ReCOV组针对奥密克戎变异株BA.5中和抗体滴度,较原型株仅下降1.77倍。而12月23日,瑞科发布的最新数据显示,针对BF.7变异株,ReCOV的中和抗体滴度较原型株仅下降2.5倍。

头对头的比对数据来看,面对BF.7突变株时,ReCOV的表现依然优于辉瑞疫苗。具体来说,ReCOV及辉瑞mRNA疫苗组诱导的中和抗体滴度值分别为6549.1和4529.6;与此同时,ReCOV组诱导的中和抗体较基线升高30.8倍,高于辉瑞mRNA疫苗的22.7倍。
“第一版疫苗设计极端重要。”刘勇强调,一款疫苗的基本性能,其实是由第一版设计所决定的,后面的升级很难突破它原来的整体框架,想去进行性能上的质的提升其实是不太容易的。因此,ReCOV的表现使得其后续的迭代更加便捷、快速。
截至2022年12月25日,牛津大学Our World in Data数据库统计,全球累计报告接种新冠疫苗130亿剂次,接种率68.84%。在国内,根据2022年12月27日國务院联防联控机制发布会的介绍,全国目前累计接种新冠疫苗超过34亿剂次,疫苗接种覆盖人数和全程接种人数分别占全国总人口的92%以上和90%以上。
然而,作为防疫的关键武器,在中国,专家们指出,许多人距离接种最后一针疫苗已经过去了很久,在疫苗、治疗等免疫压力下,为了逃避免疫,新冠病毒也从未停止变异。
中国疾控中心病毒病所所长许文波在12月20日的发布会上谈到,奥密克戎从2021年11月份出现以来,截至到2022年12月18日,已经在全球从BA.1到BA.5这五个分支演变出709个亚分支。
2022年12月17日,在中美临床微生物学与感染病学高端论坛上,与会专家一致认为,由于新冠病毒的不断变异,其可以对人群重复感染。在免疫压力下,新冠病毒毒力会不断下降,最终可能与流感病毒类似。目前国内人群整体的免疫处于洼地,需要进行新冠疫苗的第二剂次加强免疫接种。
未来,全球对新冠疫苗的需求可能将会是长期的。刘勇表示,现在全球接种率已比较高了,基础免疫这一阶段的任务基本完成。然而,接下来人类面临的是一个依然严峻、甚至愈发严峻的局面:人类与病毒间将会持续斗争。未来人们需要定期接种新冠疫苗加强针,有点类似于流感疫苗,研发公司需要跟踪、预测病毒的变异趋势,及时地对疫苗进行升级。
2022年12月13日,国务院联防联控机制下发《新冠病毒疫苗第二剂次加强免疫接种实施方案》,文件指出,现阶段,可在第一剂次加强免疫接种基础上,在感染高风险人群、60岁以上老年人群、具有较严重基础性疾病人群和免疫力低下人群中开展第二剂次加强免疫接种。

刘勇博士 (瑞科生物创始人、董事长)。
在加强针的选择方面,前述方案指出,所有批准附条件上市或紧急使用的疫苗均可用于第二剂次加强免疫。在接种方式上,优先考虑序贯加强免疫接种,或采用含奥密克戎毒株或对奥密克戎毒株具有良好交叉免疫的疫苗进行第二剂次加强免疫接种。
仅在12月初的几天,就有四家公司的新冠疫苗被纳入紧急使用,包括重组蛋白疫苗、鼻喷减毒活疫苗等。面临如此激烈的市场竞争,新推出的疫苗是否还会有市场?一位疫苗科学家表示,新一代疫苗依然有很大的需求。从技术路线来说,他的判断是,核酸疫苗的优势会有所下降,接下来新佐剂重组蛋白疫苗和粘膜免疫疫苗应该会成为主力军:这两种疫苗比核酸疫苗的免疫原性更好,且安全性和可及性有更明显优势。
2022年,《新英格兰医学杂志》上的一篇社论文章中,世界卫生组织新冠疫苗战略咨询专家组(SAGE)工作组主席Hanna Nohynek等人指出,疫苗产量已经不再是制约疫苗公平的限制因素,然而,许多原因决定了开发一系列新冠疫苗以控制大流行依然很重要。这是因为,每种疫苗都有不同特性和优缺点,而不同的国家和医疗环境、人口结构等,决定了其会受益于不同的疫苗种类。
“大流行期间使用的第一批新冠疫苗可能不是最好的长期解决方案。下一代新冠疫苗需要更广谱的抗原点位覆盖,以实现对新冠变异株的保护效力,要提供更长的保护时间,且便于及时针对变种进行更新。”该文章写道。免疫原性数据外,加强剂的频率、生产成本、物流需求、产能提升的难易程度等,都是政府决策的重要考量。
瑞科方面公布,其新冠疫苗可在室温下存放至少6个月,在2℃~8℃的情况下至少存放24个月,与传统灭活疫苗的储存要求相当。“这非常显著降低了疫苗从生产到接种过程中的运输、储存等额外成本,极大提高了疫苗的可及性。”刘勇指出。
瑞科生物在数据解读会上透露,ReCOV设计的年产能是2亿剂以上,且已取得国家有关监管部门颁发的新冠疫苗生产许可证。目前公司正在进行生产的各项准备,争取能够在上市后比较短时间内,就可以有更大的产能,能够满足市场需求。“应该说产能不是问题。”该公司表示。
ReCOV目前正在包括中国在内的全球多个国家,推进其三期临床研究,以检验其真实世界中的保护效力;談及其上市的时间表,刘勇表示,“快了。”
正如国内很多新生代疫苗厂商一样,瑞科疫苗也已经布局了其二价疫苗,亦即在原始株的基础上,增加了奥密克戎变种的抗原序列。与国内其他疫苗厂商的进度差不多,瑞科第二代疫苗已完成了设计和生产,预计在2023年的上半年完成主要的临床研究。
2022年8月,据《科学》报道,美国白宫发出了呼吁,要求开发一种可以预防未来新冠变种甚至未知冠状病毒的疫苗。白宫新冠病毒应对协调员阿希什·贾哈当时在一场疫苗峰会上表示:“我们拥有的疫苗很棒,但我们可以做得更好。最终,无论大自然扔给我们什么(新冠病毒),我们都有能够保护我们的疫苗。”
这种疫苗,便是很多疫苗科学家“梦寐以求”的通用型疫苗。瑞科也正在参与这种广谱性更好、但难度更大的新冠疫苗的研发。2020年1月10日,当中国科学家向世界同行公布新冠病毒基因序列仅几个小时之后,疫苗研发公司便开启了它们的竞赛。三年之后,这场赛跑依然在进行中。
